Современным направлением для создания экологически безопасных комплексных биопрепаратов является их получение на основе культуры клеток и тканей растений. Во многом продуктивность культивируемых клеток значительно превышает продуктивность растений для выделения биологически активных веществ, ценных для медицины, сельского хозяйства, пищевой промышленности. Цель данного исследования — разработка протокола массового получения каллусных культур фасоли, являющихся альтернативным источником получения лектинов, используемых в производстве биопрепаратов для сельского хозяйства. Оптимизированы условия введения в культуру in vitro шести сортообразцов фасоли казахстанской и зарубежной селекции, установлен оптимальный состав питательных сред для индукции каллусогенеза, определены сортообразцы, обладающие высокой каллусообразующей способностью. Установлена зависимость частоты каллусогенеза от минерального состава питательной среды и типа экспланта. Наибольшая частота каллусообразования наблюдалась в среде УМ (80–100 %), а наиболее подходящим эксплантом для индукции каллуса является эпикотиль. Показана зависимость частоты формирования морфогенного каллуса в зависимости от типа и концентрации фитогормонов. Образование морфогенных каллусов наблюдалось только в присутствии 2,4-Д. Максимальный выход морфогенного каллуса отмечен при концентрации 2,4-Д 2 мг/л. Выявлены перспективные сортообразцы фасоли, обладающие высокой способностью к накоплению каллусной биомассы и формированию морфогенного каллуса: «Актатти», «Ред Гойя», «Журавушка» и «Камелия». Разработанный протокол получения морфогенных каллусных культур фасоли может быть использован в качестве альтернативного биотехнологического подхода для выделения лектинов и получения на их основе биопрепаратов для сельского хозяйства.
Во всем мире проблема продовольствия остается одной из главных и насущных на сегодняшний день. В связи с этим в развитых сельскохозяйственных странах большое внимание уделяется разработке биологических и экологически безопасных методов защиты растений, направленных на сокращение объемов использования ядохимикатов [1, 2]. По химическому составу семена фасоли уникальны и включены в группу важных продуктов, обеспечивающих население полноценным белком. Однако белковый комплекс фасоли содержит ряд токсичных и антиалиментарных факторов питания, блокирующих активность пищеварительных ферментов, которые, возможно, принимают участие в защитных механизмах растений. Наличие антипитательных веществ (ингибиторов гидролаз, лектинов и цианогенных гликозидов) с высокой активностью в семенах фасоли делает ее перспективной с точки зрения биотехнологической переработки и получения фитопрепаратов для защиты растений, направленных на сокращение объемов использования ядохимикатов [3–5].
По оценкам ученых, с 2014 по 2019 гг. рост рынка биоудобрений возрос более чем в 1,6 млрд долл. Связано это с увеличением числа предприятий органической пищевой промышленности, их потребления и осведомленностью общества в отношении здоровья и угроз, возникающих в результате применения химических веществ в сельском хозяйстве [6]. Однако в настоящее время использование и применение биологического метода защиты растений в Казахстане развиты недостаточно. Сегодня создан и успешно применяется целый спектр микробиологических препаратов для нужд промышленности, сельского хозяйства, животноводства и охраны окружающей среды. В то же время разработка и производство биопрепаратов растительного происхождения находятся на начальном этапе. В Казахстане производится лишь 2 % биопрепаратов от мирового производства, несмотря на то, что наша республика обладает большим рыночным потенциалом для их эффективного применения в таких областях, как нефтегазовый сектор, сельское хозяйство, медицина, животноводство и др. Потребность в биопрепаратах для Казахстана имеет большое народно-хозяйственное значение, поскольку около 9000 га земель сельскохозяйственных угодий заражено вредителями, более 2,5 млн га — сорными растениями; распространено около 70 видов болезней микробного происхождения [7].
Современным направлением для создания экологически безопасных комплексных биопрепаратов является разработка методов культивирования изолированных клеток и тканей на искусственных питательных средах. Во многом продуктивность культивируемых клеток значительно превышает производительность растений для выделения биологически активных веществ, ценных для медицины, сельского хозяйства, пищевой промышленности. Кроме того, получение веществ вторичного биотехнологического синтеза из каллусных культур создает возможность использования растений, не произрастающих в данных природных условиях, и способствует проведению исследований в течение всего года [8].
В связи с этим актуальным представляется получение каллусных культур бобовых с максимальным содержанием комплекса биологически активных веществ. К ним относятся, например, лектины фасоли, которые принимают активное участие в защитных реакциях растений против насекомых, вредителей и поражения фитопатогенными грибами [9–12]. Ранее в наших работах проведен анализ содержания лектинов в коллекции фасоли, представленной сортообразцами местной и зарубежной селекции [13]. Биоскрининг позволил определить перспективные сортообразцы, характеризующиеся повышенным содержанием лектинов. Многие бобовые уже введены в культуру тканей и имеют высокую генотипическую специфичность [14]. Получение каллусных культур — важный инструмент в биотехнологии растений, который позволяет использовать клеточную биомассу для производства различных метаболитов и биологически активных веществ [15].
Таким образом, цель данного исследования — разработка протокола массового получения кал- лусных культур фасоли, являющихся альтернативным источником получения лектинов, используемых в производстве биопрепаратов для сельского хозяйства.
Методы и материалы
В качестве объектов исследования использовали 6 сортообразцов фасоли зерновых бобовых культур (семейство Fabaceae) казахстанской, российской и зарубежной селекции: «Актатти» (Казахстан), «Бийчанка» (Россия), «Журавушка» (Россия), «Иранская» (Иран), «Камелия» (США) и «Ред Гойя» (США). Семена исследуемых образцов были получены из коллекции агробиостанции КазНУ им. аль-Фараби. В качестве эксплантов использовали эпикотили и гипокотили 7–14-дневных асептических проростков. Для получения асептических проростков семена промывали теплой проточной водой и выдерживали в растворе хозяйственного мыла в течение 30 мин. Затем семена отмывали от мыльного раствора и стерилизовали 10 мин в 20 %-ном гипохлориде натрия с 2–3 каплями TWIN 20; 5 мин — в 5 %-ном H2O2; 5 мин — в 70 %-ном спирте и трижды промывали стерильной дистиллированной водой. Семена проращивали в пробирках на безгормональной питательной среде Мурасиге- Скуга в инкубаторе при 24–26 °С.
Для получения первичной культуры каллусов экспланты размером 2–3 см культивировали на средах Ушимия-Мурасиге [16], Мурасиге-Скуга [17] и Гамборга-Эвеленга В 5 [18]. Экспланты высаживали на чашки Петри по 10 эксплантов на каждую чашку. Питательные среды автоклавировали при 121 °C и 1 атм. в течение 20 мин. В качестве индукторов каллусогенеза использовали ауксины (2,4-Д и НУК) и цитокинины (кинетин). Каллусы культивировали на свету при температуре 23–25 °С, 16-часовом фотопериоде с интенсивностью освещения 10000 люкс. Эксперименты были выполнены в трехкратной повторности. Начало каллусообразования наблюдали через 7–10 дней. Процесс каллусогенеза оценивали по трем показателям: 1) частота каллусогенеза — доля эксплантатов, образовавших каллус; 2) интенсивность каллусообразования — степень накопления каллусной массы; 3) морфологический тип каллуса. Интенсивность каллусообразования оценивалась по балльной системе: 0 — отсутствие каллуса; 1 — каллусогенез охватывает до половины экспланта; 2 — каллусной тканью покрыто до 2/3 экспланта; 3 — эксплант виден лишь частично; 4 — эксплант полностью покрыт каллусом.
Индекс роста каллусных культур определялся через каждые 28 дней культивирования и вычислялся по формуле
Wo^-Wt
- = Wo ,
где Wo — начальная масса каллуса, г; Wt — масса каллуса в конце цикла выращивания, г.
Для наращивания каллусной биомассы каллусы пассировали каждые 28 дней на питательной среде того же минерального и гормонального состава. Для пассирования брали кусочки каллусной ткани весом не более 7–10 г. Для получения достаточного количества каллусной биомассы проводили 5–7 пассажей для каждого сортообразца. Изучение влияния гормонального состава среды на прирост клеточной биомассы и получение морфогенных каллусов проводили на средах с 2,4-Д и НУК в концентрациях 2, 4, 6 и 8 мг/л. Концентрация кинетина составляла 0,25 мг/л. Статистический анализ был выполнен с использованием программы однофакторного дисперсионного анализа ANOVA и программы STATISTICA.
Результаты и их обсуждение
Индукция каллусогенеза. На первом этапе исследований проводили изучение влияния минерального состава питательной среды на индукцию каллусогенеза. Для получения каллусной биомассы экс- планты (эпикотиль и гипокотиль) культивировали на питательных средах различного минерального состава, содержащие 2 мг/л 2,4-Д и 0,25 мг/л кинетина. В исследование были включены наиболее часто используемые для культивирования бобовых культур питательные среды: Ушимия-Мурасиге (УМ), Мурасиге-Скуга (МС) и Гамборга-Эвеленга (В5). Установлено, что частота и интенсивность каллусо- генеза зависят от состава питательной среды и типа экспланта. Сравнительный анализ зависимости частоты каллусогенеза от типа экспланта показал, что оба экспланта обладают каллусообразующей способностью, причем на всех питательных средах наибольшая каллусообразующая способность отмечена на экспланте эпикотиль, хотя индукция каллусогенеза на экспланте гипокотиль начиналась на 2–3 дня раньше (табл. 1).
Т а б л и ц а 1
Частота каллусогенеза у сортообразцов фасоли на различных питательных средах, %
|
Сортообразцы фасоли |
Питательные среды, экспланты |
|||||
|
УМ |
МС |
В5 |
||||
|
эпикотиль |
гипокотиль |
эпикотиль |
гипокотиль |
эпикотиль |
гипокотиль |
|
|
«Актатти» |
100 ±1,40 |
90±1,24 |
92±1,34 |
80±1,25 |
35±0,80 |
30±0,64 |
|
«Бийчанка» |
95±1,28 |
84±1,22 |
90±1,28 |
68±1,16 |
30±0,56 |
25±0,40 |
|
«Иранская» |
85±1,34 |
80±1,17 |
88±1,35 |
76±1,18 |
28±0,40 |
20±0,30 |
|
«Камелия» |
97±1,20 |
82±1,14 |
90±1,15 |
82±1,25 |
32±0,34 |
30±0,33 |
|
«Ред Гойя» |
100±1,17 |
87±1,16 |
95±1,14 |
84±1,30 |
35±0,44 |
28±0,39 |
|
«Журавушка» |
90±1,23 |
85±1,14 |
87±1,19 |
75±1,12 |
32±0,56 |
26±0,42 |
В результате проведенных исследований установлена зависимость частоты каллусогенеза от минерального состава питательной среды. Наибольшая частота каллусообразования наблюдалась на среде УМ и составляла на экспланте: эпикотиль 85–100 %, гипокотиль — 82–90 %.
На питательной среде МС частота образования каллусов была тоже высокой, но ниже, чем на среде УМ. На среде В5 частота каллусогенеза была самой низкой и не превышала 35 %. Наибольшая интенсивность каллусогенеза также отмечена при культивировании на среде УМ. На средах МС и В5 интенсивность каллусогенеза не превышала 3,45 и 1,84 балла соответственно (табл. 2).
Т а б л и ц а 2
Интенсивность каллусогенеза у сортообразцов фасоли на различных питательных средах, баллы
|
Сортообразцы фасоли |
Питательные среды, экспланты |
|||||
|
УМ |
МС |
В5 |
||||
|
эпикотиль |
гипокотиль |
эпикотиль |
гипокотиль |
эпикотиль |
гипокотиль |
|
|
«Актатти» |
4,0 ±0,48 |
3,77±0,45 |
3,20±0,89 |
2,80±0,72 |
1,84±0,70 |
1,45±0,26 |
|
«Бийчанка» |
3,27±0,98 |
3,12±0,58 |
3,25±0,45 |
2,70±0,30 |
1,35±0,75 |
1,28±0,95 |
|
«Иранская» |
2,45±0,38 |
2,30±0,78 |
2,72±0,65 |
2,70±0,30 |
1,45±0,46 |
1,35±0,62 |
|
«Камелия» |
3,75±0,48 |
3,42±0,78 |
2,58±0,88 |
2,15±0,28 |
1,44±0,46 |
1,15±0,18 |
|
«Ред Гойя» |
4,0 ±0,52 |
3,50±0,44 |
3,45±0,28 |
3,25±0,45 |
1,72±0,69 |
1,45±0,68 |
|
«Журавушка» |
3,12±0,52 |
2,35±0,35 |
2,52±0,98 |
2,41±10,42 |
1,13±0,43 |
1,12±0,40 |
Наибольшая каллусообразующая способность изученных сортообразцов фасоли на среде УМ, по- видимому, связана с тем, что содержание витаминов В1, В6 и РР в среде УМ, по сравнению со средой
МС, увеличено в 10 раз. Среды УМ и МС имеют одинаковый минеральный состав [16, 17], в связи с чем каллусообразующая способность изученных сортообразцов на данных питательных средах отличается незначительно. Поскольку среда В5 имеет другой состав макро- и микроэлементов по сравнению с УМ, МС, можно предположить, что каллусообразующая способность зависит не только от содержания витаминов, но и от минерального состава.
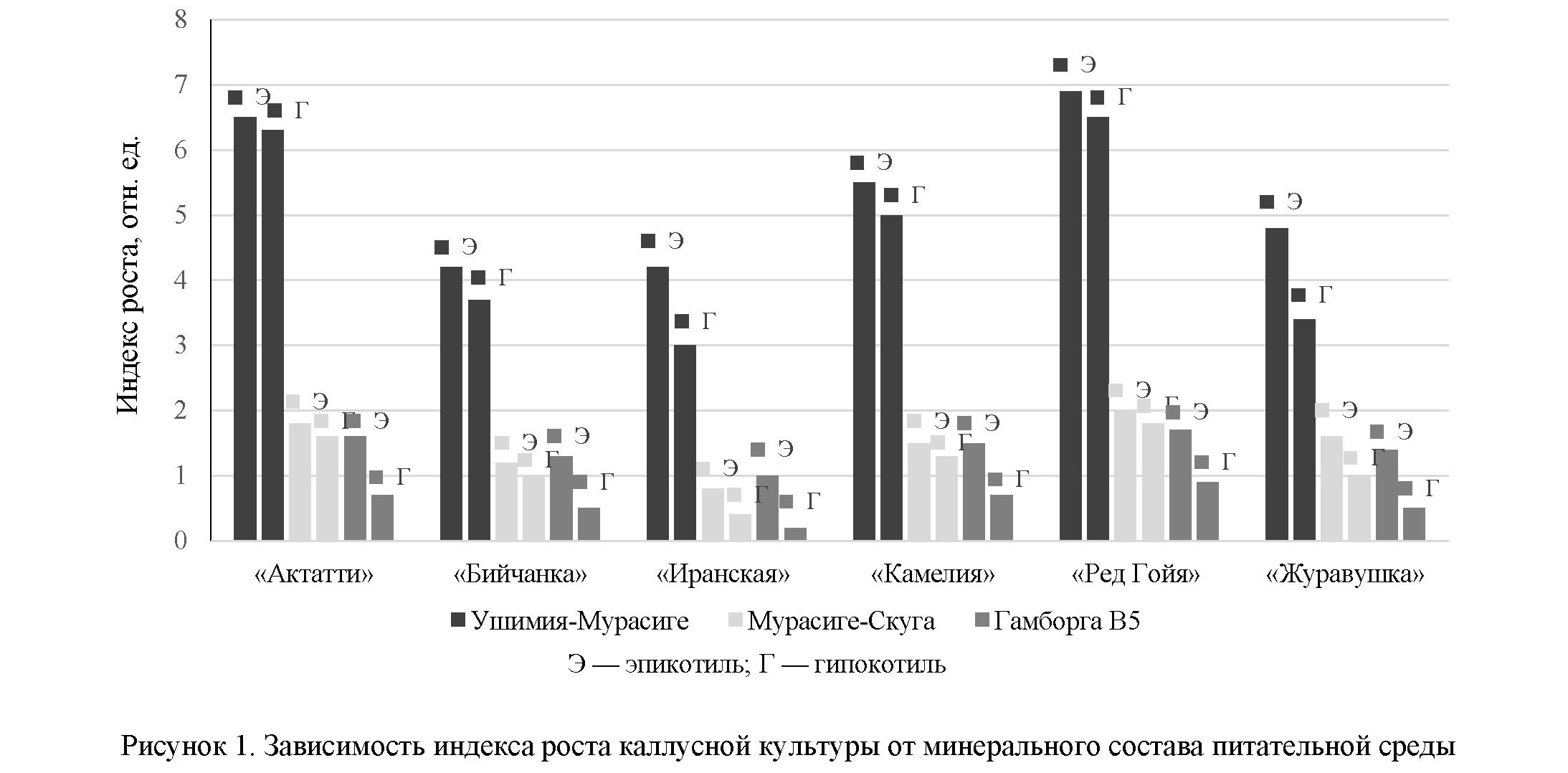
Индекс роста каллусных культур связан также с минеральным составом питательных сред. На питательной среде УМ индекс роста варьировался от 3,2 до 6,9. Максимальная скорость роста отмечена для сортообразцов «Ред Гойя» и «Актатти», минимальная — для сорта «Иранская». На средах МС и В5 индекс роста не превышал 2,0 и 1,7 соответственно (рис. 1).
Среди изученных образцов можно выделить «Актатти» и «Ред Гойя», для которых частота и интенсивность каллусогенеза были максимальными на обоих эксплантах.
Морфологическая структура каллуса определялась визуально по общепринятой методике [19]. При культивировании на среде УМ и МС формировался бело-желтый, глобулярный, рыхлый каллус с хлорофилл-содержащими участками, которые представляют собой зоны морфогенеза. Данный тип каллуса был определен как морфогенный. На среде В5 формировался плотный, компактный, малообводненный каллус, который был охарактеризован как неморфогенный. Изучение влияния минерального состава на индукцию каллусогенеза показало, что оптимальной средой является среда Ушимия- Мурасиге. Основа данной среды — среда Мурасиге-Скуга, которая чаще всего использовалась для индукции каллусных культур различных видов фасоли и других бобовых культур [20, 21].
Оптимизация гормонального состава питательных сред для получения клеточной биомассы различных сортообразцов фасоли
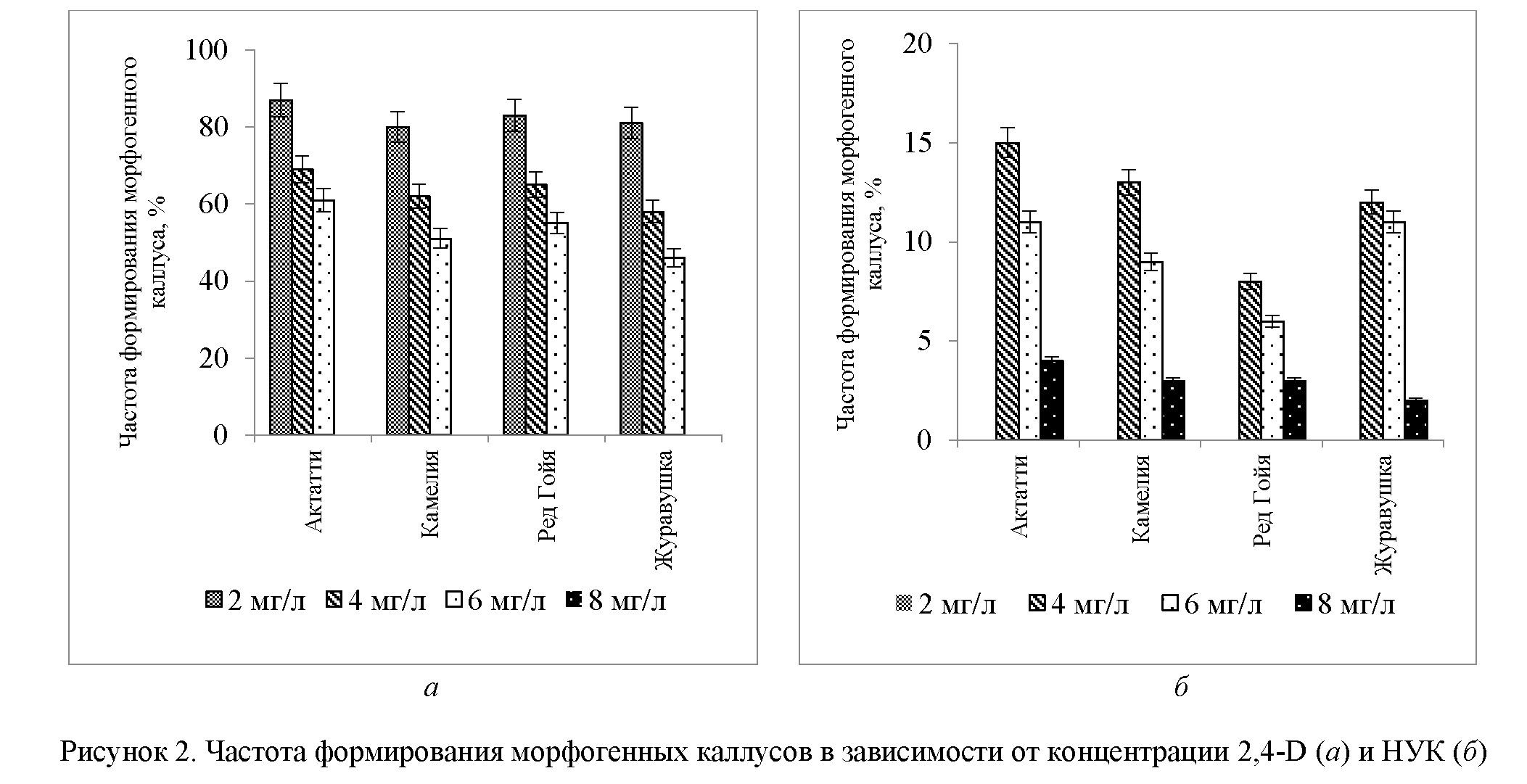
В данной серии экспериментов изучено влияние двух видов ауксинов (2,4-Д и НУК) в концентрациях 2, 4, 6 и 8 мг/л на прирост клеточной биомассы и получение морфогенных каллусов. В результате изучения 6 сортообразцов фасоли показано, что частота формирования морфогенного каллуса зависит от типа и концентрации фитогормонов. При концентрации 2,4-Д 2 мг/л выход морфогенного каллуса был наибольшим и варьировался от 80 до 87 %. Увеличение концентрации 2,4-Д до 4 мг/л и 6 мг/л незначительно влияло на прирост биомассы, но сопровождалось снижением частоты образования морфогенных каллусов. Концентрация 2,4-Д 8 мг/л оказалась летальной для каллусных культур всех образцов фасоли.
При использовании в качестве индуктора НУК частота каллусогенеза была гораздо ниже, чем на средах с 2,4-Д. Максимальный прирост каллусных культур отмечен при концентрации НУК 4 мг/л, однако, в зависимости от генотипа, частота каллусогенеза не превышала 20–40 %. При этом доля морфогенных каллусов составляла не более 15 %. При концентрации НУК 2 мг/л индукции каллусогенеза не наблюдалось. Увеличение концентрации НУК в среде культивирования до 6 мг/л и 8 мг/л вызывало резкое снижение частоты каллусогенеза и формирование ризогенного каллуса. В результате исследований нами также выявлены сортовые различия по способности к формированию морфогенного каллуса. Морфогенные структуры формировались на каллусных культурах четырех сортообразцов: «Ак- татти», «Ред Гойя», «Журавушка» и «Камелия». Максимальная частота образования морфогенных каллусов отмечена для сорттообразцов «Актатти» (87 %) и «Ред Гойя» (83 %) (рис. 2).
В большинстве исследований по изучению процессов индукции морфогенных каллусных культур фасоли показано, что в качестве индуктора эмбрио- и органогенеза чаще всего используют БАП и TDZ [22–24]. В работе А.М. Gatica с соавторами показано, что у костариканских сортов фасоли формирование эмбриогенных каллусов зависело от концентрации БАП и аденин сульфата, но генотипической зависимости установлено не было. Независимо от сорта, среда, содержащая 5 мг/л БАП и 20–40 мг/л аденин сульфата, способствовала индукции образования побегов [25]. В наших исследованиях установлено, что у изучаемых сортообразцов фасоли частота формирования морфогенных каллусов зависела от типа фитогормонов и концентрации 2,4-Д. Изучение влияния различных видов и концентраций ауксинов показало, что наиболее интенсивно морфогенные каллусы формировались на экспланте эпикотиль на среде, содержащей 2 мг/л 2,4-Д.
Концентрация 2,4-Д 8 мг/л оказалась летальной для каллусных культур фасоли. Предполагается, что при высоких концентрациях 2,4-Д сильно увеличивается скорость образования этилена и уменьшается скорость растяжения клеток. Вероятно, у двудольных растений подавление роста высокими концентрациями ауксина опосредовано их действием на синтез этилена [26]. Использование НУК не дало положительных результатов.
Ряд исследователей отмечают связь морфологии каллусов с их способностью к регенерации растений и синтезу биологически активных веществ. Культивирование каллусной ткани в условиях in vitro вызывает изменение метаболической активности клеток и выражается в модификации количества и состава биологически активных веществ в каллусной ткани по сравнению с исходным растением [27, 28]. В работе И.Ф. Шаяхметова показано, что морфогенный каллус отличается высоким содержанием лектинов, что является следствием морфогенетических процессов [29].
Ранее проведенные нами исследования по оценке лектиновой активности перспективных сорто- форм фасоли показали, что сорта «Журавушка» и «Актатти» отличаются наиболее высоким содержанием лектинов [13]. Результаты, полученные в ходе настоящих исследований, позволили определить, что сортообразцы «Актатти», «Журавушка» и «Ред-Гойя» являются наиболее перспективными для получения каллусных культур и могут в дальнейшем применяться для разработки биотехнологических подходов выделения лектинов.
Таким образом, разработанный протокол массового получения каллусных культур может быть предложен в качестве альтернативного пути для выделения лектинов фасоли и получения на их основе биопрепаратов для повышения устойчивости растений к различным биотическим и абиотическим факторам.
Заключение
Современным направлением для создания экологически безопасных комплексных биопрепаратов является их получение на основе культуры клеток и тканей растений. Данная работа посвящена разработке протоколов массового получения каллусных культур фасоли казахстанской и зарубежной селекции. На основе оптимизации минерального и гормонального состава питательных сред разработан протокол получения морфогенных каллусных культур перспективных сортообразцов фасоли, который может быть использован в качестве альтернативного биотехнологического подхода для выделения лектинов и получения на их основе биопрепаратов для сельского хозяйства.
Список литературы
- Shternshis M. Biopreparations for plant protection in Siberia: application and enhancement of activity / М. Shternshis // Journal of Agricultural Technology. — 2005. — Vol. 1, № 1. — Р. 1–18.
- Carlini C.R. Plant toxic proteins within secticidal properties. Оn their potentialities as bioinsecticides. A review / C.R. Carlini, M.F. Grossi-de-Sa // Toxicon. — 2002. — Vol. 40. — P. 1515–1539. DOI: https://doi.org/10.1016/S0041-0101(02)00240-4
- Vasconcelos I.M. Antinutritional properties of plant lectins / I.M. Vasconcelos, J.T. Oliveira // Toxicon. — 2004. — Vol. 44, № 4. — Р. 385–403. DOI: http://dx.doi.org/10.1016/j.toxicon.2004.05.005
- Sharma A. Purification and characterization of a lectin from Phaseolus vulgaris cv. (Anasazi Beans) / A. Sharma, T.B. Ng, J.H. Wong, P. Lin // Journal of Biomedicine and Biotechnology. — 2009. — Vol. 2009. — P.1–9. DOI: https://doi.org/10.1155/ 2009/929568
- Wong J.H. “Vulgarinin”, a broad-spectrum antifungal peptide from haricot beans (Phaseolus vulgaris) / J.H. Wong, T.B. Ng // The International Journal of Biochemistry & Cell Biology. — 2005. — Vol. 37, № 8. — P. 1626–1632. DOI: https://doi.org/10.1016/ j.biocel.2005.02.022
- Grobelak A. Analysis of commercialization possibilities of biopreparation “rhizofertum” for plant growth stimulation in unfavourable soil conditions / A. Grobelak, A. Napora, J. Hiller, M. Kacprzak // Acta Innovations. — 2016. — Vol. 19. — P. 45–51.
- Ремеле В.В. Экологически чистые бактериальные препараты для защиты зерновых культур от грибных болезней / В.В. Ремеле, Д.С. Ошанова // Вестн. сельскохоз. науки Казахстана. — 2012. — № 5. — С. 10–14.
- Эрст А.А. Особенности получения вторичных метаболитов в культуре клеток, тканей и органов Hedysarum theinum (Fabaceae) in vitro / А.А. Эрст, Т.В. Железниченко, Т.А. Кукушкина, Т.И. Новикова, А.А. Кузовкова, О.В. Копач, Е.В. Банаев // Turczaninowia. — 2015. — T. 18, № 4. — С. 26–35. DOI: https://doi.org/10.14258/turczaninowia.18.4.3
- Lam S.K. Lectins: Production and practical applications / S.K. Lam, T.B. Ng // Appl. Microbiol. Biotechnol. — 2011. — Vol. 89. — P. 45–55. DOI: http://dx.doi.org/10.1007/s00253-010-2892-9
- Svetleva D. Biotechnology as a useful tool in common bean (Phaseolus vulgaris L.) improvement / D. Svetleva, M. Velcheva, G. Bhowmik // Euphytica. — 2003. — Vol. 3. — P. 1189–1200. DOI: https://doi.org/10.1023/A%3A1023983831582
- Vanisree M. Plant cell cultures-an alternative and efficient source for the production of biologically important secondary metabolites / M. Vanisree, H.S. Tsay // Int. J. Appl. Sci. Eng. — 2004. — Vol. 2. — P. 29–48. DOI: 10.1079/IVP2003504
- Macedo L.R. Insecticidal activity of plant lectins and potential application in crop protection / L.R. Macedo, C.F.R. Oliveira,
- T. Oliveira // Molecules. — 2015. — Vol. 20. — P. 2014–2033. DOI: https://doi.org/10.3390/molecules20022014
- Жумабаева Б.А. Оценка лектиновой активности перспективных сортоформ фасоли / Б.А. Жумабаева, Э.Д. Джанга- лина, З.Г. Айташева, Д.А. Ыбраймолдаева, А.Б. Бегайдарова // Вестн. КазНУ. Сер. биол. — 2015. — № 63(1). — C.76–81.
- Somers D.A. Recent advances in legume transformation / D.A. Somers, D.A. Samac, M. Olhoft // Plant Physiol. — 2003. — Vol. 131. — P. 892–899. DOI: https://doi.org/10.1104/pp.102.017681
- Ramachandra R.S. Plant cell culture: chemical factories of secondary metabolites / R.S. Ramachandra, G.A. Ravishankar // Biotechnol Adv. — 2002. — Vol. 20. — P.101–153. DOI: http://dx.doi.org/10.1016/S0734–9750(02)00007–1
- dos Santos A.V.P. Organogenesis and somatic embryogenesis in tissues derived from leaf protoplasts and leaf explants of Medi- cago sativa / A.V.P. dos Santos, D.E. Outka, E.C. Cocking, M.R. Davey // Zeitschrift für Pflanzenphysiologie. — 1980. — Vol. 99, № 3. — P. 261–270. DOI: https://doi.org/10.1016/S0044-328X(80)80138-3
- Murashige T. A revised medium for rapid growth bioassays with tobacco tissue cultures / T. Murashige, F. Skoog // Physiologia Plantarum. — 1962. — Vol. 15, № 3. — P. 473–493. DOI: https://doi.org/10.1111/j.1399–3054.1962.tb08052.x
- Gamborg O.L. Nutrient requirements of suspension cultures of soybean root cells / O.L. Gamborg, R.A. Miller, K.Ojima // Experimental Cell Research. — 1968. –Vol. 50. — P. 151–158. DOI: https://doi.org/10.1016/0014-4827 %2868 %2990403-5
- Загоскина Н.В. Биотехнология: теория и практика / Н.В. Загоскина, Л.В. Назаренко, Е.А. Калашникова, Е.А. Живу- хина. — М.: Оникс, 2009. — 496 с.
- Zambre M.A. Plant regeneration from embryo-derived callus in Phaseolus vulgaris L. (common bean) and P. acutifolius A. Gray (tepary bean) / M.A. Zambre, J.De Clercq, E. Vranová, M.Van Montagu, G. Angenon, W. Dillen // Plant Cell Reports. — 1998. — Vol. 17, № 8. — P. 626–630. DOI: https://doi.org/10.1007/s002990050455
- Renato A. Benzyladenine-induced adventitious shoot regeneration from hypocotyls of adzukibean (Vigna angularis) / A. Renato, H. Kazumi // Plant Growth Regulation. — 2000. — Vol. 31, № 3. — P. 147–153. DOI: https://doi.org/10.1023/A:1006302816178
- Shamsudeen V.M. Organogenesis of Phaseolus angularis L.: high efficiency of adventitious shoot regeneration from etiolated seedlings in the presence of N6-benzylaminopurine and thidiazuron / V.M. Shamsudeen, J.M. Sung, T.L. Jeng, C.S. Wang // Plant Cell Tissue and Organ Culture. — 2006.– Vol. 86, № 2.– P. 187–199. DOI: https://doi.org/10.1007/s11240–006–9107–1
- Schryer P.A. Rapid regeneration of Phaseolus angustissimus and P. vulgaris from very young zygotic embryos / P.A. Schryer, Q. Lu, A. Vanderberg, K.E. Bett // Plant Cell Tissue and Organ Culture. — 2005. — Vol. 83, № 1. — P. 67–74. DOI: https://doi.org/ 10.1007/s11240–005–2586–7
- Veltcheva M.R. In vitro regeneration of Phaseolus vulgaris L. via organogenesis from petioles explants / M.R. Veltcheva,
- L. Svetleva // Journal Central European Agriculture. — 2005. — Vol. 6, № 1. — P. 53–58. DOI: https://doi.org/10.5513/ jcea.v6i1.246
- Gatica A.M. In vitro plant regeneration system for common bean (Phaseolus vulgaris): effect of N6-benzylaminopurine and adenine sulphate / A.M. Gatica, M.V. Jenny, R.F. Pilar, V.M. Marta // Electronic Journal of Biotechnology. — 2010. — Vol. 13, № 1. — P. 2–8. DOI:http://dx.doi.org/10.2225/vol13-issue1-fulltext-7
- Новикова Г.В. Пролиферация клеток растений и ее регуляторы / Г.В. Новикова, А.В. Носов, Н.С. Степанченко, А.А. Фоменков, А.С. Мамаева, И.Е. Мошков // Физиология растений. — 2013. — Т. 60, № 4. — С. 529–536. DOI: https://doi.org/10.7868/s0015330313040118
- Смольникова Я.В. Химический состав растения и каллусной ткани Digitalis purpurea L. / Я.В. Смольникова, Н.А. Величко // Химия растительного сырья. — 2011. — № 4. — С. 239–243.
- Jeong G. Effect of plant growth regulators on growth and biosynthesis of phenolic compounds in genetically transformed hairy roots of Panax ginseng C.A. Meyer / G. Jeong, J. Woo, D. Park // Biotechnol. Bioprocess Eng. — 2007. — Vol. 12, № 2.– P. 86–91. DOI: https://doi.org/10.1007/BF03028631
- Шаяхметов И.Ф. Роль лектина пшеницы и абсцизовой кислоты в регенерации растений / И.Ф. Шаяхметов // Успехи современной биологии. — 2004. — Т. 124, № 6.– С. 602–611.