Структурные изменения хромосом, проявляющиеся вследствие химического мутагенеза, как показывают исследования, зачастую вызваны высокими концентрациями тяжелых металлов в воздухе и пыли промышленных городов. Целью статьи явилось изучение роли цинка в образовании хромосомных аберраций. Исследована частота встречаемости хромосомных аберраций и хромосомных аномалий у лиц, проживающих в условиях повышенной химической нагрузки. Также изучен уровень хромосомных аберраций у лиц, проживающих на территории экологического бедствия. Выделены типы и характер цитогенетических нарушений. Проведен расчет индивидуальных дозовых нагрузок поступления химических веществ в организм из объектов окружающей среды. Методом моделирования представлена роль цинка в формировании хромосомных аберраций. Выявлена достоверно значимая обратная корреляционная связь между уровнем хромосомных аберраций и содержанием цинка в атмосферном воздухе (коэффициент парной корреляции Пирсона составил –0,39). Установлено, что при снижении концентрации цинка в атмосферном воздухе статистически значимо повышается уровень хромосомных аберраций. Дана характеристика ко-ферментной активности цинка в функционировании ферментов системы репарации и антиоксидантной защиты. Выявлено, что хромосомные аберрации являются рефлекторами при условиях экспозиции экологических факторов экзогенного и эндогенного происхождения, вследствие чего происходят изменения в функционировании всей клетки.
Введение
Проблема загрязнения окружающей среды является одной из наиболее обсуждаемых и волнующих на сегодняшний день во всем мире. Антропогенное воздействие на среду обитания приводит к уже случившимся последствиям, таким как увеличение частоты заболевания всех групп нозологий, превышение предельно допустимых концентраций веществ в атмосферном воздухе, в почве и в водоемах. Загрязнение окружающей среды может быть как и прямым при промышленных выбросах и добычи полезных ископаемых, так и посредственным в результате орошения почв, нерациональном использовании водных ресурсов на примере Аральского моря, выбросов автотранспорта. В результате такого воздействия в различных экологических средах накапливаются различные токсиканты, которые негативно сказываются на состоянии здоровья населения и способны оказывать генотоксический эффект. Хромосомные аберрации (ХА) являются значимым индикатором при оценке воздействия различных факторов среды на организм, поступающих ингаляционным и оральным путем.
Содержание химических веществ в атмосферном воздухе и их поступление ингаляционным путем при дыхании можно оценить с помощью расчетного метода, что дает возможность оценить текущую химическую нагрузку на организм, а также риск последствий, в зависимости от времени экспозиции и концентрации веществ.
Доза — есть измерение, определяющее количество поступления химического вещества в организм. Система «химическое воздействие — ответная реакция организма» характеризует физиологические изменения в организме на различных уровнях организации живого в ответ на количество поступления вещества и его продолжительность. Дозовую нагрузку определяют в зависимости от способа поступления химического ксенобиотика (ингаляционный, пероральный, накожный) из дифференцированных объектов экологической среды.
Расчет дозовой нагрузки включает анализ основных физических параметров, идентификацию маршрутов воздействия и оценку величины, частоты и продолжительности воздействий с расчетом поступления. Расчеты дозовых нагрузок для жителей анализируемых населенных пунктов проведены для взрослого населения. При увеличении концентрации вещества в окружающей среде повышается вероятность их проникновения в организм человека, что в результате ответной реакции организма приводит к физиологическим изменениям и оказывает общий токсический, а также генотоксический эффект. Хромосомные аберрации могут быть рефлекторами при токсикологическом воздействии экологических факторов, определяя не только ядерные и клеточные изменения, а также состояния органов и систем [1–3]. Роль отдельных микроэлементов в поддержании генетической стабильности клетки изучена в разной степени. Касательно микроэлемента цинка известно, что цинк является структурной частью множества металлосодержащих ферментов матричных процессов. Цинк определяет способность нормального функционирования этих ферментов, тем самым предотвращая риск возникновения мутаций, но при этом, однако, роль цинка в формировании хромосомных аберраций изучена недостаточно [1, 4–6].
С учетом изложенного выше, изучение механизмов ответной реакции организма на неблагоприятное воздействие окружающей среды является актуальным и насущным вопросом для биомедицинских дисциплин.
Цель — оценить роль цинка в образовании хромосомных аберраций с помощью расчетного метода оценивания.
Материалы и методы исследования
В выборке представлены 40 человек репродуктивного возраста (18–45), проживающие не менее 10 лет в зоне экологического бедствия Приаралья, признанным законодательно, а именно в г. Арысь (Туркестанская область) [7].
Проведен расчет индивидуальных дозовых нагрузок. Расчет ингаляционной дозовой нагрузки при оценки попадания химического ксенобиотика при дыхании из атмосферного воздуха в организм экспонируемого населения осуществлялся по рекомендациям, приведенным в Р 2.1.10.1920–04 «Руководстве по оценке риска для здоровья населения при воздействии химических веществ, загрязняющих окружающую среду» от 2004 г., разработанном Ю.А. Рахманиным с соавторами [8].
Измерения концентраций неорганических веществ в атмосферном воздухе проводили с помощью атомно-абсорбционного спектрометра МГА-915 (Россия), согласно М 02–09–2005 «Методике выполнения измерений массовой концентрации металлов в атмосферном воздухе атомноабсорбционным методом с электротермической атомизацией с использованием атомно-абсорбционного спектрометра МГА-915».
Формула для расчета индивидуальных дозовых нагрузок химическими загрязнителями, поступающими ингаляционным путем, представлена на рисунке 1.
Среднее значение концентрации дозовой нагрузки составило 2,83±0,19 мг/(кг/день) (нижний и верхний 95 %-ные доверительные интервалы 2,44 и 3,23 соответственно, СКО было равно 1,09, размах расчетных значений выборки был равен 4,31).
При определении генотоксических эффектов были приготовлены препараты хромосом с использованием нами модифицированного цитогенетического метода культивирования лимфоцитов периферической крови Hungerford D.A. et al. и последующий учет хромосомных перестроек в метафазных пластинках [9, 10]. Для учёта хромосомных аберраций использовали микроскоп Nikon Eclipse E400 (Япония).
I=(Ca ×Tout ×Vout)+(Ch ×Tin ×Vin)×EF×ED/(BW×AT×365), где I — величина поступления, мг/(кг/день);
Ca — концентрация вещества в атмосферном воздухе, мг/м3;
Ch — концентрация вещества в воздухе жилища, мг/м3;
Tout — время, проводимое вне помещений, ч/день (8 ч/день);
Tin — время, проводимое внутри помещений, ч/день (16 ч/день);
Vout — скорость дыхания вне помещений, м3/ч;
Vin — скорость дыхания внутри помещения, м3/ч;
EF — частота воздействия, дней/год (350 дней/год);
ED — продолжительность воздействия, год;
BW — масса тела, кг;
АТ — период осреднения экспозиции, лет.
Рисунок 1. Формула расчета дозовых нагрузок, поступающих ингаляционным путем
Всего в ходе работы было зарегистрировано и просмотрено 7252 метафаз у 40 пациентов, проживающих в зоне экологического предкризиса (г. Арысь). Выборка группы обследованных была однородна: все представители были одного возраста, уровня образования, социального статуса, имели схожие бытовые условия проживания и профессии, проживали в данной местности не менее 10 лет, не имели контакта с вредными производственными факторами среды.
Материалы исследований были обработаны математико-статистическими методами с использованием программ статистической обработки данных Statistica 10.0. Применялись методы оценки достоверности различия по t-критерию Стьюдента. В качестве критерия статистической надежности выбрано значение для двух несвязанных групп (р < 0,05).
Результаты исследования и их обсуждение
Все хромосомные аберрации были классифицированы и определены как аберрации хроматидного типа и хромосомного типа. Абсолютное значение выявленных хромосомных аберраций на 7252 метафазы составило 101 регистрацию, а уровень частоты хромосомных аберраций был равен 1,392±0,137 %, что, согласно методическим рекомендациям «Использование цитогенетического метода учёта хромосомных аберраций для исследования мутагенности в условиях неблагоприятной экологической обстановки», можно отнести к повышенному генетическому риску [10].
Уровень частоты хромосомных аберраций хроматидного типа был равен 1,047±0,119 %, а частота аберраций хромосомного типа равнялась 0,344±0,068 % для обследуемого населения, составившего выборку исследования. Результаты исследования и анализ полученных данных показали, что по типам хромосомных аберраций превалировали аберрации хроматидного типа (75 %), тогда как аберрации хромосомного типа составили 25 %. Таким образом, частота аберраций хроматидного типа в 3 раза превышала частоту аберраций хромосомного типа (см. табл.).
Таблица Типы хромосомных аберраций у экспонированного населения Приаралья (М±m%; 95 % доверительный интервал, среднеквадратичное отклонение)
|
Показатели |
М±m |
95 % ДИ |
СКО |
Р |
|
ХА хроматидного типа |
1,047±0,119 |
1,045–1,050 |
0,014 |
0,001 |
|
ХА хромосомного типа |
0,344±0,06 |
0,343–0,346 |
0,068 |
Анализ литературных данных свидетельствует, что хромосомные аберрации хроматидного типа определены воздействием химических мутагенов и процессами химического патогенеза хромосомных нарушений [1–2, 11].
Химическую причинность мутагенеза также подтвердила выявленная в ходе исследования статистически значимая обратная причинно-следственная связь между уровнем хромосомных аберраций у лиц, проживающих в зоне предкризиса, и дозовой нагрузкой цинка, поступающего ингаляционным путём (рис. 2). Коэффициент парной корреляции Пирсона составил 0,39. Установлено, что при снижении концентрации цинка в атмосферном воздухе статистически значимо повышается уровень хромосомных аберраций: у = 4,5747 – 0,7306·Х (коэффициент регрессии R = –0,39; коэффициент детерминации R2 = 0,15; коэффициент Фишера f = 5,43; оценка модели p = 0,026).
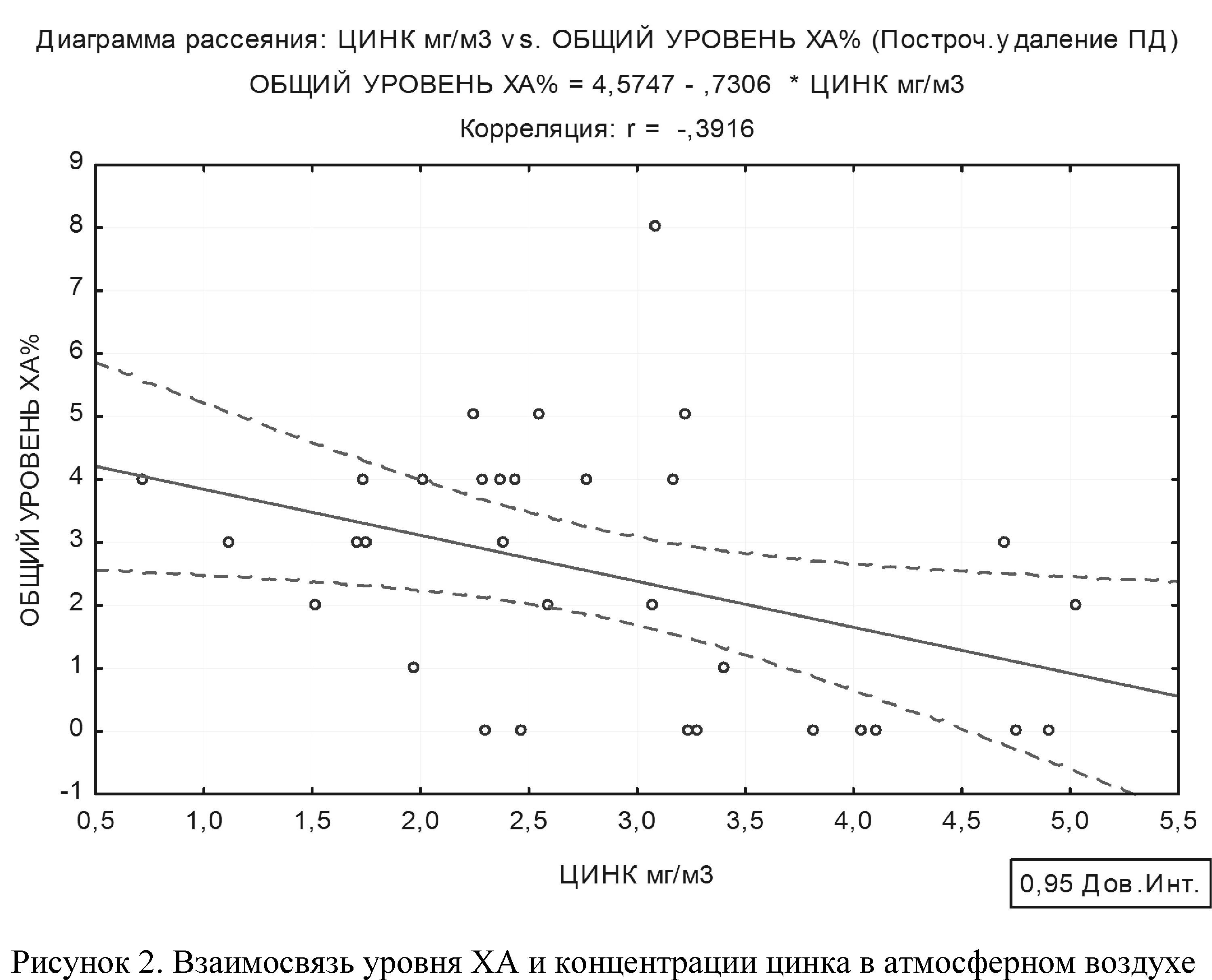
Так, при увеличении концентрации цинка в атмосферном воздухе на 10 % можно прогнозировать повышение уровня хромосомных аберраций на 8,3 %. Ряд авторов указали, что микроэлемент цинк входит в структуру активного центра ряда ферментов, некоторые из цинксодержащих ферментов участвуют в синтезе РНК и ДНК и имеют большое значение в метаболизме нуклеиновых кислот (ДНК- и РНК-полимеразы, тимидинкиназы, белки факторов транскрипции — цинк-фингер белки) [4–6]. Таким образом, значение цинка в генетической стабильности не вызывало сомнения, но тем не менее не было данных о его роли в формировании хромосомных аберраций. Кроме того, цинк в качестве ко-фермента ответствен за нормальное функционирование фермента антиоксидантной защиты супероксиддисмутазы и служит одним из активаторов биосинтеза металлотионеинов — специальных белков, выполняющих защитную функцию, активность которых может приводить к повреждению молекул ДНК [1]. Имеются данные, что дефицит цинка может оказывать влияние на развитие генетических заболеваний, например, синдром Danbolt-Closs (энтеропатический акродерматит — генетическое заболевание с аутосомно-рецессивным типом наследования) [12]. Помимо прочего, общеизвестна способность цинка уменьшать количество повреждений генетического материала, ядерных структур и клетки в целом [13, 14].
Заключение
Цитогенетические обследования и статистический анализ результатов показали, что у лиц, проживающих на территории Приаралья, факторы среды, к которым относятся тяжелые металлы (Zn), могут оказывать неблагоприятное действие на здоровье. Проявились они в виде цитогенетических нарушений, а именно наблюдалось повышение уровня хромосомных аберраций хроматидного типа (1,047±0,119), кроме того, была выявлена регрессионная модель, показывающая изменения уровня хромосомных аберраций в зависимости от концентрации Zn. По всей видимости, при недостаточной концентрации цинка происходит снижение функциональной активности ферментов матричных процессов, что, в свою очередь, приводит к возрастанию вероятности увеличения частоты хромосомных аберраций.
Список литературы
- Сабиров Ж.Б. Пути возникновения структурных мутаций при химической природе мутагенеза / Ж.Б. Сабиров // Гигиена труда и медицинская экология. — 2015. — № 2(47). — С. 26–31.
- Sabirov Z.B. Evaluation of the cytogenetic status of the population living in the area before the environmental crisis / Z.B. Sabirov // Гигиена труда и медицинская экология. — 2016. — No. 4(53). — С. 70–78.
- Namazbaeva Z.I. The Assessment of Halogenating Stress in Population by the Environmental and Health Monitoring / Z.I. Namazbaeva, G.N. Dosybaeva, Z.B. Sabirov, L.T. Bazelyuk, G.K. Asanov, I.O. Baidaulet // International Journal of Environmental and Science Education. — 2016. — Vol. 11, No. 10. — P. 3884–3893.
- Harada T. Characterization of structural and catalytic differences in rat intestinal alkaline phosphatase isozymes / T. Harada, I. Koyama, T. Matsunaga, A. Kikuno, T. Kasahara, M. Hassimoto et al. // The FEBS journal. — 2005. — Vol. 272, No. 10. — P. 2477–2486.
- Story S.V. Characterization of novel zinc-containing, lysine-specific aminopeptidase from the hypertermophilic archaeon Pyrococcus furiosus / S.V. Story, C. Shah, F.E. Ir. Jenney, M.W. Adams // J. Bacteriol. — 2005. — Vol. 187, No. 6. — P. 2077– 2083.
- Gielen M. Metallotherapeutic drugs and metal-based diagnostic agents. The Use of Metals in Medicine / M. Gielen, E.R.T. Tiekink. — Weinheim: Wiley & Sons, 2005. — 598 р.
- Закон Республики Казахстан от 30 июня 1992 г. № 1468-XII. «О социальной защите граждан, пострадавших вследствие последствий экологического бедствия в Приаралье». [Электронный ресурс]. — Режим доступа: http://adilet.zan.kz/rus/docs/Z920002600.
- Руководство по оценке риска для здоровья населения при воздействии химических веществ, загрязняющих окружающую среду: Р 2.1.10.1920–04–2004. [Введен в действие от 2004–03–05]. — М.: Федеральный центр Госсанэпиднадзора Минздрава России, 2004. — 290 с.
- Hungerford D.A. Leukocytes cultured from small inocula od whole blood and the preparation of metafase chromosomes by treatment with hypotonic KCl / D.A. Hungerford // Stain Technology. — 1965. — Vol. 40, No. 6. — P. 333–338.
- Сабиров Ж.Б. Использование цитогенетического метода учёта хромосомных аберраций для исследования мутагенности в условиях неблагоприятной экологической обстановки: метод. реком. / Ж.Б. Сабиров, З.И. Намазбаева, Л.К. Ибраева, Н.М. Жанбасинова. — Караганда: Нац. центр гигиены труда и проф. заболеваний, 2016. — 34 с.
- Намазбаева З.И. Оценка цитогенетического статуса лиц, проживающих на территории промышленного города / З.И. Намазбаева, Ж.Б. Сабиров, А.М. Айткулов, К.Б. Бекишев, Г.К. Турлыбекова // Вестн. Караганд. ун-та. Сер. Биология. Медицина. География. — 2014. — № 3(75). — С. 100–103.
- Хлебникова А.Н. Цинк, его биологическая роль и применение в дерматологии / А.Н. Хлебникова, Д.Д. Петрунин // Вестн. дерматологии и венерологии. — 2013. — № 6. — С. 100–116.
- Record I.R. Protection by zinc against UVA and UVB-induced cellular and genomic damage in vivo and in vitro / I.R. Record, M. Jannes, I.E. Dreosti // Biol Trace Elem Res. — 1996. — No. 53. — P. 19–25.
- Richard M.J. Effect of zinc supplementation on resistance of cultured human skin fibroblasts toward oxidant stress / M.J. Richard, P. Guiraud, M.T. Leccia, J.C. Beani, A Favier // Biological trace element research. — 1993. — Vol. 37, No. 2–3. — P. 187.