Лекарственные средства пептидной природы обладают избирательным действием, оказывают фармакологический эффект при низких концентрациях в крови, к тому же считаются относительно безопасными для применения [1]. В настоящее время препараты пептидной природы приобретают все большее распространение на рынке, проводятся их клинические и доклинические исследования фармакокинетики, что в свою очередь требует создания соответствующих биоаналитических методик. При определении пептидов в биологических образцах требуется высокая чувствительность методики, так как данные вещества обычно активны в низких концентрациях. В свою очередь при работе с биологическими образцами, имеющими сложный состав, необходима высокая селективность аналитического метода. В связи с вышесказанным для определения пептидов часто используется метод ВЭЖХ-МС/МС.
Данное исследование посвящено решению проблем, возникающих при разработке методики количественного определения олигопептидов методом ВЭЖХ-МС/МС. Во-первых, большая молекулярная масса олигопептида (до 10 000 Да) не всегда позволяет определить однозарядные ионы исследуемого вещества, поскольку верхний предел сканирования отношений m/z составляет около 2000 для наиболее распространенных квадрупольных масс-анализаторов. Во-вторых, молекулы олигопептидов довольно часто обладают большим количеством кислотных и основных центров, что обеспечивает многообразие n-зарядных ионов при ионизации электрораспылением [2]. В-третьих, молекулярные ионы олигопептидов не всегда склонны к фрагментации при столкновении с атомами инертного газа (Collision-induced dissociation – CID) из-за эффективной делокализации заряда и устойчивых внутримолекулярных связей, что затрудняет использование высокоселективного режима детектирования путем мониторинга множественных реакций (multiple reaction monitoring, MRM) [3]. Также следует отметить гидрофильную природу многих олигопептидов, что осложняет выбор условий разделения методом обращенно-фазовой хроматографии. Целью данного исследования была демонстрация способов решения обозначенных проблем на примере тетрадекапептида(треонил-глутамил-лизил-лизил-аргинил-аргинил-глутамил- треонил-валил-глутамил аргинил-глутамил-лизил-глутамата).
Теоретически рассчитанная молекулярная масса исследуемого тетрпдекапепида составила 1818,02 Да. Получен масс-спектр нативного тетрадекапептида при ионизации электрораспылением. Наблюдается ряд n- протонированных квазимолекулярных ионов, значения m/z которых рассчитываются по формуле: m/z = (M + nH+) / n, что полностью согласуется с теоретически рассчитанными для исследуемого вещества (909,9, 607,0, 455,5, 364,6) (рис.1).
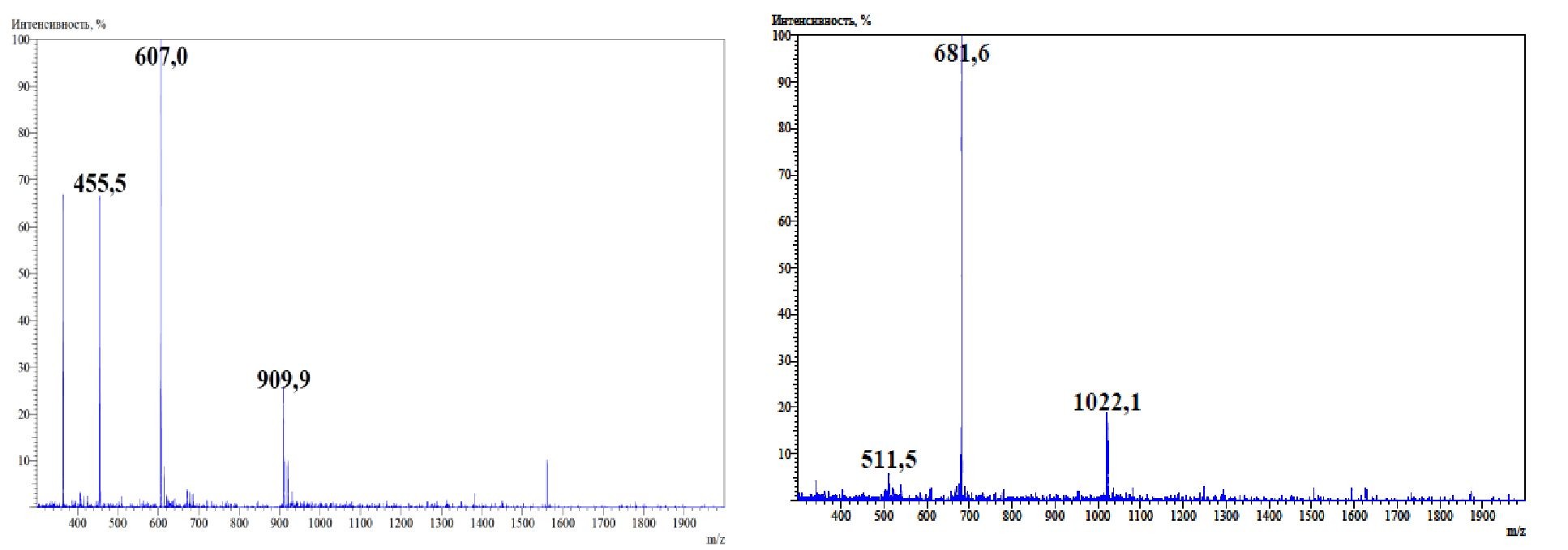
A
b
Рисунок 1. Масс-спектр нативного вещества (a) и пропионилированного производного(b) при положительной ионизации электрораспылением.
Вместе с тем, данные ионы практически не подвергаются фрагментации в ячейке соударений, что исключает работу в режиме MRM, поэтому было принято решение о проведении дериватизации исследуемой молекулы. В качестве дериватизирующих агентов были рассмотрены: дансилхлорид, тозилхлорид, фенилизотиоционат (ФИТЦ), пропионовый ангидрид [4]. Для всех производных были получены масс-спектры, согласующиеся с теоретическими расчетами.
Все производные в отличие от нативного пептида демонстрировали хорошее удерживание на колонке с сорбентом С18, поскольку в дериватизации участвуют аминогруппы, и продукты замещения обладают более высокой липофильностью. Однако, обнаружено, что дансилированные производные тетрадекапептида практически не подвергаются фрагментации, как и нативная форма. В случае тозилированных и ФИТЦ- производных удалось достигнуть незначительной фрагментации ионов, но при этом был затруднён контроль полноты протекания дериватизации в модельных образцах плазмы крови.
Лучшие результаты были получены при взаимодействии тетрадекапептида с пропионовым ангидридом. При этом для модельного образца плазмы крови удалось подобрать условия реакции, исключающие получение 3-замещённых производных в пользу 4-замещённых. В результате проведенной работы удалось достичь CID-фрагментации 4-пропионилированного производного тетрадекапептида, что позволило подобрать и оптимизировать условия детектирования в MRM-режиме.
Таким образом, изучены особенности хроматографического разделения и масс-спектрометрического детектирования тетрадекапептида, а также продуктов его взаимодействия с дансилхлоридом, тозилхлоридом, ФИТЦ-реагентом и пропионовым ангидридом. Установлено, что наиболее перспективна для разработки биоаналитической методики дериватизация тетрадекапептида пропионовым ангидридом.
- Бабина С.А. Желтышева А.Ю., Шуклин Г.О., Шуклина А.А., Япаров А.Э., «Лекарственные средства на основе пептидов: применение, технологии получения,» Международный студенческий научный вестник, № 3, pp. 21-21, 2019.
- Miladinović SM, Fornelli L, Lu Y, Piech KM, Girault HH, Tsybin YO, «In-spray supercharging of peptides and proteins in electrospray ionization mass spectrometry,» Analytical chemistry, № 84(11), pp. 4647-51, 2012.
- Ciccimaro E, Ranasinghe A, D’Arienzo C, Xu C, Onorato J, Drexler DM, Josephs JL, Poss M, Olah T., «Strategy to improve the quantitative LC-MS analysis of molecular ions resistant to gas-phase collision induced dissociation: application to disulfide-rich cyclic peptides,» Analytical chemistry, № 86(23), pp. 11523-7, 2014.
- Koller M, Eckert H., «Derivatization of peptides for their determination by chromatographic methods,» Analytica chimica acta, № 352(1-3), pp. 31-59, 1997.