АННОТАЦИЯ
Применение силденафила широко распространено, как во всем мире, так и на территории Российской Федерации. Однако, данный препарат, как и большинство других, способен вызвать различные нежелательные лекарственные реакции. Особенно это возможно при неконтролируемом врачом применении препарата при сопутствующих заболеваниях или при одновременном приеме других лекарственных препаратов. Избежать развития нежелательных лекарственных реакций возможно хорошо изучив фармакокинетику силденафила. В данной статье рассмотрено влияние применения других лекарственных средств на концентрацию силденафила.
На настоящем этапе развития фармакологии наблюдается выраженное стремление к выяснению биохимических, биофизических, клеточных и молекулярных изменений, наступающих в организме под влиянием данного лекарства. Особое значение приобретает также и выяснение потенциальных возможностей регулирования эффектов лекарства, используя свойства многих фармакологических веществ, вызывать те или иные изменения в организме. Особое значение имеют индукция и угнетение микросомныхэнзимов печени, вызывающих метаболизм лекарств. Обычно максимальный эффект фармакологических средств, стимулирующих свою собственную и других лекарственных веществ биотрансформацию, наступает после значительного латентного периода. Так например, на фоне действия энзимных индукторов (фенобарбитал, фенилбутазон, хлорциклизин и др.) наблюдается повышение энзимной активности через 24 часа, причем для достижения максимальной индуцирующей активности необходимо несколько дней (Burns и соавт.).
В качестве способа оценки метаболической активности был выбран метод фенотипирования. Фенотипирование - «прямой» метод определения активности того или иного фермента метаболизма ЛС по фармакокинетике его специфичного субстрата («маркерного» субстрата) и его метаболита. Активность того или иного фермента матеболизма определяется по фармакокинетике его специфического субстрата, называемого «маркерным» субстратом, путём измерения его концентрации и концентрации его метаболита в плазме крови или моче.
Методом фенотипирования было выбрано определение активности CYP 3A4 по отношению кортизол/6в-гидроксикортизол.
Кортизол (гидрокортизон, или 17-гидрокортикостерон), жизненно важный стероидный гормон, воздействующий на обмен веществ; секретируется наружным слоем (корой) надпочечников. Кортизол принимает участие в регуляции многих обменных (биохимических) процессов и играет ключевую роль в защитных реакциях организма на стресс и голод. При голодании, например, он обеспечивает поддержание нормального уровня глюкозы в крови, а при эмоциональном или операционном шоке препятствует падению кровяного давления ниже опасного уровня.
Благодаря тому, что в больших дозах кортизол оказывает противовоспалительное действие, этот гормон (или его синтетические производные - преднизон, преднизолон) широко используют для лечения ревматоидного артрита и других заболеваний, характеризующихся интенсивным воспалительным процессом. Кроме того, его применяют при аллергии, бронхиальной астме и аутоиммунных заболеваниях. Медики предпочитают синтетические производные кортизола, которые не вызывают повышения кровяного давления и задержки воды и солей в организме.
Все стероидные гормоны имеют в своей основе одинаковую структуру, состоящую из 17 атомов углерода, объединенных в четыре кольца, которые обозначаются буквами A, B, C и D. К кольцам в качестве боковых цепей присоединены дополнительные атомы углерода.
Все стероидные гормоны являются производными холестерина - стероидного соединения, содержащего 27 атомов углерода. В коре надпочечников происходит химическая модификация холестерина: удаляется боковая цепь, добавляются гидроксильные группы (ОН-группы) и образуются двойные связи (пары электронов, поделенные между двумя соседними атомами углерода). В молекуле кортизола гидроксильные группы находятся в положениях 17, 21 и 11, а двойная связь - между атомами 4 и 5 кольца А.
Кортизол метаболизируется в печени при участии цитохрома P450. Схема метаболизма указана на рисунке.
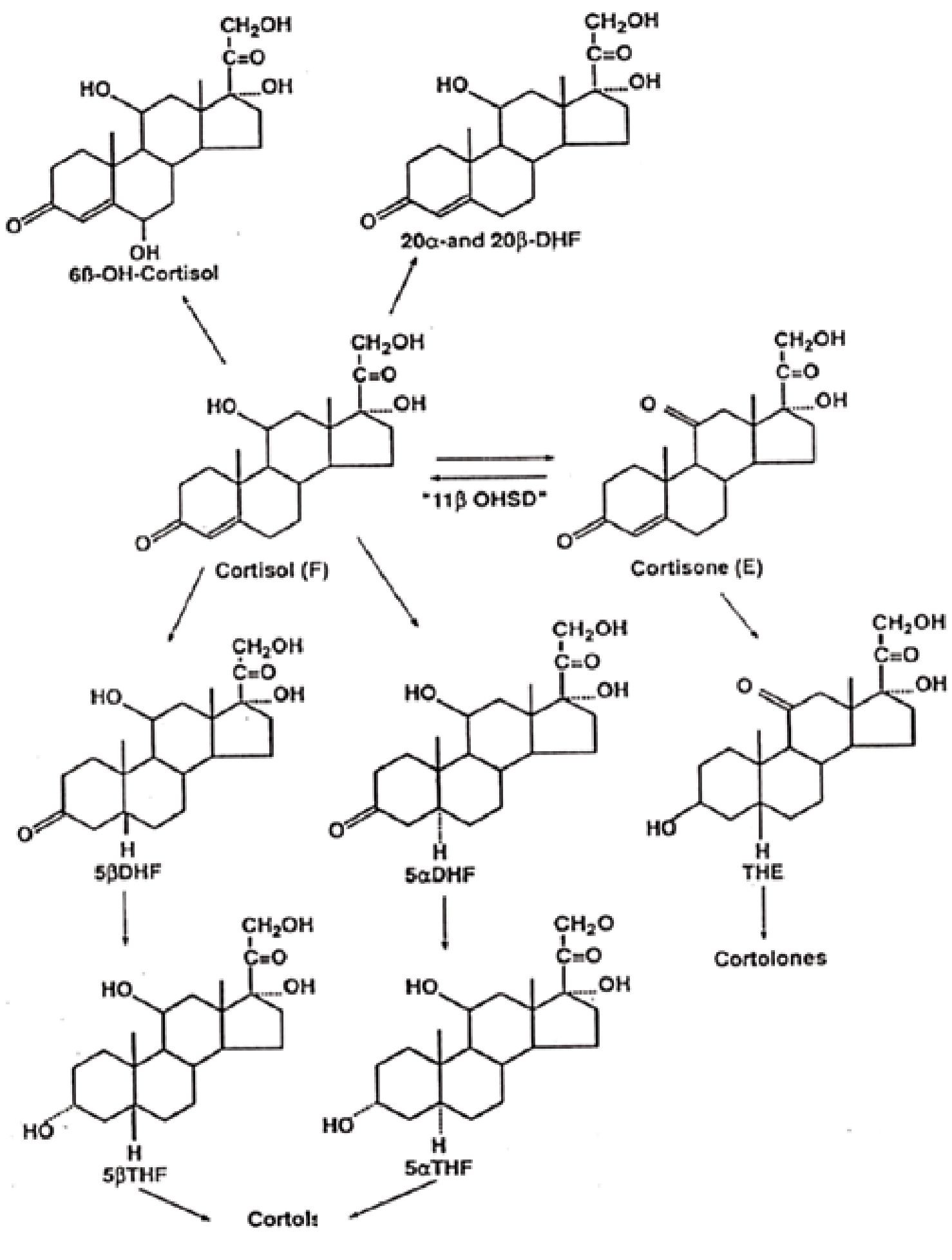
Оценка активности CYP3A4 может определяться по отношению концентрации 6-в- гидроксикортизола к концентрации кортизола (6-в-гидроксикортизол/кортизол) в утренней моче т.к. 6-в-гидроксикортизол образуется из кортизола исключительно под действием CYP3A4. На анализ берется именно утренняя моча, так как уровень кортизола самый высокий именно в утренние часы. Моча во время утреннего туалета собирается в отдельную емкость, затем из нее перемещается в пластмассовую пробирку, допускается замораживание мочи.
Также преимуществом теста является возможность сбора материала (мочи) в домашних условиях. Концентрации 6- в—гидроксикортизола и кортизола в моче определяется методом хромато-масс-спектрометрического анализа на высокоэффективном жидкостном хроматографе, что является главным недостатком теста т.к. делает его дорогим. Низкие значения отношения 6-в- гидроксикортизол/кортизол соответствует низкой активности CYP3A4, а высокие значения отношения 6-в-гидроксикортизол/кортизол- высокой активности CYP3A4.
Параллельно проводилось определение концентрации силденафила в плазме крови пациентов. Полученные результаты приведены в таблице.
|
Концентрациясилденафила (нг/мл) |
Метаболическое отношение |
|||
|
Контрольная группа |
1 |
613,6 |
1 |
5,01 |
|
2 |
574,45 |
2 |
5,53 |
|
|
3 |
636,3 |
3 |
4,39 |
|
|
4 |
635,85 |
4 |
5,71 |
|
|
5 |
560,08 |
5 |
4,32 |
|
|
6 |
602,74 |
6 |
5,18 |
|
|
7 |
612,46 |
7 |
5,48 |
|
|
I (фенобарбитал) |
1 |
589,45 |
1 |
9,61 |
|
2 |
444,83 |
2 |
10,63 |
|
|
3 |
481,48 |
3 |
5,37 |
|
|
4 |
464,41 |
4 |
16,21 |
|
|
5 |
541,79 |
5 |
5,26 |
|
|
6 |
524,25 |
6 |
7,59 |
|
|
II (ранитидин) |
1 |
650,26 |
1 |
3,86 |
|
2 |
645,13 |
2 |
1,79 |
|
|
3 |
769,59 |
3 |
2,17 |
|
|
4 |
650,27 |
4 |
3,37 |
|
|
5 |
682,63 |
5 |
4,01 |
|
|
6 |
728,45 |
6 |
3,72 |
|
Средние значения:
|
Концентрация силденафила (нг/мл) |
Метаболическое отношение |
|
|
Контрольная группа |
605,0686 |
5,088571 |
|
I (Фенобарбитал) |
507,7017 |
9,111667 |
|
II (Ранитидин) |
687,7217 |
3,153333 |
СПИСОК ЛИТЕРАТУРЫ
- N Mehrotra, M Gupta, A Kovar, et al. Phosphodiesterase-5 Inhibitor Therapy: The PK and PD of PDE5 Inhibitors. Int J Impot Res. 2007;19(3):253-264.
- Hatzimouratidis K, Hatzichristou DG. A comparative review of the options for treatment of erectile dysfunction: which treatment for which patient? Drugs 2005; 65: 1621-1650.
- Gresser U, Gleiter CH. Erectile dysfunction: comparison of efficacy and side effects of the PDE-5 inhibitors sildenafil, vardenafil and tadalafil - review of the literature. Eur J Med Res 2002; 7: 435-446.
- Eardley I, Cartledge J. Tadalafil (Cialis) for men with erectile dysfunction. Int J Clin Pract 2002; 56: 300-304.
- Nichols DJ, Muirhead GJ, Harness JA. Pharmacokinetics of sildenafil after single oral doses in healthy male subjects: absolute bioavailability, food effects and dose proportionality. Br J Clin Pharmacol 2002; 53(Suppl 1): 5S-12S.
- Walker DK, Ackland MJ, James GC, et al. Pharmacokinetics and metabolism of sildenafil in mouse, rat, rabbit, dog and man. Xenobiotica 1999; 29: 297-310.
- Kwang-Hee Shin, Yong-ju Chung, Bo-Hyung Kim et al. Effect of ketoconazole on the pharmacokinetics of udenafil in healthy Korean subjects. Br J Clin Pharmacol. 2010 March; 69(3): 307310.
- В. В. Рафальский ПОДХОДЫ К РАЦИОНАЛЬНОМУ ВЫБОРУ ИНГИБИТОРОВ ФОСФОДИЭСТЕРАЗЫ 5 ТИПА ФАРМАТЕКА »» № 19/20 - 2004