АННОТАЦИЯ
Целью данной работы являлась разработка и валидация методики количественного определения активного метаболита флударабина 2-фтор-ара-А в плазме крови. Количественное определение проводили методом высокоэффективной жидкостной хроматографии (ВЭЖХ) с масс- селективным детектированием. Разработанная методика была валидирована по следующим валидационным характеристикам: селективность, линейность, правильность, прецизионность, предел количественного определения, перенос пробы, стабильность растворов. Аналитический диапазон методики составил 0,5 нг/мл - 500 нг/мл в плазме крови. Полученный аналитический диапазон позволяет применять разработанную методику для исследований фармакокинетики препаратов флударабина.
Ключевые слова: флударабин, 2-фтор-ара-А, биоаналитическая методика, ВЭЖХ, валидация.
Введение
Согласно литературным данным для количественного определения флударабина и 2-фтор- ара-А в плазме крови применяются методы ВЭЖХ с масс-селективным [1], флуориметрическим детектированием [2] и УФ спектрофотометрическим детектированием [3]. Приведенные в литературе аналитические диапазоны данных методов позволяют считать их пригодными для фармакокинетических исследований препаратов флударабина. В качестве пробоподготовки применяют метод твердофазной экстракции [1], твердофазной экстракции с последующей дериватизацией [2] и осаждение белков [3].
В разработанной методике использовался метод ВЭЖХ с масс-селективным детектированием, а в качестве метода пробоподготовки-жидкость-жидкостная экстракция.
Данная работа была проведена с целью разработки чувствительной, селективной и удобной в выполнении методики количественного определения 2-фтор-ара-А в плазме крови.
Материалы и методы
Пробоподготовку проводили методом жидкость-жидкостной экстракции.
Количественное определение проводили на высокоэффективном жидкостном хроматографе Agilent 1200 с масс-спектрометрическим детектором MS 6120, AgilentTechnologies, США.
Подвижная фаза - ацетонитрил : вода очищенная (10:90), предварительно дегазированная.
Неподвижная фаза - хроматографическая колонка AgilentEclipce XDB-C18 4.6x150 мм; 1,8 мкм, при температуре 30 0С.
Объем вводимой пробы составил 10 мкл. Время хроматографирования -3 минуты.
Условия детектирования были следующими: тип ионизации - ES - APCI (электроспрей при атмосферном давлении, негативная полярность); режим сканирования: MSD1 - SIM режим по ионам с m/z 285,23, 286,23.
Валидация методики
Валидацию биоаналитической методики проводили на основе Руководства по экспертизе лекарственных средств Том I ФГБУ «НЦЭСМП» МЗ РФ, 2013, а также Руководств FDA (Guidance for Industry: Bioanalytical method validation (draft). U.S. Department of Health and Human Services, Food and Drug Administration, Center for Drug Evolution and Research (CDER). U.S. Government Printing Office: Washington, DC, 2013) и EMA (Guideline on validation of bioanalytical methods (draft).European Medicines Agency. Committee for medicinal products for human use: London, 2014) по следующим характеристикам:
селективность; линейность;правильность (на уровнях inter-run, intra-run, inter-run, intrarun); прецизионность (на уровнях inter-run, intra-run, inter-run, intra-run);предел количественного определения;
перенос пробы; стабильность растворов.
Селективность
Проводили анализ 7 образцов чистой плазмы, образцов чистой плазмы с прибавлением стандартного раствора 2-фтор-ара-А до достижения диапазона концентраций 0,5 нг/мл - 500 нг/мл. На хроматограммах образцов чистой плазмы не наблюдалось пиков со временем удерживания, соответствующим времени удерживания 2-фтор-ара-А.
Линейность
Проводили анализ 7 образцов чистой плазмы с прибавлением стандартного раствора 2- фтор-ара-А до получения концентраций: 0,5 нг/мл; 2,5 нг/мл; 5 нг/мл; 10 нг/мл; 25 нг/мл; 50 нг/мл, 100 нг/мл, 500 нг/мл. По полученным значениям был построен калибровочный график (r2=0,997). Полученный коэффициент корреляции соответствует нормам (не менее 0,99).
Правильность и прецизионность
Проводили анализ 4 образцов чистой плазмы с прибавлением стандартного раствора 2- фтор-ара-А до получения концентраций: 0,5 нг/мл, 10 нг/мл, 100 нг/мл 500 нг/мл. Каждый раствор хроматографировали 5 раз. Исследование проводили в течение 1-ойпоследовательности (intra-day) и 2-ойпоследовательности (inter-day). Для полученных значений концентраций были рассчитаны величины относительного стандартного отклонения (RSD, %) и относительной погрешности (е, %).Полученные величины относительного стандартного отклонения (прецизионность) и относительной погрешности (правильность) соответствуют нормам (не более 20 % для нижнего диапазона линейности, не более 15 % - для остальных точек).
Предел количественного определения
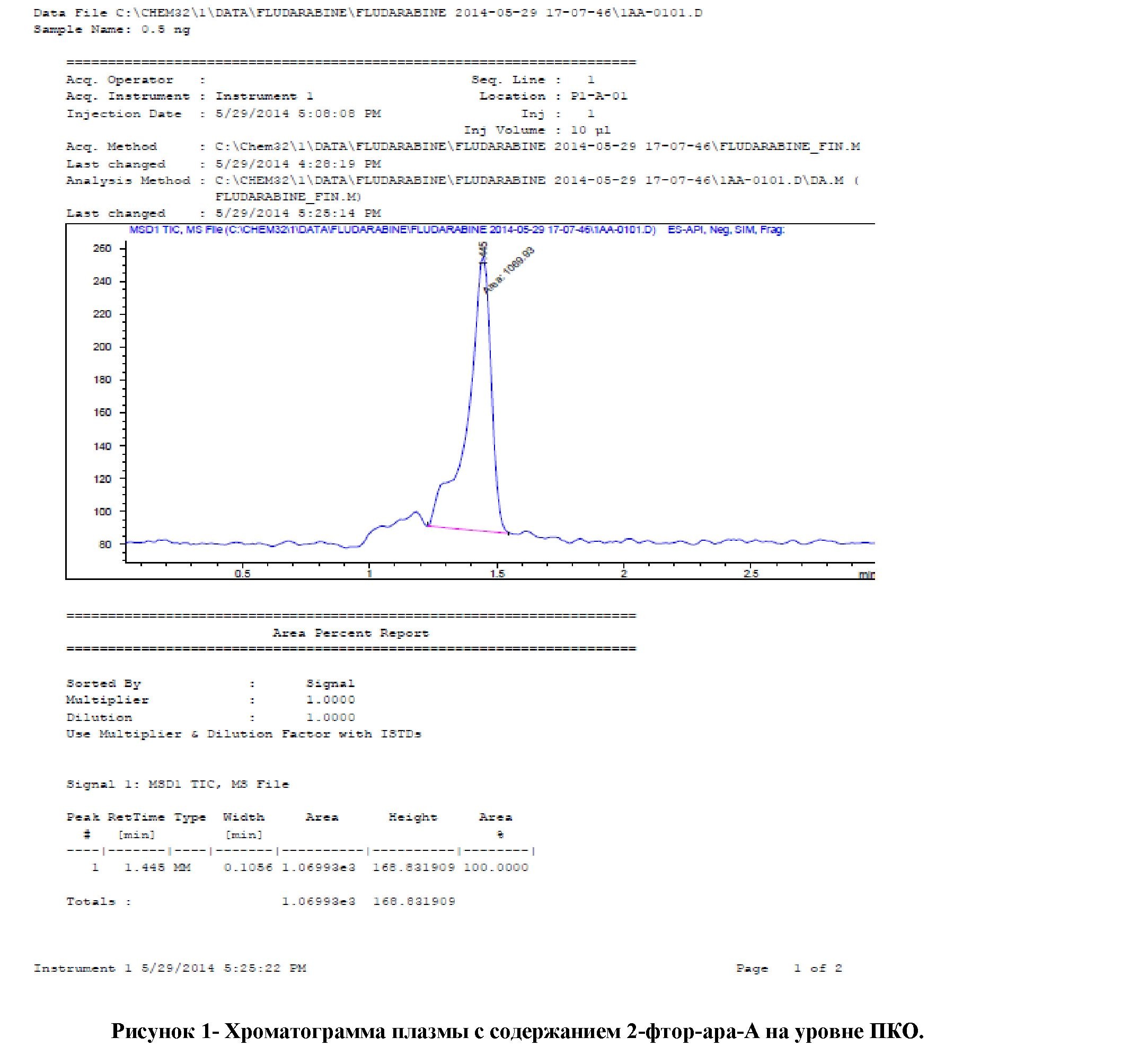
Предел количественного определения (ПКО) методики определяли на основании данных линейности, правильности и прецизионности. За ПКО методики принималась минимальная концентрация 2-фтор-ара-А в плазме, для которой возможно определение 2-фтор-ара-А со значениями RSD и е не более 20 % в диапазоне линейной зависимости. Предел количественного определения методики составил 0,5 нг/мл. Хроматограмма, демонстрирующая ПКО методики, приведена на Рисунке 1.
Стабильность
Стабильность была подтверждена для стандартных растворов 2-фтор-ара-А (при хранении раствора в течение 14 дней при температуре от 2 до 8 0С), кратковременная стабильность (для приготовленных проб в течение 24 и 48 ч при анализе на следующий день при температуре 150С), на уровне концентрации 500 нг/мл. Образцы выдерживали 3 цикла заморозки-разморозки. Площадь пика при повторных анализах не менялась более чем на 10 %.
Для исследования долговременной стабильности образцы плазмы на уровне концентрации 500 нг/мл были помещены в морозильник при температуре от - 45 до - 50 0С для последующего анализа спустя 1 месяц после заморозки. Площадь пика при повторных анализах не менялась более чем на 10 %.
Перенос пробы
При последовательном вводе пробы с концентрацией 2-фтор-ара-А 500 нг/мл и пробы чистой плазмы на хроматограмме чистой плазмы отсутствовали пики, соответствующие пику 2- фтор-ара-А. Перенос пробы отсутствовал.
Результаты и обсуждение
Разработанная методика количественного определения активного метаболита флударабина - 2-фтор-ара-А в плазме крови является достаточно чувствительной и селективной согласно своим валидационным характеристикам. Аналитический диапазон методики составил 0,5 нг/мл - 500 нг/мл. Полученный аналитический диапазон позволяет применять разработанную методику для исследований фармакокинетики флударабина. Предел количественного определения методики составил 0,5 нг/мл. По валидационным характеристикам данная методика не уступает методам количественного определения 2-фтор-ара-А, описанным в литературе. Также она является удобной в выполнении и менее затратной.
Выводы
Разработанная биоаналитическая методика количественного определения активного метаболита флударабина - 2-фтор-ара-А в плазме крови может быть использована для изучения фармакокинетических параметров при проведении исследований фармакокинетики и биоэквивалентности препаратов флударабина.
СПИСОК ЛИТЕРАТУРЫ
- Ella S.M. Ng, S. Bill Kangarloo, Andrew Daly. Improved quantitative method for fludarabine in human plasma by liquid chromatography and tandem mass spectrometry. Journal of Chromatography B, Volume 931, 2013, Pages 103-110.
- Kemena, M. Fernandez, J. Bauman, M. Keating, W. Plunkett. A sensitive fluorescence assay for quantitation of fludarabine and metabolites in biological fluids. ClinicaChimicaActa, Volume 200, Issues 2-3, 1991, Pages 95-106.
- T. Yamauchi, T. Ueda. Simple and sensitive method for quantification of fludarabine triphosphate intracellular concentration in leukemic cells using isocratic liquid chromatography. Journal of Chromatography B, Volume 799, Issue 1, 2004, Pages 81-86.