АННОТАЦИЯ
Исследован суммарное с ионами Са2+ влияние лагохилина и его некоторых производных на скорость свертывания плазмы крови. Установлено, что суммарное с ионами Са2+ влияние исследованных препаратов на свертывающую способность плазмы крови модулировано не связыванием их со стабилизаторами крови или с высвобождением ионов Са2+ плазмы, а их структурными особенностями. На основании проведенных in vitro опытов показано, что действие изученных дитерпеноидов на плазменный гемостаз реализуется в данном случае только в присутствии ионов Са2+. Установлена взаимосвязь гемостатической активности изученных дитерпеноидов от их химической структуры.
Ключевые слова: дитерпеноиды, лагохилин и его производные, система свертывания крови, гемостатическая активность, плазма крови, ионы Ca2+.
Цель исследования. Экстрактивными веществами некоторых видов растений рода Lagochilus (семейство Губоцветные - Labiatae Juss) являются дитерпеноиды - лагохилин и его другие природные производные. Несмотря на то, что для лагохилина и его некоторых производных проведены изучения фармакологических и физиологических свойств [1], на сегодняшний день остаются неизвестными многие этапы молекулярных механизмов их действия
на систему свертывания крови. Ранее нами была изучена Са2+-ионофорная активность данных соединений и установлено, что их модулирующее действие на свертывающую систему может быть связано присутствием ионов Ca2+ [2]. В связи с этим, целью настоящей работы было исследование влияния лагохилина и его некоторых производных на скорость свертывания плазмы крови в присутствии ионов Ca2+, а также без участия этих ионов.
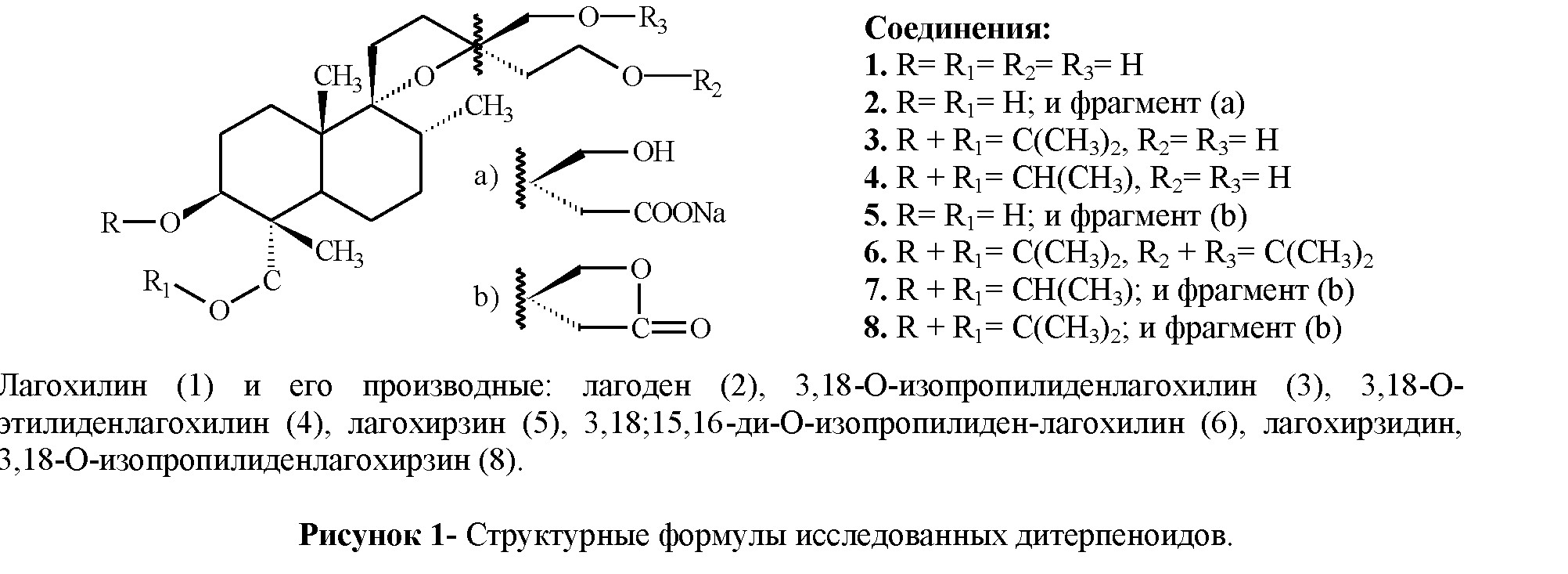
Материалы и методы. В работе были изучены дитерпеноиды, химические структуры которых показаны на рисунке 1.
Опыты проводили при температуре 37оС на водяной бане. Кровь брали из ушной концевой вены кроликов. К 9 частям крови добавляли 1 часть 1,3% раствора щавелевокислого (оксалата) натрия или 3,8% раствора лимоннокислого (цитрата) натрия, в качестве стабилизаторов крови. Полученные смеси центрифугировали в течение 15-20 минут при 1500 об./мин. Плазму отсасывали и разливали по 0,1 мл в пробирки, в таком же объеме добавляли: 0,277% раствор CaCl2 (контроль-1), 25% водный спирт (контроль-2) и 1% растворы исследуемых препаратов. Скорость свертывания плазмы регистрировали сразу после добавления веществ. Образование и качество сгустка оценивали визуально [3].
Результаты и обсуждение. Протромбин является одним из ключевых факторов свертывания крови и состоит из двух веществ: протромбина А и протромбина В, связанных между собой ионами Ca2+. В неизмененной плазме протромбин сохраняется долго, а при добавлении оксалата или цитрата к крови ионы Ca2+ осаждаются, протромбин распадается на вещества А и В, и тромбин не образуется [4].
Таблица 1 - Изменение времени свертывания оксалатной и цитратной плазмы под действием лагохилина и его производных в присутствии раствора CaCl2.
M - Средняя арифметическая величина вариационного ряда, в секундах; m - средняя ошибка
средней арифметической величины; n - число наблюдений; P - коэффициент достоверности
полученных результатов или доверительный интервал средней арифметической величины.
|
Испытуемые соединения |
Оксалатная плазма |
Цитратная плазма |
||
|
M±m (n=9) |
P |
M±m (n=9) |
P |
|
|
Контроль-1 |
121,6±11,0 |
- |
107,0±9,8 |
- |
|
Контроль-2 |
118,2±11,2 |
>0,05 |
101,2±10,3 |
>0,05 |
|
Соединение 1 |
52,6±4,2 |
<0,001 |
50,2±4,5 |
<0,001 |
|
Соединение 2 |
50,2±6,2 |
<0,001 |
45,6±4,5 |
<0,001 |
|
Соединение 3 |
63,3±6,6 |
<0,001 |
62,3±6,3 |
<0,001 |
|
Соединение 4 |
77,8±7,2 |
<0,01 |
71,0±6,5 |
<0,01 |
|
Соединение 5 |
86,4±8,4 |
<0,05 |
73,1±6,7 |
<0,01 |
|
Соединение 6 |
89,6±8,7 |
<0,05 |
75,9±6,9 |
<0,01 |
|
Соединение 7 |
95,2±8,9 |
>0,05 |
84,2±7,2 |
>0,05 |
|
Соединение 8 |
99,2±9,0 |
>0,05 |
88,4±7,4 |
>0,05 |
83
Результаты наших опытов показали, что под действием испытуемых препаратов в отсутствии ионов Ca2+ не наблюдается свертывание оксалатной плазмы. Но, в присутствии экзогенного Са2+ все исследуемые образцы в той или иной мере влияют на скорость свертывания оксалатной плазмы. Так, при добавлении только CaCl2 время свертывания плазмы составляет 121,6±11,0 секунд. Добавление лагохилина и лагодена совместно с CaCl2 укорачивало время свертывания плазмы что почти в 2,4 раза меньше, чем в контроле. Под действием остальных дитерпеноидов в сходных условиях также наблюдали уменьшение скорости свертывания плазмы в среднем в 1,5 раза меньше, чем в контроле. Хотя производные лагохилина в этих опытах показали низкую по сравнению с лагохилином и лагоденом гемостатическую активность, во всех случаях в присутствии ионов Са2+ мы наблюдали уменьшение времени свертывания оксалатной плазмы.
Предполагая, что в проявлении суммарного эффекта с ионами Са2+ лагохилин и его производные могут связываться с молекулами щавелевокислого натрия, тем самым высвобождая ионы Ca2+ плазмы, мы использовали другой стабилизатор крови - лимоннокислый натрий, и получили аналогичные результаты (см. таблицу 1). Следовательно, действие исследуемых препаратов модулировано не связыванием их со стабилизаторами или с высвобождением ионов Са2+ плазмы, а структурными особенностями лагохилина и его производных, которые оказывали влияние на суммарную с ионами Са2+ коагулирующую способность плазмы.
Различная степень влияния на скорость свертывания плазмы может быть связана со структурными особенностями исследуемых препаратов. Так, в молекулах лагохилина и лагодена в свободном состоянии находятся четыре кислородосодержащих функциональные группы, наличие которых возможно приводит к наибольшему коагулирующему эффекту. Замена гидроксильных групп изопропилиденовой и этилиденовой группой в положениях С3 и С18 в молекулах 3,18-O- изопропилиденлагохилина и 3,18-О-этилиденлагохилина, стала причиной понижения их гемостатической активности. Преобразование гидроксильных групп в положениях С15 и С16 в лактонную структуру в молекуле лагохирзина также дает низкий по сравнению с лагохилином и лагоденом коагулирующий эффект. Наконец, блокировка всех гидроксилов двумя изопропилиденовыми группами в положениях С3 и C18, С15 и С16 в молекуле 3,18;15,16-ди-О- изопропилиденлагохилина, как и ожидалось, сильно повлияла на гемостатическое действие этого вещества, ослабляя его активность.
Вывод. На основании проведенных in vitro опытов можно сделать вывод, что действие исследуемых дитерпеноидов на скорость свертывания плазмы крови реализуется в данном случае только в присутствии ионов Са2+. Также, установлена взаимосвязь гемостатической активности лагохилина и его некоторых производных от их химической структуры.
ЛИТЕРАТУРА
- Зайнутдинов У.Н., Исламов Р., Далимов Д.Н., Абдурахманов Т.Р., Матчанов О.Д., Выпова Н.Л. /Гемостатическая активность дитерпеноидов группы лагохилина ее связь со структурой. //Химия природных соединений, 2002. 3: 135-136.
- Косымбетов П.Г., Зиятдинова Р.Х., Бессонова С.В., Салахутдинов Б.А., Зиямов Дж., Зайнутдинов У.Н., Арипов Т.Ф. /Ионофорные и комплексообразующие свойства производных лагохилина. //Химия природных соединений, 2004. 3: 199-204.
- Шиффман Ф. Дж. Патофизиология крови. Перевод с английского - Москва - Санкт- Петербург: «Издательство БИНОМ» - «Невский Диалект», 2000.
- Исследование системы крови в клинической практике. Под ред. Г. И. Козинца и В. А. Макарова. - Москва: Триада-Х, 1997.