АННОТАЦИЯ
Установлено, что оптимальной дозой адреналина гидрохлорида для получения результативной и информативной биомодели катехоламинового повреждения миокарда у кроликов в условиях низкогорья (г. Бишкек, 760 м над ур. моря) является доза 0,025мг/кг массы тела животного.
Ключевые слова: экспериментальный некроз миокарда, адреналина гидрохлорид, высокогорье.
Исторически сложилось так, что в решении многих проблем, возникших перед человечеством в области биологии и медицины, решающую роль играют экспериментальные исследования на животных. Адекватно воспроизведенная модель необходимого патологического состояния позволяет изучить динамику патологического процесса, метаболические сдвиги в организме, вызванные данной патологией, и наконец, изучить конкретные особенности фармакодинамики и фармакокинетики лекарственных средств, применяемых при данной модели патологического состояния.
Понятие «животные модели» вошло в научную терминологию исследователей в 30-х годах ХХ столетия, когда Boldessarins R.J. и Fisher J.E. дали определение модели как «экспериментального компромисса, где простая экспериментальная система используется для понимания гораздо более сложной» [1].
Экспериментальная биомодель - создаваемая модель того или иного состояния, в том числе патологического, характерного или частично воспроизводящего функционирование прототипа (человека или другого животного) с помощью физических, химических или биологических факторов. Подобные модели и в настоящее время остаются незаменимыми для расшифровки механизмов развития патологических процессов и оценке эффективности применения лекарственных средств.
Вопросы метаболизма миокарда и его нарушений настолько актуальны, что вызывали и вызывают повышенный интерес исследователей во всем мире. В механизме патогенетических изменений, возникающих в поврежденной сердечной мышце и ведущих к угнетению функциональной активности миокарда, ключевая роль отводится нарушениям углеводного и липидного обменов, последовательно вызывающих в сердце появление ишемических и некротических очагов [2,3,4]. Индуцированные различными повреждающими факторами, очаги некроза значительно изменяют функциональное состояние миокарда.
Экспериментальные и клинические наблюдения [5] позволили выявить ряд нейрогуморальных механизмов, нарушение которых может приводить к возникновению некротических поражений сердечной мышцы. Основными положениями этой теории являются следующие. При эмоциональном возбуждении (а также и при некоторых других состояниях) в кровь выделяется большое количество катехоламинов. Сердечная мышца обладает способностью активно адсорбировать катехоламины из циркулирующей крови. Вследствие этого они начинают накапливаться в миокарде. Если в малых концентрациях катехоламины стимулируют энергетический обмен, оказывают положительное инотропное влияние на сердечную мышцу, то есть являются необходимыми ингредиентами для нормального функционирования миокарда, то при их больших концентрациях начинает превалировать гистотоксический эффект. Происходит исчезновение запасов гликогена из сердечной мышцы; распад макроэргических фосфорных соединений начинает преобладать над их синтезом. Кроме того, катехоламины резко повышают потребность миокарда в кислороде и, несмотря на расширение венечных сосудов, доставка кислорода с кровью начинает отставать от потребности в нем кардиальных структур. При прохождении крови по венечным артериям весь кислород утилизируется раньше, чем кровь достигнет мельчайших разветвлений коронарных сосудов. Вследствие этого участки миокарда, снабжаемые кровью через концевые капилляры, не получают кислорода; в них возникает гипоксия, и развиваются некрозы.
Несмотря на то, что работы по воспроизведению некрозов миокарда разными методами в эксперименте на животных приобрели широкое распространение, при изучении функции миокарда и его нарушений выбор экспериментальной модели кардионекроза является достаточно сложным. Широкое распространение приобрели работы по воспроизведению морфологически сходных по характеру и локализации индуцированных микронекрозов в эксперименте и некрозов, возникающих в миокарде человека.
Известно, что при введении катехоламинов экспериментальным животным развиваются некротические изменния в миокарде, размер которых находится в прямой зависимости от дозы и продолжительности действия фармакологического агента, что четко воспроизводится в эксперименте. Для моделирования катехоламинового некроза в качестве повреждающиего агента чаще всего используются адреналин и изопреналин (изадрин).
Модель катехоламинового («метаболического») инфаркта миокарда воспроизводится путем однократной или двукратной (через 24 часа) инъекции 0,1% раствора адреналина гидрохлорида внутривенно или подкожно из расчета 0,05мг/кг, 1 мг/кг или 2мг/кг массы тела животного [6,7,8,9].
Надо отметить, что в работах исследователей начала ХХ века повреждения миокарда после введения адреналина изучались в поздние сроки опытов, что затрудняло выявление адреналинового повреждения и его динамику в мышечных клетках. Поэтому основное внимание уделялось реактивным изменениям и весь процесс в целом получил наименование адреналинового миокардита. Прогресс биохимии позволил по-новому осмыслить возникающие изменения в миокарде, эти знания и легли в основу выдвинутого понятия —метаболические” нарушения миокарда, хотя вопрос о происхождении таких расстройств до сих пор окончательно не решен [10, 11,12].
Повреждающий эффект катехоламинов был известен еще в начале ХХ столетия [13,14], и в настоящее время качестве экспериментальной биологической модели «метаболического» инфаркта миокарда чаще других используется адреналиновая модель, основанная на кардиотоксическом эффекте экзогенно вводимого адреналина [6,7,15, 16, 17].
Ишемия миокарда приводит не только к изменениям сердечно-сосудистой системы и обмена веществ, но и к изменению гомеостаза электролитов, нейрогормонов и ультраструктуры миокарда. Эти изменения являются обратимыми и их можно увидеть в течение первых нескольких минут ишемии. Однако когда ишемия сохраняется, происходит постепенный переход от обратимых изменений к необратимым, и развивается инфаркт миокарда. Различие между ишемией и инфарктом миокарда, таким образом, заключается в обратимости изменений.
Существует определенная проблема и при выборе экспериментального животного, которое будет служить в качестве биомодели. У человека, ишемия миокарда чаще всего носит региональный характер, и это состояние широко изучается у интактных животных. В исследованиях in vivo собака считается традиционно наиболее часто используемым видом животных. Для изучения региональной ишемии миокарда были также использованы кролики и крысы [18], но применение аппаратуры для измерения регионального обмена веществ и функции миокарда в этом случае более ограничены из-за малых размеров сердца и коронарных сосудов.
Как показал анализ существующей литературы, выбор подопытных животных в данном случае определяющего значения, по-видимому, не имеет, т.к. положительные результаты были получены в каждом из исследованных видов, в которых инфаркт миокарда был выбран в качестве конечной точки. Эти виды в настоящее время включают собак [19], свиней [20], овец, кроликов [21], крыс [22], сурков и хорьков [23]. Однако следует признать, что большинство исследований такого рода были выполнены на крысах.
Ранний ответ на ишемию зависит в большой степени от наличия коллатерального кровообращения [24]. Было установлено, что коллатеральное кровообращение у крыс недостаточно развито, в то время как у кроликов имеются внутривидовые различия. Так, например, морские свинки имеют настолько разветвленную сеть коллатералей, что после окклюзии коронарной артерии инфаркт не развивается [25, 26].
Таким образом, обобщая вышеизложенное можно заключить, что повреждения миокарда достаточно высокими дозами адреномиметических средств является широко применяемой экспериментальной биомоделью, при воспроизведении которой в миокарде животных образуются многочисленные диффузные микронекрозы с воспалительной реакцией вокруг них. Катехоламиновые некрозы миокарда - одна из широко применяемых биомоделей для изучения кардиопротекторных свойств лекарственных средств.
Однако, в доступной нам литературе мы не нашли работ выполненных в условиях высокогорья, где исследовались некротические изменения при адреналиновом поражении миокарда у кроликов, эксперименты подобного рода проводились исследователями в основном на лабораторных крысах и собаках. В связи с этим целью настоящего исследования явилось изучение морфологических изменений миокарда у экспериментальных кроликов при моделировании катехоламинового кардионекроза в условиях низкогорья в зависимости от дозы введенного экзогенного адреналина.
Материалы и методы исследований. В эксперименте были использованы 18 кроликов породы «шиншилла» обоего пола с массой тела 2,5-3,0 кг. 6 кроликов составляли контрольную группу животных. Катехоламиновый кардионекроз провоцировали однократным внутривенным введением адреналина гидрохлорида в дозах 0,025 мг/кг (2-я группа, 6 кроликов) и 0,05 мг/кг (3-я группа, 6 кроликов) массы тела. Для анализа результативности и информативности воспроизведения биомодели адреналинового повреждения миокарда использовали макроскопические, гистологические и морфометрические методы исследования. Для выявления площади кардионекроза и контрактурных повреждений парафиновые срезы окрашивали гематоксилин-эозином по Эрлиху, исследование проводилось методом точечного счета с помощью окулярной морфометрической сетки [27,28]. Степень поражения выражалась в процентах по отношению площади повреждения кардиомиоцитов к общей площади среза. Отдельно определяли площадь поражения субэндокардиального, интрамурального и субэндокардиального отделов левого и правого желудочков сердца.
Результаты исследований. Как показали наши исследования, после введения адреналина гидрохлорида в дозе 0,025 мг/кг массы тела у кроликов наблюдались малоподвижность, вялость, животные не принимали пищу, у них появлялась выраженная одышка, поза «лежания пластом».
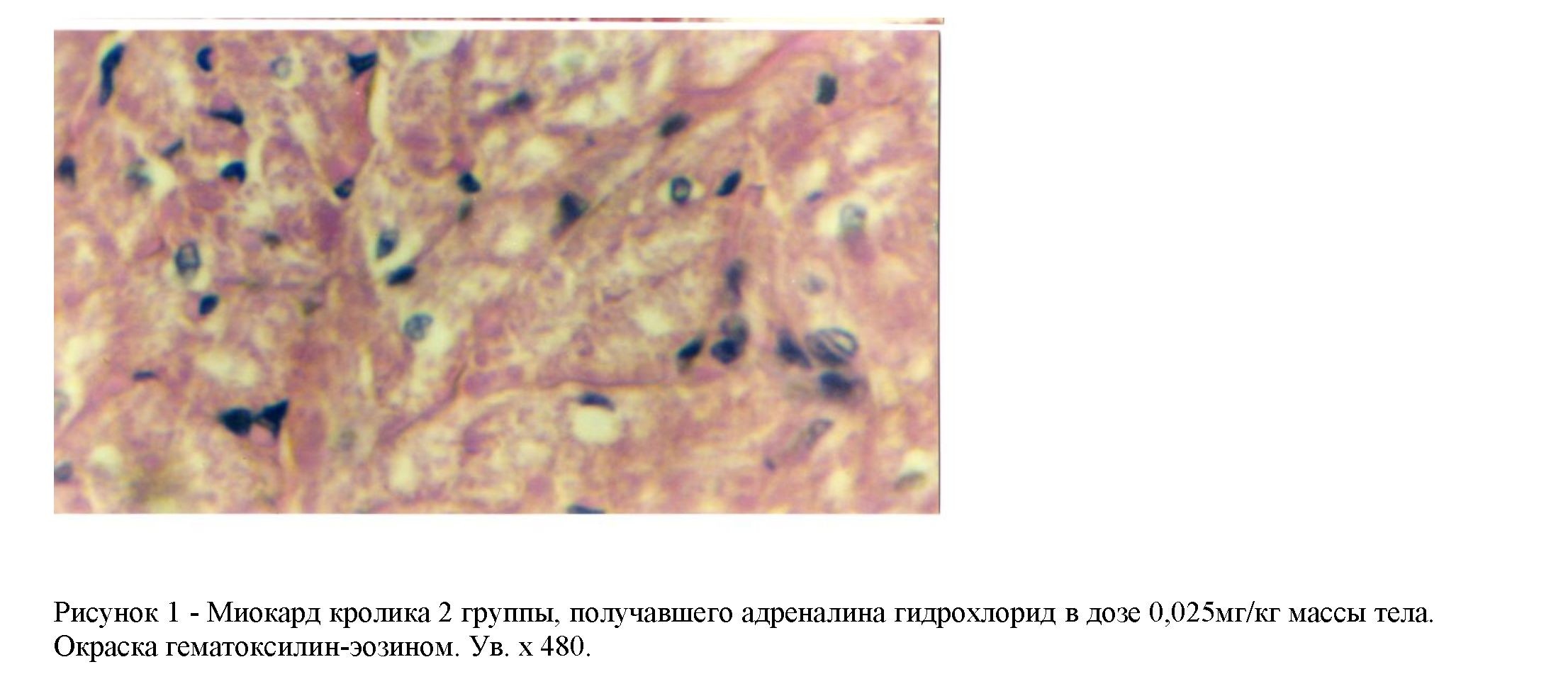
При гистологическом исследовании миокарда у кроликов, умерщвленных через 3 суток после введения адреналина, в субэпикардиальных и интрамуральных отделах обоих желудочков сердца выявляются рассеянные очаги некроза кардиомиоцитов (рис. 1) с лейкоцитарной инфильтрацией.
При морфометрическом исследовании площадь некроза миокарда левого желудочка сердца составила 17±0,2% от общей площади среза, в правом желудочке - 4±0,6% от общей площади среза. В перифокальных участках некроза при малом увеличении (ув. х 70) отмечается фрагментация кардиомиоцитов с мелко- крупноглыбчатым их распадом. При большом увеличении (ув. х 240, ув. х 480) выявляются признаки острой дистрофии кардиомиоцитов с явлениями вакуолизации отдельных из них.
У кроликов третьей группы, которым адреналина гидрохлорид вводили в дозе 0,05мг/кг массы, после введения препарата отмечались резкая одышка, беспокойство, выделение пенистой жидкости из ноздрей. В течение 10-30 минут после введения препарата животные погибали.
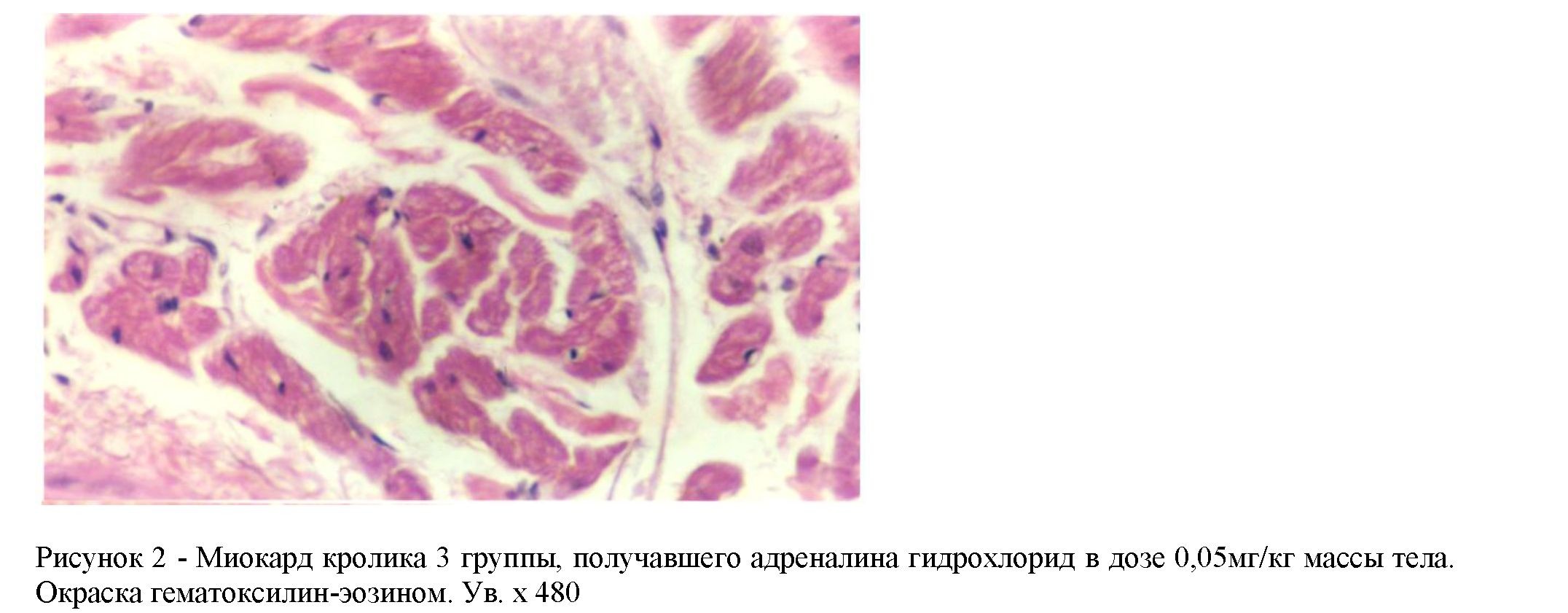
При гистологическом исследовании миокарда у животных этой группы выявлены рассеянные участки некроза от мелких до крупных с выраженной лейкоцитарной инфильтрацией. В зоне некроза присутствуют гистологические признаки субсегментарных и сегментарных контрактур, кариоцитолиза, острой дистрофии, очаговой фрагментации кардиомиоцитов с глыбчатым распадом (рис.2).
При морфометрическом исследовании площадь некроза составила в левом желудочке 30±0,6%, в правом желудочке 7±0,3% от общей площади среза.
Проведенные эксперименты позволили сделать следующие выводы:
моделирование катехоламинового некроза миокарда у кроликов в условиях низкогорья сопровождается нарушением микроциркуляции, ишемией и некрозом кардиомиоцитов очагового характера;
выявленные морфофункциональные изменения в миокарде кроликов при экспериментальном моделировании кардионекроза находятся в прямой зависимости от дозы введенного адреналина;
введение адреналина кроликам в дозе 0,05мг/кг массы тела приводит к развитию адреналинового повреждения миокарда, несовместимого с жизнью животного. Летальность в этой группе животных составила 100%;
оптимальной дозой адреналина гидрохлорида для получения результативной и информативной биомодели катехоламинового повреждения миокарда у кроликов в условиях низкогорья (г. Бишкек, 760 м над ур. моря) является доза 0,025мг/кг массы тела животного.
СПИСОК ЛИТЕРАТУРЫ
- Boldessarins R.J., Boldessarins R.J., Fisher J.E. Model systems in Biological Psychiatry. Cambrige 5MFT Press, 1975. - р.251.
- Меерсон Ф.З. Патогенез и предупреждение стрессорных и ишемических повреждений сердца. М.: Медицина, 1984. - 268 с.
- Захаров Г.А. Гормонально индуцированный стресс и инфаркт миокарда у собак. - Бишкек: Илим, 1991. - 250 с.
- Гацура В.В. Фармакологическая коррекция энергетического обмена ишемизированного миокарда. - М.,1993. - 254 с.
- Raab W. Myocardial electrolyte derangement: Crucial feature of pluricausal, so-cold coronary, heart disease. Ann. N. Y. Acad- Sci. - 1969. - p,627-686.
- Маатов Т.О. Особенности течения экспериментального миокардита у крыс различного возраста под влиянием кардиотонических средств. Автореф. Дисс канд.мед. наук. - Фрунзе, 1884. - 25с.
- Захаров Г.А. Влияние среднегорья на механизмы развития и течения экспериментального инфаркта миокарда: Автореф. дисс. докт. мед. наук. -Бишкек,1996-.40с.
- Епинетов М.А. Способ оценки эффективности фармакологической кардиопротекции в условиях гипоксии-ишемии. Патент РФ. Дата публикации: 2004.12.27 (21) Регистрационный номер заявки:
2002132077/14 .
- Антонов А.Р., Ефремов А.В., Новоселов Я.Б., Летягина В.В., Волкогонова А.А. Влияние общей
9
управляемой гипертермии на активность тканевой РААС после экспериментального инфаркта миокарда // Успехи современного естествознания. - 2006. - № 5 - С. 76-77.
- Данилова К.М. О сущности экспериментального адреналинового миокардита. - Архив патологии. - 1961. - № 1I.-C 11-17.
- Мясников А.Л., Чазов Е.И., Шхвацабая И.К., Кипшидзе Н.Н. Экспериментальные некрозы миокарда. - м., 1963.
- Целлариус Ю.Г. Гистопатология адреналиновых повреждений миокарда. Автореф. докт дне. - Новосибирск. -1969. -35с.
- Ziegler K. Beitr. Path. Anat., 1905. - Bd.38. - S. 222-254
- Gellhorn E. Methoden zum Nachweis des Adrenalins. - Abderhaldens Handbuch d. Biologischen Arbeitsmethoden. - Berlin - Wien, 1926. - 251s.
- Непомнящих, Л. М. Альтернативная недостаточность мышечных клеток сердца при метаболических и ишемических повреждениях / Л.М. Непомнящих. - М., 1998. - С. 56
- Гофман Б. Катехоламины и средства, влияющие на адренэргическую передачу / Б. Гофман // Клиническая фармакология по Гудману и Гилману. Книга 1. - М., 2006. - С. 185.
- Чуваев, И.В. Оптимизация адреналиновой модели инфаркта миокарда на крысах / И. В. Чуваев, С. В. Глотова // Материалы Всероссийского съезда ветеринарных фармакологов и токсикологов «Эффективные и безопасные лекарственные средства в ветеринарии», СПб., 2009. - С. 28-31
- Selye H., Bajusz E., Grasso S., Mendel P. Simple techniques for the surgical occlusion of coronary vessels in the rats.Angiology. - 1960. - №11. - Р. 398-407
- Murry C.E, Jennings R.B, Reimer K.A. Preconditioning with ischemia: a delay of lethal cell injury in ischemic myocardium. Circulation. - 1986,75:1124-1136
- Obata T., Hosokawa H., Yamanaka Y. In vivo monitoring of norepinephrine and OH generation on myocardial ischemic injury by dialysis technique. Am J Physiol . - 1994. - № 266. - Р. 903 - 908
- Cohen M.V., Liu G.S., DowneyJ.M. Preconditioning causes improved wall motion as well as smaller infarcts after transient coronary occlusion in rabbits. Circulation. - 1991. - №84. - Р. 341-349
- Liu Y., Downey J.M Ischemic preconditioning protects against infarction in rat heart. Am J Physiol. - 1992. - №263. Р.1107-111
- Mc Kean T., Mendenhall W. Comparison of the responses to hypoxia, ischaemia and ischaemic preconditioning in wild marmot and laboratory rabbit hearts. - J Exp Biol1. -1996. - № 99. - Р.693-697
- Harken A.H., Simson M.B., Hasilgrove J., WetsteinL., Harden W.R. 3rd, Barlow C.H. Early ischemia after complete coronary ligation in the rabbit, dog, pig, and monkey. Am J Physiol.- 1981. - №241. - Р.202-210
- Schaper W, Bernotat-Danielowski S, Nienaber C, Schaper J. Collateral Circulation. In: Fozzard HA, Haber E, Jennings, RB, Katz AM, editors. The Heart and Cardiovascular System. New York: Raven Press, 1992. - Р. 1427-1464.
- Автандилов Г.Г. Введение в количественную патологическую морфологию. - М.: Медицина, 1980. - С.213.
- Автандилов Г.Г. Медицинская морфометрия. - М-: Медицина. - 1990. - 384с.