Мақалада оқшауланған гепатоциттердің ультрақұрылымдық ұйымы зерттелген және олардың өсу ди- намикасындағы жасушаішілік өзгерістердің сипаты анықталған. Нативтік қасиеттері сақталған гепато- циттерді өсіру әдісін әзірлеу, әртүрлі сыртқы факторлардың, химиялық қосылыстардың және жаңа дә- рілік препараттардың гепатотоксикалық әсерлерін зерттеу үшін және бауырдың тұқым қуалайтын не- месе терминалды ауруларын емдеуде жасушалық трансплантацияны жүргізуге мүмкіндік беретін қа- жеттілігімен анықталды. Бастапқы гепатоциттерді өсіру үлгілері бауыр метаболизмін, секрециясын және регенерациясын зерттеу үшін қолданылады. Бастапқы гепатоциттерді өсіру стандартты қоректік ортада жүргізілген, ал өсу динамикасы ағынды цитофлуориметрия, жарық және электронды микрос- коптар арқылы зерттелген. Стандартты қоректік ортада өсірілген бастапқы гепатоциттерді зерттеу нә- тижесінде, гепатоциттердегі базальды аутофагиянның жоғарылауы гликофагия мен митофагия түрінде көрініс берді. Аутофагия стандартты өсірілген жағдайда оқшауланған гепатоциттердің жасушалық го- меостазын сақтауға мүмкіндік береді.
Кіріспе
Соңғы уақытта бастапқы гепатоциттер жасушаларын өсіру бауырдың тұқым қуалайтын немесе терминалдық ауруларын емдеуде трансплантация жүргізу қажеттілігі туындауына байланысты қарас- тырылуда [1]. Бауырдың ерекшелігі - патологиялық факторлар жойғаннан кейін, бауырдың қалыпты құрылымының қалпына келуі [2]. Бауырда көптеген функцияларды — паренхиматозды жасушалар не- месе гепатоциттер атқарады [3]. Бауырдың паренхиматозды жасушасы — гепатоцит күрделі, энерге- тикалық қарқынды, поляризацияланған эпителиальды жасушалар болып табылады [1]. Гепатоциттер регенерация кезінде ағзаның тіршілігін қамтамасыз ететін бауырдың маңызды функцияларын сақтай отырып, 1000-нан астам гендерді экспрессиялайды [4].
Бауыр метаболизм мен залалсыздандырудың орталық органы болып табылатындықтан, оқшау- ланған гепатоциттер дәрілік препараттардың фармакологиялық және токсикологиялық реакцияларын анықтау үшін үлгі ретінде пайдаланылады [5]. Сонымен қатар, бастапқы гепатоциттерді өсірудің оң- тайлы әдісі мен тиімділігін анықтау мәселелері сақталуда [6].
Жасушаішілік немесе жасушадан тыс микроортаның өзгеруі жағдайында жасушалардың гомеос- тазын сақтау механизмі аутофагия болып табылатыны белгілі [7]. Аутофагиялық механизм жасушадан тыс микроортаның метаболикалық өзгерістеріне өте сезімтал және стрестік жағдайларды жеңу үшін бейімделген аутофагиялық жауап маңызды болады [8]. Аутофагия және апоптоз — жасушаішілік екі қарама-қарсы үрдіс. Аутофагия — жасушаның тіршілігін сақтап қалу тәсілі [9], ал апоптоз — жасуша- ның жойылу түрінің бірі [10]. Аутофагия жасушалық гомеостазды сақтау және энергия өндіруге арнал- ған субстраттарды қамтамасыз ететін лизосомалардағы дұрыс оралмаған ақуыздар мен зақымдалған цитоплазмалық компоненттердің тозу жолын білдіреді [11].
Зерттеу жұмысының мақсаты — оқшауланған гепатоциттердің цитоплазмасындағы базальды аутофагияны, оларды өсіру динамикасында зерттеу.
Зерттеу материалдары және әдістері
Гепатоциттерді бөліп алу және өсіру. Зерттеу бастапқы өсірілген гепатоциттерде жүргізілді. Салмағы 180–200 г. Вистар саласындағы аталық егеуқұйрықтардың гепатоциттері 0,03 % коллагеназа ерітіндісін («ICN Biomedicals, Inc», АҚШ) пайдалана отырып, рециркуляторлы ферментативті перфузия әдісін қолданып, дифференциалды центрифугалау арқылы паренхимиялық емес жасушалардан бө- лініп алынды. Жасушалардың тіршілік ұзақтығы трипанды көкті («Serva», Германия) жасушалар құра- мынан шығару әдісімен бағаланды. Экспериментке тіршілік ұзақтығы 90 %-дан кем емес жасушалар алынды. Алынған жасушаларды концентрациясы 10∙104 жасуша/ойық коллагенмен жабылған 6-ойығы бар планшеттерге (Corning) отырғызылды. Гепатоциттер келесі қоректік ортада RPMI-1640 (Gibco, АҚШ), рН 7,4, құрамында 10 % сиырдың эмбрионалды сарысуы (Gibco, АҚШ), 100 бірл./мл пенициллин, 50 мкг/мл гентамицин стандартты жағдайларда (5 % СО2, 37 °С температурада және 95 % ылғал- дылықта) өсірілді.
Өсірілетін гепатоциттердің жасушалық циклын бағалау. Өсірілген гепатоциттердің жасушалық циклын талдау үшін Пропидий йодидінің (PI) интеркалибрлеуші флуоресцентті бояғыш ДНҚ қолдану арқылы, ағынды цитофлуориметрия әдісі қолданылды. Жасушалар 1, 24 және 48 сағат бойы өсірілді. Жасушаларды пластиктен алу үшін TrypLE реагентті (Gibco, АҚШ) пайдаланылды, центрифугалаумен жасушалар тұнып, фосфатты-тұзды буфермен (PBS) жуылды және мұздатылған 70 % этанолмен бекі- тілді. ДНҚ экстракциясы үшін буфермен инкубациядан кейін жасушалар қайтадан центрифугаланып және PBS-пен жуылды. Пропидий йодидімен боялған жасушалар CytoFlexS (Beckman Coulter, АҚШ) ағынды цитофлуориметрмен талданды.
Трансмиссиялық электронды микроскоп. Гепатоциттердің ультрақұрылымдық ұйымдастыры- луын зерттеу үшін Хенкс ортасында дайындалған параформальдегидтің 4 % ерітіндісінде жасушала- рының белгілі мөлшері фиксацияланды, одан кейін 1 сағат ішінде фосфатты буферде (pH=7,4) 1 % ОѕО4 ерітіндісінде тағы да фиксация жүргізілді, дегидратацияны этил спиртінің ұлғаю концентрация- сында жүргізіп, эпонмен (Serva, Германия) қапталды. Қалыңдығы 1 мкм болатын жартылай жіңішке кесінділер Leica EM UC7 (Leica Microsystems, Германия) ультрамикротомында дайындалды, толуи- динді көкпен боялып, сәулелі микроскоп «LEICA DME» (Leica Microsystems, Германия) арқылы зерт- телді. Қалыңдығы 70–100 нм болатын ультражіңішке кесінділерді сулы ерітіндіде қаныққан уранилацетат және қорғасын цитратымен контрастылығын келтіріп, электронды микроскоппен JEM 1010 (JEOL, Жапония) зерттелді.
Морфометрия және статистикалық мәліметтерді өңдеу. Морфометриялық талдау ImageJ (Wayne Rasband, АҚШ) компьютерлік бағдарламаның көмегімен жүргізілді. Гепатоциттердің ядро- лары мен цитоплазмасының диаметрі, ядролар мен цитоплазманың көлемі және ядролық-цитоплазма- лық арақатынасы анықталды. Жасушаішілік органеллалардың концентрациясын 500 нүктеден тұратын жабық тест жүйесін пайдалана отырып, ×30000 ұлғайған кезде бағаланды. Орташа мән (М) және стан- дартты ауытқу (SD) Microsoft Excel (Microsoft, АҚШ) бағдарламалық жасақтамасын пайдалану арқылы есептелді. Зерттелетін параметрлер арасындағы айырмашылықтардың анықтығы 95 % (P<0,05) сенім- ділік деңгейінде U-критерия Манна-Уитни көрсеткішін қолдану арқылы Statistica 6.0 (StatSoft, АҚШ) бағдарламалық қамтамасыз ету көмегімен анықталды.
Зерттеу нәтижелері және оны талдау
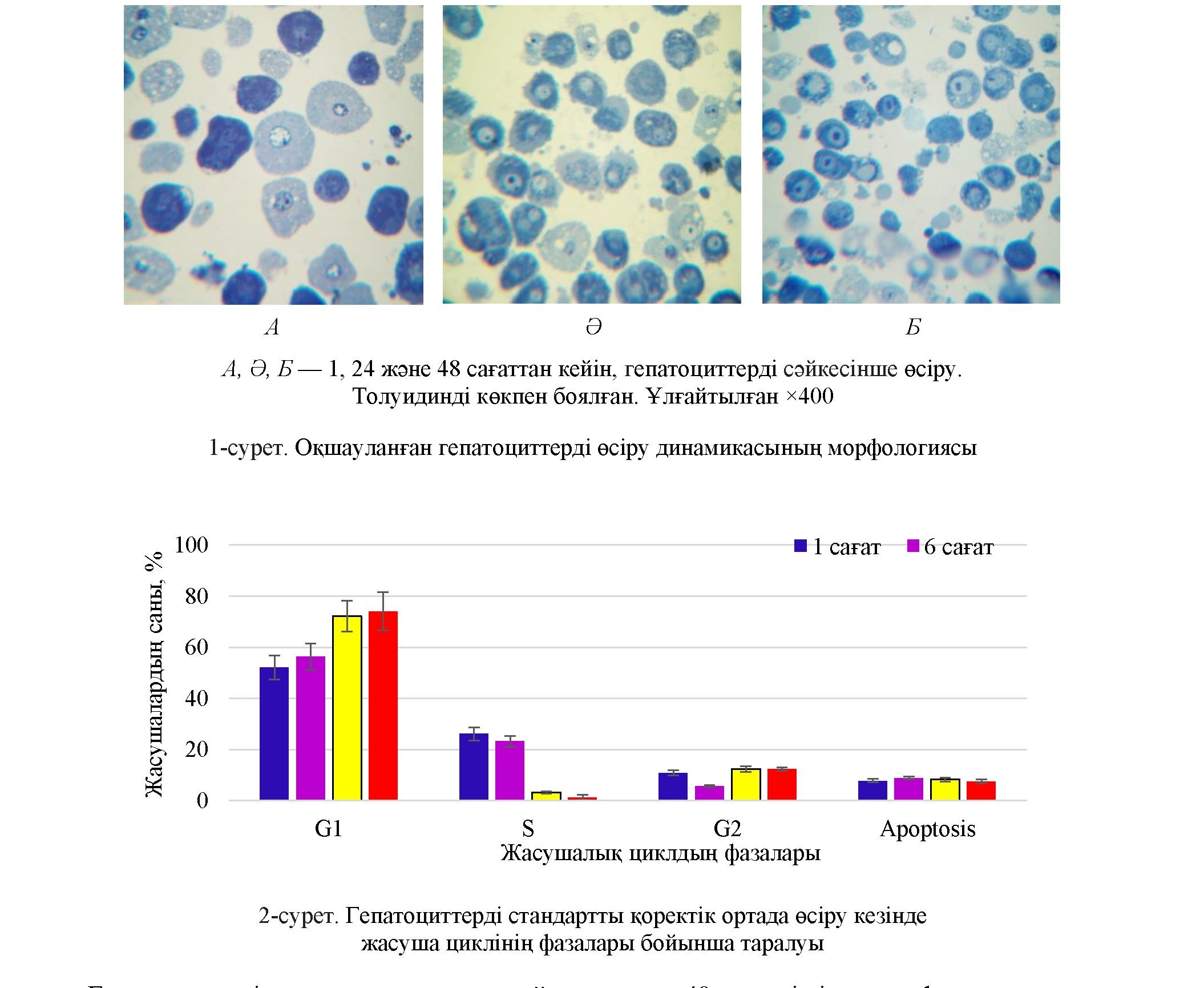
Оқшауланған гепатоциттерді өсіру кезінде 48 сағат ішінде жасушалардың абсолюттік көлемінің біртіндеп төмендегені байқалды. Өсірілген гепатоциттер жасушасының көлемі 24 сағаттан кейін 57 %-ға кеміді, ал 48 сағаттан кейін 76 %-ға кеміді, 1 сағат өткендегі жасушалар көлемімен салыстыр- ғанда. Бұл ретте гепатоциттер ядроларының абсолюттік көлемі нақты өзгерген жоқ. Ядролық-цито- плазмалық арақатынас 24 сағаттан кейін 2 есе, 48 сағаттан кейін 4 есе артты (1 А-Б сурет). Демек, өсіру процесінде гепатоциттер көлемінің төмендеуі, жасушалардың цитоплазмасының көлемдік үлесінің тө- мендеуі есебінен жүрді.
Жасушалық циклды бағалау стандартты қоректік ортада өсіру кезінде 24 сағаттан кейін G0/G1-де гепатоциттердің тоқтауын көрсетті. 48 сағат ішінде зерттеу апоптоз сатысындағы жасушалар пайызы- ның көтерілмегенін, гепатоциттер өздерінің тіршілік ұзақтығын сақтап қалғанын айқындады (2-сурет).
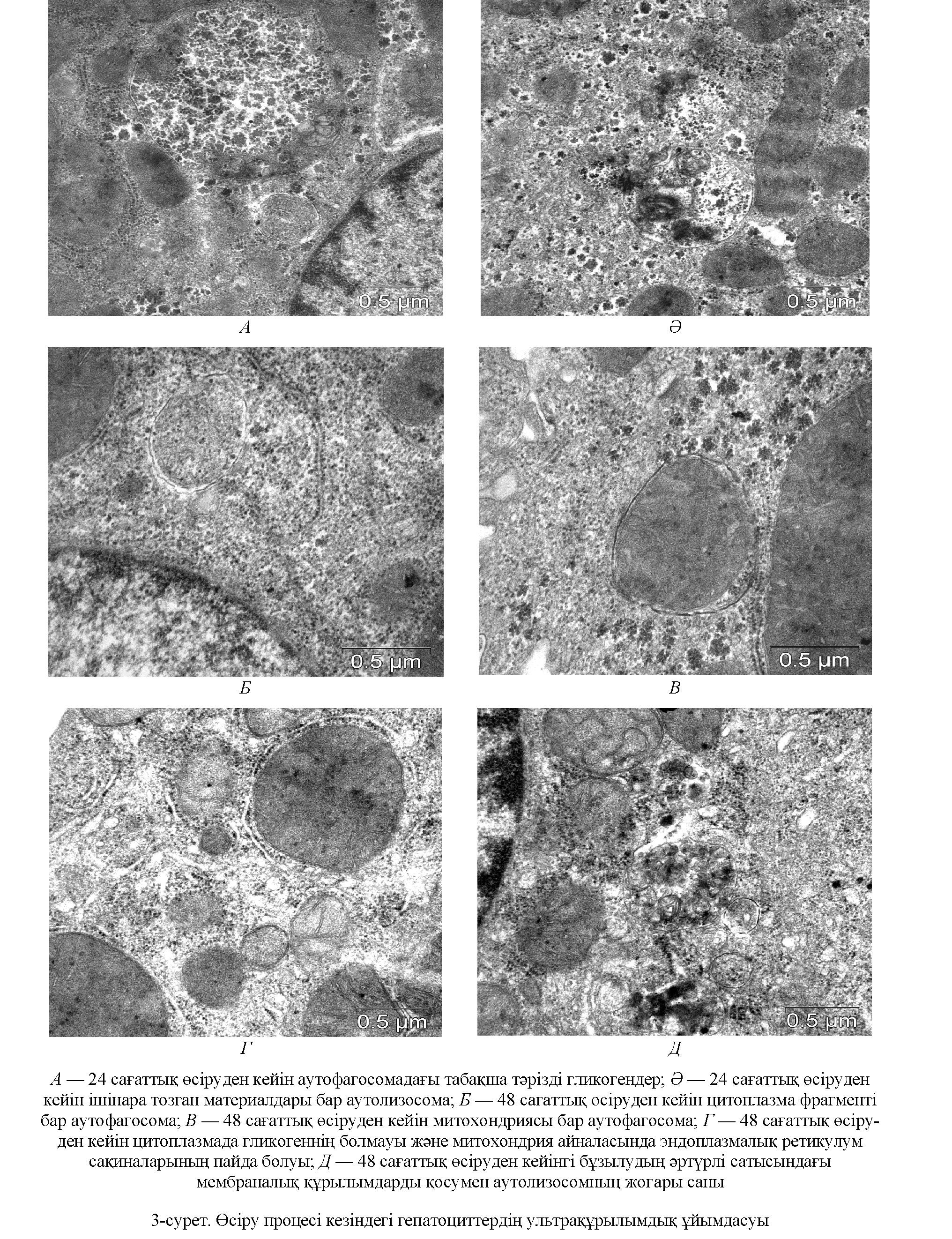
Гепатоциттердің ультрақұрылымдық ұйымдасуын зерттеуде 24 сағаттық өсіруден кейін гепато- циттердің цитоплазмасында табақша тәрізді гликогендер мен цитоплазма фрагменттерінде аутофаго- сомалар (3А сурет) және ішінара тозған материалмен аутолизосом анықталды (3Ә сурет).
Егер 24 сағаттық өсіруден кейін аутофагосом құрамында гликогеннің түйіршіктері байқалса, онда гепатоциттердің ультрақұрылымдарын 48 сағаттан кейін зерттеу кезінде цитоплазма және митохон- дрияның фрагменттері бар аутофагосомалар анықталды (3Б, В сурет). Митохондриялар түйіршікті эн- доплазмалық ретикулум цистерналарымен жиі қоршалған (3Г сурет). Сонымен қатар, митохондриялардағы кристалар құрылымының бұзылу және ыдырап-бұзылудың әртүрлі сатысындағы мембрана- лық құрылымдардың қосылуымен аутолизосомалардың санының жоғарылауы байқалды (3Д сурет).
Гепатоциттердің ультрақұрылымдық ұйымдасуына 48 сағат ішінде морфометриялық зерттеу жүргізу, өсірілген гепатоциттерде гликогеннің және митохондрияның көлемдік тығыздығы 84 % және 27 % (p<0,05) сәйкес төмендегенін көрсетті (1-кесте). Бұл ретте, аутофагосом және аутолизосомның көлемдік тығыздығы 50 % және 7 есеге (p<0,05), сәйкес артты (1-кесте).
1-кесте
|
Параметрлері |
1сағат |
24 сағат |
48 сағат |
|
Гепатоциттер, V (мкм3) |
8089,77±3465,86 |
7322,782±3682,01* |
4154,77±1904,82* |
|
Гепатоциттер ядросы, V (мкм3) |
423,04±137,21 |
427,73±127,91 |
514,83±124,8 |
|
ЯЦИ |
0,052±0,0215 |
0,074±0,0515 |
0,179±0,0315* |
|
Митохондрия, Vv (%) |
14,2±2,72 |
14,7±1,78 |
10,4±2,38* |
|
ЭПР, Vv (%) |
4,41±0,43 |
3,92±1,04 |
2,02±0,56 |
|
Аутофагосомдар, Vv (%) |
5,87±1,45 |
21,2±5,13* |
8,78±3,56*# |
|
Аутолизосомдар, Vv (%) |
0,94±1,22 |
2,65±2,51* |
6,88±2,21*# |
|
Гликоген, Vv (%) |
5,41±1,14 |
1,42±1,08* |
0,86±0,84* |
Гепатоциттерді өсіру динамикасындағы морфометрияның нәтижелері (M±SD)
Ескертпе. Vv — құрылымдардың көлемді тығыздығы; ЭПР — эндоплазматикалық ретикулум; ЯЦИ — ядролық-цито- плазмалық индекс (VV ядро/VV цитоплазмалар). 1, 24, 48 сағат — гепатоциттерді өсіру уақыты. * — 1 сағ. өсіру арқылы сәйкес шамалардан айырмашылығы, # — 24 сағ. өсіру арқылы сәйкес шамалардан айырмашылығы (p≤0,05).
92
Вестник Карагандинского университета
Алынған мәліметтерді талқылау
Аутофагия макромолекулалық ақуыз агрегаттарын, қосалқы қоректік заттардың жасушалық орга- неллаларын (гликоген мен липидтер) жоюға және тозуына бағытталған, жасушалық гомеостазды ұстап тұруға және стресс жағдайында белсендіретін, катаболикалық бағдарлама болып табылады. Аутофагия нәтижесінде лизосомаларда түзілетін метаболиттер макромолекулаларды синтездеу үшін энергия көз- дері немесе құрылыс блоктары ретінде қайта пайдаланылады [12].
Гепатоциттер энергетикалық ресурс — гликогеннің түзілуі мен сақталуында маңызды, шешуші рөл атқаратыны белгілі [13]. Әдебиет деректері аутофагия мен көмірсулар алмасуы арасындағы өзара әрекеттесуді және аутофагия мен жасушалық энергетикалық баланс арасындағы динамикалық кері байланыстың болуын көрсетеді [12]. Гликоген аутофагосомалармен танылуы және сіңірілуі мүмкін, содан кейін ыдырау үшін лизосомаға беріледі. Бұл процесс «гликофагия» деп аталады [14]. Біздің зерт- теуде гепатоциттерді өсіру кезінде 24 сағаттан кейін гликогені бар аутофагосомалар басым болды, ал 48 сағаттан кейін митохондриясы бар аутофагосомалар пайда болды. Бұл кезеңде жасушалық циклдің S-фазасындағы жасушалардың саны ең аз болса, G0/G1 сатысындағы жасушалардың жоғары пайызы- ның болуы анықталды. Аминқышқылдарының жетіспеушілігі жағдайында ақуыз синтезі мен митоз тоқтайтыны белгілі, ал аутофагиялық сигналдық жол тіршілікке маңызды ақуыздарды синтездеу үшін аминқышқыл пулының қолжетімділігін қамтамасыз ету мақсатында ақуыздарды ыдырату жолымен аминқышқылдарын босату үшін белсендіріледі [14].
Гепатоциттердің жасушалық культураларын медицинада пайдалануды шектейтін мәселелердің бірі өсіру кезінде жасушалардың митоздық белсенділігінің жоғалуы болып табылады [15]. Жасушалық циклді тоқтату біздің зерттеуде де көрсетілген. Сонымен қатар, өсірудің 48 сағатында гепатоциттердің базальды аутофагия деңгейі өсті және апоптоз жағдайындағы жасушалар саны ұлғайған жоқ. Бұл жағ- дайда аутофагия, гепатоциттердің дифференциялану деңгейін қолдап, жасушалық гомеостазды сақтау- дың тиімді тәсілі болып табылды [16].
Қорытынды
Біздің алған мәліметтеріміз оқшауланған гепатоциттерді теңдестірілген қоректік ортада өсіру ке- зінде жасушалардың цитоплазмасында базальды аутофагияның өсуін көрсетеді. Тәжірибеден соң 24 сағаттан кейін гликофагия дамыды, өйткені аутофагосомаларда негізінен жасуша үшін энергия көзі болып табылатын материал — гликоген түйіршіктері болды. Гликофагияға қосымша, 48 сағаттан кейін жасушалардың амин қышқылдарына деген қажеттілігіне және ақуыз кешендерінің ыдырауына байла- нысты митофагия байқалды. Алынған мәліметтер гепатоциттердің бастапқы культурасының тіршілік етуіне аутофагияның қосқан үлесін көрсетеді және оларды өсіру жағдайларының жеткіліктілігінің көр- сеткіші ретінде пайдалануға болады.
Сонымен, ағынды цитофлуориметрия, жарық және электрондық микроскопия әдістерімен стан- дартты қоректік ортада бастапқы гепатоциттердің өсіру динамикасы сипатталды. 24 сағаттан кейін жа- сушалық циклдің G0/G1 сатысында өсірілген гепатоциттердің тоқтауы және апоптоз сатысында сол жасушалардың пайызы көбеймей, олардың тіршілік ұзақтығы сақталғаны анықталды. Жасушалардың цитоплазмасында базальды аутофагияның артуы — гликофагия мен митофагияның басым болуы, ге- патоциттерді өсіру процесінде жасушалық гомеостазды сақтау механизмі болып табылады.
Әдебиеттер тізімі
- Ogoke O. Bioengineering considerations in liver regenerative medicine / O. Ogoke, J. Oluwole, N. Parashurama // J. Biol. Eng. — 2017. — Vol. 11. — P. 46. — https://doi.org/ 10.1186/s13036–017–0081–4.
- Leevy C.B. Abnormalities of liver regeneration: a review/ C.B. Leevy // Dig. Diseases. — 1998. — Vol. 16(2). — P. 88–98. https://doi.org/10.1159/000016852.
- Пашков А.Н. Культивирование гепатоцитов на твердом носителе / А.Н. Пашков, П.И. Кошелев, К.А. Сапин // Материалы Междунар. конф. хирургов-гепатологов. — М., 2003. — С. 65.
- Michalopoulos G.K. Hepatostat: Liver regeneration and normal liver tissue maintenance / G.K. Michalopoulos // Hepatology. — 2017. — № 65(4). — P. 1384–1392. — https://doi.org/10.1002/hep.28988
- Robust A.S. Long-term culture of endoderm-derived hepatic organoids for disease modeling / A.S. Robust, G.G. Sevinç, N. Er- soy, O. Basak, K. Kaplan, K. Sevinç, E. Ozel, B. Sengun, E. Enustun, B. Ozcimen, A. Bagriyanik, N. Arslan, T.T. Önder, E. Erdal // Stem Cell Reports. — 2019. — Vol. 13, No.4. — P. 627–641. — https://doi.org/10.1016/j.stemcr.2019.08.007.
- Nicolas C.T. Concise review: liver regenerative medicine: from hepatocyte transplantation to bioartificial livers and bioengineered grafts / C.T. Nicolas, R.D. Hickey, H.S. Chen, S.A. Mao, M. Lopera Higuita, Y. Wang, S.L. Nyberg // Stem Cells. — 2017. — Vol. 35, No. 1. — P. 42–50. — https://doi.org/ 10.1002/stem.2500.
- Sica V. Organelle-specific initiation of autophagy / V. Sica, L. Galluzzi, J.M. Bravo-San Pedro, V. Izzo, M.C. Maiuri, G. Kroemer // Mol. Cell. — 2015. — Vol. 59, No. 4. — P. 522–39. — https://doi.org/10.1016/j.molcel.2015.07.021.
- Kroemer G. Lysosomes and autophagy in cell death control / M. Jäättelä // Nat. Rev. Cancer. — 2005. — Vol. 5, No. 11. — P. 886–897. — https://doi.org /doi: 10.1038/nrc1738.
- Klionsky D.J. Guidelines for the use and interpretation of assays for monitoring autophagy (3rd edition / D.J. Klionsky, K. Ab- delmohsen, A. Abe, M.J. Abedin, H. Abeliovich, Acevedo Arozena // Autophagy. — 2016. — Vol. 12, No. 1. — P. 1–222. — https://doi.org / 10.1080/15548627.2015.1100356.
- Edinger A.L. Death by design: apoptosis, necrosis and autophagy / A.L. Edinger, C.B. Thompson // CurrOpin Cell Biol. — 2004. — Vol. 16, No. 6. — P. 663–669. — https://doi.org/10.1016/j.ceb.2004.09.011
- Malik B.R. Autophagic and endo-lysosomal dysfunction in neurodegenerative disease / B.R. Malik, D.C. Maddison, G.A. Smith, O.M. Peters // Mol. Brain. — 2019. — Vol. 12, No. 1. — P. 100. — https://doi.org/10.1186/s13041–019–0504-x.
- Ha J. AMPK and autophagy in glucose/glycogen metabolism / J. Ma, K.L. Guan, J. Kim // Mol. Aspects Med. — 2015. — Vol. 46. — P. 46–62. — https://doi.org/ 10.1016/j.mam.2015.08.002.
- Cao L. Effects of hypoxia on the growth and development of the fetal ovine hepatocytes in primary culture / L. Cao, J. Wang, L.Bo, D.W. Li, N. Yin, A.W. Zhou, C.P. Mao // Biomed. Environ. Sci. — 2019. — Vol. 32, No. 8. — P. 592–601. — https://doi.org/10.3967/bes2019.077.
- He L. Autophagy: the last defense against cellular nutritional stress / L. He, J. Zhang, J. Zhao, N. Ma, S.W. Kim, S. Qiao, X. Ma // Adv. Nutr. — 2018. — Vol. 9, No. 4. — P. 493–504. — https://doi.org/ 10.1093/advances/nmy011
- Krause P. Cultured hepatocytes adopt progenitor characteristics and display bipotent capacity to repopulate the liver / P. Krause, K. Unthan-Fechner, I. Probst, S. Koenig // Cell Transplant. — 2014. — Vol. 23, No. 7. — P. 805–817. https://doi.org/10.3727/ 096368913X664856.
- Olsavsky Goyak K.M. Hepatocyte differentiation / K.M. Olsavsky Goyak, E.M. Laurenzana, C.J. Omiecinski // Methods Mol. Biol. — 2010. — Vol. 640. — P. 115–138. — https://doi.org/10.1007/978–1-60761–688–7_6.