В данной статье представлены результаты исследования безопасности и иммуногенности интраназальной векторной вакцины для профилактики туберкулеза ТВ/FLU-04L на основе аттенуированного рекомбинантного гриппозного штамма, экспрессирующего протективные микобактериальные антигены ESAT-6 и Ag85A.
Введение
Согласно оценкам ВОЗ, треть населения планеты инфицирована Mycobacterium tubercolosis, при этом каждый год приблизительно у 9 миллионов человек развивается туберкулез, 2 миллиона из них умирают. Туберкулез (ТБ) известен человечеству уже достаточно давно. Из регистрируемых ежегодно 9 миллионов случаев заболевания ТБ около 1 миллиона (11%) приходится на детей в возрасте до 15 лет. Из них 75% случаев регистрируют в 22 странах с наиболее тяжелым бременем ТБ, что составляет около 80% случаев ТБ у детей, регистрируемых во всем мире. В целом в разных странах на долю детей приходится от 3-25% и более от общего числа заболевших [1].
В странах Западной и Центральной Европы заболеваемость ТБ снижается, однако в странах Восточной Европы бремя этой болезни все еще остается на высоком уровне и продолжает повышаться [2].
В Казахстане ситуация по ТБ также не стабильна, однако заболеваемость и смертность от ТБ по сравнению с предыдущими годами снизилась. Однако уровень заболеваемости указывает на то, что в Казахстане продолжается эпидемия ТБ, поскольку по стандартам ВОЗ болезнь приобретает эпидемиологический характер, если число больных составляет 50 человек на 100 тыс. населения [3].
Текущая и единственная вакцина против ТБ B acille Calmette–Guerin (BCG) используется во всем мире в течение нескольких десятилетий, но у этой вакцины много недостатков, включая переменную эффективность у людей, неспособность защитить от реактивации и повторного заражения, а также патогенность в организме-хозяине с ослабленным иммунитетом [4, 5].
В Республике Казахстан в настоящее время все показатели эффективности лечения впервые выявленных больных ТБ легких остаются на крайне низком уровне, что обусловлено распространенностью устойчивости микобактерий к химиопрепаратам, снижением способности организма больных к репаративным процессам. Снижение эффективности лечебных мероприятий, реверсия распространенных, остро прогрессирующих форм инфекции и значительный рост лекарственно-устойчивого ТБ свидетельствует о необходимости профилактики данной инфекции [6]. Для решения данной проблемы в НИИПББ КН МОН РК разработана рекомбинантная вакцина против ТБ на основе гриппозного вектора, экспрессирующего микобактериальные антигены Esat6 и Ag85A low. Целью настоящих исследований было проведение доклинических испытаний вакцины на лабораторных животных, являющихся одним из основных и обязательных этапов при разработке и внедрении иммунобиологических препаратов в медицинскую практику.
Эксперименты in vivo – один из важнейших этапов доклинических исследований фармакологических и лекарственных средств. К сожалению, существующие экспериментальные модели редко полностью соответствуют тому, что наблюдается в клинике, тем не менее, они в какой-то мере имитируют условия, в которых назначают лекарственные вещества [7].
Работа выполнялась в соответствии правилами доклинических (неклинических) исследований биологически активных веществ и по защите позвоночных животных, используемых для экспериментальных и иных научных целей [8-10].
Материалы и методы В работе была использована векторная вакцина TB/FLU-04L для профилактики ТБ на основе гриппозного вектора вирусов гриппа А с рекомбинантным геном NS1, полученного с использованием технологии обратной генетики.
- Безопасность и иммуногенность вакцины ТВ/FLU-04L на обезьянах
- Исследования проводились на обезьянах Macaca fascicularis самцах 2,5 - 6 летнего возраста (n=10). Исследуемый препарат вводили интраназально в дозе 107.5 ТИД50/животное с помощью распылителя (500 мкл /доза).
- Определение безопасности вакцины
Мониторинг общего состояния животных проводился ежедневно в течение 42 суток. Осуществлялось взвешивание, термометрия, гематологический анализ крови, сбор носовых смывов, сывороток и др.
Сбор носовых смывов производили до вакцинации, на 2-й , 3-й, 4-й и 6-й дни исследования после иммунизации, затем полученный материал исследовали на присутствие вакцинного вируса.
Для определения вирусной нагрузки после вакцинации образцы носовых смывов были проанализированы в РТ-ПЦР. Также проводили выделение вакцинного вируса на клетках Vero в культуральной среде OptiPROSFM; Invitrogen. Мониторинг состояния клеточного монослоя осуществляли ежедневно, на 4 день гемагглютинирующая активность оценивалось в РГА с использованием 0,5 % суспензии куриных эритроцитов. В тот же день проводили «слепой пассаж» со свежим однодневным монослоем клеток Vero. В качестве контроля вирусной репликации использовали вакцинный вирус, в качестве отрицательного контроля 1 мл поддерживающей среды. Расчет 50% тканевой инфекционной дозы (ТИД50) проводили по методу L. Reed и H. Muench [11] и выражали в lgТИД50/мл. Чувствительность метода 1,5 lgТИД50/мл.
- Определение иммуногенности вакцины
Определение концентраций цитокинов в супернатантах, полученных при стимуляции мононуклеарных клеток периферической крови (МПК) обезьян проводили с помощью коммерческих наборов для мультиплексного измерения цитокинов приматов (Th1/Th2) методом проточной цитометрии согласно инструкциям производителей. Измерения проводили на приборе BD Canto II, обработка результатов велась с помощью программного обеспечения FCAP 1,0 (BD).
- Изучение острой токсичности вакцины ТВ/FLU-04L
Целью исследования являлось изучение острой токсичности препарата ТВ/FLU-04L при внутрибрюшинном введении мышам и подкожном введении морским свинкам.
В работе использовали белых беспородных мышей обоего пола, весом 18-20 г, возраст 6-8 недель и морских свинок (самцы и самки) массой 250-300 г. Животные распределялись по группам случайным образом. В качестве критерия приемлемой рандомизации считали отсутствие внешних признаков заболевания и гомогенность групп по массе тела (±20%). Изучение острой токсичности вакцины при однократном введении изучали с использованием плацебо-контроля (буферный раствор).
Исследуемый образец вводили в максимально допустимом объеме для каждого вида животных. Мышам (n=10) вводили внутрибрюшинно дозу эквивалентную разовой дозе для человека (0,05 мл раствора), что с учетом массовых коэффициентов в 2500 раз превышает дозу для человека.
Морским свинкам (n=10) подкожно вводили дозу эквивалентную 10 дозам, рекомендованных для человека (5 мл на животное), что с учетом массовых коэффициентов, в 1250 раз превышает дозу для человека. Контрольным животным вводили эквивалентное количество препарата плацебо (буферный раствор) [12-13].
После введения препарата непрерывное наблюдение вели в течение 2-х часов после инъекции и на протяжении 10 суток. В ходе исследования животных осматривали ежедневно. После окончание опыта была осуществлена эвтаназия животных для патоморфологического исследования внутренних органов.
- Безопасность противотуберкулезной вакцины ТВ/FLU-04L на хорьках
С целью оценки безопасности препарата ТВ/FLU-04L самцы хорьков 2-3 месячного возраста (n=6) были иммунизированы и/н (с помощью инсулинового шприца и приспособления для распыления в виде аэрозоля) вакциной в дозе 107.5 ТИД50/животное (500 мкл). После иммунизации в течение 40 дней проводилось ежедневное наблюдение, включающее контроль за развитием у животных клинических симптомов инфекции (чихание, выделения из носа), уровня активности, наличия поведенческих отклонений, потери аппетита и неврологических проявлений. Термометрию проводили на 0, 10, 20, 30, 40 сутки после иммунизации. Массу тела хорьков измеряли в течение 40 дней после вакцинации (на 2-й, 4-й, 8-й, 20-й, и 40-й дни). В контрольной группе (n=5) вводили фосфатно – буферный раствор (PBS). Для наркоза применяли комбинацию двух препаратов: ксилозин в дозе 0,1 мл на 1 кг веса и золетил в дозе 0,05 мл.
На 4-й день с целью сбора образцов ткани была осуществлена эвтаназия 5 животным из опытной группы и 1 из контрольной получивших плацебо. Эвтаназию животных осуществляли эфиром. Для патоморфологического исследования были взяты образцы следующих органов: сердце, легкие, печень, почки, селезенка.
Результаты исследования 1. Изучение безопасности и иммуногенности вакцинного кандидата ТВ/FLU-04L на обезьянах.
- Безопасность
За время наблюдения ни у одного из вакцинированных животных не было выявлено развития клинических симптомов инфекции, каких-либо неврологических проявлений, снижения массы тела (рисунок 1).
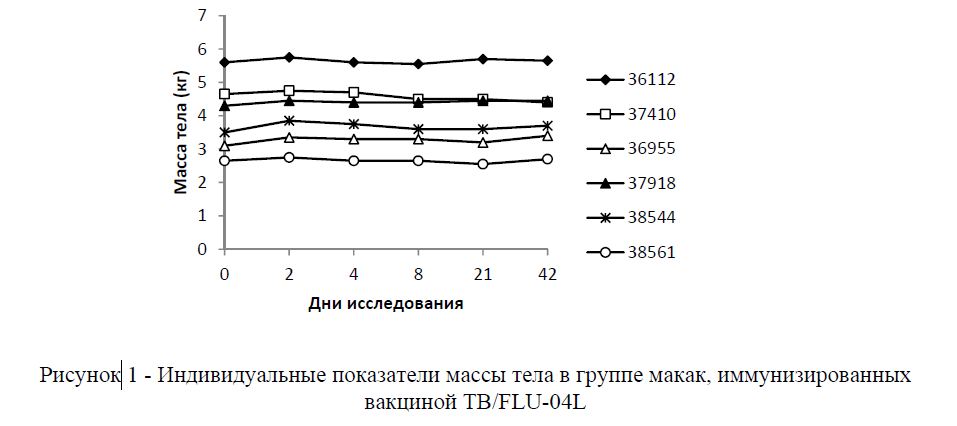
Рисунок 1 - Индивидуальные показатели массы тела в группе макак, иммунизированных вакциной ТВ/FLU-04L
Также за время наблюдения ни у одного из животных не было отмечено повышения температуры тела (рисунок 2), превышающего физиологическую норму (норма от 37,5°C до 39,5°C).
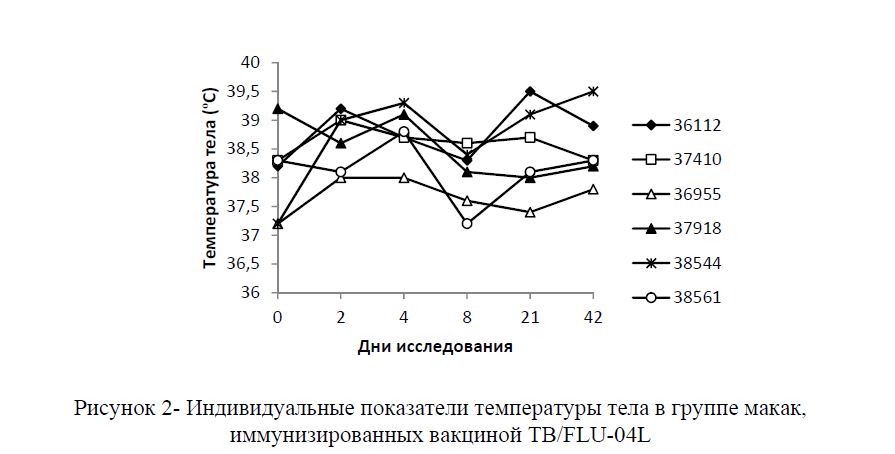
Рисунок 2- Индивидуальные показатели температуры тела в группе макак, иммунизированных вакциной ТВ/FLU-04L
Согласно данным гематологического анализа в ходе наблюдения были выявлены только незначительные спорадические изменения некоторых нормативных параметров. В целом, влияния вакцинного препарата на гематологическую картину выявлено не было.
При анализе назальных смывов, полученных на 2, 4 и 6 день после вакцинации в РТ- ПЦР, вакцинный вирус был выявлен в трех случаях (у животного №37918 на 2 день исследования и у животного №36112 на 2 и 4 день исследования). Однако, в культуре клеток Vero вирус из данных образцов не был выделен, в том числе, и при «слепом» пассаже (таблица 1). На 6 день исследования (120 часов после иммунизации) ни у одного животного вакцинный вирус в исследуемых образцах не выявлен.
Таблица 1 - Выделение штамма ТВ/FLU-04L из респираторного тракта вакцинированных животных
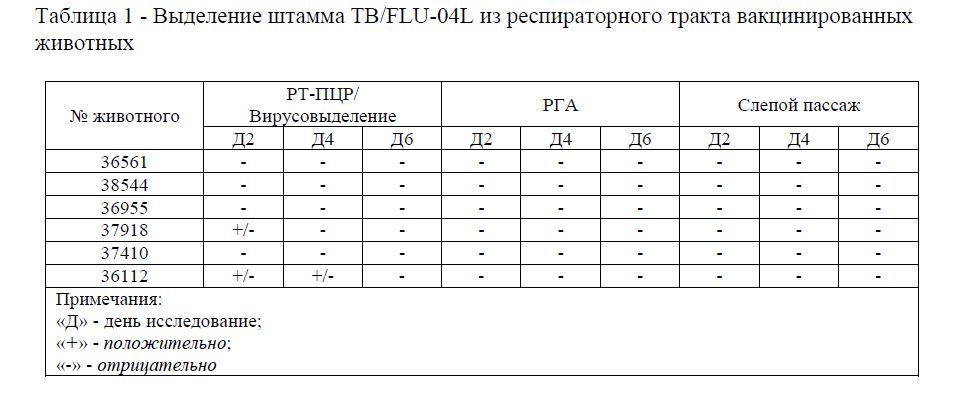
Полученные данные свидетельствуют о неспособности вакцинного вируса ТВ/FLU- 04L к репродукции в респираторном тракте обезьян.
- Иммуногенность
У всех вакцинированных животных, был детектирован клеточный иммунный ответ по выработке ИФН-гамма в ответ на спецефическую стимуляцию in vitro культур МПК белками ESAT-6 и Ag85A. При этом выработка цитокина отмечена в ответ на оба индуктора. Рисунок 3.
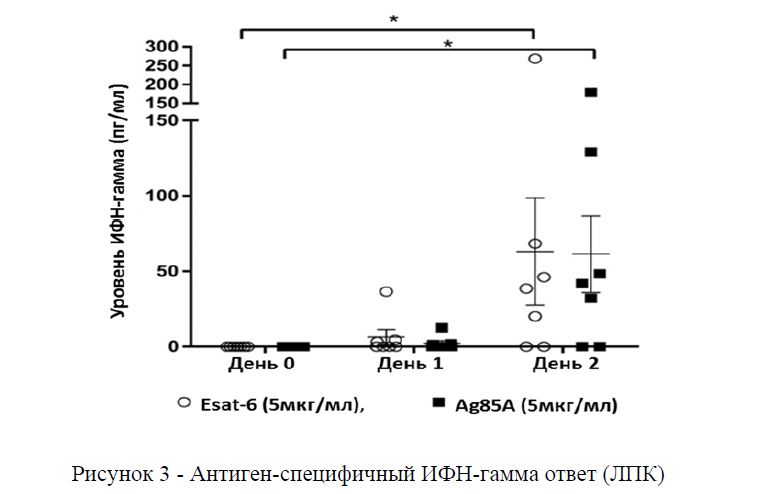
Рисунок 3 - Антиген-специфичный ИФН-гамма ответ (ЛПК)
Изучение острой токсичности на мышах и морских свинках
При однократном введении вакцины TB/FLU-04L по вышеуказанной схеме падежа животных в экспериментальных группах не зафиксировано. При клиническом наблюдении после введении вакцины общее состояние (интенсивность и характер двигательной активности, координация движений, тонус скелетных мышц, поведенческие реакции, потребление воды, корма, реакция на раздражители) в течение эксперимента были в пределах нормы у лабораторных животных всех групп.
Во всех группах отмечена положительная динамика массы тела. Прирост наблюдался на 10-е сутки после введения препарата (рисунок 4,5).

Рисунок 4 - Динамика массы тела у белых мышей (n=10)
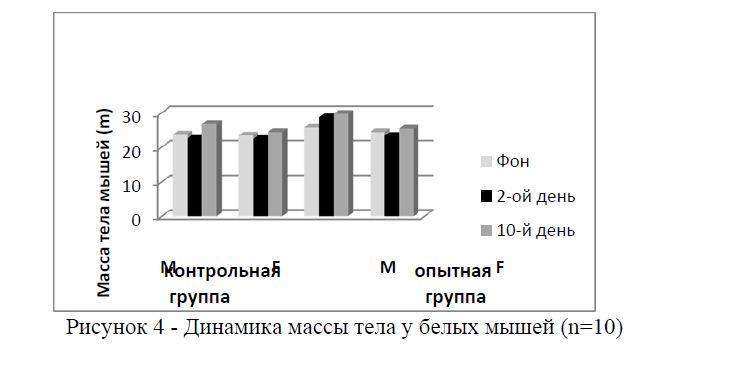
Рисунок 5 - Динамика массы тела у морских свинок (n=10)
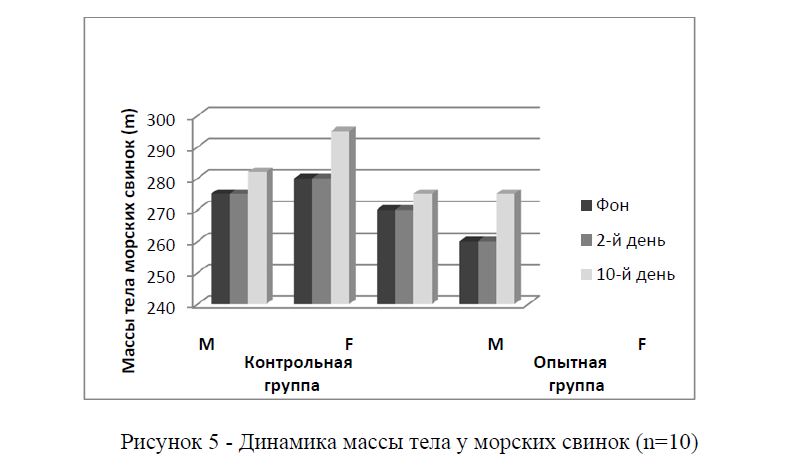
Приведенные на рисунках 4 и 5 данные показывают, что некоторое незначительное снижение массы тела имело место только на второй день после введения вакцины и в дальнейшем не отмечалось. Это проявлялось примерно в равной степени, как у опытных, так и контрольных животных. Последнее обстоятельство позволяет заключить, что в основе этого эффекта лежит не действие препарата, а процедура введения, связанная со стрессовым воздействием на животных.
На протяжении исследования изменения спонтанной двигательной активности не наблюдалось. Контрольные и опытные животные не имели достоверных отличий на всех сроках исследования.
При проведении патологоанатомического исследования не обнаружено дегенеративно-дистрофических процессов, изменений связанных с некробиозом, патологической пролиферации, воспалительно-репаративных изменений внутренних органов экспериментальных животных.
- Изучение безопасности вакцины ТВ/FLU-04L у хорьков
На протяжении всего периода наблюдения общее состояние и поведение животных экспериментальных групп соответствовало обычному. Различий по показателям между опытной и контрольной группами не отмечалось.
Интенсивность и характер двигательной активности, координация движений, тонус скелетных мышц сохранялись на фоновом уровне. Поведенческие реакции не отклонялись от нормы.
За время наблюдения ни у одного животного не было отмечено повышения температуры тела, превышающей физиологическую норму. На рисунке 6 представлены средние значения наблюдения в целом по каждой из групп животных.
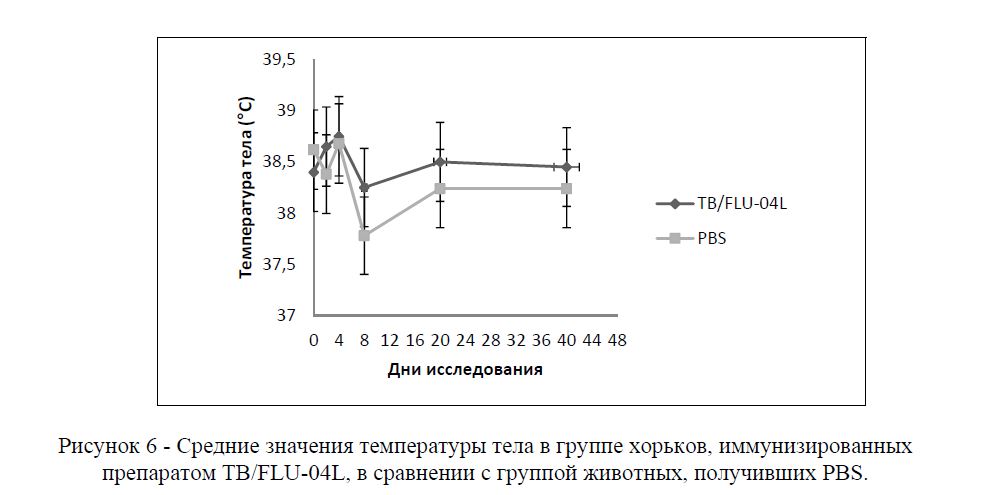
Рисунок 6 - Средние значения температуры тела в группе хорьков, иммунизированных препаратом ТВ/FLU-04L, в сравнении с группой животных, получивших PBS.
Массу тела хорьков измеряли в контрольные дни в течение 40 дней после вакцинации. Рисунок 7 иллюстрирует показатели массы тела в группе иммунизированных животных в сравнении с контрольной группой.
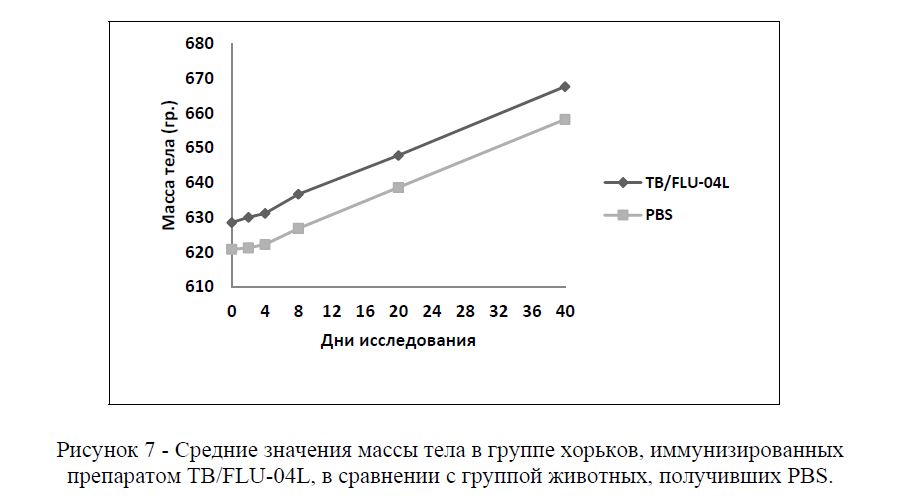
Рисунок 7 - Средние значения массы тела в группе хорьков, иммунизированных препаратом ТВ/FLU-04L, в сравнении с группой животных, получивших PBS.
За время наблюдения не зафиксировано снижения массы тела иммунизированных животных, значимых различий массы тела животных между двумя исследованными группами не выявлено.
При патоморфологическом исследовании изъятых органов (сердце, легкие, печень, почки, селезенка) на 4-й день деструктивных изменений не было выявлено.
Обсуждение результатов Разработка методов «обратной генетики» для вируса гриппа позволила задуматься о возможности использования аттенуированных вакцинных штаммов в качестве векторов для экспрессии антигенов других возбудителей. Концепция гриппозного вектора основана на полученных методами «обратной генетики» рекомбинантных штаммах вируса гриппа с модифицированным по длине геном NS.
Ранее было доказано, рекомбинантные вирусы гриппа, содержащие NS ген, кодирующий только половину нормального размера NS1 белка, резистентны к действию цитокинов и обладают способностью к репликации их [14]. При оценке иммуногенности на обезьянах при интраназльном введении был индуцирован клеточный иммунный ответ по выработке ИФН-гамма в ответ на специфическую стимуляцию in vitro. В РТ-ПЦР было показано, что вакцинный вирус неспособен к репродукции в респираторном тракте животных.
Результаты доклинических исследований определения острой токсичности отечественной векторной вакцины ТВ/FLU-04L были аналогичны результатам доклинических исследований зарубежных вакцин [15-16].
Исследуемая вакцина является безопасной на основании данных клинического наблюдения, в результате которых установлено, что показатели массы тела и показаний термометрии у хорьков до и после введения вакцины были в пределах нормы. Таким образом, установлено, что вакцина не оказывает токсического влияния на организм экспериментальных животных.
Выводы Разработанная в НИИПББ интраназальная векторная вакцина ТВ/FLU- 04L для профилактики туберкулеза на основе рекомбинантного гриппозного штамма, экспрессирующего протективные микобактериальные антигены ESAT-6 и Ag85A:
- в дозе 105 ТИД50/животное при интраназальном введении полностью безвредна для яванских макак Macaca fascicularis 2,5 - 6 летнего возраста;
- вакцинный вирус неспособен к репродукции в респираторном тракте Macaca fascicularis;
- в дозе 105 ТИД50/ животное при интраназальном введении индуцирует клеточный иммунный ответ по выработке ИФН-гамма клеток;
- не оказывает токсического влияния на организм белых мышей и морских свинок в дозах превышающих рекомендованную для человека;
- безопасна для хорьков при интраназальном введении в дозе 105 ТИД50/ животное.
Литература
- Руководство по лечению туберкулеза у детей, для национальных программ борьбы с туберкулезом, 2006/World Health Organization WHO_HTM_TB 371.
- Surveillance of Tuberculosis in Europe – Euro TB (In VS/KNCV) and the national coordinators for tuberculosis surveillance in the WHO European Region. Report on tuberculosis cases notified in 2000. Saint-Maurice, Institute de Veille Santaire, 2003
- Под редакцией Исмаилова Ш.Ш. Статистический обзор по туберкулезу в Республике Казахстан.//Статистический сборник– 2011. С. 5-13.
- Ann , Graham J. Hatcha, Simon O. Clarka, Karen E. Goocha, и другие /Evaluation of vaccines in the EU TB Vaccine Cluster using a guinea pig aerosol infection model of tuberculosis/ Tuberculosis (2005) 85, P 29–38
- Gupta D. & Katoch V.M. /Animal models of tuberculosis for vaccine development/ Indian Journal of Medical Research – 2009. - Vol. 129. – P. 11 – 19.
- Под редакцией Исмаилова Ш.Ш. Статистический обзор по туберкулезу в Республике Казахстан.//Статистический сборник– 2008. С. 5-9.
- Асанжанова Н.Н., Табынов К.К., Кыдырбаев Ж.К., Сансызбай А.Р., Хайруллин Б.М., Рыскельдинова Ш.Ж., Кожамкулов Е.М., Инкарбеков Д.А., Гоцкина Т.М., Сатыбалдиева Ж.А., Шин С.Н., Шнаукшта В.С. Доклиническое испытание острой токсичности сезонной трехвалентной гриппозной сплит-вакцины на модели лабораторных животных // Сборник статей юбилейной научно–практической конференции НИИгриппа «Грипп: эпидемиология, вирусология, профилактика и лечение», г. Санкт-Петербург, РФ С.57- 58
- Правила проведения доклинических (неклинических) исследований биологически активных веществ от 19 ноября 2009 г.
- Европейская конвенция о защите позвоночных животных, используемых для экспериментов или в иных научных целях (ETS N 123) Страсбург, 18 марта 1986 г.
- Каркищенко Н.Н., Руководство по лабораторным животным и альтернативным моделям в биомедицинских технологиях М., 2010. – С. 123-151.
- Red J., Muench H. A simple method of estimating fifty percent endpoints // Am J Hyg. 1938. – V.27. – P. 493 – 497.
- Миронов А.Н. и др. Методические рекомендации по оценке аллергизирующих свойств лекарственных средств. В сб. Руководство по проведению доклинических исследований лекарственных средств М., Минздрав РФ – Ч.2 – С. 52-61.
- Hodge et Clinical Toxicology of Commercial Products. Acute Poisoning, Ed. IV, Baltimore, 1975)
- Kittel C1, Sereinig S, Ferko B, Stasakova J, Romanova J, Wolkerstorfer A, Katinger H, Egorov Rescue of influenza virus expressing GFP from the NS1 reading frame // Virology. 2004 Jun 20 - 324(1). – P. 67-73.
- Миронов А.Н., Бушменков Д.С., Дылдина Н.В., Романова А.А., Цаан А.А., Брызгалова С.И., Никитина О.В., Колбасов С.Е. Результаты доклинического изучения гриппозной живой моновалентной вакцины «ИНФЛЮВИР».//Журнал микробиологии эпидемиологии и иммунологии. – 2010. - №2. – С.35 – 39. УДК 616-074(075.32)
- Миронов А.Н., Романова А.А., Дылдина Н.В., Бушменков Д.С., Цаан А.А., Алсынбаев М.М., Загидуллин Н.В., Колбасов С.Е. Результаты доклинического изучения гриппозной инактивированной субъединичной адсорбированной моновалентной вакцины«ПАНДЕФЛЮ».//Журнал микробиологии эпидемиологии и иммунологии. – 2010. - №3.– С.27 – 32. УДК 616-074(075.32)