Аннотация В работе предоставлены результаты исследовании по выделению чистых иммуноглобулинов класса G из cыворотки крови коров. Выделение предварительно очищенных белков, содержащие все классы иммуноглобулинов осуществлено каприловой кислотой. Высокоочищенные препараты иммуноглобулинов G1 и G2 получены колоночной хроматографией на ДЭАЭ - сефадексе А-50. Проверка чистоты выделенных белков и их идентификация выполнена электрофорезом в агаровом геле и иммуноэлектрофорезом.
Ключевые слова: Белки, сыворотка крови, белки сыворотка крови, иммуноглобулины, иммуноглобулин G, иммуноглобулины М, иммуноглобулин А, электрофорез.
Введение Иммуноглобулины класса G – главные носители специфических антител (1, 2,3,4). В этих фракциях находится основная масса антител против вирусов и различных бактерий. У человека IgG встречается в виде четырех подклассов: G1, G2, G3 и G4, различающихся строением постоянных участков тяжелых цепей, биологическими и антигенными свойствами. У овец (Жумашев и др. 1985) и крупного рогатого скота (Туганбекова, Жумашев, Сеитов, 1981; Жумашев и др. 1982) обнаружили и идентифицировали два подкласса иммуноглобулинов G, причем в сыворотке крови этих видов животных иммуноглобулин G1 преобладает над G2. Биологическое значение иммуноглобулинов G заключается в том, что они составляют основу иммунного статуса животных. Однако выделение и получение чистых препаратов иммуноглобулинов класса IgG в виде подклассов - IgG1и IgG2 у животных представляют серьезные трудности из- за близости их физико-химических и антигенных свойств
Материалы и методы исследования Материалом для выделения иммуноглобулинов класса G служила сыворотка двух клинически здоровых коров алатауской породы. Выделение иммуноглобулинов класса G состояло из двух этапов:
а) получение предварительно очищенного белка каприловой кислотой, б) получение высокоочищенных иммуноглобулинов G1 и G2 ионообменной хроматографией на ДЭАЭ-сефадексе А-50.
Выделение иммуноглобулинов каприловой кислотой
Для выделения иммуноглобулинов класса G использовали надосадочную жидкость, получаемую каприловой кислотой (Жумашев. 1994). Нормальную сыворотку крови разбавляли 0.1 н раствором уксусной кислоты до содержания белка 50 г/л. доводя ее рН до
5.0. К разбавленной сыворотке крови коров медленно, по каплям добавляли каприловую кислоту, из расчета 6 мл на100 мл разбавленной сыворотки.
После добавления каприловой кислоты смесь перемешивали в течение 30 минут магнитной мешалкой. Осадок удаляли центрифугированием, рН надосадочной жидкости, где содержались иммуноглобулины, доводили до 7.3 и использовали для колоночной хроматографии.
Колоночная хроматография на ДЭАЭ – Сефадексе А-50
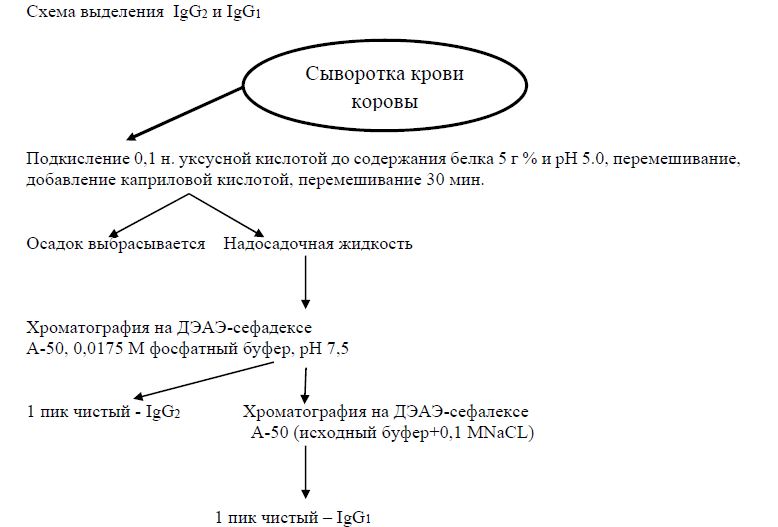
Процесс выделение IgG1 и IgG2 можно представить в виде схемы.
Выделение IgG2. Иммуноглобулин G2, получали хроматографией на ДЭАЭ – сефадексе А-50, пропуская через колонку 0,0175 М фосфатный буфер, рН 7,5.
Сыворотка крови коровы, белки , полученные каприловой кислотой и препараты IgG 2 и IgG1 выделенные колоночной хроматографией на ДЭАЭ-сефадексе А-50 были исследованы электрофорезом в агаровом геле и иммуноэлектрофорезом. Электрофорез в агаровом геле проводили в боратно-ацетатном буфере, рН 8,6, в электрофоретической камере, сделанной из плексигласа .Состав буфера: 43,55 г ацетата натрия, 52,58 г борной кислоты и 76,28 г буры растворяли в 10 л дистиллированной воды. рН буфера - 8,6.Очистка и приготовление 2% раствора агара.43 гагара вносили в колбу вместимостью 2 л, заливали дистиллированной водой, перемешивали оставляли на сутки. Сменяли воду еще 2 раза. После осветления промывной жидкости воду сливали через марлевые фильтры, заливали агар свежей порцией дистиллированной воды до отметки 2 л и расплавляли его на водяной бане. Расплавленный до однородного состояния горячий раствор агара фильтровали на воронке Бюхнера через ватномарлевые фильтры. Фильтрат охлаждали при комнатной температуре до 70оС, затем снова нагревали в кипящей водяной бане и повторно отфильтровывали. Горячий раствор агара разливали в колбы вместимостью 0,5 л, консервировали мертиолатом и хранили в холодильнике при 4°С.
Заливка агарового геля. Камеру устанавливали на строго горизонтальной поверхности и заливали 1% - раствором агара в боратно-ацетатном буфере, охлажденном до 43-45оС. После застывания геля в кюветах заливали всю верхнюю часть подноса раствором агара до образования слоя толщиной 4-5 мм. Затем в середине пластинки устанавливали трафарет для образования лунок.
Нанесение исследуемых образцов.
После формирования геля трафарет вынимали и в образовавшиеся лунки наносили исследуемые пробы.0,25 мл сыворотки крови коровы разбавляли 0,75 мл изотонического раствора хлорида натрия и к подгретому до 38-40° С образцу добавляли 1 мл 2% агара.После тщательного перемешивания образцы наносили в лунки. Поверхность лунок заплавляли 2% раствором агара и через 10 мин аппарат подключали к электрической сети. Проведение электрофореза: боратно-ацетатный буфер, рН 8,6, сила тока 100 мА, напряжение 220 В, источник питания УИП-1, электроды-платиновые, продолжительность электрофореза 7 ч.
Фиксация белков, после окончания электрофореза пластинку с гелем вынимали из подноса и погружали в фиксирующий раствор N 1 (200 мл уксусной кислоты доводили до 2 л водой). Через 15 мин гель переносили с пластинки на стекло такого же размера и оставляли в растворе на 3 ч., затем переносили в раствор № 2 (140 мл глицерина и 100 мл уксусной кислоты), которую доводили до 2 л водой и оставляли на 1 ч.
Сушка геля. После фиксации белков поверхность геля покрывали фильтровальной бумагой, пропитанной 5% раствором уксусной кислоты, следя за тем, чтобы не оставались пузырков воздуха между гелем и бумагой. Электрофореграмму высушивали при комнатной температуре в вытяжном шкафу.
Окрашивание и отмывание электрофореграмм.2 г краски амидо-черного 10Б небольшими порциями растворяли в 2 л 10% раствора уксусной кислоты и после полного растворения краски раствор отфильтровали через складчатые бумажные фильтры. Высушенную гелевую пластинку вместе с бумагой погружали в раствор краски и через 10 мин удаляли бумагу, легко отстающую от геля. Окрашивание проводили 2 ч, затем краску сливали и гелевую пластинку отмывали от избытка краски фиксирующими растворами №1 и №2. Отмытую от краски агаровую электрофореграмму высушивали при комнатной температуре.
Иммуоэлектрофорезпроводился также в агаровом геле с использованием боратно– ацетатного буфера, рН 8.6 и антисывороток против белков быка.
Результаты исследования и их обсуждение. Электрофоретическое и иммуноэлектро-форетическое изучение надосадожной жидкости показало, что при добавлении каприловой кислоты в сыворотку, при рН 5,0 осаждаются все белки, кроме IgG1 и IgG2, а также IgМ. Однако иммуноэлектрофорезом обычно обнаруживаются следы IgA, β–и редко α-глобулинов. По нашим данным, с помощью каприловой кислоты относительно легко можно выделить достаточно чистые препараты иммуноглобулинов G1 и G2 из сыворотки крови крупного рогатого скота.Электрофоретическое изучение белкового состава сыворотки крови коровыи препаратов полученных каприловой кислотой показана на рис.1 и 2.



Выводы Из сыворотки крови коровы каприловой кислотой, получена фракция белка, состоящая из иммуноглобулинов G1 и G2 c примесью иммуноглобулинов М и А.
Важным результатом проведенной работы заключается в том, что методом колоночной хроматографии на ДЭАЭ-сефадексе А-50 получены наиболее важные иммуноглобулины – носители специфических антител- IgG1 и IgG1. Иммуноглобулиновый состав препарата, полученного каприловой кислотой и чистота полученных хроматографией иммуноглобулинов доказана электрофорезом в агаровом геле и иммуноэлектрофорезом. Полученные препараты общих иммуноглобулинов и иммуноглобулинов G1 и G2 могут быть использованы как важный фактор повышения иммунного статуса новорожденных телят.
Литература
- Жумашев Ж.Ж., Алимжанова Ш.С. Выделение и характеристика иммуноглобулинов овец // Вестн. с-х. науки Казахстана. – 1981. - N – С. 61-66.
- Жумашев Ж.Ж., Туганбекова М.А., Сеитов З.С. Количественное определение иммуноглобулинов и белков сыворотки крови коров алатауской породы // Изв. АН КазССР. Сер.биол. – 1982. - N 2. – С. 75-79.
- Жумашев Ж.Ж., Алимжанова Ш.С., Туганбекова М.А., Сеитов З.С., Турсынбаев К.Ш. Выделение, идентификация и количественное определение иммуноглобулинов в сыворотке крови овец и крупного рогатого скота. / Методические рекомендации. – Алма- Ата, 1985. – 50 с.
- Жумашев Ж.Ж., Мартинес М.Р., Туганбекова М.А., Сеитов З.С. Выделение и иммунохимическая характеристика иммуноглобулинов крупного рогатого скота // Вестн. АН. КазССР – 1981 – N8. – С.60-67.
- Жумашев Ж.Ж., Алимжанова Ш.С., Горяев М.И., Сеитов З.С. Электрофоретическое изучение белкового состава сыворотки овец // Изв. АН. КазССР. Сер.биол. – 1973. - N 5. – С. 66-71.
- Жумашев Ж.Ж., Сеитов З.С., Туганбекова М.А., Фогель Н.А. Алимжанова Ш.С. Иммуноэлектрофоретический спектр иммуноглобулинов овцы, коровы и лошади // ХI Менделеевский съезд по общей и прикладной химии. / Биохимия. – М.: Наука, 1975 – С. 57.
- Жумашев Ж.Ж, Алимжанова Ш.С., Горяев М.И., Сеитов З.С. Электрофоретическое изучение белкового состава сыворотки овец // Изв. АН. КазССР. Сер.биол. – 1973. - N 5. – С. 66-71.