Культуры пыльников и изолированных микроспор являются самыми технологичным методами андрогенеза на сегодняшний день. Это надежные и эффективные методы получения удвоенных гаплоидов. Для получения дигаплодных линий яровой мягкой пшеницы в культуру пыльников введены 10 гибридов F1-F3 поколения и 3 сорта. По всем генотипам изучен эмбриогенез на разных вариантах жидких питательных сред для индукции и их регенерация. Выделены 4 отзывчивых генотипа к технологии культуры пыльников (Казахстанская 25 х TR3, Казахстанская 25 х TR1, Самгау, Кайыр). Получено 51 зеленых растений-регенерантов.
Введение
За последние годы значительные достижения биотехнологии в области сельского хозяйства достигнуты в широком использовании гаплоидной технологии. Роль гаплоидной технологии в селекции велика. Применение ее позволяет быстрее найти нужную комбинацию, сокращает время создания сорта. Опубликованы данные о получении дигаплоидов более 200 изучаемых видов [1,2,3]. Интеграция технологии гаплоидии вместе с другими имеющимися биотехнологическими инструментами, такие как маркерная селекция (MAS), индуцированного мутагенеза и генноинженерные технологии могут значительно ускорить селекцию сельскохозяйственных культур [4]. При этом данная технология у пшеницы сопровождается рядом проблем: низкий процент выхода дигаплоидных растений, большой процент выхода безхлорофильных проростков (альбиносов), воспроизводимость полученных результатов в различные сезоны и для различных генотипов низкая. Учеными разрабатываются эффективные протоколы и непрерывно оптимизируются питательные среды, условия культивирования, предобработка и другие факторы, увеличивающие выход дигаплоидных линий пшеницы.
В рамках проекта «Создание методами классической селекции и прикладной биологии адаптивные к различным экозонам, устойчивые к болезням, высокопродуктивные, качественные сорта озимой пшеницы и тритикале», регистрационный номер 0115РК02302 (2015-2017гг.) в Казахском НИИ земледелия и растениеводства проводятся исследования по получению дигаплоидных линий из гибридов F1-F3 поколения методом культуры пыльников.
Материал и методика исследований
Материалом исследований служили 10 гибридов F1-F3 поколения и 3 сорта яровой мягкой пшеницы (Самгау, Кайыр, Казахстанская 15) для отработки критических точек технологии.
Все донорные растения яровой мягкой пшеницы были выращены на полевом стационаре отдела зерновых культур и отдела яровой мягкой пшеницы в два срока посева. Оценка стадии развития микроспор определялась по общепринятой методике временных давленых препаратов при увеличении х1000 на Микроскопе Meiji Techno серии МТ4000 [5].
Стерилизация колосьев проводилась 20% раствором гипохлорита натрия с каплей Твин-80 в течение 8-10 мин и дальнейшей промывкой стерильной дистиллированной водой. После холодовой предобработки колосьев при температуре +2-4°C в течение 20-25 дней [6] пыльники были выделены из колоса в асептических условиях и помещены в пластиковые чашки Петри диаметром 50 мм (150-200 пыльников/чашка Петри), содержащую 6 мл жидкой питательной среды для индукции. В раствор был добавлен антибиотик (цефатоксим) с концентрацией 200 мг/л для предотвращения контаминации. В течение трех дней пыльники подвергли высокотемпературному шоку (30-35оС), после чего они были перенесены в термостат с температурой 25°C до появления новообразований [7].
Для эксперимента были использованы 3 варианта питательных сред для индукции:
- MS (1) (Murashige & Skoog, 1962), с добавлением 90 г/л мальтозы, 2 мг/л 2,4-Д, 30 г/л фиколл 400.
- MS (2) (Murashige & Skoog, 1962), с добавлением 90 г/л мальтозы, 2 мг/л 2,4-Д;
- АП по прописи АЦФГР [7] .
С первой недели введения пыльников в жидкую питательную среду для индукции проводились цитологические наблюдения при увеличении х40 на Микроскопе Meiji Techno серии МТ4000.
Образовавшиеся из микроспор эмбриоподобные структуры (ЭС) были пересажены на среду для регенерации (базовая среда Murashige & Skoog с добавлением 2 мг/л кинетина, 4 мг/л зеатина, 3 г/л Phytogel и 30г/л сахарозы) [8] .
Учет образования ЭС проводился в соотношении с количеством пыльников в одной чашке Петри.
Результаты исследований
Колосья донорных растений были отобраны на стадии средней и поздней одноядерной микроспорs, рисунок 1. На этой стадии микроспоры являются самыми восприимчивыми к андрогенной индукционной обработке. В результате цитологического контроля было установлено, что одноядерная стадия развития микроспор соответствует морфологической фазе, когда влагалище второго листа от флагового находится посередине колоса (пыльник темно-зеленого цвета).

Для увеличения частоты выхода каллусов и спонтанного удвоения хромосом растения подвергались холодовому стрессу в течение 20-25 дней. Выход микроспор из пыльцевого мешка в питательную среду протекал очень быстро и составил 80-90%. Цитологические наблюдения за состоянием микроспор показали высокий процент жизнеспособности микроспор (75-85%).
В культуре пыльников после 3-4 недель культивирования наблюдались первые эмбриоподобные структуры, полученные из микроспор, которые стали видимыми в жидкой среде. Каждую неделю проводились цитологические наблюдения, учеты за делением микроспор и развитием каллусов и эмбриоструктур (рисунок 2).

Рисунок 2 – Эмбриогенез в культуре пыльников яровой пшеницы
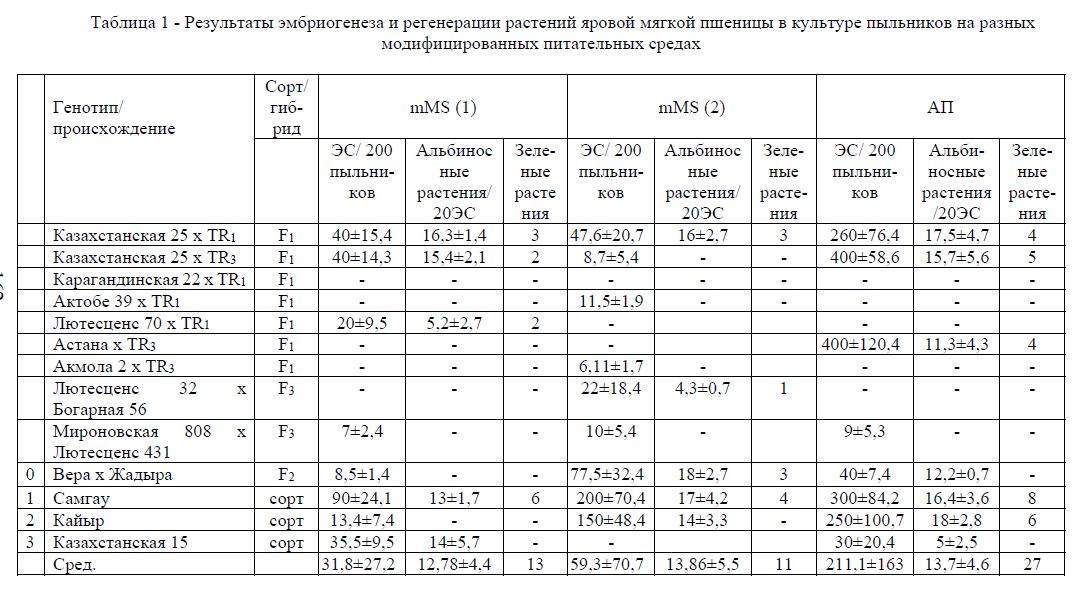
Результаты эмбриогенеза и регенерации растений яровой пшеницы в культуре пыльников представлены в таблице 1. Выход эмбриоподобных структур варьировал на разных питательных средах от 7 до 400 ЭС/200 пыльников одной чашки Петри. По результатам оценки образования эмбриоподобных структур на разных вариантах питательных сред выделены отзывчивые генотипы: Казахстанская 25 х TR3, Казахстанская 25 х TR1, Самгау, Кайыр. У гибрида Карагандинская 22 х TR1 не было зафиксировано образование ЭС на всех трех вариантах питательных сред. Низкую отзывчивость на технологию культуры пыльников показали гибриды Актобе 39 х TR1, Акмола 2 х TR3, Мироновская 808 х Лютесценс 431, Лютесценс 32 х Богарная 56 у которых из микроспор в результате деления образовалось в среднем от 0 до 22 ЭС с одной чашки Петри. Наиболее высокий выход ЭС был получен на среде для индукции по прописи АЦФГР (до 400 ЭС).
Эмбриоструктуры достигшие 2-2,5 мм пересаживались на среду для регенерации в чашки Петри 90 мм диаметром в количестве 18-20 ЭС. Более мелкие ЭС оставляли в среде для дальнейшего роста.
Оценка регенерации гибридов и сортов пшеницы показала, что выход альбиносных растений (безхлорофильных проростков) был высоким и составил 13,4 шт с одной чашки Петри (из 20 ЭС), что составляет 67%. Регенерация альбиносных растений пересаженных из среды mMS (1) составила в среднем 12,78 шт., из среды mMS (2) – 13,86 шт. и из среды АП по прописи АЦФГР - 13,7 шт с одной чашки Петри.
Выход зеленых растений был очень низким. По всему опыту в настоящее время получено 51 зеленых растений, из них из среды mMS (1) - 13 шт., из среды mMS (2) – 11 шт. и из среды АП по прописи АЦФГР - 27 шт.
По нашим наблюдениям, одним из критических факторов, влияющих на регенерационную способность, является степень развития эмбриоида. Если вовремя не пересадить зрелый эмбрион (достигшие 2-3 мм) на среду для регенерации, возможен процесс его дедифференцировки. При раннем пассировании – развития эмбриоида не происходит.
Следующим этапом является адаптация растений – регенерантов в грунте. Этот этап является наиболее критическим этапом в культуре пыльников. Среди полученных зеленых растений были отобраны зеленые проростки на стадии трех листьев с хорошо развитой корневой системой для высадки в грунт. В настоящее время проводятся наблюдения за адаптацией и основными фазами развития растений.
Таблица 1 - Результаты эмбриогенеза и регенерации растений яровой мягкой пшеницы в культуре пыльников на разных модифицированных питательных средах
Выводы
Исследование технологии культуры пыльников на трех питательных средах для индукции эмбриогенеза позволил выделить среду АП по прописи АЦФГР, как наиболее эффективную. Выход на данной среде эмбриоподобных структур из микроспор составил в среднем 200-250 ЭС с одной чашки Петри.
Выделены 4 отзывчивых генотипа к технологии культуры пыльников (Казахстанская 25 х TR3, Казахстанская 25 х TR1, Самгау, Кайыр).
Зафиксирован высокий выход безхлорофильных проростков (альбиносов) – 13,4 шт из 20 каллусов, что составляет 67%. Получено 51 шт. зеленых растений.
Литература
- Wedzony M., Foster B.P., Zur I., Golemiec E., Szechynska-Hebda M., Dubas , Gotebiowska G. Progress in doubled haploid technology in higher plants // В кн.: Advanced in haploid production in higher plants / под ред. A.Touraev, B.P. Foster, E.M. Jain. - SpringerScience + BusinessMedia B.V., 2009. – Р. 1-35
- Weyen J. Barley and wheat doubled haploids in breeding // В кн.: Advanced in haploid production in higher plants / под ред. Touraev, B.P. Foster, E.M. Jain. - SpringerScience + BusinessMedia B.V., 2009. – Р. 179-189.
- Germana M.A. Anther culture for haploid and doubled haploid production // Plant Cell Tiss Org Cult. - 2011. - Vol. 104. - P. 283-300.
- Zheng M.Y. Microspore culture in wheat (Triticum aestivum) — doubled haploid production via induced embryogenesis // Plant Cell Tiss Org - 2003. - Vol. 73. - P. 213-230.
- Паушева З.П. Практикум по цитологии растений. Москва: Агропромиздат,Вып. 4. – С.58-100.
- Lantos, , Weyen, J., Orsini, J. M., Gnad, H., Schlieter, B., Lein, V., Pauk, J. (2013). Efficient application of in vitro anther culture for different European winter wheat ( Triticum aestivum L.) breeding programmes// Plant Breeding, 132(2), 149–154. doi:10.1111/pbr.12032
- Исмагул А., Башабаева Б.М., Искакова Г., Абугалиева А.И., Елибай С., Кененбаев С.Б. Культура изолированных микроспор пшеницы. Методическое пособие, Алматы, 2013 – 19 с.
- Rubtsova , Gnad H., Melzer M., Weyen J., & Gils M. (2013). The auxins centrophenoxine and 2 , 4-D differ in their effects on non-directly induced chromosome doubling in anther culture of wheat (T . aestivum L.). Plant Biotechnol Rep, 7, 247–255. doi:10.1007/s11816-012-0256-x