Лейкоз крупного рогатого скота (ЛКРС) является широко распространенным заболеванием и наносит огромный ущерб, связанный с гибелью и преждевременной выбраковкой высокопродуктивных коров, снижением продуктивности, качества молока и рождением телят с иммунодефицитами [1].
ЛКРС — хроническая инфекционная болезнь, вызываемая РНК-содержащим вирусом лейкоза крупного рогатого скота (ВЛКРС или BLV — bovine leukosis virus) из семейства Retroviridae. Лейкозом болеет крупный рогатый скот (КРС) всех возрастов, но в основном молочных пород. Вначале заболевание протекает бессимптомно, а затем переходит в персистентный лимфоцитоз (persistent lymphocytosis (PL)) и (или) образует опухолевидные разрастания в кроветворных и других органах и тканях. Клинически болезнь проявляется чаще у животных в возрасте старше 4 лет [2].
Источником возбудителя ВЛКРС является инфицированное животное, поэтому заражение может происходить при совместном содержании здоровых и инфицированных ВЛКРС животных. В этой связи на первый план ставятся вопросы раннего выявления животных — носителей ВЛКРС.
Некоторые исследования подтверждают факт присутствия антител к ВЛКРС в сыворотке крови человека [3]. Установлено, что работники рынков, непосредственно контактирующие с инфицированным мясом КРС, подвергаются трехкратно повышенному риску заболевания миелоидной лейкемией и высокому риску заболевания раком легких по сравнению с контрольной интактной группой [4]. Последние исследования, проведенные в Южной Корее, показали, что инфекция животных не является причиной заболеваемости человеческой лейкемией и раком легких у корейцев [5].
Основу диагностики ЛКРС составляет серологический метод исследования, т.е. степень реакции иммунодиффузии (РИД) в агарозном геле, но он имеет относительно низкий предел чувствительности. Кроме того, случаи отрицательных ответов в тест-системе РИД при тестировании инфицированных ВЛКРС могут быть связаны с индивидуальными особенностями взаимодействия в системе «вирус-хозяин» [6]. Иммуноферментный анализ (ИФА) является наиболее чувствительным среди серологических реакций и может также применяться для молока [7]. Раннее диагностирование зараженных телят затруднено тем, что антитела к ВЛКРС, передаваемые молозивом, невозможно отличить от антител, возникающих в результате их естественного инфицирования вирусом лейкоза.
Известно, что ВЛКРС присутствует в организме в виде ДНК-копий (провируса), встраиваясь в клеточный геном животного и при этом могут отсутствовать детектируемые антитела к ВЛКРС. Установлено, что транскрипция генома вируса ЛКРС в новых раковых клетках или лейкоцитах периферической крови у инфицированных животных плохо обнаруживается с помощью традиционных методов исследования [8]. Ее обнаружение становится возможным при применении современных молекулярно-биологических методов, в частности, метода ПЦР.
В настоящее время широко проводятся исследования по изучению генотипического разнообразия вируса лейкоза, циркулирующего на сельскохозяйственных предприятиях. Мониторинг эпизоотологической ситуации по лейкозу КРС часто проводят с помощью «nested» ПЦР по гену env. Хотя, в зависимости от подхода к генотипированию, количество генотипов вируса несколько варьирует. Так, анализ полиморфизма длин рестрикционных фрагментов (ПДРФ) env гена позволил выявить 7 генотипов вируса [9]. Современными исследователями изучается не только географическое распределение генотипов ВЛКРС, но и их возможное влияние на результаты серологических исследований.
Как диагностический метод, ПЦР характеризуется высокой специфичностью, которая обусловлена выбором праймеров и чувствительностью. Метод ПЦР может использоваться для диагностики лейкоза крупного рогатого скота наряду с серологическими методами, а также в качестве подтверждающего теста.
Целью настоящей работы является разработка duplex-ПЦР для идентификации провируса лейкоза крупного рогатого скота.
Материалы и методы
Пробы цельной крови были получены у животноводческого предприятия Акмолинской области. Препараты ДНК выделяли из лейкоцитов периферической крови животных по методу, основанному на селективном лизисе эритроцитов крови с помощью слабосолевых растворов согласно нашим модификациям и с помощью набора для выделения ДНК фирмы «Promega». ДНК оценивали по выходу мг\мл биологической жидкости (концентрация) и по «чистоте», оцениваемых как отношение А260 /А280.
В предварительных экспериментах по изучению основных генотипов ВЛКРС, циркулирующих на территории Казахстана, проведен «nested» ПЦР по гену env с последующим секвенирова-нием. Далее на основе уже полученных нуклеотидных последовательностей провируса ЛКРС, а также известных последовательностей гена env 7 охарактеризованных генотипов (http://blast.ncbi.nlm.nih.gov/Blast.cgi) был проведен дизайн олигонуклеотидных праймеров, пригодных для идентификации провируса ЛКРС и разработки ПЦР тест-системы.
Амплификацию гена провируса ВЛКРС проводили на приборе DNA Engine Tetrad 2 Cycler (Bio-Rad) с использованием подобранных олигонуклеотидных праймеров (5534 и 4932) (Синтол, Россия). В качестве внутреннего контроля (ВКО) использованы праймеры (alphafs4 и alphars4), специфичные к гену альфаглобина (a-globin) КРС (Синтол, Россия). Состав подобранной нами ПЦР реакционной смеси: dNTPs (2 mmol/l each) 2,5 pl, 10 х PCR buffer 2,5 pl, target DNA (0,05 pg/pl) 5 pl, Taq DNA polymerase 1U, 10 pmol primers 0,5 pl. Общий объем смеси доведен до 25 pl водой, свободной от нук-леаз. Температурные условия: преденатурация при 95 0C в течение 3 мин, а также 40 циклов: денатурация при 94 0C 30 сек, отжиг при 64 0C 30 сек и элонгация при 72 0C 40 сек. Последняя элонгация проводилась при 72 0C в течение 7 мин. Для визуализации ПЦР-продуктов проведен электрофорез в 2 %-ном агарозном геле при 120V с последующим окрашиванием в растворе этидиум бромида и гельдокументированием на приборе GelDoc (BioRad, США).
Результаты и их обсуждение
Результаты ПЦР представлены на электрофореграмме (рис. 1), где видно, что использование пары праймеров, специфичных к гену a-Globin, позволило генерировать ампликоны (длиной ~ 900 н.п.) из геномной ДНК, выделенной из крови серопозитивных (131, 140, 131d, 131 Pr, 140 Pr) и одного се-росомнительного (152 Pr) образцов КРС, а также у серонегативного образца (14 образец). В негативных контролях ЦК, VK, GlK), содержащих только реагенты, а также пару праймеров 4932 + 5534 (V), или alphafs4 + alphars4 (Gl), или смесь обеих пар (Mix), ПЦР-продуктов не выявлено. Кроме того, на данном рисунке видно, что при ПЦР с отдельно взятыми BLV-специфичными праймерами и в смеси с a-глобиновыми праймерами у всех серопозитивных ДНК образцов выявлен ампликон, по длине соответствующий 598 н.п. Следует заметить, что при использовании обеих пар праймеров в ПЦР-смеси не всегда образуются четко выраженные продукты (см. на рис.1 дорожки Mix с 140 Pr и 152 Pr образцами). Поэтому мы продолжили работу по оптимизации условий duplex-ПЦР с использованием смеси праймеров 4932 + 5534 и alphafs4 + alphars4, которые были лучшими парами праймеров для детекции провируса ЛКРС. Использование образцов ДНК, выделенных двумя различными методами (14, 131, 140, 131d и 140d образцы выделены по модифицированному методу, а 131 Pr, 140 Pr и 152 Pr — коммерческим набором) не показало различий при проведении duplex-ПЦР.
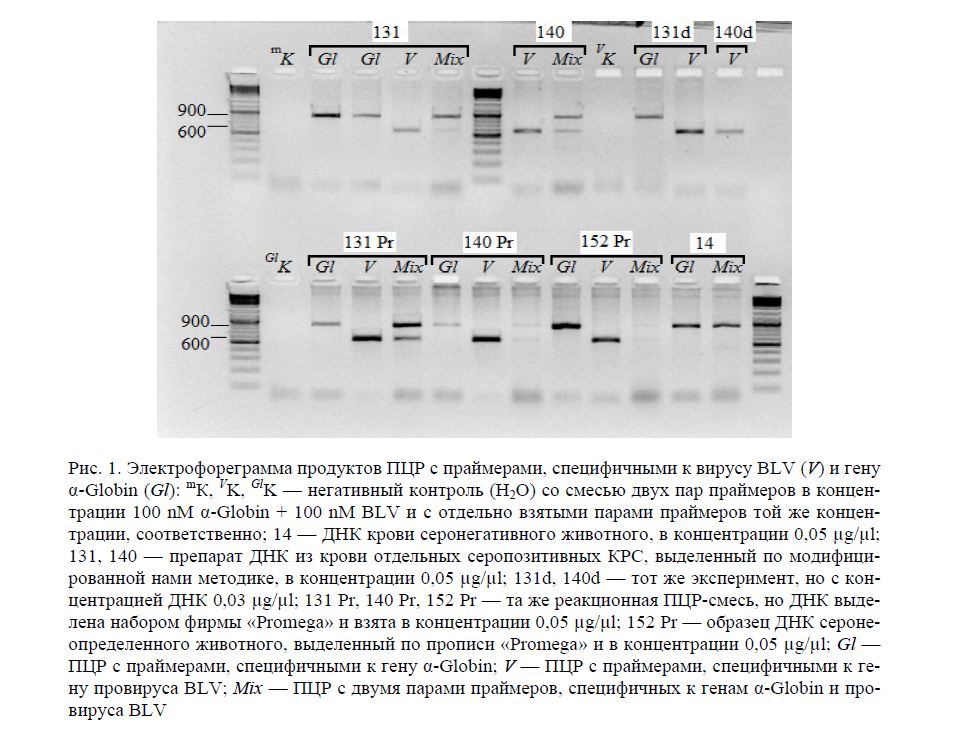
Рис. 1. Электрофореграмма продуктов ПЦР с праймерами, специфичными к вирусу BLV (V) и гену a-Globin (Gl): "Ж, VK, giK — негативный контроль (Н2О) со смесью двух пар праймеров в концентрации 100 nM a-Globin + 100 nM BLV и c отдельно взятыми парами праймеров той же концентрации, соответственно; 14 — ДНК крови серонегативного животного, в концентрации 0,05 pg/pl; 131, 140 — препарат ДНК из крови отдельных серопозитивных КРС, выделенный по модифицированной нами методике, в концентрации 0,05 pg/pl; 131d, 140d — тот же эксперимент, но с концентрацией ДНК 0,03 pg/pl; 131 Pr, 140 Pr, 152 Pr — та же реакционная ПЦР-смесь, но ДНК выделена набором фирмы «Promega» и взята в концентрации 0,05 pg/pl; 152 Pr — образец ДНК сероне-определенного животного, выделенный по прописи «Promega» и в концентрации 0,05 pg/pl; Gl — ПЦР с праймерами, специфичными к гену a-Globin; V — ПЦР с праймерами, специфичными к гену провируса BLV; Mix — ПЦР с двумя парами праймеров, специфичных к генам a-Globin и про-вируса BLV
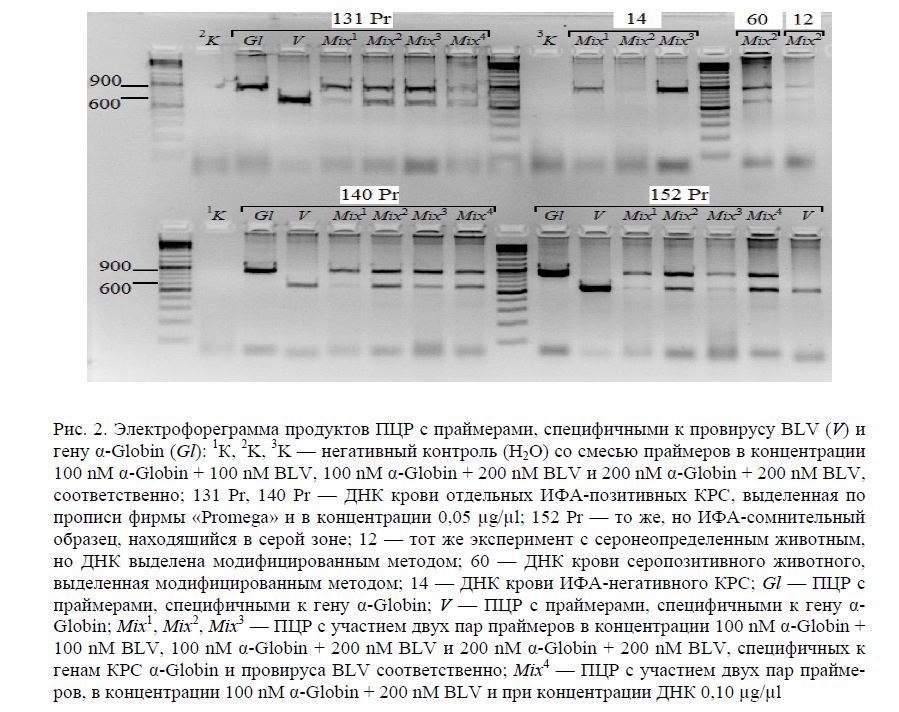
В целях подбора оптимальной концентрации каждой пары праймеров для duplex-ПЦР использованы следующие концентрации: 100 nM a-Globin + 100 nM BLV (Mix1), 100 nM a-Globin + 200 nM
BLV (Mix2), 200 nM a-Globin + 200 nM BLV (Mix3), а также Mix4 содержал ту же концентрацию праймеров, что и Mix2, но в ПЦР-смесь добавлена ДНК в концентрации 0,10 pg/pl.
Результаты ПЦР амплификации (рис. 2) образцов ДНК (131 Pr, 140 Pr,152 Pr, 60 и 12) показали, что увеличение концентрации BLV праймеров до 200 nM в смеси Mix2 позволило получить четко выраженные ПЦР-продукты обоих генов, в сравнении с Mix1, где имеется одинаковое (100 nM) содержание смеси данных праймеров. Что касается ПЦР-продуктов, полученных в смеси Mix3, то выявлено, что эквивалентное увеличение концентраций обеих пар праймеров в реакционной смеси все же приводит к большему получению ПЦР-продуктов, соответствующих контрольному гену a-Globin, чем ампликонов, по длине соответствующих гену провируса BLV (см. рис. 2, Mix3 с 131 Pr, 140 Pr,152 Pr). В негативном контроле (К) и серонегативном образце (14) ДНК продуктов амплификации прови-руса BLV не было обнаружено. При ПЦР с использованием праймеров в концентрации 100 nM a-Globin + 200 nM BLV (Mix2) и при увеличении концентрации ДНК в смеси (см. рис. 2, Mix4 с 131 Pr, 140 Pr,152 Pr) наблюдалась наработка визуально эквивалентного количества ампликонов, соответствующих генов. Это свидетельствует о существовании корреляции между исходными концентрациями ДНК и используемых праймеров и возможности улучшения ПЦР амплификации гена провирусной ЛКРС путем увеличения концентрации ДНК до 250-500 нг в ПЦР смеси.
В целях оценки воспроизводимости результатов оптимизации условий duplex-ПЦР проведена амплификация с использованием смеси праймеров в концентрации 100 nM a-Globin + 200 nM BLV (Mix2) и образцов ДНК, выделенных от 23 животных.
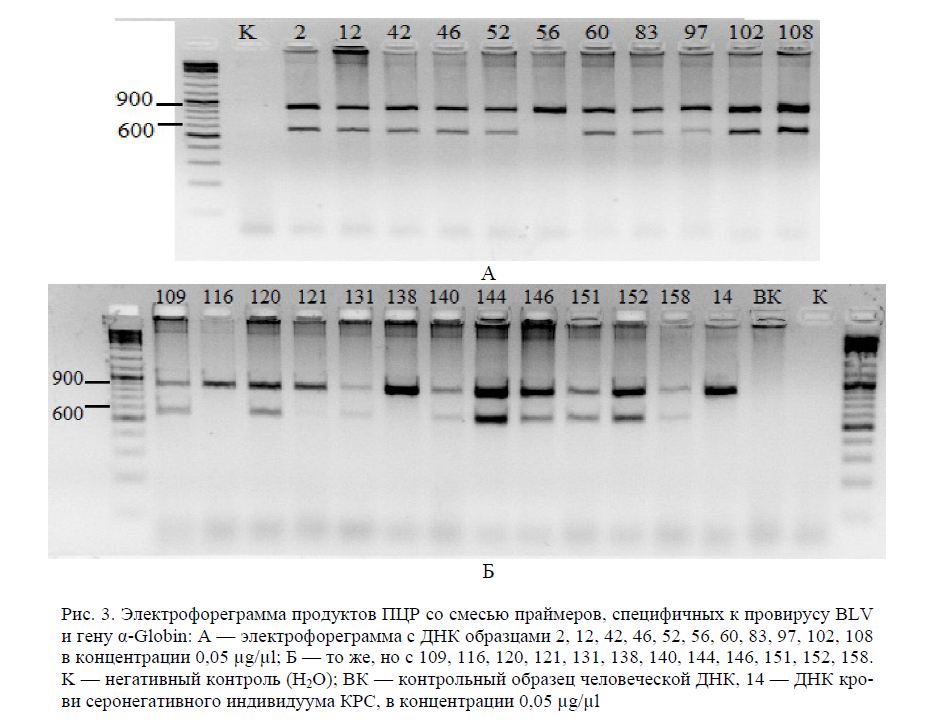
По результатам ИФА у 23 исследуемых животных были выявлены следующие 12 серопозитив-ных образцов: 42, 46, 52, 97, 102, 108, 109, 131, 138, 140, 144 и 158, а также 6 серосомнительных — 2, 12, 116, 146, 151, 152 и пять ИФА-негативных образцов — 56, 60, 83, 120 и 121. Результаты же электрофореза (рис. 3) демонстрируют, что у 11 из 12 исследуемых серопозитивных ДНК-образцов происходит амплификация ПЦР-продуктов длиной в 598 н.п., соответствующий провирусу ЛКРС. Все ИФА-серосомнительные образцы по результатам ИФА при ПЦР анализе показали наличие провируса лейкоза КРС, кроме 116-го образца (OD=0,409). После ПЦР анализа из 5 ИФА-негативных образцов выявлено наличие гена env провируса ЛКРС у 3 образцов (см. рис. 3 А и Б, 60, 83, 120 и 121). Причем количество амплифицированного гена провирусной ДНК у 121 образца было незначительным с соответствующим слабым свечением (см. рис. 3 Б, 121), что связано с низкокопийностью ДНК провируса, интегрированного в геном животного.
В предварительных экспериментах ИФА-позитивный (OD=0,593) образец 138 при ПЦР с отдельно взятой парой праймеров (4932f и 5534r), специфичных к гену провируса BLV, также показал негативный для лейкоза результат (данные не предоставлены), как и при duplex-ПЦР (см. рис.3 Б, 138). Это можно объяснить тем фактом, что при диагностировании зараженных телят можно обнаружить наличие антител ВЛКРС, которые передаются молозивом матери, и их невозможно отличить от антител, возникающих при инфекцировании животного. Кроме того, известно, что поли- и монокло-нальные антитела против поверхностного вирусного лейкозного белка gp51 обладают вируснейтра-лизующей активностью, подавляют синцитийобразующую активность вируса, препятствуют его выходу из клеток и вызывают лизис инфицированных клеток в присутствии комплемента [10]. Недостатком ИФА-тест-систем является наличие перекрестной реакции с другими антигенными детермин-тами [7].
Результаты duplex-ПЦР позволили выявить наличие ампликонов, соответствующих провирусу ЛКРС у ИФА-неопределенных (сомнительных) 2, 12, 146, 151 и 152 образцов, а также у ИФА-негативных 60, 83, 120 и 121, что объясняется установленным фактом, когда провирус BLV может интегрироваться в рассеянные сайты генома хозяина и не транскрибироваться in vivo [11], т.е. наблюдается отсутствие детектируемых BLV антител. В сыворотке крови антитела против ВЛКРС появляются обычно через 3-8 недель после заражения [2].
Заключение
В настоящее время выделение антигенных компонентов вириона ЛКРС позволило разработать различные серологические и вирусологические методы диагностики лейкоза. При этом диагностика лейкоза КРС является обоснованной при исключении неспецифической реакции иммунного ответа на антигенную стимуляцию и гистохимической идентификации клеток крови [2].
Отрицательные результаты в серологических тест-системах для выявления ЛКРС могут быть связаны не только с индивидуальными особенностями взаимодействия животного организма и вируса, но и с наличием в геноме хозяина генов противовирусной защиты и наличием в геноме вируса вариантов генов, способных наиболее эффективно воздействовать на клеточные системы организма хозяина, т. е. для более эффективной стратегии выживания [6].
Метод ИФА разработан главным образом на основе использования частично очищенного прови-русного гликопротеина gp51 и моноклональных антител к эпитопам gp51 [7]. Установлено, что специфические антитела в крови способны проявлять не только цитотоксическое, но и блокирующее действие, оказывая тем самым эффект утомления опухолевого роста. Это подтверждает, что лейкоз ассоциирован с иммунологическим дефектом организма.
Таким образом, ПЦР тест-системы для выявления патогенов животных могут служить эффективным диагностическим средством и применяться для дополнения и контроля результатов традиционных методов микробиологического и иммунохимического анализов. Для улучшения ПЦР диагностики генетически вариабельных штаммов ВЛКРС может потребоваться более, чем одна пара прай-меров, которая позволит подтвердить результаты простого ПЦР и выявить позитивные образцы среди серонегативных и вероятных ложнопозитивных результатов ИФА и РИД [12].
Результаты наших исследований позволили подтвердить наличие гена env провируса лейкоза крупного рогатого скота (BLV) в серопозитивных образцах крови, а также довыявить животных-вирусоносителей среди серонеопределенных и негативных образцов при постановке duplex-ПЦР с целевыми праймерами и праймерами, специфичными к гену КРС a-Globin, использованного в качестве внутреннего контроля.
Для диагностики интегрированного в геном животных провируса BLV предоставляется реальная возможность использования разработанного нами метода duplex-ПЦР. Основываясь на том факте, что количество копий провируса BLV в периферических одноядерных клетках крови у различных серо-позитивных животных может быть различным, то, соответственно, для улучшения ПЦР амплификации возможно увеличение финальной концентрации матричной ДНК (до 250-500 нг) при duplex-ПЦР с двухкратно большей концентрацией праймеров, нацеленных на гены провируса, в сравнении с праймерами, специфичными к гену внутреннего контроля.
Список литературы
- Староселов М.А., Басова Н.Ю. Иммунобиологические показатели инфицированных вирусом лейкоза КРС и больных лейкозом коров в сравнении с интактными // Научный журнал КубГАУ. — 2008. — № 40(6). — С. 10-18.
- Методические указания по диагностике лейкоза крупного рогатого скота / Утв. Минсельхозом РФ от 23.08.2000. N 137-2/2130.
- Johnson E.S., Nicholson L.G., DurackD.T. Detection of antibodies to avian leucosis/sarcoma viruses (ALSV) and reticuloendo-theliosis viruses (REV) in humans by ELISA // Cancer Det. Prev. — 1995. — 19. — Р. 394-404.
- Johnson E.S., Dalmas D., Noss J. et al. Cancer mortality among workers in abattoirs and meatpacking plants: an update // Am. J.Indust. Med. — 1995. — 27. — P. 3 89-403.
- Lee J., Kim Y., Kang Ch. Suk et al. Investigation of the Bovine Leukemia Virus Proviral DNA in Human Leukemias and Lung cancers in Korea // J.Korean Med. Sci. — 2005. — 20. — P. 603-606.
- Дробот Е.В. Результаты изучения генотипического разнообразия вируса лейкоза крупного рогатого скота и особенности эпизоотологического и гематологического проявления лейкоза: Автореф. дис. ... канд. биол. наук. — Новосибирск,— 22 с.
- De Giuseppe A., Feliziani F., Rutili D. et al. Expression of the Bovine Leukemia Virus Envelope Glycoprotein (gp51) by Recombinant Baculovirus and Its Use in an Enzyme-Linked Immunosorbent Assay // Clinic. and diag. lab. Immun. — 2004. — 11. — № 1. — P. 147-151.
- Jimba M., Takeshima Sh., Matoba K. et al. BLV-CoCoMo-qPCR: Quantitation of bovine leukemia virus proviral load using the CoCoMo algorithm // Retrovirology. — 2010. — 7. — P. 91-110.
- Moratorio G., Obal , Dubra A. et al. Phylogenetic analysis of bovine leukemia viruses isolated in South America reveals diversification in seven distinct genotypes // Arch. Virol. — 2010. — Vol. 155. — Р. 481-489.
- Bruck, C., Portetelle D., Mammerickx M. et al. Epitopes of bovine leukemia virus glycoprotein gpSl recognized by sera of infected cattle and sheep // Leukemia Res. — 1984. — 8. — P. 315-321.
- Kettmann R., Deschamps J., Cleuter Y. et a Leukemogenesis by bovine leukemia virus: proviral DNA integration and lack of RNA expression of viral long terminal repeat and 3' proximate cellular sequences // Proc. Natl Acad. Sci. USA. — 1982. — Vol.79. — Р. 2465-2469.
- Marsolais G., Dubuc R., Bergeron J. et al. Importance of primer selection in the application of PCR technology to the diagnosis of bovine leukemia virus // J.Vet. Diagn. Invest. — 1994. — 6. — P. 297-301.