В данной работе представлены результаты подбора адъювантов для новой векторной противобруцеллезной вакцины на основе вируса гриппа, экспрессирующих антигены В.abortus. Установлено, что новый кандидат вакцины против B. abortus - состоящий из смеси рекомбинантного вируса гриппа А, экспрессирующий рибосомальный белок L7/L12 и Omp16, при испытании на морских свинках наилучшей протективной эффективностью обладает с адъювантом Montanide Gel01, которая по данному показателю была сопоставима с коммерческой вакциной B. abortus S19
Введение
Бруцеллез представляет собой мировую проблему для здравоохранения и животноводства. Среди инфекционных болезней бруцеллез сельскохозяйственных животных занимает особое место, его удельный вес в инфекционной патологии составляет 43 %. Миграции способствуют чаще всего совместное содержание или совместный выпас разных видов животных [1-4]. Появление бруцеллеза в хозяйстве в значительной степени тормозит воспроизводство стада в связи с абортами, рождением нежизнеспособного плода и яловостью зараженных животных [5, 6].
Профилактика этого опасного заболевания среди КРС в настоящее время проводиться с использованием живых аттенуированных вакцин из штаммов B. abortus S19 и RB 51. Однако используемые в ветеринарной практике вакцины не обеспечивают 100 % защиту животных от бруцеллеза, ни одна из существующих вакцин не считается совершенной. Проблемным вопросом считается также отсутствие точного критерия определения поствакцинального иммунитета от постинфекционного [7]. Перечисленные недостатки вакцин являются одним из причин широкого распространения в настоящее время бруцеллеза, как среди крупного рогатого скота, овец, так и среди населения Казахстана [8].
Поэтому разработка эффективной и вместе с тем безопасной вакцины против бруцеллеза КРС на сегодня является актуальной проблемой.
В НИИПББ для решения данной проблемы, представляющей большую эпидемиологическую значимость для Казахстана, ведутся работы по созданию живой векторной вакцины против бруцеллеза КРС на основе вируса гриппа. С этой целью впервые были получены рекомбинантный вирус гриппа А субтипов Н5N1 и H1N1, экспрессирующие бруцеллезные рибосомальный белок L7/L12 и поверхностный мембранный белок Omp16. Для повышения эффективности вакцины для крупного рогатого скота было решено прибегнуть к подходу, способному существенно повысить протективность препарата, а именно добавление адъювантов, для повышения имуностимулируешего ответа, который выполняет ключевую роль в противобруцеллезном иммунитете.
На сегодняшний день имеется большой выбор новых коммерческих готовых адъювантных продуктов, а также адъювантов на стадии разработки и испытаний, предназначенных для разных видов животных, направленных на инициацию различных типов иммунного ответа, сочетающих в себе различные уровни показателей эффективности и безопасности. Поэтому исследования по включению различных типов адъювантов в состав вакцин весьма актуальны, их проводят большинство компаний мира, занимающихся производством биопрепаратов для ветеринарии и медицины [9, 10, 11].
В предыдущей работе для подбора адъюванта к векторной вакцине против бруцеллеза нами в качестве сравнения были использованы адъюванты Montanide Gel01 и хитозан. Наивысший уровень защиты был показан с Flu-L7/L12-Omp16-Montanide Gel01 при конъюктивальном способе введения у КРС; эффективность вакцинации составила 100%. Самая низкая эффективность вакцинации (40%) наблюдалась у КРС, вакцинированного векторной вакциной Flu-L7/L12-Omp16-chitosan [12].
В данной работе для разработки новой векторной вакцины нам были предложены другие коммерческие адъюванты для сравнения с предыдущими данными. Настоящая работа является продолжением серий исследований направленных на разработку эффективной и безопасной вакцины против B. abortus.
Материалы и методы
Приготовление образцов вакцины
Образцы вакцин были подготовлены из смеси вирусных конструкций Flu-NS1- 124-L7/L12-H5N1, Flu-NS1-124-Omp16-H5N1, накопленных в 10-суточных куриных эмбрионах (КЭ) при температуре 34°С в течение 48 ч. Полученный вируссодержащий материал вирусных конструкций объединены в смесь следующих штаммов FLU-NS1- 124-Omp 16+FLU-NS1-124-L7/L12 в соотношении 1:1, чтобы получить бивалентную вакцинную формуляцию для векторной вакцины [12, 13]. Получившуюся смесь вирусных конструкций растворяли с такими коммерческими и экспериментальными адъювантами, Montanide Gel01 (Seppic, France), V+XC55 (Россия) и AdvaxTM (Австралия) по инструкции изготовителя.
Лабораторные животные и дизайн исследований
В исследованиях использованы 42 беспородные морские свинки, весом 300-350 граммов. Морские свинки методом рандомизации были равномерно распределены на 6 групп: четыре опытные, вакцинированные векторной вакциной против бруцеллеза с использованием подкожного способа введения с такими адъювантами приготовленных как растворитель, это Montanide Gel01 (Seppic, France), V+XC55 (Россия) (n=21) и внутримышечного (n=7) методов введения AdvaxTM (Австралия) по инструкции изготовителя, одна контрольная негативная (ФБР, n=7) и одна контрольная позитивная (B. abortus S19, n=7) группы. В качестве критериев приемлемости рандомизации считали отсутствие внешних признаков заболеваний и гомогенность групп по весу тела. Животные на протяжении всего опыта имели свободный доступ к воде и стандартному корму для грызунов.
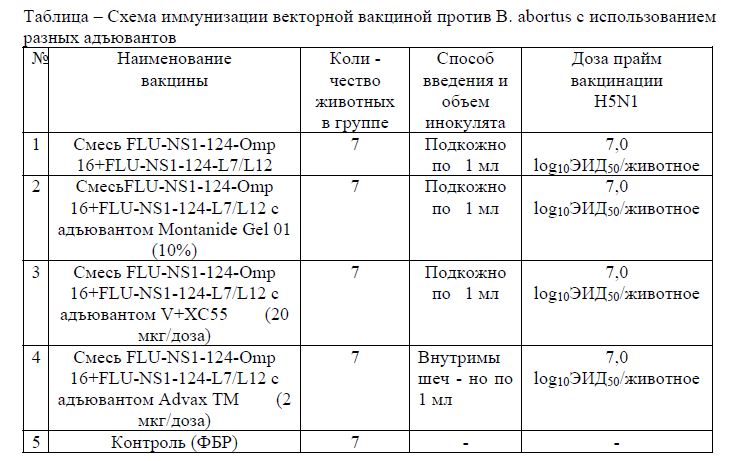
Вакцинация морских свинок векторной вакциной проводилась однократно подкожным, внутримышечным методами с использованием следующих образцов: смесь вирусных конструкций, экспрессирующих бруцеллезные белки Omp16 и L7/L12 (без адъюванта); вирусные конструкции, содержащие коммерческий адъювант Montanide Gel01 (Seppic, France), экспериментальный пептидный адъювант V+XC55 (Россия), а также коммерческий адъювант AdvaxTM (Австралия). Детальная схема иммунизации животных показана в таблице. Морским свинкам из группы негативного контроля в качестве инокулята вводили ФБР, а животным из группы позитивного контроля коммерческую вакцину B. abortus S19 в дозе 2 х 109 КОЕ/животное (подкожно).
Таблица – Схема иммунизации векторной вакциной против В. аbortus с использованием разных адъювантов
Оценка иммуногенности образцов вакцины по наличию антител к гриппозным векторам
Один из параметров оценки иммуностимулирующей эффективности подобранных адъювантов заключался в определении иммуногенности самих гриппозных векторов в составе различных образцов вакцин. Для этого у всех привитых морских свинок на сутки после вакцинации отбирались образцы сыворотки крови для исследования в реакции торможения гемагглютинации (РТГА) с целью выявления титра антигемаглютинирующих антител к гриппозным векторам. РТГА ставили по методике, описанной в наших ранних работах [14, 15].
Оценка протективности образцов вакцины
Оценку протективности образцов вакцин определяли путем контрольного заражения вакцинированных морских свинок (на 21 день после вакцинации) вирулентным штаммом B. abortus 544 подкожным способом в дозе 50 КОЕ/животное. На 30 сутки после контрольного заражения все морские свинки были умерщвлены с помощью СО2 асфиксии, вскрыты в асептических условиях для взятия следующих органов: заглоточный, нижнешейный, правый паховый, левый паховый и парааортальный лимфатические узлы, печень, почку, селезенку и костный мозг. Из изъятых органов делали посевы в пробирки со средой триптоз-соевого агара (TСA). Посевы инкубировали в термостате при температуре 37°С в течение 4 недель, в период которых периодически проводили учет роста бактериальных культур. Результаты бактериологического исследования оценивали индивидуально на животное по количеству органов, из которых выделялись культуры бруцелл (индекс инфицированности). Для сравнительного анализа рассчитывали среднее значение показателя индекса инфицированности на группу животных.
Статистическая обработка
Определяли среднеарифметические значения исследуемых параметров, а также их стандартную ошибку. Достоверность различий между показателями определяли с использованием статистической программы GraphPad Prism 6 (GraphPad Software, Inc., La Jolla, CA, USA). Значение Р< 0,05 считали значимым.
Результаты и обсуждение
Иммуногенность векторной вакцины против КРС с различными адъювантами
В экспериментальных условиях на лабораторных морских свинках установлено, что изготовленные образцы вакцин на основе разных типов адъювантов обладают различной антигенной активностью, что обусловлено различием в титрах специфических антител у иммунизированных животных. Показано, что наиболее антигенно активным оказался вариант вакцины, изготовленный с включением адъюванта MONTANIDE GEL 01 (рисунок 1). Титры антител в РТГА в этой группе животных составил 1:580±170,4 и было статистически достоверно выше (Р< 0.05) по сравнению с другими группами, привитых образцами вакцин с такими адъювантами как V+XC55 (20 мкг/доза) средний геометрический титр показал 1:250±42,6 и Advax TM (2 мкг/доза) 1:256±112,8 соответственно. В негативной контрольной группе животных антигемаглютинирующие антитела не обнаруживались (данные не показаны).
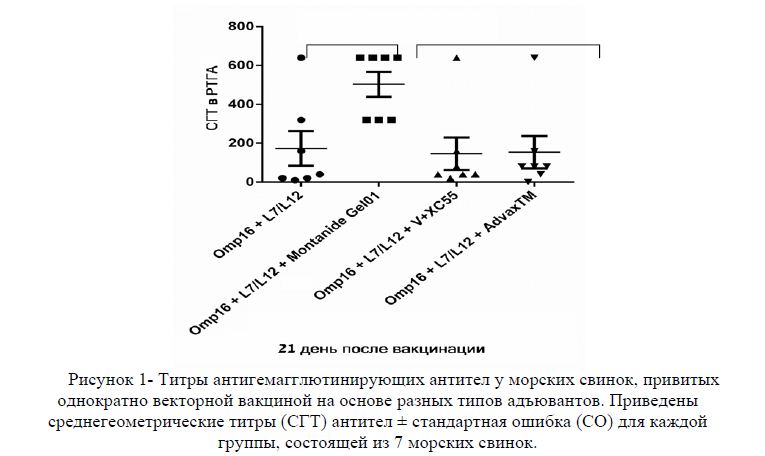
Рисунок 1- Титры антигемагглютинирующих антител у морских свинок, привитых однократно векторной вакциной на основе разных типов адъювантов. Приведены среднегеометрические титры (СГТ) антител ± стандартная ошибка (СО) для каждой группы, состоящей из 7 морских свинок.
Протективность образцов вакцин от вирулентного штамма B. abortus 544
Наиболее важным этапом настоящих исследований являлось оценка протективности векторной вакцины в зависимости от используемого адъюванта. Результаты проведенных исследований показали (рисунок 2), что все образцы векторной вакцины вне зависимости от использованного адъюванта или без него обеспечивали достоверную защиту (Р< 0.05) привитых морских свинок от B. abortus инфекции.
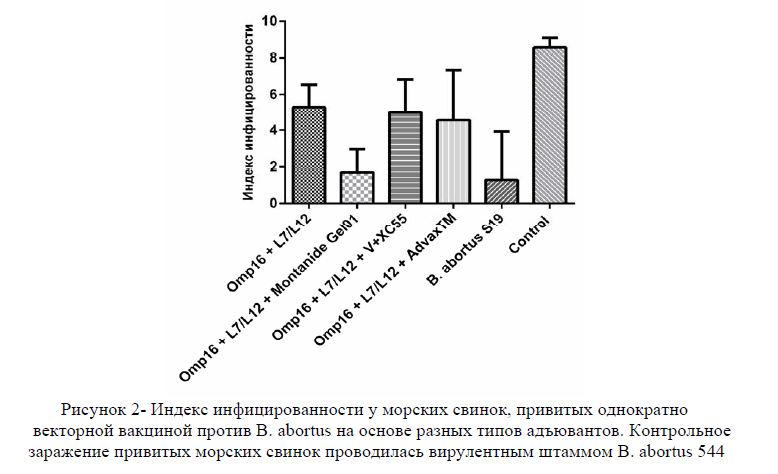
Рисунок 2- Индекс инфицированности у морских свинок, привитых однократно векторной вакциной против B. abortus на основе разных типов адъювантов.
Контрольное заражение привитых морских свинок проводилась вирулентным штаммом B. abortus 544 Образцы векторной вакцины, содержащие адъюванты, по показателю протективности демонстрировали более высокие результаты, однако при этом статистически достоверной разницы (Р< 0.05) между ними не наблюдалось. Следует отметить, что все образцы векторной вакцины, за исключением образца с адъювантом Montanide Gel01 по индексу инфицированности достоверно (Р< 0.05) уступали коммерческой вакцине B. abortus S19. Результаты проведенных исследований показали, что среди испытанных адъювантов наиболее эффективным в плане повышения протективности является Montanide Gel01, который в составе векторной вакцины у привитых морских свинок обеспечивал защиту, сопоставимую (Р< 0.05) с коммерческой вакциной B. abortus S19.
Заключение
Таким образом, можно заключить, что предлагаемый нами новый кандидат вакцины против B. abortus - состоящий из смеси рекомбинантных вирусов гриппа А, экспрессирующих рибосомальный белок L7/L12 и Omp16, в сочетании с различными адъювантами и без них обладает хорошей протективностью на модели морских свинок. При этом наилучшие результаты по иммуногенности и протективности достигнуты с образцом векторной вакцины, содержащей адъювант Montanide Gel01, который в плане обеспечения защиты от B. abortus 544 инфекции был сопоставим с коммерческой вакциной B. abortus S19.
Литература
- Козловский С.В., Емельяненко П.А. / Ветеринарная микробиология. - М.: Колос. - 1982 .- С.
- Колычев Н.М., Росманов Р.Г. / Ветеринарная микробиология и иммунология. -М.: Колос. - 2003 – С. 432.
- Ассонов Н.Р. / Микробиология. - М.: Колос. - 2002. – С
- Moore A., Carpenter T.E. Spatial analysis methods and geographic information systems: use in health research and epidemiology // Epidemiol. Rev. - 1999. - Vol. 21. - P. 143-161.
- Беляков В.Д., Дегтярев А.А., Иванников Ю.Г. / Качество и эффективность противоэпидемических мероприятий. - Л.: Медицина. - 1981. – С.
- Гулюкин М.И., Альбертян М.П., Искандаров М.И., Федоров А.И. Конструирование слабоагглютиногенных вакцин против бруцеллеза // Междунар. рабоч. Совещание: Бруцеллез - пограничная инфекция животных и человека, требующая общих усилий разных стран. - Серпухов. - 2008. - С. 15-16.
- Schurig G.G., Sriranganathan N., Corbel M.J. Brucellosis vaccines: past, present and future // Vet Microbiol. - 2002. - Vol. 90. - Р. 479-496.
- Ashford A., di Pietra J., Lingappa J., Woods C., Noll H., et al. Adverse events in humans associated with accidental exposure to the livestock brucellosis vaccine RB51 // Vaccine. - 2004. - Vol.22. - Р. 3435-3439.
- Мамков, Н.С. Масляные адъюванты для противоящурных вакцин: автореф. дисс. докт. вет. наук / Н.С. Мамков.- Владимир. 1999.- 19с.
- Gallucci S., Lolkema M., Matzinger P. Natural adjuvants: Endogenous activators of dendritic cells. Nat. Med. 1999.- № P. 1249-1255.
- Niblack J.F., Otterness I.G., Hemsworth G.R., Wolff J.S., Hoffman W.W. and Kraska A.R. CP-20,961: a structurally novel, synthetic adjuvant. J. Reticuloendofh. Sot. - №26. P. 655-666.
- Tabynov K., Kydyrbayev Zh., Ryskeldinova Sh., Yespembetov B., Zinina , Assanzhanova N., Kozhamkulov Y., Inkarbekov D., Gotskina T., Sansyzbay A. Novel influenza virus vectors expressing Brucella L7/L12 or Omp16 proteins in cattle induced a strong T-cell immune response, as well as high protectiveness against B. abortus infection // Vaccine. – 2014. - № 32 (18): 2034-41.
- Tabynov K., Kydyrbayev Z., Ryskeldinova S., Yespembetov B., Syrymkyzy N., Akzhunusova I., Sansyzbay A. Safety of the novel vector vaccine against Brucella abortus based on recombinant influenza viruses expressing Brucella L7/L12 and OMP16 proteins, in cattle. – J. Vaccines Immun. – 2014. – 1: 101.
- Tabynov K., Kydyrbayev Z., Sansyzbay A., Khairullin B., Ryskeldinova , Assanzhanova N., Kozhamkulov Y., Inkarbekov D. Immunogenic and protective properties of the first Kazakhstan vaccine against pandemic influenza A (H1N1) pdm 09 in ferrets.// Virol Sin. – 2012. № 27(6): 345-52.
- Tabynov , Sansyzbay A., Kydyrbayev Z., Yespembetov B., Ryskeldinova S., Zinina N., Assanzhanova N., Sultankulova K., Sandybayev N., Khairullin B., Kuznetsova I., Ferko B., Egorov A. Influenza viral vectors expressing the Brucella OMP16 or L7/L12 proteins as vaccines against B. abortus infection. // Virol J. – 2014. – 11(1): 69.