Основные характеристики бензапирена. Развитие нефтедобывающей и нефтеперерабатывающей отраслей является одним из приоритетных направлений для Казахстана в ближайшие десятилетия. Увеличение объемов добычи нефти при использовании устаревших технологий предопределяют большую степень загрязнения биосферы, высокий экологический риск для природных экосистем и значительную опасность для здоровья населения. На сегодняшний день нефтепродукты признаны одним из основных загрязнителей окружающей среды, оказывающим долговременное негативное влияние на экологическую обстановку в зоне воздействия /1,15,19/. Наибольшее распространение среди нефтепроизводных получили полициклические ароматические углеводороды (ПАУ), обладающие ярко выраженным канцерогенным эффектом.
Под ПАУ понимают, как правило, соединения с числом конденсированных колец от двух до шести. Известно огромное количество соединений этой группы. Причем, они встречаются практически во всех сферах окружающей человека среды. ПАУ в составе отработанных газов промышленных предприятий и транспорта представлены бензапиреном, пиреном, антраценом и другими соединениями. Высокая чувствительность различных организмов к бензапирену (БП) определяет использование его в качестве индикатора состояния окружающей среды для всех ПАУ. Бензапирен - это полициклический углеводород состава C20H12, образующийся при воздействии высокой температуры на некоторые органические вещества. Молекулярный вес составляет 252 а.е.м. В чистом виде представляет собой желтые иглообразные кристаллы. Из смеси бензол-метанол кристаллизуется форма с температурой плавления 175-176,50С и плотностью 1,351 г/см3, из амилацетата – с температурой плавления 179,5-180,50С и плотностью 1,282 г/см3. Как и все ароматические углеводороды, он практически нерастворим в воде (образует коллоидные растворы), но хорошо растворяется во многих органических растворителях, водном растворе метанола, маслах и жирах, в связи с чем накапливается в живых организмах, в основном в жировой ткани. Дает стабильные комплексы с серебром (1:1 и 1:2). Гидрируется в присутствии PtO2 в 4,5-дигидро-1,2-бензапирена и 1΄,2΄,9΄,10΄-тетрагидро-1,2-бензапирена. Окисляется хромовой кислотой до 1,2-бензапирен-3,8-диона (температура плавления 2950С) и 3,4-бензапирен-5,8-диона (температура плавления 2450С). Ацилируется уксусным ангидридом в присутствии AlCl3 в 8-ацетил-1,2-бензапирен /30/.
Структурная формула бензапирена довольно проста: пять сочлененных в определенной последовательности бензольных колец (рисунок 1).
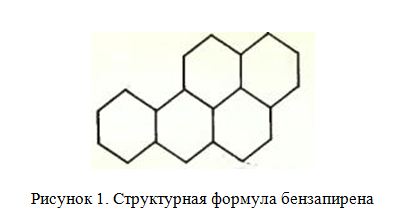
Причем важна именно последовательность сочленения колец. Бензпирены — это углеводороды из пяти циклов, являющиеся производными пирена — тетрациклического углеводорода, лишенного канцерогенной активности. Будет канцерогенен углеводород из пяти колец или нет, зависит от того, как присоединится пятое кольцо. Если так, как у бензапирена, или если произойдет перестройка и образуется молекула 1, 2, 5, 6-дибензантрацена, то у вещества будет способность вызывать злокачественные опухоли. Если же пять колец образуют иную структуру, то образуются малоактивные соединения (напр. 4,5-бензпирен).
Индикаторная роль БП определяется следующими особенностями:
1) БП всегда находят там, где присутствуют другие ПАУ; его относительное содержание варьирует в пределах 1-12% от общего количества ПАУ;
2) БП наиболее распространен в окружающей среде из ряда канцерогенных полиароматических углеводородов;
3) по сравнению с другими ПАУ именно БП обладает наибольшей относительной стабильностью в объектах окружающей среды;
4) БП отличается наиболее выраженной биологической, в частности канцерогенной активностью; вклад бензапирена в суммарную канцерогенность преобладает и варьирует от 40 до 90%, по сравнению с другими ПАУ; между концентрацией БП и общим содержанием ПАУ и их канцерогенной активностью существуют статистически значимые линейные зависимости с высокими коэффициентами корреляции (0,90-0,99) /26/;
5) существующие физико-химические методы индикации БП в различных средах являются наиболее чувствительными среди методов определения ПАУ.
В нашей стране установлены предельно допустимые концентрации (ПДК) бензапирена практически для всех объектов среды: атмосферный воздух - 0,1 мкг/100м3, почва - 0,02 мг/кг, поверхностные воды - 5 нг/дм3, донные отложения - 0,02 мг/кг. Эти ПДК очень строги. Так, в воздухе рабочей зоны допускается не больше 0,15 мкг/м3, в то время как ПДК для другого распространенного загрязнителя атмосферы - сернистого газа, составляет 500 мкг/м3. Т.е. ПДК на бензапирен в полмиллиона раз меньше, чем на SO2. При этом следует помнить, что влияние доз, находящихся даже вблизи значений предельно допустимых, на объекты живой природы, уже нежелательно, а при сочетании низкой концентрации с большой длительностью воздействия нередко наблюдается более сильный отрицательный эффект, чем при сочетании высокой концентрации и короткого воздействия. Необходимо также учитывать, что в биосфере БП, как и все химические вещества, не может существовать длительное время отдельно, а взаимодействует с другими поллютантами, что ведет к образованию структур, токсичность которых может быть более высокой, чем исходных веществ.
Главным условием образования БП является температура 800-10000С, поэтому основными антропогенными источниками являются промышленные выбросы от нефтеперерабатывающих, металлургических, коксохимических, и иных производств, предприятия теплоэнергетики, а также наземный транспорт, авиация, водный транспорт. Установлено, что только за 1 минуту работы газотурбинный двигатель современного самолета выбрасывает в атмосферу 2—4 мг БП. Даже приблизительные расчеты показывают, что в атмосферу от этого источника поступает ежегодно более 5000 тонн БП. Содержание описываемого канцерогена в воздухе городов достигает максимального значения зимой, а минимального - летом. Общий выбросБП только в атмосферу Земли оценивается более 10 тыс. в год [6,20]. Глобальная эмиссиябензапирена в природную среду составляет более 20000 т. в год. Причем 61% приходится на сжигание угля, 20% — на производство кокса, 4% — на сжигание древесины, 8% — на открытое сжигание леса и сельскохозяйственных культур, 1% — на выбросы транспорта и лишь 0,09% и 0,06% — на сжигание нефти и газа соответственно/28/.
Поскольку в нефтях содержание БП колеблется в очень широких пределах (от 250 до 8050 мкг/кг), то весьма актуальной представляется проблема загрязнения окружающей среды сырой нефтью в результате ее добычи и транспортировки. В 1970—80-е годы началось строительство супертанкеров грузоподъемностью 100—500 тысяч тонн. В результате аварий таких танкеров происходят разливы нефти с соответствующими экологическими последствиями. Показательно нефтяное загрязнение Средиземного моря: в порты Средиземноморья привозится ежегодно около 500 млн. тонн нефти, но из этого количества от 5 до 10% попадает в море. Площадь подобного загрязнения составляет примерно 175 тыс. кв. км, т.е. — 7% от всей акватории /11/.
Миграция бензапирена. Как и все вещества БП включается в биосферный круговорот веществ, переходит из воздуха в почву, из почвы в растения, из последних в корма для животных и, наконец, попадает в пищу человека, подвергается различным превращениям, в том числе и деструкции (например, под влиянием фотоокислителей или почвенных микроорганизмов). Во всех средах бензапирен, как и большинство ПАУ, практически не существует в молекулярно-дисперсном состоянии, а, как правило, связывается с другими загрязнителями (в воздухе - с твердыми частицами атмосферной пыли, в воде - с различными поверхностными компонентами).
В воздушной среде (здесь наибольший интерес представляют приземные слои атмосферы, содержащие большую часть загрязнений) распространение БП определяется дисперсностью частиц, на которых он сорбирован, удаленностью источника выброса от поверхности земли и такими климатическими факторами, как ветер, влажность, температура, атмосферные осадки. Мелкодисперсная пыль остается в верхних слоях атмосферы, в то время как частицы средней дисперсности (1— 10 мкм) длительно персистируют в зоне дыхания человека, животных и растительных организмов. Более крупные частицы, размерами свыше 10 мкм, вследствие седиментации и с осадками выпадают из воздуха и переходят в почву, растения, воду /5,9/.
В водной среде транслокация БП включает в себя как его перераспределение между отдельными объектами (вода, планктон, донные отложения и др.), так и аккумуляцию живыми организмами и распространение с водой. Попадая в водоем вместе с промышленными стоками и атмосферными, осадками БП быстро растекается по его поверхности, образуя эмульсию, изменяющую физико-химические показатели воды. Даже тончайшая пленка БП изолирует воду от кислорода воздуха, что приводит к ухудшению газообмена, повышению температуры поверхностного слоя воды. Некоторая часть БП, испаряясь с водой, может попадать и в атмосферный воздух. Основная же часть сорбированных на средне- и крупнодисперсных частицах БП оседает на дно, формируя уровень загрязнения донных отложений, и поступает в растения. Соответственно концентрация БП в воде существенно ниже, чем в донных отложениях. Более того, последние являются своеобразным депо для вторичного загрязнения воды описываемым углеводородом. Поступивший в растения и фитопланктон БП аккумулируется в них и попадает в другие водные организмы. Концентрация БП в верхних слоях пресноводных донных отложений сильно зависит от близости водоемов к индустриальным центрам и объемов сжигания топлива, а также от интенсивности транспортного движения. Так, в донном иле Великих озер США концентрация БП изменяется от 10 до 1000 нг/г. В озерных отложениях стран Европы содержание БП составляет 100-700 нг/г (Швейцария) и 200-300 нг/г (Германия) /7, 10,12,14, 32/.
В почву БП поступает, в основном, с атмосферными осадками. Заметим, что максимальное содержаниеБП наблюдается преимущественно в поверхностных слоях почв. Это связано с тем, что гумусовые горизонты, содержащие наибольшее количество органических веществ, обладают более высокой сорбционной способностью по отношению к БП. Далее из почвы БП поступает в подземные части растений, которые затем могут быть использованы человеком в пищу, или на корм скоту. Обычно содержание БП в поверхностном слое почв сельских районов, находящихся вдали от индустриальных центров, не превышает 5-8 нг/г сухой массы. Наиболее сильно земли загрязнены БП в регионах, насыщенных нефтепромыслами и нефтеперерабатывающими предприятиями, а также в местах аварий на нефтепроводах. Предложена следующая оценка степени загрязнения почв БП: умеренная - до 20-30 нг/г, значительная - 31-100 нг/г, высокая - свыше 100 нг/г /8,26,33/. Продолжительность самовосстановления почвы при среднем уровне загрязнения оценивается периодом от 10 до15 лет /2, 29/.
При попадании БП в почву изменяется весь комплекс свойств характеризующих ее плодородие: ухудшается водно-воздушный режим, резко снижается содержание подвижных соединений азота и фосфора, развивается солонцовый процесс. Попадая в почву, БП опускается вертикально вниз под влиянием гравитационных сил и распространяется вширь под действием поверхностных и капиллярных сил. Такое проникновение приводит к нарушению сложившегося геохимического баланса в экосистеме. Скорость продвижения БП в почве зависит от ее свойств и соотношения БП, воздуха и воды. В загрязненных почвенных горизонтах уменьшается кислотность почвенного раствора, резко изменяется интенсивность окислительно-восстановительных ферментативных реакций. С этими биологическими процессами связан распад БП в почве, важнейшими деструкторами остатков которого у почвенных микроорганизмов являются ферменты каталаза и дегидрогеназа. В почвах сильно загрязненных БП происходит снижение их активности из-за избытка органического вещества, обогащенного серой и сероуглеродом, являющимися ингибиторами этих ферментов /4/.
Многие почвенные микроорганизмы оказались высокочувствительными к действию БП, что изменяет сложившиеся микробиоценозы и влияет на биологическую продуктивность почвы. Так внесение в почву БП в концентрациях 40—100 мкг/кг резко угнетает рост сапрофитных микроорганизмов, но стимулирует размножение кишечной палочки и грибов, главным образом, актиномицетов. Вследствие малодоступности БП почвенным бактериям, процесс его разрушения идет очень медленно /27/.
Как указывалось выше, БП может аккумулироваться растениями, поступая в подземные органы из почвы и в надземные части растений из атмосферы. Отмечено, что в индустриальных районах содержание в растениях БП существенно выше, чем у тех же видов, собранных в "чистых" районах, и превышает фоновый уровень. Более того, установлено, что лекарственные растения, произрастающие в непосредственной близости от оживленных автомагистралей, содержат повышенное количество БП.
Помимо накопления во всех объектах среды также происходят процессы трансформации бензапирена. В воздухе деградация БП осуществляется за счет воздействия УФ-излучения и различных фотооксидантов, прежде всего озона, а также окислов азота, формальдегида, акролеина, органических перекисей, накапливающихся в городской атмосфере. В почве деградация БП происходит как под влиянием ультрафиолета (поверхностный слой), так и, главным образом, ферментных систем микроорганизмов /3/. В воде окислительная деградация БП и других ПАУ протекает также под действием УФ-излучения (глубина проникновения зависит не только от интенсивности иррадиации, но и мутности воды, ее цветности, температуры и т.п.), микрофлоры водоема, а также под влиянием других химических соединений, поступающих в эти водоемы.
Многие виды животных и растений способны аккумулировать БП. Например, пресноводные и морские моллюски — перловицы, устрицы, мидии за счет того, что в них не происходит (или происходит очень медленно) метаболизм БП, способны его накапливать в своем организме в большом количестве. В эксперименте с внесением в воду аквариумов БП в концентрации 0,1 мкг/л, в тканях черноморских мидий Mutilus galloprovincialis этот индикатор ПАУ обнаруживался через 60—120 дней в 20—30 раз в больших количествах, чем у контрольных моллюсков. В мидиях накапливается до 55, а в устрицах—до 90 мкг/кг БП. Это позволяет использовать моллюсков-фильтраторов в качестве биоиндикаторов загрязненности водной среды ПАУ. Промысловые рыбы являются наиболее оптимальными индикаторами нефтяного загрязнения и накопления техногенных ПАУ. Накопление БП, в основном, происходит в печени, жабрах, костях, мышцах. Здесь необходимо отметить, что рыбы, ведущие придонный образ питания и рыбы со значительным содержанием липидов, в большей степени аккумулируют его. На примере черноморских рыб показано, что по степени накопления БП виды рыб можно ранжировать следующим образом: глосса > султанка > смарида > горбыль > хамса > ставрида > мерланка. В свежей рыбе, выловленной в загрязненной ПАУ акватории, содержание БП достигает 15 мкг/кг. Среднее содержаниеБП в морской рыбе находигся в диапазоне 0,1-0,2 мкг/кг. Исключение составляют угорь (1,1 мкг/кг) и лосось (5,96 мкг/кг). В речной рыбе содержание БП также зависит от степени загрязнения водоема. Например, при концентрации бензапирена в донном иле 2,1-4,3 мкг/кг в плотве было найдено 0,03-3,04 мкг/кг, а в окуне— 0,02-1,9 мкг/кг /17, 21-24/.
Способность БП к аккумуляции в различных объектах окружающей среды обуславливает возможность загрязнения им пищевых продуктов и кормов, а, следовательно, попадание в организм человека.
Биологические эффекты бензапирена Влияние БП на живые организмы широко исследовано многими учеными. Установлено, что бензапирен, в комплексе с другими ПАУ, обладает способностью усиливать рост и размножение ряда растений. Впервые это было показано на водорослях Obelia geniculata еще 60 лет назад /31/. С тех пор многочисленными исследованиями подтверждено, что в малых концентрациях БП обладает ростостимулирующим действием. Своеобразный эффект отмечен и на низших позвоночных. При аппликации БП на поверхность тела планарии возникали образования, которые могут быть истолкованы по разному — как проявления тератогенного, органогенного или канцерогенного эффектов. Вообще, поскольку канцерогенное действие ПАУ было выявлено относительно рано (еще в те времена, когда чистые вещества этой группы не были выделены или синтезированы), то именно опухолеродное действие БП, как одного из составляющих ПАУ, наиболее исследовано /18/.
По оценке экспертов МАИР (Международное агентство по изучению рака) прямые эпидемиологические доказательства о канцерогенности ПАУ для человека отсутствуют и индикаторное вещество этого класса соединений — БП отнесено к группе 2А, т.е. к категории потенциально опасных. Вместе с тем многие специалисты относят БП к группе 1 — безусловным канцерогенам для людей. Кроме того, в разряд канцерогенов группы 1 включены также производственные процессы и отрасли промышленности, где определенные группы рабочих подвергаются экспозиции к ПАУ. Большинство таких факторов вызывают опухоли кожи и легких, имеются результаты эпидемиологических исследований, свидетельствующих об их возможности вызывать также новообразования мочевого пузыря, желудочно-кишечного тракта, кроветворной системы, почек, гортани и полости рта /35/.Во многих экспериментах показано, что БП способствует образованию опухолей, поражает дыхательную и нервную системы. В опытах на мышах попадание спиртового раствора БП на кожу вызывает развитие опухоли в течение 90-100 сут., внутримышечная инъекция приводит к быстрму развитию саркомы. Помимо того, что БП провоцирует возникновение ряда онкологических заболеваний, он также способствует изменению состава крови, приводит к нарушению нервной деятельности /19/. Известно также, что опухоли у человека вызывает в основном воздействие комплекса ПАУ (в присутствии бензапирена) /16, 34/.
БП в комплексе с другими ПАУ обладает мутагенным действием. В частности индуцирует прямые и обратные мутации у тестерных штаммов бактерий, мутации у дрозофилы, а также сестринские хроматидные обмены, хромосомные аберрации, точковые мутации in vivo и in vitro, и ряд других генетических изменений. Кроме того, БП обладает эмбриотоксическим и тератогенным эффектами /25/.
Постоянное поступление БП в организм человека из окружающей среды приводит к ослаблению иммунной системы, способствуя развитию ряда хронических заболеваний пищеварительной, дыхательной и нервной систем. В производственных условиях при экспозиции к БП у людей, в зависимости от способа контакта, могут возникать дерматиты, язва желудка, раздражение верхних дыхательных путей, а также повышен риск возникновения ишемической болезни сердца, хронических заболеваний легких и других нарушений респираторной системы. Например, гигантский смог в Лондоне 5—13 декабря 1951 года унес 2850 жизней. Содержание БП в этом смоге составило до 222 мкг/100 куб.м /3/.
Принимая во внимание убиквитарность БП в среде обитания человека, его способность к аккумуляции, присутствие в различных звеньях трофической цепи, а также многообразие вызываемых биологических эффектов, данный полютант можно отнести к наиболее приоритетным экологически опасным факторам, инициирующим злокачетвенное перерождение клеток и других патологических процессов организма
Литература
- Амиргалиев Н.А. Некоторые вопросы гидрохимического режима дельты реки Урал // Рыбные ресурсы водоемов Казахстана и их использование. 1966г. С.46-55.
- Базарбеков К.У., Бондаренко А.П. Изменение основных свойств почвы, загрязненной нефтепродуктами // Материалы международной научно-практической конференции Экология и здоровье человека. Павлодар, 2002. С. 297–301.
- Базарбеков К.У., Бонадернко А.П., Калиева А.А. Ликвиация нефтяных разливов и загрязнений нефтепродуктами почвы и воды при помощи микроорганизмов // Материалы первой ежегодной конференции по химии и коммерциализации. Москва 27-29 сентября 2004 г. С. 35-38.
- Белых Л.И., Киреева А.Н., Смагунова А.Н., Малых Ю.М., Пензина Э.Э. Количественное определение бенз(а)пирена в почвах с помощью низкотемпературной люминисценции // Аналитика и контроль. 2000, Т.4, №1. С. 24-30.
- Белых Л.И., Малых Ю.М., Пензина Э.Э., Смагунова А.Н. Источники загрязнения атмосферы ПАУ в промышленном Прибайкалье // Оптика атмосферы и океана. 2002. Т.15. №10. С. 994-998.
- Белых Л.И., Малых Ю.М., Смагунова А.Н., Пензина Э.Э., Козлов В.А. Оценка составляющих погрешности отбора проб газопылевых организованных выбросов в атмосферу при определении бенз(а)пирена // Журнал Аналитической Химии. 2003. Т. 58. № 7. С. 746-753.
- Белых Л.И., Пензина Э.Э., Попов Л.Г., Баженов Б.Н., Хуторянский В.А., Серышев В.А. Бенз(а)пирен в воде и донных отложениях Ангары, Байкала и их притоков // Водные ресурсы. 1997. Т. 24. №6. С. 734-739.
- Белых Л.И., Серышев В.А., Пензина Э.Э., Белоголова Г.А., Хуторянский В.А. Содержание бенз(а)пирена в почвах некоторых районов Иркутской области // Почвоведение. 1998. № 3. С. 334-341.
- Белых Л.И., Киреева А.Н., Пензина Э.Э., Малых Ю.М., Смагунова А.Н., Серышев В.А., Ратовский Г.В. Закономерность распределения бенз(а)пирена в объектах окружающей среды города с расположенным на его территории алюминиевым заводом // Экологическая химия. 2000. Т.9. Вып. 4. С. 246-259.
- Белых Л.И., Пензина Э.Э., Попов Л.Г., Ратовский Г.В. Промышленные стоки как загрязнитель водоемов бенз(а)пиреном. В сб.: Природные ресурсы, экология и социальная среда Прибайкалья. Иркутск: Университеты России. т.1. 1995. С. 198-203.
- Биотестирование и прогноз изменчивости водных экосистем при антропогенном загрязнении // Отв. ред. Г.Г.Матишов. Изд-во КНЦ РАН, 2003. 469 С.
- Велдре И.А., Итра А.Р., Паальме Л.П. Опыт изучения миграции бенз[а]пирена в системе вода-донные отложения одного озера Эстонии // В кн.: Миграция загрязняющих веществ в почвах и сопредельных средах. Труды 2-го Всесоюзного совещания. М.: Гидрометеоиздат. 1980. С.243-249.
- Гичев Ю.П. Загрязнение окружающей среды и здоровье человека // Новосибирск: Наука. 2002. 229 С.
- Ежегодник качества поверхностных вод по территории деятельности Приволжского УГКС Госкомгидромета (Татарская АССР, Ульяновская, Пензенская, Куйбышевская, Саратовская, Оренбургская обл.) за 1986г. Куйбышев. 1987. с. 178.
- Жанбуршин Е.Т. Экологическая оценка влияния загрязнителей нефтегазового комплекса на природную среду (на примере Мангистауской области) // Диссертация на соискание ученой степени доктора технических наук. Тараз. 2005.
- Злокачественные новообразования в России в 2000 г. (Заболеваемость и смертность)//Под ред. В.И. Чиссова, В.В. Старинского, М. МНИОИ им. П.А. Герцена. 2002. С. 264.
- Ильин Г.В.Современные уровни химического загрязнения промысловой ихтиофауны // Экология промысловых рыб Баренцева моря. Изд-во КНЦ РАН, 2001. С. 296-217.
- Канцерогенные вещества // Пер. с англ., под ред. В.С. Турусова, М., 1987. 356 С.
- Кенжегалиев, А.К. О проблемах загрязнения Прикаспийской зоны нефтегазовым комплексом // Материалы международной конференции Перспективы устойчивого развития экосистем Прикаспийского региона. Алматы. 2004. С. 14-15.
- Контроль химических и биологических параметров окружающей среды./Под. ред. Исаева Л.К. Сп.б.: Эколого-аналитический информационный центр «Союз». 1998. 896 С.
- Оценка загрязнения промысловых объектов Баренцева моря. Региональная программа. Отчет о научно-исследовательской работе. 1997. 35 С.
- Оценка загрязнения промысловых объектов Баренцева моря. Региональная программа. Отчет о научно-исследовательской работе. 1998. 52 С.
- Оценка загрязнения промысловых объектов Баренцева моря. Региональная программа. Отчет о научно-исследовательской работе. 1999. 42 С.
- Оценка загрязнения промысловых объектов Баренцева моря. Региональная программа. Отчет о научно-исследовательской работе. 2000. 44 С.
- Ракитский В.Н., Турусов В.С. Мутагенная и канцерогенная активность химических соединений // Вестник РАМН. 2005.№ 3. С 7–9.
- Ровинский Ф.Я., Теплицкая Т.А.,Алексеева Т.А. Фоновый мониторинг полициклических ароматических углеводородов // Л.: Гидрометеоиздат. 1988. 224 С.
- Рыбак, В.К., Овчарова Е.П., Коваль Э.Э. Микрофлора почвы, загрязненной нефтью // Микробиологический журнал. 1984. Т. 46. №4. С. 29-32
- Филиппов С.П., Павлов П.П., Кейко А.В., Горшков А.Г., Белых Л.И. Экспериментальное определение выбросов сажи и ПАУ котельными и домовыми печами // Известия Академии Наук. Энергетика. 2000. №3. С. 107-117.
- Химическое загрязнение почв и их охрана // М. Агропромиздат. 1991. 303 С.
- Хим энциклопедия // т. 1 гл. Ред. И.Л. Кнунянц, Советская энциклопедия,М. 1988,623 с.
- Шабад Л. М. О циркуляции канцерогенов в окружающей среде М.1973. 295 С.
- Шилина А.И. Миграция бенз[а]пирена в окружающей среде. //В кн.: Комплексный глобальный мониторинг загрязнения окружающей природной среды. Труды 2-го Международного симпозиума. Л.: Гидрометеоиздат. 1982. С.238-242.
- Яценко-Хмелевская М.А., Цибульский В.В. Выбросы стойких органических загрязнителей на территории России // Экологическая химия. 1999. Т.8.№2. С. 73-79.
- Franks L. M., Teich N. M. Cellular and molecular biology of cancer. // Third Edition. Oxford University Press. Oxford. N.Y. Tokyo. 1997. V 1. P 458.
- Nisbet I.C., La Goy P.K. Toxic equivalency factors (TEFs) for policuclic aromatic hydrocarbons (PAHs) // Regulatory Toxicology and Pharmocology. 1992. V. 16:3. P. 290-300.
- Sanner T. at al. Potency grading in carcinogen classification. Molecular carcinogenesis. 1997. №20. P.280-287.