Защита среды обитания живых организмов от различных экологически опасных факторов приобретает все большую остроту в связи с увеличивающимися объемами различных загрязнителей, попадающих в окружающую среду. По эффективности биологические методы защиты пока уступают химическим средствам. Поэтому применение пестицидов в ближайшие годы представляется неизбежным и необходимым. /1-3/. Пестициды, в отличие от других антропогенных факторов, сознательно вводятся человеком в биосферу, причем в постоянно возрастающих масштабах, и входят в первую десятку ее загрязнителей /2, 4, 5/. С каждым годом ассортимент и количество пестицидов возрастает.
В настоящее время проблема токсического воздействия пестицидов на здоровье населения и окружающую природу является одной из наиболее актуальных эколого-гигиенических проблем во всем мире, которая усугубляется зачастую бесконтрольным и бессистемным применением пестицидов. Пестициды способны долгое время сохраняться в почве. Мигрируя, они загрязняют поверхностные и подземные воды, почвы, накапливаются в растительных организмах и по пищевой цепочке попадать в организм человека /6/.
В результате действия пестицидов происходит нарушение состава популяций в агро- и биоценозах, уничтожение естественных хищников и паразитов вредителей, негативное влияние на полезную фауну, возникновение устойчивых к пестицидам популяций вредных видов, изменение качества урожая в связи с возможным содержанием в нем остатков ядохимикатов, а также отрицательное действие на генетический аппарат живых организмов /7, 8/.
В связи с вышеизложенным, целью настоящего исследования явилось изучение содержания фипронил-сульфона в печени, почках и мышцах экспериментальных животных.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Объектами исследования явились ткани внутренних органов (печень, почки, мыщцы) белых беспородных крыс-самцов в возрасте 1, 6 и 12 месяцев, получавших фипронил-сульфон (МВ 46136) в дозе 21,8 мг/кг, что соответствует 1/10 ЛД50.
Всего в экспериментах было использовано 30 белых беспородных крыс-самцов в возрасте 1, 6, 12 месяцев, разделенных на 6 групп по 5 крыс в каждой: I-III – животные трех возрастных групп, получавших однократно (острое воздействие) перорально водный раствор фипронил-сульфона; IV-VI – животные трех возрастных групп, получавших в течение 10 дней (подострое воздействие) перорально водный раствор ксенобиотика.
Перед забоем определяли общий вес и вес исследуемых органов каждой крысы. Приготовление материала для газохроматографического анализа проводили по модифицированной методике /9-13/. Пробы из тканей лабораторных животных (печень, почки, мышцы) измельчали и экстрагировали смесью растворителей ацетонитрила и гексана (1:1). Готовые экстракты проб выпаривали в термостате и сухой осадок каждого экстракта растворяли в 200 мкл гексана и вводили в газовый хроматограф (Yuonglin instrument, South Korea) по 1 мкл пробы. Концентрация стандартных растворов фипронил-сульфона составляла 1 мкг/мл гексана.
Условия хроматографии: температура на вводе - 160 C°, скорость потока – 1 мл/мин, дозирование с делением потока – 1:10, колонка – DB 5 - 30 м/0,55 мм, начальная температура – 160 C°, скорость нагрева 1 газоносителя – 1-3, конечная температура 1 – 250 C°, скорость нагрева 2 газоносителя – 2-8, конечная температура 2 - 260 C°, скорость нагрева 3 газоносителя – 3-16, конечная температура 3 газоносителя - 310 C°.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Результаты газохроматографического анализа содержания метаболита фипронил-сульфона в печени, почках и мышцах интоксицированных животных разных возрастных групп представлены в таблице. Установлено наличие фипронил-сульфона (МВ 46136), одного из метаболитов фипронила, в исследуемых органах крыс разного возраста после острого и подострого воздействия.
Из представленных данных видно, что в зависимости от продолжительности воздействия фипронил-сульфона и возраста интоксицированных крыс содержание метаболита меняется. Так, если у животных в возрасте 1 месяца, подвергнутых острому воздействию, его содержание в печени, почках и мышцах составило соответственно 0.027, 0.029 и 0.005 мг/кг массы тела, то у животных в возрасте 6 месяцев – 0.036, 0.042 и 0.006, а у годовалых – 0.055, 0.060 и 0.009 мг/кг массы тела. Несмотря на увеличение с возрастом животных абсолютных чисел, отражающих количество ксенобиотика в изучаемых тканях, достоверное увеличение его содержания наблюдалось только в мышечной ткани годовалых крыс по сравнению с месячными особями, которое увеличилось в 1,8 раза (Р<0.05), что отражено на рисунке 1.
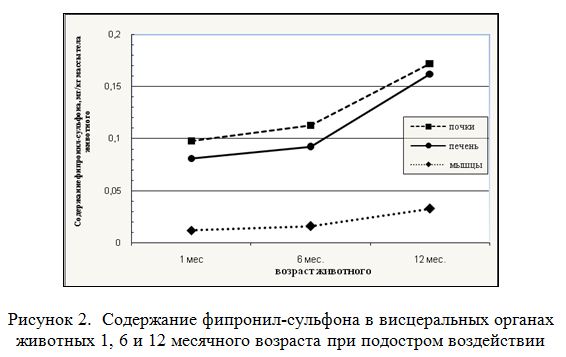
Газохроматографический анализ образцов печени, почек и мышц крыс, интоксицированных в течение 10 дней (подострое воздействие) также выявил наличие метаболита в органах. При этом, достоверное увеличение содержания МВ 46136 в печени в 2,1 (Р<0.01) раза наблюдалось только у 12 месячных крыс по сравнению с месячными животными, а у годовалых по сравнению с полугодовалыми – в 1,8 раза (Р<0.01).
Таблица – Содержание фипронил-сульфона (МВ 46136) в печени, почках и мышцах крыс при остром и подостром воздействии
|
Условия опыта |
Возраст животных (мес.) |
Содержание фипронил-сульфона (мг/кг) |
||
|
печень |
почки |
мышцы |
||
|
острое воздействие |
1 |
0.027 ± 0.008 |
0.029 ± 0.007 |
0.005 ± 0.001 |
|
6 |
0.036 ± 0.009 |
0.042 ± 0.005 |
0.006 ± 0.001 |
|
|
12 |
0.055 ± 0.013 |
0.060 ± 0.013 |
0.009 ± 0.001 |
|
|
подострое воздействие |
1 |
0.081 ± 0.009** |
0.098 ± 0,018** |
0.012 ±0.005 |
|
6 |
0.092 ± 0.002*** |
0.113 ± 0.025* |
0.016 ± 0.004* |
|
|
12 |
0.169 ± 0.019** |
0.172 ± 0.024** |
0.033 ± 0.008* |
|
|
Примечание: *-p<0.05, **-p<0.01, ***-p<0.001 в сравнении с длительностью воздействия |
||||
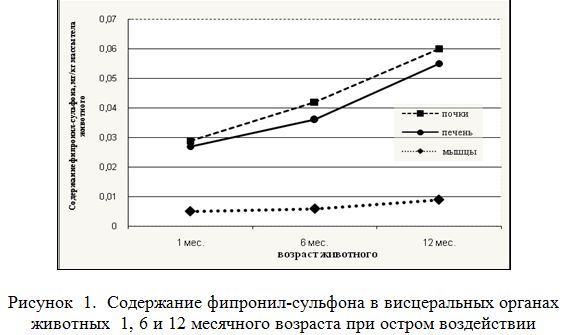
Сравнительный анализ метаболита в почках интоксицированных животных при подостром воздействии показал, что у животных 6 месячного возраста по сравнению с животными месячного возраста не наблюдалось его превышения, а у 12 месячных, наоборот, увеличение составило 1,8 раза (Р<0.01). У 12 месячных животных по сравнению с 6 месячными животными содержание метаболита в почках превысило в 1,5 раза, однако эта разница была также статистически недостоверной (рисунок 2).
МВ 46136 в мышцах 6 и 12 месячных животных было в 1,3 и 2,8 раза выше по сравнению с месячными, однако, достоверное увеличение отмечено только у годовалых крыс (Р<0.05).
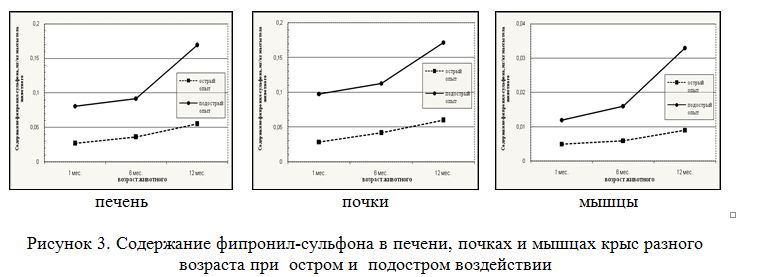
Содержание фипронил-сульфона в печени, почках и мышцах крыс при остром и подостром воздействии представлено на рисунке 3.
Сравнительный анализ количества фипронил-сульфона в печени животных, интоксицированных в остром и подостром опыте, свидетельствует о накоплении метаболита при многократном его воздействии на крыс.
Как видно из представленного на рисунке графика, с увеличением продолжительности воздействия метаболита на крыс его содержание в печени возросло у животных 1, 6 и 12 месяцев в 3,0 (Р<0.01), 2,6 (Р<0.001) и 3,1 (Р<0.001) раза по сравнению с животными аналогичных возрастных групп, подверженных острому воздействию. В почках эти показатели достоверно увеличились в 3,4 (Р<0.01), 2,7 (Р<0.05) и 2,9 (Р<0.01) раза, соответственно. В мышцах достоверное увеличение концентрации ксенобиотика наблюдалось только у животных в возрасте 6 и 12 месяцев в 2,7 (Р<0.05) и 3,7 (Р<0.05) раза, соответственно.
Таким образом, в результате проведенного газово-хроматографического исследования образцов тканей экспериментальных животных разных
возрастных групп, подвергнутых острому и подострому воздействию фипронил-сульфона, было установлено, что содержание метаболита в печени, почках и мышцах интоксицированных животных зависит от продолжительности воздействия ксенобиотика. При многократном применении метаболита происходило достоверное увеличение его содержания в изучаемых тканях. Кроме того, отмечена зависимость его накопления в организме животных от возраста.
Представленная работа выполнена в рамках проекта Фонда науки Республики Казахстан, № ГР 0106РК00279 (2006-2008 гг.).
ЛИТЕРАТУРA
- Бигалиев А.Б., Абилев С.К. Генетика и окружающая среда. –Караганда.: КарГУ, 1989. –141с.
- Бариляк Н.Р., Бужиевская Т.И., Быкорез А.И. Генетические последствия загрязнения окружающей среды. Киев: Наук. Думка, 1989, 228 с.
- Савченко В.К. Геносфера. Минск: Навука i тэхнiка, 1991.- 158 с.
- Влияние пестицидов, используемых в сельском хозяйстве, на общественное здравоохранение. – Женева: ВОЗ, 1993.- 140 с.
5. Кленкин А.А., Короткова Л.И. Экоаналитические исследования загрязнения Азовского моря стойкими хлорорганическими пестицидами // Экология и промышленность России. – 2007. – № 1. – С. 34–40.
6.Короткова Л.И. Накопление хлорорганических соединений в промысловой рыбе северо-восточной части Черного моря // Ихтиологические исследования на внутренних водоемах. Матер. Междун. научн. конф. Саранск: Мордов. гос. ун-т. − 2007. – С. 91–93.
7. Nina T. Holland, Paurene Duramad, Nathaniel Rothman, Larry W. Figgs, Aaron Blair, Alan Hubbard and Martyn T. Smith. Micronucleus frequency and proliferation in human lymphocytes after exposure to herbicide 2,4-dichlorophenoxyacetic acid in vitro and in vivo // Mutation Research / Genetic Toxicology and Environmental Mutagenesis. - 2002, v. 521. 1-2 - p. 165-178.
8. Marina González, Sonia Soloneski, Miguel A. Reigosa and Marcelo L. Larramendy. Effect of dithiocarbamate pesticide zineb and its commercial formulation, azzurro. IV. DNA damage and repair kinetics assessed by single cell gel electrophoresis (SCGE) assay on Chinese hamster ovary (CHO) cells // Mutation Research / Genetic Toxicology and Environmental Mutagenesis. - 2003, v. 534. 1-2. – p. 145-154.
9. John Casida/ Proc Natl Acad Sci USA. 1996.- Nоvember, 12; 93 (23): 23764-12767.
10. Consuelo Sanchez-Brunete and other. Determination of fipronilin honey and pollen samples by gas chromatography. Depat. de Medio Ambiente, Madrid, Spain.
11. Jose Luis Vilchez and other. Determination of fipronil by solid-phase microextraction and gas chromatography-mass spectrometry. Dep. of Analitical Chemistry, University of Granada, Spain, March, 2001.
12. Zhou Pai and other. Dynamics of fipronil residue in vegetable-field ecosystem. Res. and Env. Science Dep. of Shanghai Jiao Tong University, China, and Dep. of Env. SiencesGeologyUniversity of CaliforniaRiverside , USA, June, 2004.
13. Калинин В.А., Довгилевич Е.В., Калинина Т.С., Довгилевич А.В. Временные методические указания по определению остаточных количеств фипронила и его метаболита фипронил-сульфона в воде, почве, клубнях картофеля, зерне и соломе зерновых колосовых культур методом газожидкостной хроматографии. М.: МСХА им. К.А. Тимирязева.-1997.-26 с.