Работа посвящена исследованию возможностей использования в экспериментально-клинической практике трансплантационного метода лечения сахарного диабета. Показано, что в перспективе этот метод, в отличие от инсулинотерапии, несомненно, может стать методом излечения. Подчеркнуто, что особое значение имеет получение достаточного количества материала для трансплантации в виде изолированных и выделенных из поджелудочной железы панкреатических островков, качественная очистка их от примесей и подготовка к трансплантации путем культивирования с использованием ростовых факторов. Показана важная роль визуального гистологического контроля каждой партии получаемых островков; авторами приведены собственные результаты гистологического и гистохимического контроля полученного материала с помощью модифицированных ими всех известных на сегодня в мире основных высокоспецифичных методов исследования состояния гистоструктуры и оценки содержания инсулина в В-клетках. На основании собственного значительного многолетнего опыта работы в западноевропейских лабораториях авторами предложены полезные замечания по вопросам организационного характера при проведении исследований в этом направлении.
В течение последних десятилетий в мире идет интенсивный рост числа зарегистрированных больных сахарным диабетом (СД): от 290 млн в 2000 г. до 366 млн в 2011 г. и 422 млн в 2015 г. [IDF Diabetes Atlas, 2011]. В 1992 г. диабет признан ВОЗ как «неинфекционная эпидемия ХХ-го века» а позже — как «угроза миру». Казахстан не является исключением. Число пациентов с зарегистрированным СД по республике составило: в 1965 г. — 29 000, в 1998 г. — 93 000 (около 0,8 % от общей численности населения), в 2011 г. — 208 000 (1,3 % от общей численности населения) и в 2017 г. — 309 000 (1,7 %). К этому надо добавить еще почти столько же лиц с невыявленным явным диабетом и 100 000-150 000 с латентными формами диабета. Общее число больных СД приближается, таким образом, к 800-850 тыс. человек. На сегодня число больных с СД явно превышает число онкологических больных и, возможно, число больных сердечно-сосудистыми заболеваниями (ССЗ), уверенно занимающими уже много лет позиции № 2 и № 1 как причина смерти в большинстве стран. Сегодня СД по этому показателю вышел на позицию № 3. Наиболее тревожным фактом является то, что скорость роста заболеваемости СД превышает скорость роста числа больных ССЗ и онкологическими заболеваниями, составляя порядка 1,6-1,7 % (7,1 %, включая невыявленных больных по данным IDF)от общей численности населения (0,8 % в 1998 г.). Если в среднем по миру удвоение числа больных происходит в течение 10–15 лет, то в Казахстане за 18 лет их количество утроилось.
В различных странах, согласно отчету Международной федерации диабета (2011), заболеваемость диабетом является очень различной: в России в 2011 г. — 7,6 % от численности населения, Франции — 7,3 %, Финляндии — 9,0 %, Германии — 8 %, Австрии — 9,1 %, Италии — 7,8 %, Польше — 10,6 %, Швеции — 5,7 %, Мексике — 18 %, Израиле — 9 %, в странах Карибского бассейна — от 12,8 % в Антигуа до 16,4 % в Гайане; драматическое увеличение числа больных в странах Персидского залива длится 10–15 лет: в Саудовской Аравии — 16,2 %, Кувейте —15,9 %, Катаре — 14,1 %, ОАЭ — 12,6 %; на Ямайке — 15,9 %, Китае — 9,3 %, Индии — 8,3 %, Малайзии — 11,7 %, Сингапуре — 11,1 %, США — 10,8 %, Узбекистане — 4,9 %, Кыргызстане — 4,8 % и в мире в среднем — 8,5 % [IDF Diabetes Atlas, 2011].
Основным методом лечения с 1922 г. являются заместительная терапия препаратами синтетического или животного инсулина, терапия таблетированными фармпрепаратами в сочетании со многими рекомендациями, касающимися питания, двигательной активности и пр. Этот принцип позволяет лечить, но не излечивать больных.
В последние годы за рубежом после многолетних экспериментальных пересадок на животных постепенно начал внедряться в клиническую практику трансплантационный метод лечения СД, предусматривающий пересадку больным изолированных панкреатических островков (В-клеток) поджелудочной железы, вырабатывающих гормон — инсулин. Конечной целью такого принципа является излечение больных. Наилучший достигнутый результат на сегодня — полная или близкая к полной компенсация потребностей организма в инсулине примерно на 2 года после одной трансплантации (это однократная, относительно несложная операция по трансплантации суспензии, состоящей минимально из 150–200 тыс. выделенных из поджелудочной железы очищенных панкреатических островков).
Мысль о пересадке островков возникла около 80 лет тому назад, однако тормозом в ее реализации являлась техническая невозможность изолирования и выделения из ткани поджелудочной железы панкреатических островков. Главным потенциальным и очевидным преимуществом ее является существующая реальная перспектива излечения СД, в отличие от заместительной терапии инсулином.
Переломным явился 1967 г., когда, наконец, был предложен эффективный метод ферментативного выделения из поджелудочной железы островков, радикально изменивший ситуацию [1]. Почти сразу же, с 1970 г. начались попытки экспериментальной пересадки изолированных островков больным диабетом животным. Под объединяющим началом Европейской Диабетологической Ассоциации (EASD) эта работа достаточно активно ведется в последние 30–35 лет. В Европе имеется множество центров диабетологической трансплантологии при различных клиниках и госпиталях, где шаг за шагом постепенно улучшают результаты трансплантации. На сегодня этот метод является экспериментально-клиническим. Основной недостаток заместительной терапии инсулином известен и состоит в том, что как только прекращается введение гормона — появляется прямая угроза жизни больного. Заместительная терапия инсулином, кроме того, по своему определению не имеет никаких перспектив стать методом излечения больного.
Данной проблеме уделяется серьезное внимание в Европе. Финансирование исследований в этом направлении все эти десятилетия постепенно только нарастает. Имеющиеся данные свидетельствуют о том, что сомнений в отношении перспективности данной работы нет и что через какое-то время этот метод постепенно станет значительно более широко распространенным в Европе. Сегодня уже нескольким тысячам больных осуществлена экспериментальная трансплантация островков. Суть трансплантологического метода лечения СД сводится к следующему:
Из поджелудочной железы животных ферментативным методом в результате дезагрегации волокон соединительной ткани изолируются панкреатические островки, подвергаются очистке и прекультивированию, после чего они готовы к пересадке. Для изоляции островков применяют фермент коллагеназу, расщепляющий коллагеновые волокна экзокринной ткани поджелудочной железы. В результате дезагрегации образуется суспензия, состоящая из изолированных островков, смешанная с фрагментами экзокринной ткани, подвергшейся дезагрегации. Их отделение осуществляют путем создания с помощью декстрана или фиколла градиента плотности. Островки при этом в плоскости занимают узкое пространство, откуда их отбирают пипеткой. Окончательная очистка производится 3–4-кратным промыванием в растворе Хенкса с последующим центрифугированием при малых оборотах. Количество поврежденных островков составляет в среднем от 10 до 15 % от общего числа изолированных. Последующее культивирование осуществляют в питательной среде с использованием ростовых факторов и глюкозы. Гистологические срезы залитых в парафин изолированных островков окрашивают на инсулин одним из нескольких методов с целью анализа состояния гистоструктуры и содержания депонированного инсулина (см. рис.) [2–15].
- Ткань поджелудочной железы крысы. Цинк-инсулиновый комплекс в В-клетках. Люминесцентная реакция на цинк с толуолсульфониламинхинолином; замороженный срез; ×140. Препарат и фото Диабетологической исследовательской группы.
- Изолированный панкреатический островок неонатальной крысы. Диэтилпсевдоизоцианин. Гистоструктура без изменений; значительное содержание инсулина в В-клетках (ярко-красная флюресценция); ×140. Препарат и фото Диабетологической исследовательской группы, 1990.
- Ткань поджелудочной железы крысы. Диэтилпсевдоизоцианин. Гистоструктура без изменений; значительное содержание инсулина в В-клетках (ярко-красная флюоресценция); ×140. Препарат и фото Диабетологической исследовательской группы.
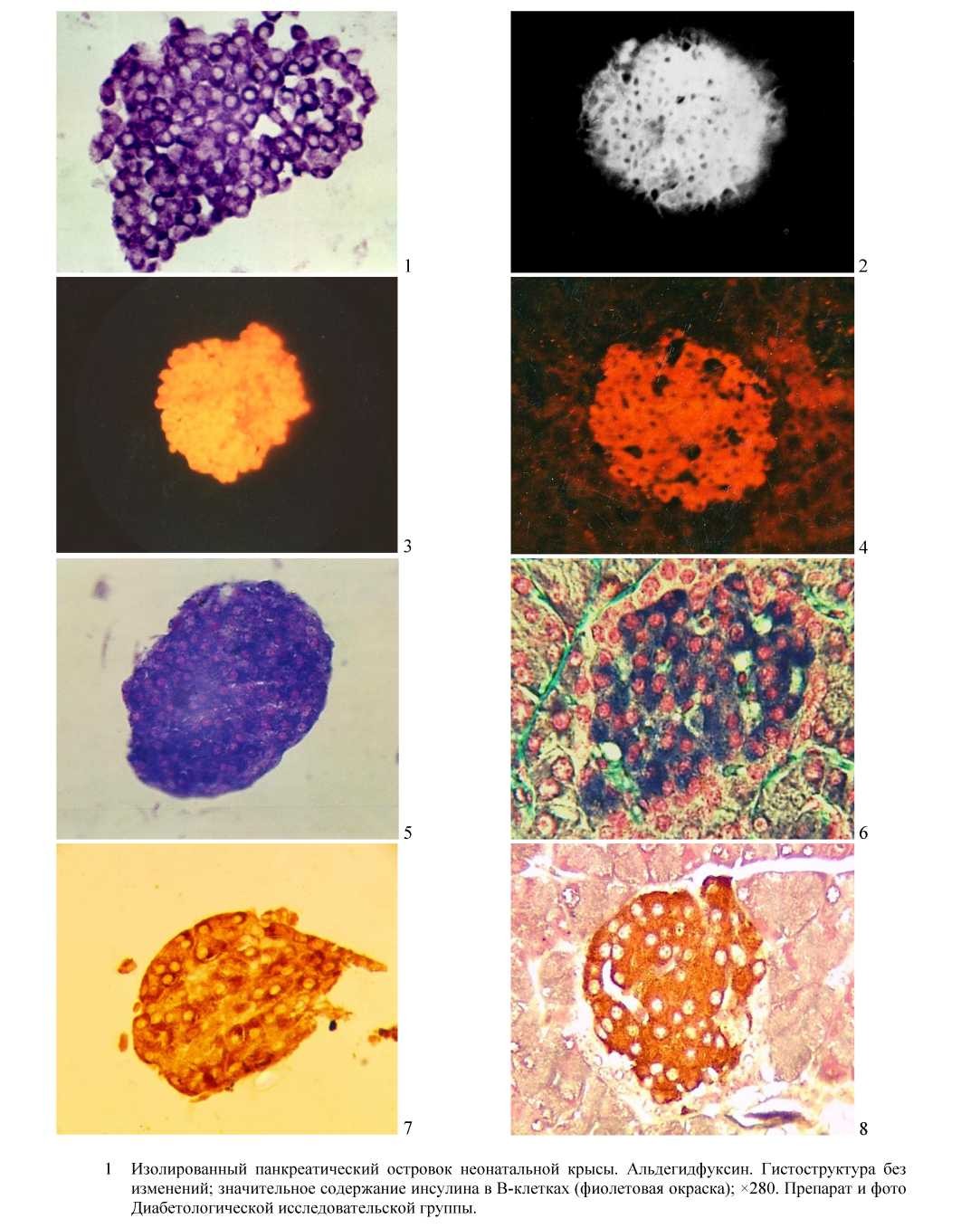
- Изолированный панкреатический островок неонатальной крысы. Виктория 4R. Гистоструктура без изменений; значительное содержание инсулина в В-клетках (фиолетовая окраска); ×280. Препарат и фото Диабетологической исследовательской группы.
- Ткань поджелудочной железы крысы. Виктория 4R. Гистоструктура без изменений; значительное содержание инсулина в В-клетках (фиолетовая окраска), А-клетки (розовый цвет); ×280. Препарат и фото Диабетологической исследовательской группы.
- Изолированный панкреатический островок неонатальной крысы. Иммуногистохимический метод. Гистоструктура без изменений; значительное содержание инсулина в В-клетках (коричневая окраска); ×280. Препарат и фото Диабетологической исследовательской группы.
- Ткань поджелудочной железы крысы. Иммуногистохимический метод. Гистоструктура без изменений; значительное содержание инсулина в В-клетках (коричневая окраска); ×280. Препарат и фото Диабетологической исследовательской группы.
Рисунок 1. Изолированные и очищенные панкреатические островки и ткань поджелудочной железы неонатальных крысят и крыс. Гистоструктура и содержание инсулина в В-клетках. Препараты и микрофотографии получены в Диабетологической исследовательской группе, г. Караганда (1977–2016 гг.)
Изоляция островков взрослых животных осуществляется несколько иным способом: раствор коллагеназы вводится в артерию поджелудочной железы, т.е. расщепление коллагеновых волокон происходит изнутри ткани.
Трансплантация в эксперименте осуществляется чаще в ткань печени путем инъекции суспензии островков в воротную вену (есть варианты пересадки под кожу, в мышечное ложе и др.) с помощью однократного введения их в количестве не менее 150 000–200 000. В настоящее время исследуются результаты трансплантации всеми способами, однако на сегодня в большей степени склоняются к пересадке в ткань печени.
Основная и самая затратная часть работы — получение материала, т.е. культуры изолированных и очищенных островков в необходимых количествах. Хирургический компонент не требует специальной операционной (5–10 % всех усилий и затрат).
Сегодня далеко не все вопросы в этой сфере мировой диабетологии решены в полной мере, но, несомненно, что пройдена значительная часть этого пути. Основной компонент — налаживание методов получения высокоочищенной суспензии изолированных островков (животных и доноров) в необходимых количествах. С этой целью при трансплантологических центрах организуются группы, занимающиеся решением связанных между собой проблем, которые условно можно разделить на две группы: 1) совершенствование технологии изоляции и подготовки панкреатических островков к экспериментальной (животным) и экспериментально-клинической (пациенту) трансплантации; 2) изучение отдаленных результатов трансплантации.
В составе таких подразделений имеются высокопрофессиональные гистологи и гистохимики с большим опытом работы в качестве гистолога (без высшего образования, или со средним образованием).
В гистологии и гистохимии поджелудочной железы за последние 50–60 лет уровень ручной работы сохранился почти полностью, так как встроить в этот процесс машинные технологии невозможно, аналогично тому, как если бы ручную работу реставратора картин попытаться заменить работой машин; по опыту нашей работы, если принять всю ручную работу гистолога поджелудочной железы за 100 % в 1964 г., то в 2015 г. ее объем составил не менее 95–98 % от уровня 1964 г., т.е. движения почти не произошло.
Представляется целесообразным следующий вариант возможной структурной организации работы.
- Группа 1 (лаборатория) по совершенствованию изоляции и культивирования панкреатических островков. Состав: препараторы-гистологи с длительным опытом и стажем работы в практическойгистологии и гистологии ткани поджелудочной железы, а также руководитель (с медицинским образованием), специалист-гистолог с опытом работы в практической гистологии поджелудочной железы.
Задачи Группы:
- совершенствование методов изоляции панкреатических островков ферментом коллагеназой;
- совершенствование очистки полученного материала;
- совершенствование культивирования островков при подготовке их к экспериментальной трансплантации животным.
Конечные цели в соответствии с задачами:
а) получить максимальное количество островков при минимальном проценте поврежденных;
б) максимальная очистка островков от примесей в виде обрывков экзокринной ткани, фрагментов поврежденных нежизнеспособных островков;
в) совершенствование методов культивирования: выбор наиболее подходящих питательных сред и ростовых факторов, способствующих более качественному и быстрому росту и дифференциации клеток;
г) овладение методами инкапсулирования островков при подготовке к трансплантации.
- Группа 2 экспериментальной трансплантологии. Ее имело бы смысл организовать в качестве функционирующей отдельной структуры в составе имеющихся центров или отделений трансплантации в городах, где они имеются.
Структурно группы могут входить в состав различных учреждений, но сотрудничающих по одной программе. При отборе препараторов-гистологов и руководителя кандидаты желательно должны:
- уметь самостоятельно изъять поджелудочную железу у экспериментального животного, зафиксировать ее, выполнить проводку, приготовить срезы и окрасить их по двум из описанных в данной статье методик с таким же качеством под наблюдением специалистов за проведением всех процедур;
- для руководителя дополнительно — иметь публикации с использованием гистологических методов окраски ткани поджелудочной железы. Группа 1 (лаборатория) не должна отвлекаться на обучение, специализации, подготовку магистрантов, докторантов и пр., что должно быть официально отражено в миссии и подтверждено соответствующим приказом руководителя, запрещающим все посторонние виды деятельности, поскольку ее задача — быть узко специализированным подразделением, а не учебным центром по совместительству.
Препараторы-гистологи должны отбираться из числа лаборантов-гистологов без высшего образования, имеющих длительный непрерывный, не менее 5 лет, опыт работы в практической гистологии в должности препаратора или лаборанта-гистолога и не менее 2-3 лет работавших с тканью поджелудочной железы.
О финансировании. На всех этапах, задачи которых определены выше и связаны с получением высококачественной культуры изолированных островков, необходимо финансирование не по грантовой системе, а постоянное, как и центры иного профиля (перинатальные, кардиологические и т.д.), в случае, если данная проблема будет сочтена вышестоящими инстанциями действительно актуальной и заслуживающей такого решения. Без решения проблемы финансирования вопрос об организации лаборатории может быть приостановлен. В конечном итоге, рано или поздно к положительному решению проблемы финансирования мы, вероятно, все же вынуждены будем прийти, так как постоянно нарастающая заболеваемость диабетом будет оказывать все возрастающее давление.
Органные трансплантации (сердца, почек и др.) отягощены необходимостью решения ряда сложных технических и организационных проблем, таких как техническая сложность трансплантации, поиск доноров, иммунологическая несовместимость. Нетрудно заметить, что трансплантация изолированных островков является относительно несложной процедурой, в значительно меньшей степени отягощенной названными выше проблемами, характерными для органных трансплантаций.
Учитывая определенные сложности, касающиеся поиска методик гистологического контроля состояния изолированных островков, ниже авторами приводятся детальные прописи фиксации и проводки ткани поджелудочной железы и методики окраски срезов на инсулин.
Методика окраски ткани поджелудочной железы альдегидфуксином Гомори в нашей модификации
1) ксилол — 5 мин; 2) ксилол № 2 — 5 мин; 3) ксилол № 3 — 5 мин; 4) абс. спирт 100º № 1 — 5 мин; 5) абс. спирт № 2 — 5 мин; 6) спирт 80º — 5 мин; 7) водопр. вода — 5 мин; 8) окислитель — 2 мин; 9) 2 % раствор щавелевой кислоты до обесцвечивания; 10) дист. вода — 5 мин; 11) альдегид- фуксин («MERCK», ФРГ; «SERVA», ФРГ) — 5-7 мин; 12) 70º подкисленный спирт 1 — дифференцировать; 13) 70о подкисленный спирт № 2 — дифференцировать; 14) смесь Хальми —1 мин;
- дист. вода — 5 мин; 16) дист. вода — 5 мин; 17) абс. спирт № 3 — 5 мин; 18) абс. спирт № 4 — 5 мин; 19) ксилол № 3 — 5 мин; 20) ксилол № 4 — 5 мин; 21) заключение в бальзам. Результат: инсулин окрашивается в фиолетовый цвет (см. рис., поз. 1 и 2).
Методика окраски ткани поджелудочной железы диэтилпсевдоизоцианином по Coalson
1) ксилол № 1 — 5 мин; 2) ксилол № 2 — 5 мин; 3) ксилол № 3 — 5 мин; 4) абс. спирт 100º № 1 — 5 мин; 5) спирт 90º — 5 мин; 6) спирт 80º — 5 мин; 7) водопр. вода — 5 мин; 8) окислитель — 2 мин; 9) 2 % раствор щавелевой кислоты — до обесцвечивания; 10) дист. вода — 5 мин; 11) 0,4 % водный раствор псевдоизоцианина (производства фирмы «SERVA», ФРГ) — 15–20 мин; 12) 70º подкисленный спирт 1 — дифференцировать; 13) сполоснуть в 2-х порциях дист. воды и оставить в холодильнике на 2 ч; 14) люминесцентная микроскопия (длина волны 360–370 нм; желтый возбуждающий светофильтр на лампе; запирающий фильтр на окуляре). Результат: инсулин в В-клетках флюоресцирует ярко-красным светом (см. рис., поз. 3 и 4).
Методика окраски ткани поджелудочной железы реактивом «Victoria 4R» (диметилнафтил- метан, цв. индекс 42563)
Растворы:
- Протравливающий раствор: охлажденная жидкость Буэна (100 мл) + алюмохром (3–4 г).
- Окислитель: 0,3 % раствор KMnO4 (50 мл) + 0,3 % раствор серной кислоты.
- Раствор «Victoria Blue»: 96º спирт + реактив «Victoria 4R» (1 г).
- Красящий раствор: раствор «Victoria Blue» (25 мл) + 96º спирт (100 мл) + глицерин (300 мл) + + 1 % ледяная уксусная кислота (25 мл). Наилучшие результаты получены на 10–20 дни после приготовления раствора.
Процедуры:
1) фиксация поджелудочной железы в жидкости Буэна 24–48 ч; промыть в 70º спирте; 2) заливка в парафин; 3) приготовить срезы толщиной 5 мкм; 4) парафиновые срезы поместить ненадолго в воду и затем в протравливающий раствор на 24–72 ч при +37 ºС; 5) промыть срезы в проточной воде до обесцвечивания; 6) окислитель — 3–5 мин; 7) хорошо промыть в воде; 8) промыть в 2–5 % растворе бисульфита натрия 1 мин; 9) хорошо промыть в воде; 10) 70º спирт — 1 мин; 11) окраска красящим раствором 45 мин — 24 ч при комнатной температуре, В-клетки окрашиваются в синий цвет; 12) промыть в воде; 13) дифференцировать в 70º спирте до обесцвечивания других типов клеток; 14) промыть в дистиллированной воде 1 мин; 15) окраска 0,5 % раствором флоксина 30–120 с;
промыть в дистиллированной воде 1 мин; 17) 5 % раствор фосфорвольфрамовой кислоты — 1–2 мин; 18) промыть в проточной воде 1–2 мин до возвращения красной окраски флоксина; 19) промыть в дистиллированной воде; 20) окраска водным 0,5 % раствором «Светлого зеленого» 1–2 мин; 21) дегидратация 2 раза в 96º спирте, просветление в ксилоле и заливка в бальзам.
Результат:
Гранулы инсулина в В-клетках окрашены в синий цвет. А-клеток — в красный. Ядра красные, экзокринная ткань — пурпурно-розового, коллагеновые волокна — зеленые, эластические волокна — синие (см. рис., поз. 5 и 6).
Иммуногистохимический метод окраски инсулина в В-клетках
Для окраски используются готовые стандартные наборы реактивов, выпускаемые зарубежными производственными объединениями, в которых количество процедур окраски сведено к минимуму и не требует высокой квалификации сотрудника. По стоимости окраски одного препарата метод в несколько раз дороже описанных выше методик и несопоставим с альдегидфуксиновым методом и методом «Victoria 4R», значительно превосходящими иммуногистохимический метод по возможности оценки состояния гистоструктуры панкреатических островков и экзокринной ткани. Комплекс инсу- лин–антитело окрашивается в насыщенный коричневый цвет (см. рис., поз. 7 и 8).
Выводы
- По проблеме № 3 «Сахарный диабет» в Республике Казахстан пока нет какого-либо института данного профиля или диабетологических исследовательских центров, в отличие от двух первых проблем медицины — № 1 «Сердечно-сосудистые болезни» и № 2 «Онкологические заболевания» (имеются кардиоцентры почти в каждой области, спеццентры кардиохирургии и онкоцентры, а также специализированные НИИ). В дальнейшем, в связи с продолжающимся интенсивным ростом распространенности СД, возрастающая острота проблемы рано или поздно приведет к необходимости организации такой структуры экспериментально-клинического характера.
- В этом направлении предстоит терпеливая и кропотливая рутинная работа, к чему надо быть готовыми. Существует и альтернативный вариант, а именно в течение ближайших 5-10 лет следует ожидать дальнейшего прогресса в этой области, после чего можно активизировать работу у нас.
- Согласно имеющимся тенденциям, у трансплантационного метода лечения при диабете, несомненно, хорошие перспективы стать методом более радикального лечения диабета. Конечные траты будут, очевидно, заметно меньшими: достаточно сказать, что по состоянию на сегодняшний день специальные хирургические центры по пересадке островков на начальном этапе вряд ли потребуются, так как вся хирургическая часть трансплантации островков на сегодня не представляет особой технической сложности.
Руководитель работы выражает признательность производственным объединениям «Boehringer Mannheim>>(ΦPΓ), <<Hoechst>>(ΦPΓ), «SERVA» (ФРГ), «FERAK» (ФРГ), «MERCK» (ФРГ), «SARTORIUS» (ФРГ), «Pharmacia Fine Chemicals» (Швеция) за безвозмездно предоставлявшиеся в течение многих лет реактивы и препараты, необходимые для выполнения исследований.
Список литературы
- Lacy R.E. Method for the isolation of intact islets of Langerhans from the rats pancreas / R.E. Lacy, M. Kostianovsky // Diabetes. — 1967. — Vol. 16, No. 1. — P. 35-39.
- Kvistberg D. Staining of insulin with aldehyde fucshin / D. Kvistberg, G. Lester, A. Lasarov // J. Histochem Cytochem. — 1966. — Vol. 14. — P. 609-611.
- Ortman R. Concerning the staining properties of aldehyde basic fucshin / R. Ortman, W. Forbes, A. Balasubramanian // J. Histochem. — 1966. — Vol. 14. — P. 104-111.
- Orci G. Some aspects of the morphology of insulin secreting cells / G. Orci // Acta Histochem. — 1976. — No. 1. — P. 147158.
- Schiebler T.H. Uber den Nachweisvon Insulin mitden metachromatisch reagierenden Pseudoisocyaninen / T.H. Schiebler, S. Schiessler // Histochemie. — 1959. — Vol. 1. — S. 445-465.
- Coalson R.E. Pseudoisocyanine staining of insulin and specifity of emperical islet cell stain / R.E. Coalson // Stain Technol. 1966. — No. 2. — P. 121-129.
- Meyramov G.G. Fluorescent histochemical method staining of insulin in B-cells of isolated pancreatic islets by diethylpseudoisocyanine chloride / G.G. Meyramov, A.A. Kikimbaeva, A.G. Meyramova // Acta Diabetologica, the European Diabetes Journal. — 2005. —Springer, Vol. 42, No. 1. — P. 66.
- Wohlrab F. On the specifity of the insulin staining by Victoria Blue 4R / F. Wohlrab, H. Dorsche, I. Krautschick, S. Schmidt // Histochem. Journal. — 1985. — Vol. 17. — P. 515-518.
- Meyramov G.G. “Victoria 4R” method staining of insulin in B-cells of isolated pancreatic islets / G.G. Meyramov, A.A. Kikimbaeva, A.G. Meyramova // Acta Diabetologica, the European Diаbetes Journal. — Springer Int., 2003. — Vol. 40, No. 4.P. 208.
- Meyramov G.G. The histofunctional method appreciating of functional state of isolated pancreatic B-cells in the tissue culture / G.G. Meyramov, G.T. Tusupbekova, R.G. Meyramova // Diabetes Research and Clinical Practice, the Journal of International Diabetes Federation. — New York - Amsterdam: Elsevier, 1988. — Vol. 5. — P. 226, 227.
- Meyramov G.G. Gluthation's reduced form protect B-cells from destruction caused by diabetogenic ligands / G.G. Meyramov, A.S. Shaybek et al. // Diabetes, a Journal of American Diabetes Association. — 2015. — Vol. 64, No. 7, S. 1. — P. 735.
- Sternberger L.A. Immunocytochemistry. — 2nd Ed. / L.A. Sternberger. — New York - Chichester - Brisbane - Toronto: John Willey & Sons, 1979.
- Meyramov G.G. The high specific method for revealing of zinc ions in pancreatic B-cells/ G.G. Meyramov,
- T. Tusupbekova, R.G. Meyramova // Diabetes, a Journal of American Diabetes Association. — 1991. — Vol. 40, S. 1. — P. 65.
- Мейрамов Г.Г. Гистохимическое выявление инсулина в культуре эндокринной ткани поджелудочной железы с помощью псевдоизоцианинового и иммунофлюоресцентного методов / Г.Г. Мейрамов, К.-Д. Конерт, Р.Г. Мейрамова // Проблемы эндокринологии. — М., 1990. — Т. 36, № 1. — С. 66-69.
- Kikui Y. Differential staining method for A- and B-cells in the pancreatic islets of Langerhans / Y. Kikui, H. Seguchi,
- A. Mizoguti // Acta Histochem. Cytochem. — 1977. — Vol. 10, No. 1. — P. 10-13.