Своевременная диагностика — залог успешного проведения профилактических мероприятий по устранению тех или иных болезней. Для быстрой детекции и точной идентификации возбудителя вызывающего пятнистость листьев пшеницы необходима разработка высокочувствительного и скоростного метода анализа. В данных исследованиях проведены работы по разработке высокоспецифичного метода ПЦР для диагностики фитопатогенного гриба Zymoseptoria tritici. В результате исследований были отобраны нуклеотидные последовательности для Zymoseptoria tritici из базы данных GenBank. Используя данные последовательности, были сконструированы и синтезированы специфические праймеры. Проведены работы по отработке оптимальных условий проведения ПЦР по таким параметрам, как концентрации ДНК полимеразы, ионов Mg2+ и дНТФ. Также осуществлены работы по определению чувствительности и специфичности разработанного метода ПЦР. Чувствительность данного метода составила 0,69 пг ДНК патогена в исследуемом материале. В результате исследований специфичности установлено, что разработанный метод не выявил ДНК гетерологичных грибов. Таким образом, разработанный метод диагностики на основе ПЦР для выявления гриба Zymoseptoria tritici показал высокую специфичность и чувствительность который в дальнейшем может использоваться в качестве диагностического набора на основе ПЦР для выявления гриба Zymoseptoria tritici.
Введение
Мировые эксперты в области продовольствия утверждают, что самым важным показателем национальной безопасности страны является производство зерна пшеницы. По данным международной продовольственной и сельскохозяйственной организаций, огромные потери урожая пшеницы происходят от вредителей на 34 %, а от болезней на — 12 % [1]. Десятилетиями Казахстан производит зерно, которое покрывает не только внутренний рынок страны, но и рынок республик Средней Азии. Являясь одним из крупных производителей зерна республика ежегодно теряет более 30 % от общего количества урожая [2; 38, 3]. Одной из причин этому являются грибковые болезни пшеницы, среди которых немаловажную роль в причинении урона урожаю отводится Z. tritici.
Z. tritici является разновидностью мицелиального гриба, аскомицета из семейства Mycosphaerellaceae. Данный возбудитель поражает только листья и проявляется на ранней стадии развития растения. Патоген вызывает пятнистость листьев, которую трудно контролировать из-за устойчивости к множественным фунгицидам [4]. Контроль над Z. tritici был основан на комбинации применения фунгицидов и селекции устойчивых сортов [5, 6]. Повышение уровня нечувствительности к системным фунгицидам и принятие политики по сокращению пестицидов в соответствии с европейским законодательством [7] означают, что сейчас существует большая потребность в разработке современных диагностических средств, для своевременного выявления ДНК гриба Z. tritici. Сегодня для диагностики гриба Z. tritici наряду с морфологическими исследованиями широко используют молекулярно-биологические и иммунологические методы. Однако недостатки данных методов, обусловленные низкой чувствительностью, трудоемкостью проведения работы, и затраты длительного времени создают необходимость разработки более чувствительного и быстрого метода детекции.
Молекулярно-биологические и генно-инженерные достижения последнего десятилетия создают возможность разработки различных методов для специфической диагностики фитопатогенных микроорганизмов. Метод полимеразной цепной реакции (ПЦР) по сравнению с традиционными иммунологическими методами более чувствителен и специфичен. ПЦР широко используется в целях дифференциации и своевременном обнаружении возбудителей различных заболеваний. Для диагностики возбудителей видов септориоза были разработаны многочисленные методы молекулярной идентификациигрибов на основе ПЦР [8-12]. Недостатки данных методов, обусловленные ограниченной специфичностью, необходимостью создания стандартной кривой при каждой постановке реакции, а также трудности, связанные с контаминацией смеси при постановке реакции в режиме реального времени, создают необходимость разработки классического метода анализа обладающей высокой специфичностью. Исходя из изложенного выше, целью данной работы является разработка метода ПЦР для диагностики фитопатогенного гриба Z. tritici.
Материалы и методы исследования
Подбор и синтез праймеров. Подбор праймеров осуществляли с использованием GenBank NCBI (http://www.ncbi.nlm.nih.gov/GenBank) и программного обеспечения CLC GenomicsWorkbench 11.0.1 (Qiagen). Специфичность олигонуклеотидных праймеров проверяли в программе BLAST. Синтез оли- гонуклеотидных праймеров проводили на автоматическом синтезаторе фирмы K&A Laborgeraete, модели DNA/RNA Synthesizer H-16 (производство Германии), амидофосфитным методом согласно инструкции производителя.
Выделение и выращивание возбудителя септориоза. Выделение и выращивание чистой культуры проводили по стандартной методике [13].
Выделение ДНК грибов. Выделение ДНК проводили как из чистой культуры, так и из образцов пораженных листьев. К 100 мкл пробы добавляли 700 мкл буфера СТАВ предварительно разогретого до 65 °С (после нагревания в буфер добавляли ß-меркаптоэтанол 400 мкл на 20 мл буфера). И тщательно перемешивали. Далее заливали такой же объем хлороформа и тщательно вортексировали. Центрифугировали в течение 5 мин при 13000 об/мин, супернатант переносили в новые 1,5 пробирки. Повторяли этап экстракции хлороформом. К супернатанту добавляли 2/3 объема изопрапанола, вортек- сировали и центрифугировали в течение 5 мин при 13000 об/мин. Надосадок аккуратно сливали и проводили промывку осадка 75 % спиртом. Центрифугировали в течение 60 с при 13000 об/мин, надосадки аккуратно сливали и осадки подсушивали при комнатной температуре с открытой крышкой. Осадок растворяли в 50 мкл стерильной дистиллированной воде [14].
ПЦР-амплификация. ПЦР-реакция проводилась с использованием амплификаторов Master- cyclerProS (Eppendorf, Германия) и SimpliAmpThermalCycler (AppliedBiosystems, США). В реакционную смесь использовали 10× ПЦР буфер (Sileks, Москва, Россия), 10 мМдНТФ (Invitrogen, США), 25 мМ MgCl2 (Sileks, Москва, Россия), Taq полимераза (Sileks, Москва, Россия).
Анализ результатов. Разделение продуктов амплификации проводили с использованием электрофореза в 1 % агарозном геле, содержащем 1 мкг/мл бромистого этидия в трис-ацетатном буфере. Для детекции результатов ПЦР использовали трансиллюминатор BioRad.
Секвенирование ДНК грибов. Секвенирование фрагментов амплификации выполняли с помощью набора BigDyeTerminatorCycleSequencingkit v 3.1 («AppliedBiosystems», США), согласно инструкции изготовителя, на 3130xl GeneticAnalyzer («AppliedBiosystems», США). Сборку и анализ полученных в результате секвенирования последовательностей проводили с использованием программы Sequencher v. 5.4.1.
Результаты исследований и их обсуждение
В наших исследованиях по подбору специфических праймеров мы остановились на участках внутренних транскрибированных спейсерах (ITS1-ITS2). Два ITS регионы часто используют для дифференциации грибов на уровне родов и видов. Эти участки генома грибов окружают последовательность, кодирующую 5.8S рРНК, и расположены между генами, кодирующими 18S рРНК (малая субъединица — SSU) и 28S рРНК (большая субъединица — LSU). Регион ITS очень стабилен, присутствует в нескольких повторностях и обычно консервативен внутри вида [15]. Для подбора праймеров был проведен поиск нуклеотидных последовательностей ITS в международной базе данных GenBank. Были отобраны последовательности для гриба Z. tritici. Выравнивание нуклеотидных последовательностей и подбор специфических праймеров проводили с использованием программы CLC Genomics Workbench v.11.0.1. Подобранные праймеры были проверены на специфичность с использованием программы BLAST. Для дальнейших работ были выбраны праймеры, показывающие 100 % специфичность с соответствующим возбудителем. Таким образом, была подобрана пара специфических праймеров — ZT191F и ZT444R, амплифицирующие участок длиной 254 п.н., характерный только для Z. tritici.
Подобранные праймеры были синтезированы на синтезаторе олигонуклеотидов фирмы K&A Laborgeraete. Представленные характеристики праймеров полностью соответствуют требуемым параметрам олигонуклеотидов, используемых для постановки ПЦР.
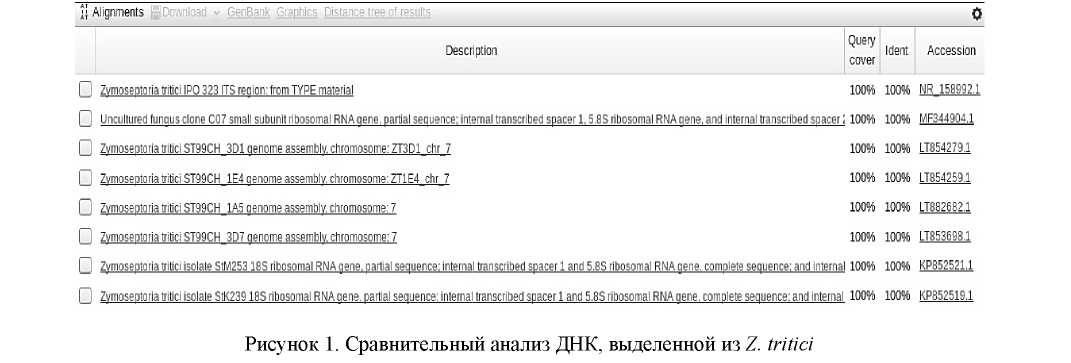
Важным этапом при начальной отработке ПЦР является наличие специфичной ДНК. С целью получения качественной и специфичной ДНК проводили наработку моноконидиальных культур грибов. Чистоту культуры подтверждали микроскопическим методом. Из полученной культуры выделяли ДНК и определяли его видовую идентичность с помощью секвенирования. Для этого проводили наработку ПЦР-продукта с использованием универсальных праймеров на ITS регион (ITS-4 — TCCTCCGCTTATTGATATGC и ITS-5- GGAAGTAAAAGTCGTAACAAGG) [16]. Полученный ПЦР- продукт секвенировали на 16-капиллярном секвенаторе 3130xl GeneticAnalyzer. Полученные в ходе секвенирования нуклеотидные последовательности сравнивали с помощью программы BLAST с последовательностями, размещёнными в международном банке генов GenBank. Результаты сравнительного анализа представлены на рисунке 1.
Таким образом, было получено 100 %-ное подтверждение чистоты имеющихся культур, что необходимо для оптимизации всех параметров ПЦР.
Для получения специфической и эффективной амплификации проводили работы по определению оптимальной концентрации каждого реагента входящего в состав смеси. Оптимизированы были такие реагенты, как Taq ДНК полимераза, концентрации дНТФ, праймеров и ионов Mg2+. При амплификации использовали следующие параметры: начальная ПЦР-активация при 94 ºС — 3 мин, денатурация при 94 ºС — 30 с, отжиг при 60 ºС — 30 с, элонгация при 68 ºС — 1 мин 20 с, финальная элонгация при 68 ºС — 5 мин, амплификацию ПЦР осуществляли в течение 35 циклов.
Активность ДНК полимеразы является одним из наиболее важным при проведении оптимизации ПЦР. Концентрация полимеразы подбирается в зависимости от праймеров или мишени НК. При высокой концентрации может наработаться неспецифический продукт, при более низкой нарабатывается недостаточное количество амплификата. Обычно рекомендуется использовать ДНК полимеразу в конечной концентрации 0,5-2,5 ед. на 50 мкл реакционной смеси. Для отработки оптимальной концентрации ДНК полимеразы нами был выбран диапазон от 0,5 до 4 ед. Состав реакционной смеси содержал 0,2 мM дНТФ, 2 мM Mg2+ и 400 нM каждого праймера. Результаты представлены на рисунке 2.
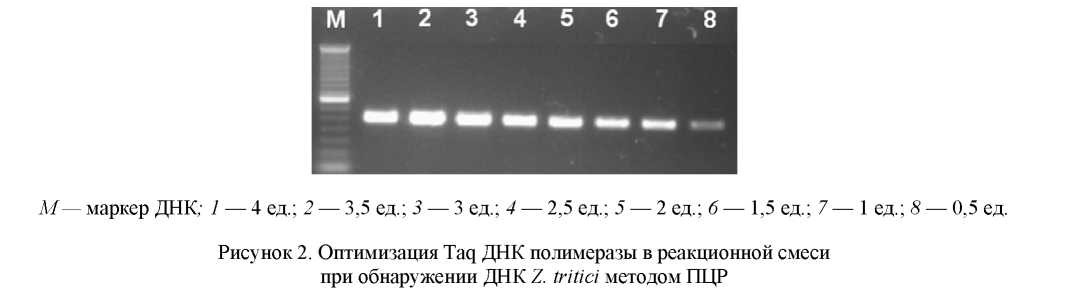
Как видно из рисунка 1, концентрация Taq ДНК-полимеразы влияет на выход конечного продукта. Видно, что с повышением концентрации фермента в реакционной смеси происходит увеличение интенсивности полос, а, следовательно, и концентрации ДНК. Однако при активности фермента всего 0,5 ед. нарабатывается ПЦР-продукт, который достаточно легко визуализировать в 1 %-ном агарозном геле в присутствии бромистого этидия под УФ-светом. Для дальнейшей отработки метода была выбрана концентрация 1 ед. Taq ДНК полимеразы.
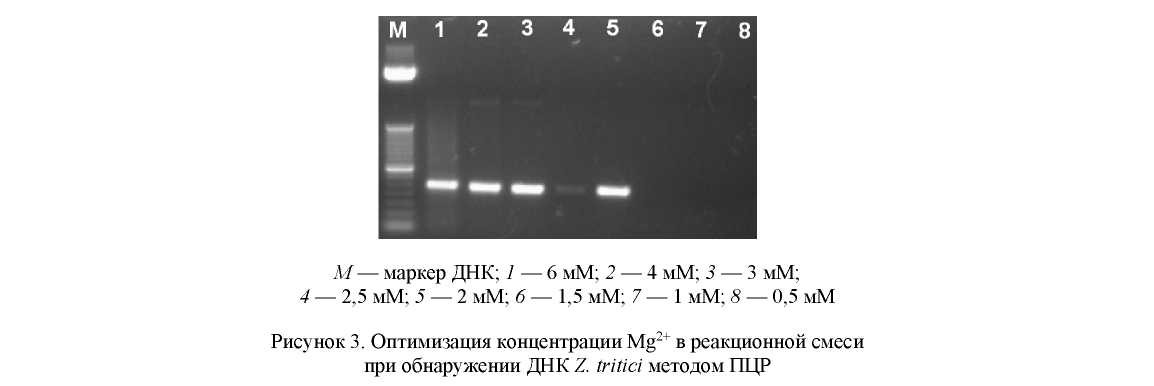
При постановке ПЦР немаловажную роль играет и концентрация Mg2+ в реакционной смеси. Ионы Mg2+ взаимодействуют с другими компонентами реакционной смеси, формируют комплексы с дНТФ и стабилизируют двухцепочечную ДНК. Концентрация Mg2+ также влияет на отжиг праймеров и денатурацию образца. Однако его избыток может вызывать образование неспецифических продуктов, а недостаток может приводить к низкой эффективности амплификации. Рекомендуемая концентрация Mg2+ составляет 1–4 мМ, однако оптимальная концентрация должна быть определена экспериментально. В экспериментах мы испытывали концентраций Mg2+ от 0,5 до 6 мМ (рис. 3). Реакционная смесь содержала 1 ед. ДНК полимеразы, 0,2 мМдНТФ и 400 нМ каждого праймера.
Как видно из данных на рисунке 3, амплификация специфичного продукта наблюдается при концентрациях от 2 до 6 мМ, однако при концентрации Mg2+ выше 2,5 мМ наблюдается появление неспецифических продуктов реакции. В результате для дальнейших экспериментов использовали ионы Mg2+ в концентрации 2 мМ.
Дезоксирибонуклеозидтрифосфаты (дНТФ) служат субстратами для процесса элонгации. Также дНТФ уменьшает количество свободных ионов Mg2+, что, в свою очередь, влияет на активность фермента и температуру отжига праймеров. Оптимальная концентрация дНТФ обычно составляет 0,2 мМ. Для оптимизации данного параметра мы испытывали концентрации дНТФ в пределах от 0,01 до 1 мМ (рис. 4). Реакционная смесь содержала 1 ед. ДНК полимеразы, 2 мМ Mg2+ и 400 нМ каждого праймера.
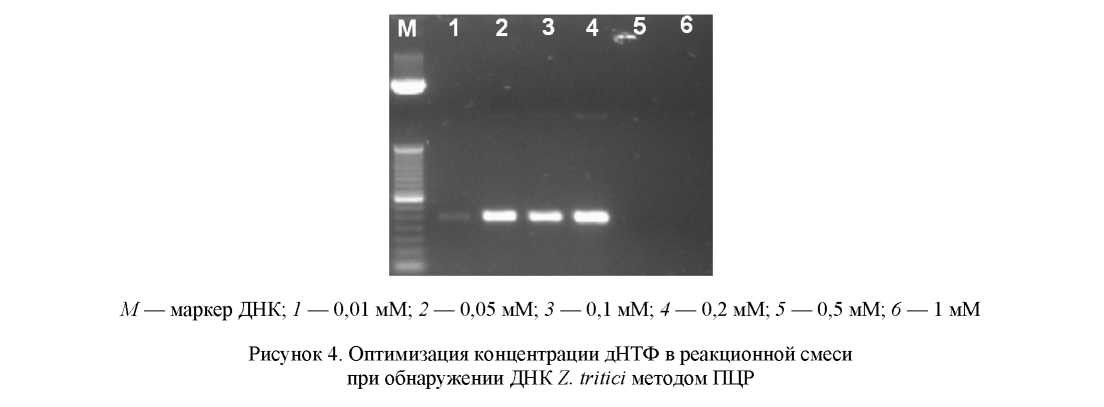
Как видно из рисунка 4, наработка ПЦР-продукта прекращается при использовании концентрации дНТФ от 0,5 мМ и выше. Для проведения дальнейших исследований была выбрана оптимальная концентрация дНТФ — 0,2 мМ.
В результате оптимизации компонентного состава были определены следующие оптимальные концентрации реакционной смеси — 1 ед. ДНК полимеразы, 0,2 мМ дНТФ, 2 мМ Mg2+ и по 400 нМ каждого праймера.
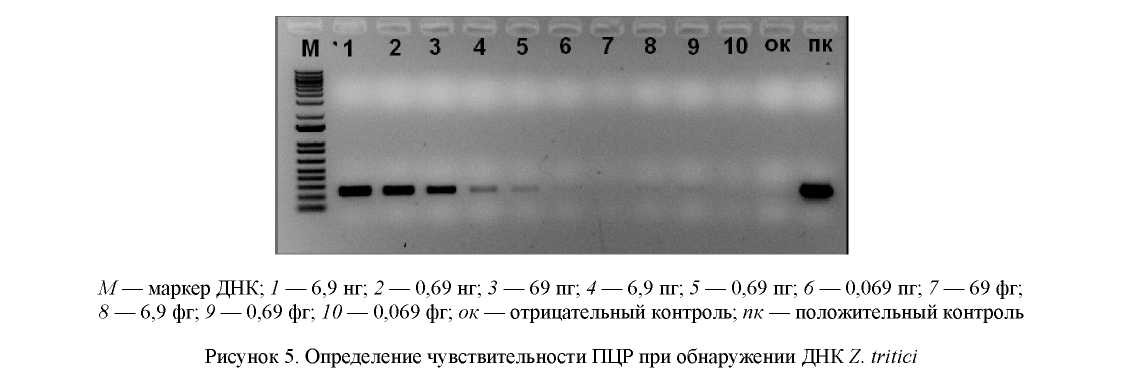
Основными факторами, определяющими преимущества одного метода диагностики над другим, являются чувствительность и специфичность. Известно, что достоинством ПЦР является чрезвычайно высокая чувствительность этого молекулярно-биологического исследования. Далее, используя оптимальный состав реакционной смеси, определяли чувствительность разрабатываемого метода ПЦР. При определении чувствительности разработанной ПЦР использовали 10-кратные разведения ДНК от 69 нг до 0,069 фг. Результаты данных опытов представлены на рисунке 5.
Чувствительность данного метода ПЦР составила 0,69 пг ДНК Z. tritici в пробе (рис. 5). Данные результаты показали, что отработанный метод ПЦР обладает высокой чувствительностью.
Специфичность метода ПЦР многократно превосходит любые другие используемые методы диагностики, в том числе ИФА. Далее проводили определение специфичности разработанного метода ПЦР. Для идентификации гриба Z. tritici использовали ДНК гриба Z. tritici и ДНК гетерологичных грибов Pyrenophoratritici-repentis, Parastagonosporanodorum, AlternariaInfectoria, AlternariaAlternata, Fusarium, Epicoccum, Ascomycota, Leconicillium, Stemphylium, подтвержденные секвенированием, а в качестве положительного контроля ДНК Z. tritici ITC и отрицательного контроля — воду. Результаты проведенных исследований представлены на рисунке 6.
Как видно из рисунка 6 только в пробах, содержащих ДНК гриба Z. tritici, нарабатываются специфические продукты реакции размером около 254 п.н. (дорожки 1 и пк). Отрицательные результаты

были получены при использовании в качестве матриц ДНК остальных гетерологичных грибов, кроме ДНК Epicoccum-28 (дорожка 10). Однако данный продукт нарабатывается более тяжелым размером, тем самым эта ДНК не является специфическим продуктом для данной реакции. Отсутствие каких- либо продуктов амплификации наблюдается и с деионизированной водой. Полученные результаты демонстрируют высокую специфичность разработанного нами способа диагностики ДНК гриба Z. tritici.
Таким образом, в результате проведенных исследований установлено, что во всех пробах, содержащих ДНК гриба Z. tritici, нарабатывался специфический ПЦР-продукт, соответствующий расчетному размеру.
Заключение
В результате проведенных исследований при разработке ПЦР для диагностики фитопатогенного гриба Z. tritici были подобраны видоспецифические праймеры, отработаны оптимальные параметры для постановки реакции. Разработанный способ диагностики на основе ПЦР для выявления гриба Z. tritici показал высокую специфичность и чувствительность (0,69 пг ДНК).
Исследования выполнены при поддержке Министерства сельского хозяйства Республики Казахстан в рамках ПЦФ «Разработка инновационных систем для повышения устойчивости сортов пшеницы к особо опасным болезням в Республике Казахстан» на 2018–2020 гг. (№ BR06249329).
Список литературы
- FAO statistical yearbook. World food in agriculture. — Rome. — 2013. — P. 289.
- Койшыбаев М. Болезни зерновых культур / М. Койшыбаев. — Алматы: Бастау, 2002. — С. 38–40.
- Рсалиев Ш.С. Анализ состава популяций стеблевой и листовой ржавчины пшеницы на территории Казахстана / М.К. Койшибаев, А.И. Моргунов, Д. Колмер // Материалы междунар. науч.-практ. конф. — Алматы, 2005. — С. 267–272.
- Stukenbrock E.H. Whole-Genome and Chromosome Evolution Associated with Host Adaptation and Speciation of the Wheat Pathogen Mycosphaerella graminicola / E.H. Stukenbrock, F.G. Jørgensen, M. Zala, T.T. Hansen, B.A. McDonald, M.H. Schierup // PLoS Genetics. — 2010. — No. 6. — С. 12.
- Orton E.S. Mycosphaerella graminicola: from genomics to disease control / E.S. Orton, S. Deller, J.K.M. Brown // Molecular Plant Pathology. — 2011. — No. 12. — Р. 413–424.
- Torriani S.F.F. Zymoseptoriatritici: a major threat to wheat production, integrated approaches to control / S.F.F. Torriani, J.P.E. Melichar, C. Mills, N. Pain, H. Sierotzki, M. Courbot // Fungal Genetics and Biology. — 2015. — No. 79. — Р. 8–12.
- Jess S. European Union policy on pesticides: implications for agriculture in Ireland / S. Jess, S. Kildea, A. Moody, G. Rennick, A.K. Murchie, L.R. Cooke // Pest Management Science. — 2014. — No. 70. — Р. 1646–1654.
- Beck J.J. Polymerase chain reaction assays for the detection of Stagonospora nodorum and Septoriatritici in wheat / J.J. Beck, J.M. Ligon // Phytopathology. — 1995. — Vol. 85. — Р. 319–324.
- Fraaije B.A. Rapid detection and diagnosis of Septoriatritici epidemics in wheat using a polymerase chain reaction / PicoGreen assay / B.A. Fraaije, D.J. Lovell, E.A. Rohel, D.W. Hollomon // Journal of Applied Microbiology. — 1999. — Vol. 86. — Р. 701– 708.
- Абрамова С.Л. Диагностика фитопатогенных грибов Septoriatritici и Stagonospora nodorum методом FLASH ПЦР / С.Л. Абрамова, Д.Ю. Рязанцев, Т.М. Воинова, С.К. Завриев // Биоорганическая химия. — 2008. — № 34. — С. 107–113.
- Abd-Elsalam K. Detection of Mycosphaerella graminicola in Wheat Leaves by a Microsatellite Dinucleotide Specific-Primer / K. Abd-Elsalam, A.H. Bahkali, M. Moslem, P.J. De Wit, J.A. Verreet// International Journal Molecular Science. — 2011. — Vol. 12. — Р. 682–693.
- Consolo V.F. A conventional PCR technique to detect Septoriatritici in wheat seeds / V.F. Consolo, C.M. Albani, C.M. Beron, G.L. Salerno, C.A. Cordo // Australasian Plant Pathology. — 2009. — Vol. 38. — Р. 222–227.
- Bilay V.I. Methods of experimental mycology / V.I. Bilay. — Kiev: Naukova Dumka, 1973. — Р. 30–187.
- Edwards S.G. PCR-based detection and quantification of mycotoxigenic fungi / S.G. Edwards, J.O'Callaghan, A.D.W. Dobson // Mycology Res. — 2002. — Vol. 106. — Р. 1005–1025.
- Hughes K.W. Using heterozygosity to estimate a percentage DNA sequence similarity for environmental species' delimitation across basidiomycete fungi / K.W. Hughes, R.H. Petersen, E.B. Lickey // New Phytology. — 2009. — Vol. 182. — Р. 795–798.
- White T.J. Amplification and direct sequencing of fungal ribosomal RNA genes for phylogenetics: PCR Protocols: a Guide to Methods and Applications / T.J. White, T. Bruns, S. Lee, J. Tailor. New York: Academic Press Inc, 1990. — Р. 315–322.