В статье проанализированы исторические аспекты развития хирургии рака пищевода в Южно- Казахстанской области. Анализирован 17 летний опыт хирургического лечения 342 больных раком пищевода. Мужчин было 253 (74%), женщин 89 (26%). I-II стадией было 39 (11,4%), III стадией 281 (82,2%), IV стадией 22 (6,4%) больных. Гистологический плоскоклеточный рак выявлен у 334 (97,7%), аденокарци-нома у 8 (2,3%) больных. Экстирпация пищевода произведена 11 больным (3,2%), операция типа Льюиса 331 больным (96,8%). В послеоперационном периоде осложнения отмечены у 17-х больных (5%), в 12 случаях (3,5%) наблюдалась несостоятельность анастомоза, у 5-х послеоперационный рубцовый стеноз анастомоза (1,5%). Общая послеоперационная летальность составила 22 (6,4%) случаев. Основными причинами летальных исходов были несостоятельность анастомоза и сопутствующие сердечно-сосудистые заболевания. При динамическом наблюдении одногодичная летальность составила 17,8%, что в основном связано с возникновением локорегиональных метастазов и прогрессирования процесса. При контрольном осмотре 64% больных живут 3 года. Пятилетняя выживаемость составила 18,2%.
Ключевые слова: рак пищевода,онкологические больные, операция, стандарты лечения.
Проблема заболеваемости и смертности, а также своевременное лечение рака пищевода остается одной из актуальных проблем современной онкологии. Рак пищевода занимает восьмое место в структуре заболеваемости (4,1-4,5 на 100 тыс. населения) и пятое в структуре смертности (5,2%) злокачественными опухолями в Республике Казахстан. Вместе с тем, одногодичная летальность при этой патологии находится на одной из первых мест среди онкологических больных, составляя 23,9-25%. В Южно-Казахстанской области (ЮКО) в структуре злокачественных новообразований рак пищевода занимает 4-е место. Чаще всего он встречается у лиц старше 50-60 лет. Но и сегодня отдаленные результаты хирургического лечения рака пищевода особо не удовлетворяют клиницистов. При первичном осмотре в I-II стадии выявляются 20-22% больных, в III стадии 65,5% , в IV стадии 12% больных. Пятилетняя выживаемость составляет 13,5-14%. Вместе с тем, одногодичная летальность при этой патологии находится на одном из первых мест среди онкологических больных [2, 5, 6, 7].
Изучение проблемы лечения больных раком пищевода убедительно показывают сложность лечения злокачественных новообразований пищевода и подтверждают тезис о нерешенности проблемы рака пищевода как таковой. Предметами дискуссий по-прежнему остаются ряд кардинальных вопросов: 1) выбор метода лечения (хирургический, лучевая терапия, комбинированное и/или комплексное лечение) и определение критериев отбора больных на тот или иной вид лечения; 2) выбор адекватного хирургического доступа к пищеводу; 3) объем резекции пищевода, соседних органов, пораженных опухолью, и его лимфатического аппарата; 4) выбор пластического материала для замещения удаленного пищевода; 5) способ формирования и место расположения пищеводного анастомоза; 6) целесообразность и методы паллиативного лечения больных с местнораспространенными и метастатическими формами рака пищевода; 7) тактика лечения локальных рецидивов и прогрессирования опухоли после ее удаления [3, 6, 7, 8].
Исторически хирургия рака пищевода начиналась с наиболее доступного с анатомической точки зрения его участка – шейного отдела. Впервые резекцию пищевода при раке в этом сегменте выполнил Czerny в 1877г. Первой пластической операцией на пищеводе можно считать вмешательство, произведенное I. Mikulicz в 1886г., когда дефект пищеводной стенки был закрыт лоскутом кожи [4, 7].
В настоящее время повсеместно во всех ведущих клиниках мира широко распространена пластика пищевода желудком. Идея заместить резецированную часть пищевода желудком принадлежит Biondie (1895г.). В дальнейшем его экспериментальные исследования продолжили Gosset (1903) и I. Mikulicz (1904). Несмотря на активную работу, решение данной проблемы не получило заметного развития, что было связано с отсутствием эффективных методов борьбы с операционным пневмотораксом и плевро-пульмональным шоком, частыми геморрагическими и инфекционными осложнениями, а также низким уровнем анестезиологии того времени. Впервые антеторакальную пластику пищевода с использованием целого желудка осуществил в 1913г. Е. Fink [20]. Однако первый
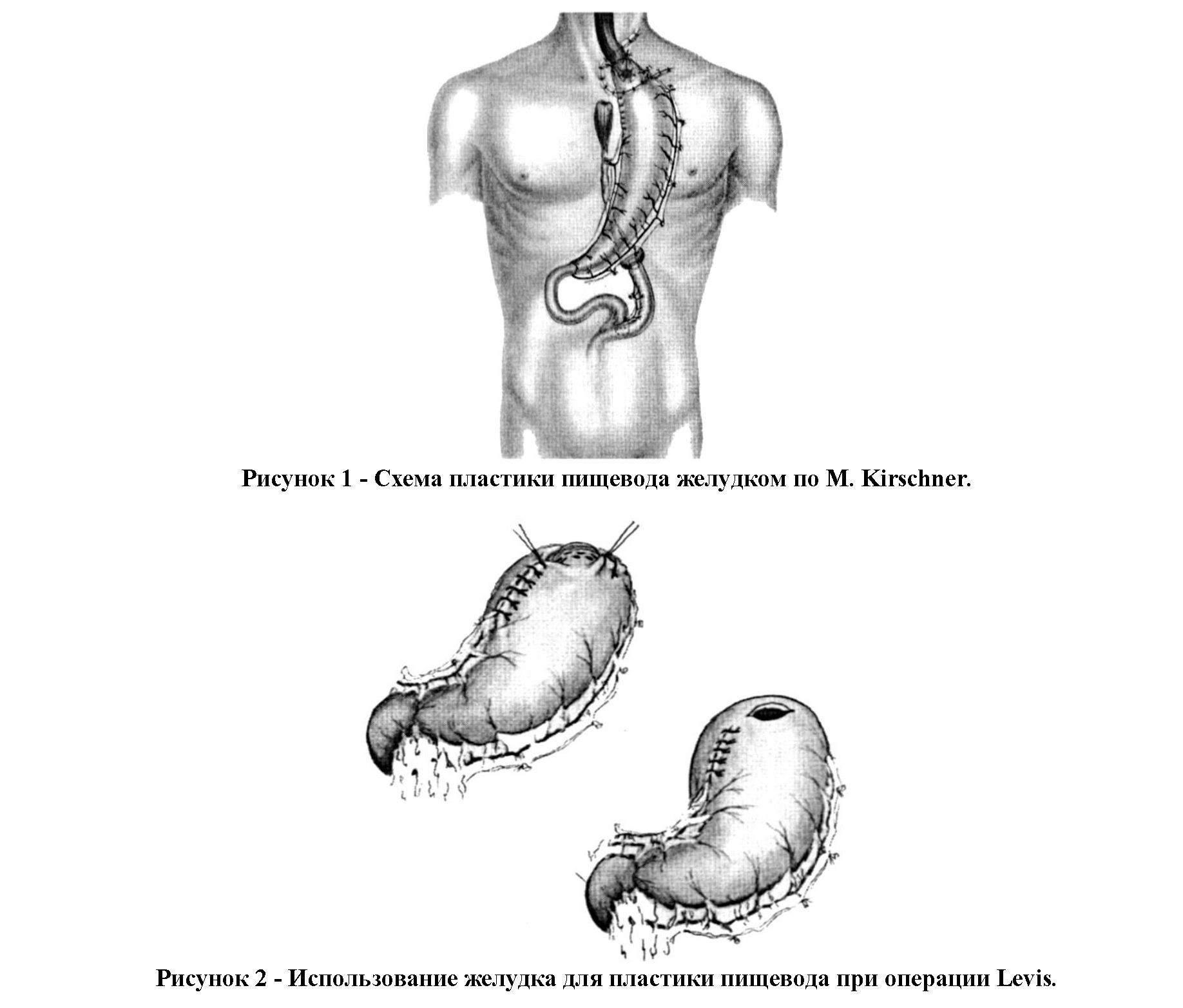
опыт был неуспешным - больной умер на 6-й день после операции. В 1920 г. М. Kirschner [4] разработал оригинальную методику пластики пищевода, которая заключалась в мобилизации всего желудка с сохранением обеих правых желудочных артерий. После пересечения пищевода в абдоминальном его отделе, последний соединялся с тощей кишкой У-образным анастомозом для отведения пищеводного секрета. Отверстие в желудке зашивалось и он проводился антеторакалыю с формированием эзофагогастроанастомоза на шее (рис. 1). По описанной методике автор выполнил 3 операции. У одной больной результат был благоприятным, 2 пациента погибли в ближайшем послеоперационном периоде. В последующие годы пластика пищевода по М. Kirschner получила значительное развитое в работах К. Nakayama [5]. В отличие от автора, японский хирург производил оперативное вмешательство не одномоментно, а в 2 или 3 этапа, уменьшая тем самым ее травматичность и продолжительность. Это позволяло ему успешно завершать вмешательство даже у ослабленных больных и добиться очень хороших результатов: из 200 больных после эзофагопластики по Kirschner-Nakayama умерли лишь 5 (2,5%) пациентов. Несмотря на прекрасные непосредственные результаты операции в руках автора, в Европе данная методика не прижилась.
В 1922 г. W. Kummel сообщил о принципиально новом способе пластики пищевода желудком. Суть его заключается в выделении пищевода на всем протяжении со стороны шеи и брюшной полости. Одновременно производилась мобилизация желудка с сохранением питающих сосудов. Подтягивая пищевод со стороны шеи, последний выводился в рану со сводом желудка. Затем следовала резекция пищевода с формированием эзофагогастроанастомоза.
Стремясь улучшить кровоснабжение желудочного трансплантанта, хирурги шли различными путями. В 1946 г. Levis предложил новый способ резекции грудного отдела пищевода, использовав для ее мобилизации правостороннюю торакотомию. Автор разделил операцию на два этапа. Первым этапом
4после лапаротомии мобилизовался желудок с тщательным сохранением сосудистых аркад вдоль малой и большой кривизны (рис. 2).
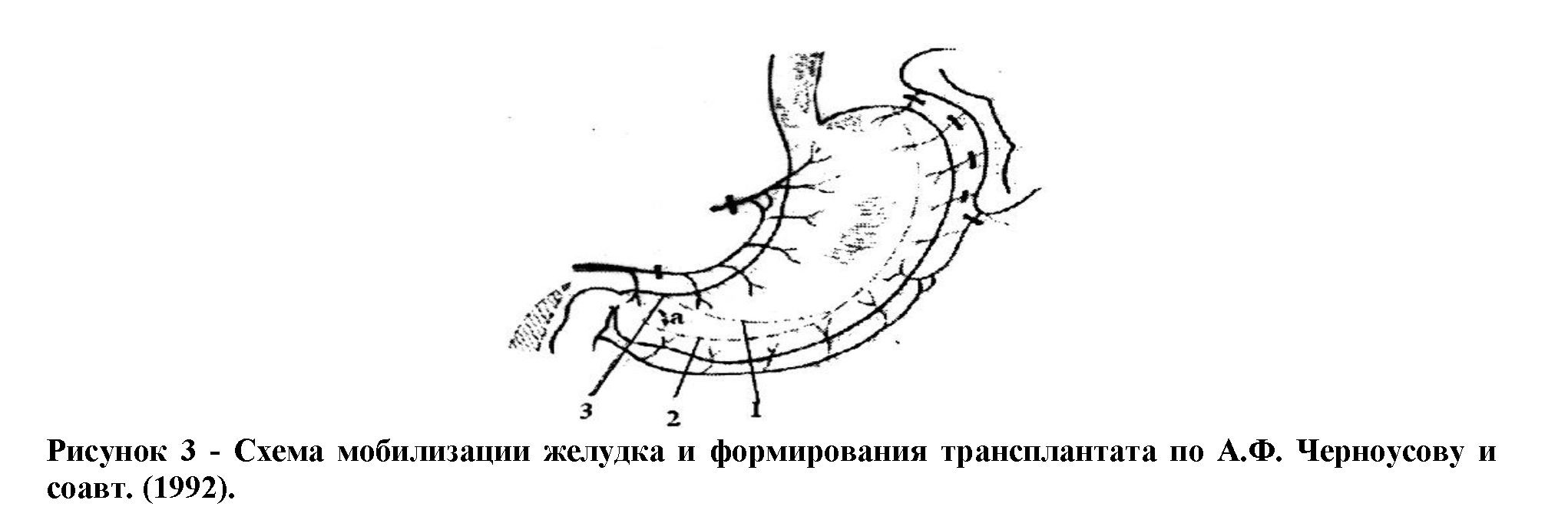
Вслед за этим формировалась гастростома. Спустя 1-2 нед производился второй этап, во время которого после перевязки непарной вены вместе с клетчаткой и лимфатическими узлами заднего средостения выделялся пищевод, расширялось пищеводное отверстие диафрагмы, и через него в плевральную полость выводился ранее мобилизованный желудок. Пищевод с опухолью резецировался и формировался эзофагогастроанастомоз «конец-в-бок». В 1948 г. Mс. Manus обосновал возможность и целесообразность одномоментного выполнения этой операции, что придало данному вмешательству широкое распространение в 50-е годы XX века. Затем эта операция была несколько забыта хирургами ведущих клиник России и Европы в связи с стремлением к выполнению экстирпации пищевода шейно- лапаротомным доступом, широко известная среди хирургов как операция по А.Ф. Черноусову (рис. 3). Однако эта операция оказалась не менее травматичной других, с высокими процентами послеоперационных осложнений (до 75%) в виде несостоятельности и рубцовых стриктур анастомоза, высокой послеоперационной летальностью (25%).
Начиная с конца 80-х и начала 90-х годов 20 столетия в Российском онкологическом научном центре им акад. Н.Н. Блохина в отделении торакоабдоминальной хирургии под руководством академика РАН и РАМН проф. М.И. Давыдова и соавт. начались новые исследования по возрождению, техническому усовершенствованию и применению в клинической практике резекции пищевода со стандартной 2-х зональной лимфодиссекцией через комбинированный лапаротомно-торакотомный доступ с одномоментной пластикой целым желудком, с формированием эзофагогастростомии в куполе правой плевральной полости. Данная операция в настоящее время широко применяется в ведущих клиниках СНГ, Европы, Китая, Японии, стала стандартом хирургического лечения рака грудного отдела пищевода и справедливо носит название – резекция пищевода по Льюису в модификации М.И. Давыдова [3, 6, 7, 8].
В 1960-1970-х годах рак пищевода занимал лидирующее место среди онкологических заболеваний ЮКО, в связи, с чем на базе областного онкологического диспансера (ООД) ЮКО начали внедряться операции по резекции пищевода. Первые операции по поводу рака пищевода в ЮКО были выполнены в 1968-1972г.г. в ООД главным врачом к.м.н., проф. Юнусметовым И.Р. Он же впервые в Казахстане успешно выполнил 1972-1973гг. резекцию грудного отдела пищевода с формированием прямого пищеводно-пищеводного анастомоза при раке грудного отдела пищевода. После операции первый больной прожил без прогрессирования заболевания 5,5 лет. Начиная с 1970г. в ЮКО ООД была впервые применена усовершенствованная методика химиолучевой терапии рака рудного отдела пищевода с химиомодификацией Колхаминовой мазью (патент на изобретение РК № 10756 «Способ лечения рака пищевода», Юнусметов И.Р. с соавт.) После перехода проф. И.Р. Юнусметова на другую работу проблемы хирургии рака пищевода в ЮКО были забыты до 1999-2000гг. [11, 12]
С приходом главным врачом к.м.н. Ж.Ж. Жуматаева и начальника департамента здравоохранения д.м.н., проф. Б.Б. Баймаханова началось второе бурное развитие хирургии рака пищевода в ООД ЮКО. За 2000г. были выполнены более 12 экстирпаций пищевода по А.Ф. Черноусову, более 6 резекций грудного отдела пищевода по Льюису. Начиная с 2001г. резекция пищевода по поводу рака прочно вошла в повседневную практику отделения торакоабдоминальной хирургии ООД ЮКО и в настоязее время стала «рутинной» при хирургическом лечении больных раком пищевода[6, 7, 8].
Ключевые моменты оперативного вмешательства. Согласно данным современных публикаций, большинство практикующих хирургов придерживаются мнения, что с онкологических позиций радикальная операция при РП должна отвечать следующим требованиям:
 5
5
- Быть одномоментной, т.е. включать как радикальный, так и реконструктивный этапы. Сегодня нет таких больных, которые не могут быть по каким-либо причинам оперированы одномоментно. Следовательно, обладая рядом неоспоримых преимуществ, одномоментные вмешательства не имеют принципиальных противопоказаний.
- Удалять пищевод следует целиком при раке верхнегрудного отдела пищевода (тотальная резекция, эзофагэктомия) или выполнять субтотальную резекцию при раке средне- и нижнегрудного отделов. Эта позиция основана на нередком мультицентрическом расположении очагов, преимущественно инфильтративном росте опухоли в краниокаудальном направлении, частом интрамуральном метастазировании. Экстирпация грудного отдела пищевода предполагает формирование внеполост- ного соустья на шее, которое имеет два важных преимущества: а) его несостоятельность более безопасна, чем внутриплеврального; б) оно более доступно хирургической реконструкции. Кроме того, культя собственного пищевода должна быть не более 5-6 см в длину, тогда ее кровоснабжение наилучшее. Кстати, мы предпочитаем накладывать двухрядные инвагинационные пищеводные анастомозы. Однорядные соустья применяем редко из-за высокой частоты их несостоятельности — около 18%.
- При выборе оперативного доступа необходимо учитывать возможность выполнения расширенной ЛАЭ. Многие современные авторы подчеркивают необходимость торакотомии для осуществления адекватной медиастинальной ЛАЭ, независимо от уровня поражения пищевода.
Несмотря на то, что хирургический метод остается ведущим в лечении рака пищевода, в настоящее время все больше клиницистов сходятся о мнении комбинированной и комплексной терапии этой патологии. Применение химиолучевой терапии на различных этапах лечения больных раком пищевода дают более обнадеживающие результаты. Снижается процент ранних локо-региональных рецидивов и метастазов, повышается трех- и пятилетняя выживаемость больных.
Материал и методы. За последние 18 лет (2001-2018 г.г.) в ООД ЮКО на «Д» учет взято 2970 больных раком пищевода, из них I-II стадия процесса была у 668 (22,5%), с III стадией 1965 (66,2%), с IV стадией 337 (11,3%) больных. В основном больные были старше 60 лет, средний возраст составил 62,7 лет. В ООД лечение получили 2212 (74,5%) больных.
В данной статье нами проанализированы результаты только хирургического лечения больных раком пищевода за 17 лет (2002 по 2018г.г.), в хирургическом лечении рака пищевода в 2001-2002г.г. нами применялась экстирпация пищевода из шейно-диафрагмотомного доступа (11 больных), далее с 2003г. по 2015г. применялась только субтотальная резекция пищевода из комбинированного доступа – 1й этап лапаротомия мобилизация желудка, оментэктомия, лимфодиссекция, 2й этап правосторонняя торакотомия мобилизация и резекция пищевода, лимфодиссекция с формированием пищеводножелудочного анастомоза в куполе правого гемиторакса (комбинированный лапаротомно-торакотомный доступ с одномоментной пластикой целым желудком - операция типа Льюиса в сочетании со стандартной 2-х зональной лимфодиссекцией). Вторым этапом больным проводилась лучевая терапия по радикальной программе обычным фракционированием до суммарно-очаговой дозы 40-44 грей. Начиная с 2015г. в связи с изменениями стандартов лечения злокачественных новообразований в РК лучевой этап лечения проводиться в неоадъювантном режиме, то есть до операции больные получают химио-лучевую терапию до суммарно-очаговой дозы 60-70 грей с химиомодификацией цисплатином и фторурацилом.
За 2001-2018г.г. нами прооперировано 342 больных в возрасте от 42 до 75 лет. Мужчин было 253 (74%), женщин 89 (26%). I-II стадией было 39 (11,4%), III стадией 281 (82,2%), IV стадией 22 (6,4%) больных. Гистологический плоскоклеточный рак выявлен у 334 (97,7%), аденокарцинома у 8 (2,3%) больных. Экстирпация пищевода произведена 11 больным (3,2%), операция типа Льюиса 331 больным (96,8%). В послеоперационном периоде осложнения отмечены у 17-х больных (5%), в 12 случаях (3,5%) наблюдалась несостоятельность анастомоза, у 5-х послеоперационный рубцовый стеноз анастомоза (1,5%), который устранен эндоскопическим путем и бужированием. Послеоперационная летальность составила 22 (6,4%) случаев. Основными причинами летальных исходов были несостоятельность
анастомоза и сопутствующие сердечно-сосудистые заболевания.
При динамическом наблюдении одногодичная летальность составила 17,8%, что в основном связано с возникновением локорегиональных метастазов и прогрессирования процесса. При контрольном осмотре 64% больных живут 3 года. Пятилетняя выживаемость составила 18,2%.
Таким образом, в истории Мировой хирургии развитие хирургического лечения рака пищевода на протяжении более чем 120 лет была трагичной и сложной. В настоящее время ведущими клиниками разработаны стандарты лечения больных раком пищевода. Основным методом лечения рака пищевода остается хирургический (операция типа Льюиса в модификации М.И. Давывдова). Однако комбинированное лечение (операция + лучевая терапия) рака пищевода является одним из радикальных методов лечения, которая позволяет снизить частоту местных рецидивов и повышает трех- и пятилетнюю выживаемость больных. В целях повышения эффективности результатов лечения больных раком пищевода нами разрабатываются и внедряются методы неоадъювантной регионарной химиотерапии и мультимодальной терапии.
Литература
- Арапов Д.А. Резекция пищевода по поводу ракового поражения с последующей антеторакальной пластикой // Вести, хир. - 1952. - № 2. - С. 65.
- Арзыкулов Ж.А. Сейтказина Г.Д. Показатели онкологической службы Республики Казахстан за 2006г. (статистические материалы). Алматы. – 2005, - 66с.
- Давыдов М.И., Стилиди И.С. Рак пищевода. – М., - Медицина, 2002, 476с.
- Зубарев П.Н., Бисенков Л.Л., Синенченко Ш. и др. Одномоментные операции в хирургическом лечении рака пищевода и кардии // Вести, хир. - 1992. - № 4. - С. 3-7.
- Кулакеев О.К., Жуматаев Ж.Ж., Арыбжанов Д.Т. и др. Опыт хирургического лечения рака грудного отдела пищевода по данным ООД ЮКО//В сб. научных трудов «Современная медицина и онкология» посвященная 10-летию кафедры онкологии ЮКГМА, - Шымкент, 2004, С.127-128
- Кулакеев О.К., Рысбеков М.М., Юнусметов И.Р., Арыбжанов Д.Т. Современное состояние хирургии рака пищевода // Вестник ЮКГМА, - Шымкент, № 20-21, -2004, -С. 249-257
- Кулакеев О.К., Арыбжанов Д.Т., Юнусметов И.Р. Современные аспекты желудочной пластики в хирургии рака пищевода // В сб. научных трудов «Хирургия XXI века» посв. 70-летию проф. С.В. Лохвицского, - Караганда, -2005, -С.188-192.
- Кулакеев О.К., Жуматаев Ж.Ж., Баймаханов Б.Б., Арыбжанов Д.Т. и др. Хирургическое лечение рака пищевода // Вестник хирургии Казахстана, №3, Алматы, -2005, С. 58
- Мирошников Б.М., Лабазанов М.М., Павелец К.В., Каливо Э.А. Методика формирования желудочного трансплантата для эзофагопластики // Вести, хир. - 1995. - № 2. - С. 24-28.
- Мирошников Б.Л., Лебединский К.М. Хирургия рака пищевода. - СПб.: ИКФ «Фолиант», 2002-304 с. 11. Рысбеков М.М., Юнусметов И.Р., Арыбжанов Д.Т. и др. Прямые пищеводно-пищеводные анастомозы после их резекции // В сб. "Вопросы морфологии и клиники", вып. 5, Алматы 2001, с 453-456.
- Рысбеков М.М., Юнусметов И.Р., Арыбжанов Д.Т. Несостоятельность швов и ее профилактика при резекции пищевода // Хирургия Узбекистана № 63, Материалы международной конференции
"Вахидовские чтения-2002" Бухара, 2002
- Черноусов А.Ф, Богополъский П.М., Курбанов Ф.С. Хирургия пищевода.- М.: Медицина,2000.-350 с.
- Akiyama Е., Tsurumaru M., Udagawa H. et al. Radical lymph node dissection for cancer of the thoracic esophagus // Ann. Surg. - 1994. - Vol. 220, № 3- - P. 364-373
- Matsubara Т., Veda M., Vchida C., Takahashi T. Modified Stomach Roll for safer Reconstruction After Subtotal Esophagectomy //J. Surg. Oncol. - 2000. - Vol. 74, № 12 - P. 1115-1117.