Резюме
В статье представлен анализ результатов исследования морфологического строения стенки пищевода с использованием аутопсийных материалов больных. Морфология стенки пищевода исследована в секционных материалах 56 умерших больных, в том числе: 22 - цирроза печени и 9- умерших больных после эндоскопической склеротерапии. Группу наблюдения составили 25 больных с отсутствием клинико-морфологических признаков цирроза печени и изменений пищевода. Выявлена
эффективность миниинвазивных мероприятий при лечении больных циррозом печени. Исследования позволили также морфопатогенетически обосновать поддержку метода эндоскопической склеротерапии с целью профилактики и лечения геморрагического синдрома при циррозе печени с синдромом портальной гипертензии.
Ключевые слова: цирроз печени, морфологическое строение, аутопсийный материал, эндоскопическая склеротерапия кровотечение, асцит, рецидив
Введение. Наиболее грозным осложнением цирроза печени (ЦП) является возникновение синдрома портальной гипертензии с варикозным расширением вен пищевода и кардии желудка и кровотечением [3]. Варикозно-расширенные вены пищевода выявляют у 25-94,2% больных с ЦП [2,6], летальность уже при первом кровотечении достигает 50-80% [1,4]. Совершенствование эндоскопической техники позволило расширить возможности лечения кровотечений у больных ЦП, применяя эндоскопическую склеротерапию (ЭС) [5]. В литературе имеется неоднозначное отношение к ЭС, что объясняется различными представлениями патогенеза развития варикозных вен пищеводно-желудочного коллектора.
Целью настоящего исследования являлась оценка возможностей миниинвазивных вмешательств на основании изучения и морфопатогенетического обоснования применения ЭС в лечении и профилактике геморрагического синдрома портального генеза, при циррозе печени.
Материал и методы исследования. В основу настоящего исследования положены материалы, полученные при анализе результатов изучения морфологической структуры стенки пищевода на аутопсийном материале больных. Морфологию стенки пищевода мы изучали на 56 секциях умерших больных, из них: 22 – циррозом печени, 9 – умершие больные, ранее подвергнутые ЭС. При этом 25 больных составили контрольную группу, у которых отсутствовали клинико-морфологические признаки цирроза печени и патологии других органов, повлекшие за собой изменения в пищеводе.
Во время аутопсии пищевод выделялся и вырезался в едином блоке с кардиальным отделом желудка и фиксировался в расправленном виде в 10% забуференном растворе формалина, с заполнением просвета органа. После фиксации путем циркулярных и продольных срезов готовили фрагменты для гистологического исследования. Исследованию подвергались различные участки стенки пищевода. После высушивания биоптат заливался парафином с последующим приготовлением кусочков-срезов толщиной до 7-8 мкм и окрашиванием гематоксилин-эозином. Проводили общегистологическое и морфометрическое исследования полученных фрагментов. Материал просматривали и фотографировали в бинокулярном микроскопе фирмы Nikon (Япония).
Результаты и их обсуждение. При исследовании морфологического материала в контрольной группе больных стенка пищевода была представлена следующими слоями: слизистой оболочкой, подслизистой основой, мышечной оболочкой и адвентицией. Слизистая оболочка состоит из эпителия, собственной и мышечной пластинок. Пищевод выстлан многослойным плоским, неороговевающим эпителием. По данным морфометрии средняя толщина составляет 262±46мкм. В слизистой оболочке пищевода постоянно происходят
п оцессы десквамации с обновлением клеток плоского эпителия ( ис 1)
61
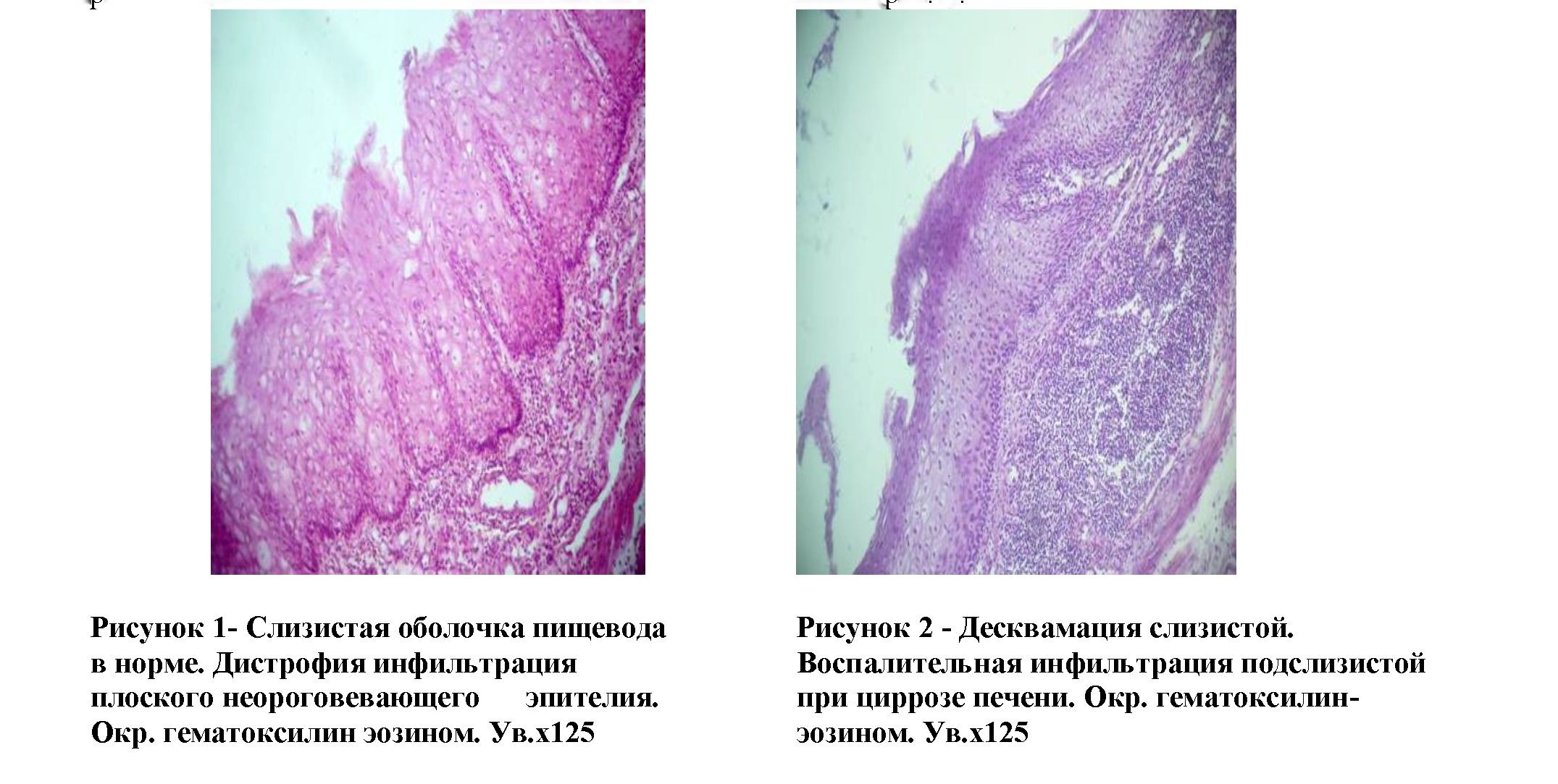
Собственная пластинка представлена тонким слоем рыхлой соединительной ткани. В зоне перехода пищевода в кардиальный отдел желудка имеются множество венозных сосудов мелкого калибра, расположенные под эпителиальным покровом. Мышечная пластинка слизистой оболочки представлена скоплением гладкомышечных клеток, число которых максимально выражено в дистальных отделах пищевода.
Подслизистая основа представлена рыхлой соединительной тканью, где расположены сосуды венозного типа, нервы и собственные железы пищевода. Толщина подслизистой основы колебался от 606 до 488 мкм. Мышечная оболочка состоит из поперечно-полосатой и гладкомышечной мускулатуры. Мышечная оболочка пронизана мелкими перфорантными сосудами, соединяющие подслизистое сплетение с межмышечными и адвентициальными. Адвентиция представлена рыхлой соединительнотканной оболочкой, где выражены эластические и коллагеновые волокна.
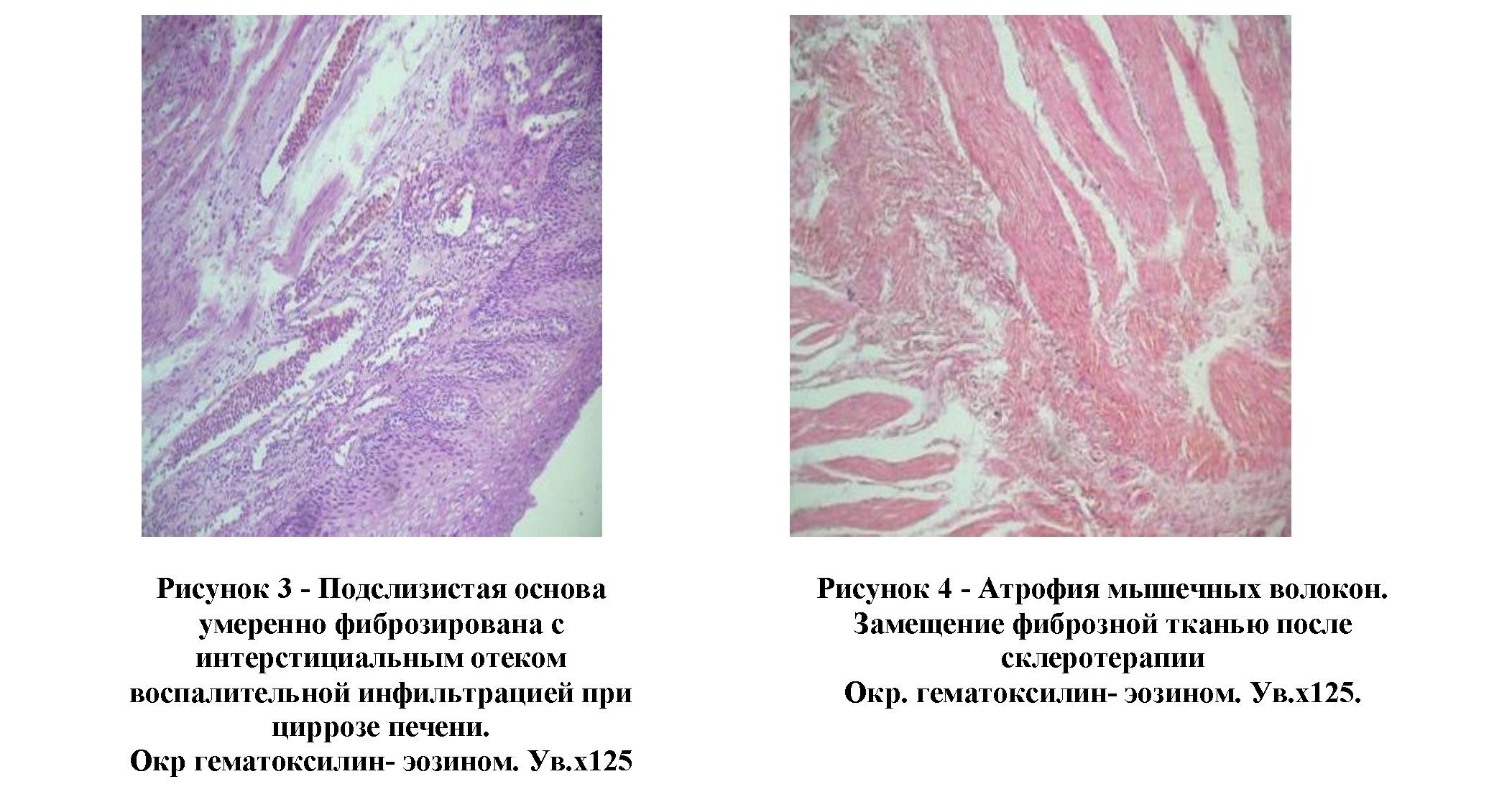
При ЦП исследованы 22 – пищеводов. При этом во всех наблюдениях отмечены уплотнение и истончение стенки пищевода, некоторое его удлинение. Слизистая резко истончена, морщиниста, выражен рельеф подслизистых вен. Также отмечается выраженная десквамация покровного эпителия с образованием трещин, изъязвлений и разрывов, осложненным пищеводным кровотечением (рис.2). Подслизистая основа умеренно фиброзирована, с интерстициальным отеком и воспалительной инфильтрацией (рис.3). Мышечная оболочка – с атрофией мышечных волокон, замещением их фиброз-ной тканью. Отмечается отек и обильная венозная васкуляризация. Сосудистая система мышечной оболочки и адвентиции подвержена склерозированию с уменьшением просвета. В адвентициальной оболочке также выявлены процессы отека и фиброзирования, там же встречаются единичные крупные венозные стволы.
Морфологическая структура пищевода после ЭС при ЦП изучена у 9 больных, умершие в сроки от 10 суток до 2 лет после ЭС. Причинами неблагоприятного исхода явились прогрессирующая печеночная недостаточность, развитие рефрактерного асцита. После ЭС во всех случаях отмечается выраженное уплотнение стенки пищевода с некоторым сглаживанием рельефа слизистой оболочки. После ЭС наступает атрофия или исчезновение гладкомышечных элементов, практически не дифференцируются и замещается фиброзной тканью собственная и мышечная пластинки слизистой оболочки.
Происходит уменьшение количества и диаметра мелких венозных сосудов, местами они находятся в состоянии запустения. При этом толщина эпителиального пласта значительно превышает идентичный показатель при циррозе печени, где ЭС не проводилась. Средняя толщина эпителиального пласта по данным морфометрии варьировал в пределах от 128 до 56 мкм. Выраженные изменения после ЭС отмечены в подслизистой и мышечной оболочках, венозные сосуды которых представлены в виде эластичных тяжей. При этом превалирующим компонентом на фоне нарушения структурной архитектоники является наличие фиброзной ткани. Наблюдается объединение в пучки подслизистых венозных сосудов. При паравазальном способе введения склерозанта отмечается тромбирование просвета сосуда с последующей организацией тромботических масс и фиброзированием. Стенка венозных сосудов с неравномерной толщиной и тенденцией к утолщению. Границы стенки венозного сосуда определяется с трудом, местами отмечается ее полное
62
слияние с окружающей фиброзной тканью. Происходит атрофия, фрагментация пучков гладкомышечных волокон с трансформацией в фиброзную ткань (рис.4). Со стороны мышечной ткани также происходит разрастание элементов соединительной ткани между волокнами, в результате чего отсутствует четкая граница между подслизистой и мышечной оболочками.Наблюдается уменьшение количества коммуникантных вен соединяющие подслизистую основу с адвентициальной оболочкой и нередко зоны фрагментации мышечных пучков с наличием межмышечных инфильтратов. Сравнительная оценка данных морфометрии стенки пищевода при циррозе печени и после миниинвазивных вмешательств представлены в таблице 1.
Таблица 1 - Сравнительная оценка данных морфометрии стенки пищевода при циррозе печени и после миниинвазивных вмешательств (данные в мкм)
|
Оболочки стенки |
Цирроз печени (22) |
После ЭСТ (9) |
Контрольная группа (25) |
|
Эпителиальная |
59±17 |
92±36 |
262±46 |
|
Подслизистая |
971±43 |
678±37 |
547±59 |
|
Мышечная |
1089±112 |
798±56 |
1718±143 |
|
Адвентициальная |
398±53 |
354±48 |
387±69 |
Как видно из таблицы, при ЦП с портальной гипертензией происходит атрофия и истончение слизистой оболочки, с уменьшением ее толщины. При этом дальнейшее усугубление процесса может обусловить возникновение дефектов на слизистой оболочке с появлением эрозий или язв.
Подслизистая оболочка пищевода при ЦП с явлениями интерстициального отека, воспалительной инфильтрации и умеренно замещена фиброзной тканью. Средняя толщина мышечного слоя уменьшена за счет процессов атрофии мышечных волокон и замещения фиброзной тканью. После ЭС склеротические процессы с замещением фиброзной тканью отмечены во всех слоях стенки пищевода с наибольшей выраженностью в подслизистом и мышечном, что отмечено по данным морфометрии в виде снижения толщины указанных слоев.
Выводы. 1. Морфологические особенности стенки пищевода при циррозе печени с портальной гипертензией характеризуются атрофией и истончением слизистой оболочки, выраженной десквамацией эпителия с возникновением эрозивного процесса. Развитие процессов склероза и замещения фиброзной тканью наиболее выражены в подслизистом и мышечном слоях. 2. Возникновение застойных процессов в венозной системе и гипоксия тканей при циррозе печени ведет к снижению регенераторного потенциала слизистой и ухудшению ее репаративной способности. Совокупность вышеупомянутых факторов в значительной мере повышают риск развития геморрагического синдрома. 3. Морфологические изменения после ЭС в отдаленные сроки сводятся стойкому тромбированию варикозных вен пищевода, резкому снижению числа и уменьшению калибра подслизистых и мышечных вен. Степень выраженности этих изменений определяют прогноз развития варикозных вен, частоту и вероятность рецидива геморрагии. Развитие склеротического процесса с замещением фиброзной тканью отмечены во всех слоях с наибольшей выраженностью в подслизистом и мышечном, что подтверждается данными морфометрии в виде снижения параметров составляющих структур стенки пищевода.
Литература
- .Батвинков Н.И. О тактике хирурга при массивном кровотечении из гастроэзофагеальных вен. Хирургия портальной гипертензии (ошибки и опасности). – М.,1984.-С.38-39.
- .Байбеков И.М. и др. Функциональная морфология пищевода, желудка и печени при циррозе, холестазе и лазеротерапии.-Т.,1995.-240 с.
- .Ерамишанцев А.К. Развитие проблемы хирургического лечения кровотечений из варикозно расширенных вен пищевода и желудка. Анналы хирургической гепатологии.- 2007.- Т.12.- №2.-С. 8-15.
- . Назыров Ф.Г., Акилов Х.А., Мансуров А.А. Тактика лечения кровотечения из варикозных вен гастроэзофагеального коллектора у больных с циррозом печени, осложненным портальной гипертензией. Вестник хирургии им. И.И.Грекова. - 2002. - №3. - C. 81-83.
- .Нартайлаков М.А., Мингазов Р.С., Курбангулов И.Р., Зарипов Ш.А., Сатаева Н.М., Латыпова Г.Р., Трофимова Л.В. Комплексный подход к лечению и профилактике пищеводных кровотечений у больных с портальной гипертензией. Анналы хирургической гепатологии.-2005.- Т.10.- №2.-С. 84.
- . Сакс Ф.Ф., Медведев М.А. и др. Функциональная морфология пищевода. М., Медицина, 1987.