Среди разнообразных низкомолекулярных биологически активных веществ, синтезируемых растениями, заметное место занимают иридоиды [1]. Иридоиды рассматриваются в настоящее время как перспективный для поиска новых лекарственных препаратов класс природных соединений [2-4]. Растения рода Phlomis являются перспективными источниками иридоидов [5].
Целью нашей работы является исследование иридоидов растения Phlomis severtzovii (сем. Lamiaceae). Объектом исследования является растение Phlomis severtzovii (сем. Lamiaceae), произрастающее в Средней Азии, в частности в Ташкентской и Ферганской областях.
Для выделения иридоидов, высушенная и измельченная надземная часть растения Phlomis severtzovii экстрагировали метиловым спиртом. Экстракт концентрировали и разбавляли равным объемом воды. Полученный осадок удаляли фильтрацией, а метанол упаривали. Водную часть последовательно экстрагировали сначала хлороформом, затем бутанолом-1. После упаривания растворителей под вакуумом были получены хлороформная и бутанольная фракции. Бутанольную фракцию упаривали на роторном испарителе. Получили остаток в виде густой смолистой массы. Из бутанольной фракции хроматографическим разделением на колонке с силикагелем были выделены несколько фракции, рехроматографированием которых, в системах хлoроформ-метанол 100:1, 50:1, 40:1, 30:1, 20:1, 15:1, 9:1,
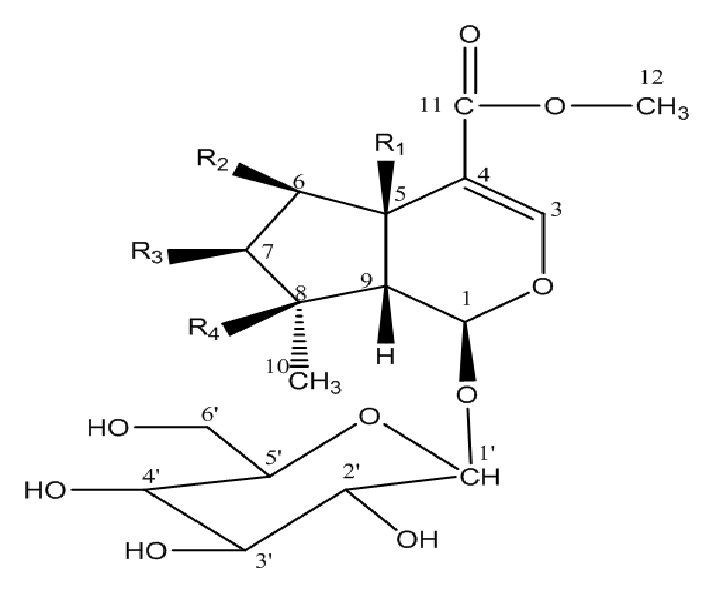 4:1 выделили индивидуальные соединения 6β-гидроксиполамид (1), логанин (2), пулчеллозид (3), метиловый эфир шанцизида (4) и флоригидосид С (5).
4:1 выделили индивидуальные соединения 6β-гидроксиполамид (1), логанин (2), пулчеллозид (3), метиловый эфир шанцизида (4) и флоригидосид С (5).
- R1 = OH, R2 = OH, R3 = H, R4 = OH
- R1 = H, R2 = H, R3 = OH, R4 = H
- R1 = OH, R2 = OH, R3 = OH, R4 = H
- R1 = H, R2 = OH, R3 = H, R4 = OH
- R1 = H, R2 = OH, R3 + R4 = O
Строения всех выделенных соединений идентифицированы на основании анализа УФ-, ИК-, 1Н и 13С ЯМР-спектров.
Изучение биологической активности суммы иридоидов из Phlomis severtzovii. Для исследования иммуномодулирующих свойств суммы иридоидов из Phlomis severtzovii получили этанольный экстракт при комнатной температуре. Экстракт отфильтровали, растворитель отгоняли досуха на роторном испарителе. Сухой экстракт растворили в воде, водную смесь обработали сначала хлороформом, затем бутанолом 5 раз. Растворитель отгоняли в вакууме на роторном испарителе. В остатке получили желтый порошок. Бутанольную вытяжку обрабатывали смесью хлороформ - этанол 6:1 и получили обогащенную сумму иридоидов.
Эксперименты проводили на белых беспородных мышах массой 18-20 г. Для оценки влияния препарата на гуморальный иммунитет использовали реакцию Jerne, Nordin [11].
В результате исследования установлено, что сумма иридоидов полученная из растения Phlomis severtzovii, обладает иммуностимулирующей активностью, при этом не является иммунотоксическим.
Ранее было установлено, что иридоиды полученные из надземной части растения Phlomis severtzovii обладают гепатопротекторными свойствами и благоприятно влияют на функциональное состояние печени [12]. Учитывая этот факт нами исследовано влияние суммы иридоидов и иридоида 6β-гидроксиполамида на острую алкогольную интоксикацию. Результаты проведенных нами исследований показали, что изученные соединения в зависимости от вводимой дозы оказывают антитоксическое действие при острой алкогольной интоксикации.
Таким образом,
- Из растения Phlomis severtzovii нами впервые выделены и идентифицированы иридоиды 6β- гидроксиполамид (1), логанин (2), пулчеллозид (3), метиловый эфир шанцизида (4) и флоригидосид С (5).
- Установлено, что сумма иридоидов из растения Phlomis severtzovii, обладает иммуномодулирующей активностью: стимулирует гуморальный иммунитет, усиливая процесс выработки антител; стимулирует показатели клеточного иммунитета, повышая клеточность центральных и периферических органов иммунитета - тимуса и лимфатических узлов; снижает воспалительную реакцию при развитии реакции гиперчувствительности замедленного типа.
- Установлено, что сумма иридоидов, а также иридоид 6β-гидроксиполамид оказывают антитоксическое действие при острой алкогольной интоксикации.
Список литературы
- Galves M., Martin-Cordero C., Houghton P. J., Jesus Ayoso M. Antioxidant activity of methanol extracts from Plantago Species // Agricultural and food chemistry. 2005.
- Yang L., Jia Z. – J., Su B. – N. Neolignan, phenylpropanoid and iridoid glycosides from Pedicularis verticillata // Phytochemistry .- 1997. – Vol.45, № 6. – P. 1271 – 1273.
- Lucjan Swigtek. Glukozydy iridoidowe w rodzinie Scrophullariaceae// Acta Polon Pharm. 1973. – XXX.- №2.- P.-203-212.
- Поводыш М.Н. Разнообразие иридоидов в семействе Lamiaceae и их биологическая активность // Растительные ресурсы. – Т. 42. – вып.2. – 2006. – С. 131-149.
- Максудов М. С. «Иридоиды растений семейств Scrophulariaceae, Bignoniaceae и Lamiaceae». Дис. к.х.н. – Ташкент. 1996. 127 с.
- Stermitz, Frank R.; Abdel-Kader, Maged S.; Foderaro, Tommaso A.; Pomeroy, Marc Iridoid glycosides from some butterflies and their larval food plants Phytochemistry (1994), 37(4), 997-9.
- Taguchi, Heihachiro; Yokokawa, Yuriko; Endo, Tohru Constituents of Patrinia villosa Yakugaku Zasshi (1973), 93(5), 607-11.
- Milz, Sabine; Rimpler, Horst Pulchelloside I, a new iridoid from Verbena pulchella Sweet Tetrahedron Letters (1978), (10), 8958. CODEN:TELEAY ISSN:0040-4039.
- Yoshio Takeda, Hiroshi Nishimura, Hiroyuki Inouye. Two new iridoid glucosides from Messaenda parviflora and Mussaenda shikokiana. Phytochemistry (1977), 16(9), 1401-1404.
- S. Kobayashi, A. Mima, M. Kihara, Y. Imakura, Chem.Pharm.Bull., 34, 876, (1986)
- Jerne N.K, Nordin A.A. Plague formation in agar by single antibody producing cells // Science. - 1963.-Vol. 140.-P. 405.
- Набиев А.Н., Хушбактова З.А., Захидов У.В., и др. Гепатопротекторные свойства иридоидных гликозидов при остром токсическом поражении печени гелиотрином у мышей. Химико-фарм. Журн.-1999.№8.-С.11.