Резюме
В связи с высоким уровнем инфицирования Helicobacterpylori, был проведен обзор литературы последних лет и докладов рабочего совещания МаастрихтV для популяризации новых исследований в данной области. Это позволит улучшить результаты лечения больных с инфекцией Н. pylori и снизить риск осложнений (в первую очередь, рак желудка).
Ключевые слова: Helicobacterpylori, гастроэзофагеальная рефлюксная болезнь, эрадикационная терапия
Казахстан относится к странам с высоким уровнем инфицирования Н. pylori - от 67,5 до 92%, поэтому решение вопросов профилактики и эрадикации HP-инфекции является для страны актуальной медико-биологической задачей. Для сравнения, в России инфицированность взрослого населения колеблется от 50 до 80%, а в некоторых регионах она приближается к 100%. Китай также относится к странам с высоким уровнем инфицирования Н. pylori - от 87 до 100%, причем в этой стране регистри-руется самая высокая инфицированность цитотоксическими штаммами, создающими высокий риск развития рака желудка.Выявлена обратная связь с социально-экономическим уровнем жизни, чем ниже материальная обеспеченность семьи, тем выше зараженность Н. pylori: низкий уровень - 90%, средний - 79%, хороший - 69%. Для Казахстана, как и для других развивающихся стран, решение проблемы искоренения хеликобактерной инфекции предвидится не скоро и в неменьшей степени зависит от таких же действий соседних государств[1,2].
15–17 сентября 2016 г. в Магдебурге (Германия) состоялось международное рабочее совещание Европейской группы по изучению инфекции H.pyloriимикробиоты для оптимизации схем эрадикацион-ной терапии. Большое внимание было уделено значению борьбы с инфекцией в предупреждении развития рака желудка. В подготовке согласительного документа приняли участие 43 эксперта из 24 стран. Было создано 5 рабочих групп, отвечавших за его определенные разделы: показания к эрадикации и связь H. pyloriс развитием заболеваний (1-й), диагностика инфекции (2-й), лечение (3-й), профилактика и общественное здоровье (4-й), H. pyloriи микробиота желудка (5-й)[3].
В ходе обсуждения состоялся обмен мнениями о возможной защитной роли H. pyloriв возникновении различных заболеваний. В докладе A. Muller (Швейцария) [4] было показано, что в экспери-ментальных исследованиях H. pyloriзащищает мышей от развития у них бронхиальной астмы, вызванной овальбумином, а применение экстракта, содержащего данные бактерии, увеличивает выделение слизи и предохраняет от возникновения воспалительных заболеваний кишечника. В свою очередь, J. Labenz (Германия) [5], первым обративший внимание на повышение частоты гастроэзофа-геальнойрефлюксной болезни (ГЭРБ) после устранения инфекции H. pylori, предположил, что рост заболеваемости ГЭРБ в таких случаях может быть связан с повышением массы тела, поскольку H. pyloriподавляет аппетит за счет снижения постпрандиального уровня грелина.
Согласно положениям 2-го раздела согласительного документа, посвященного диагностике инфекции H. pylori, 13С-уреазный дыхательный тест (13С-УДТ) является сегодня наиболее изученным и в контексте стратегии «testandtreat» его следует рекомендовать к применению в первую очередь; для диагностики может быть использовано также определение моноклонального антигена H. pyloriв кале (УД — умеренный, СР — умеренная)[6].
Если больному проводится эндоскопическое исследование и нет противопоказаний для биопсии, то диагностическим тестом первой линии становится быстрый уреазный тест (БУТ): его положительные результаты служат показанием для проведения эрадикационной терапии. Биоптаты при этом должны браться из антрального отдела и тела желудка. Применение БУТ не желательно для контроля эрадикации [УД - умеренный, СР - умеренная]. Что касается серологических методов, то они могут применяться только после их валидизации; при этом следует избегать быстрых («оффисных») серологических тестов с использованием цельной крови [УД - умеренный, СР- умеренная]. Получение культуры H. pyloric последующим определением чувствительности к антибиотикам рекомендуется при неэффективности проведенной эрадикации [УД - низкий, СР — сильная].
Прием ИПП должен быть прекращен по меньшей мере за 2 недели до тестирования на H. pylori, а антибиотики и препараты висмута отменены как минимум за 4 недели до исследования [УД - умеренный, СР - умеренная].
13С-УДТ - в настоящее время лучший тест для контроля эрадикации. Он должен проводиться не ранее чем через 4 недели после окончания терапии. В качестве альтернативы может рассматриваться определение антигена H. pyloriв кале c применением моноклональных антител (УД - высокий, СР - сильная).
3-й раздел согласительного документа, посвященный мерам по устранению H. pylori, начинается с положения, констатирующего рост резистентности инфекции к антибиотикам в большинстве стран мира [УД — умеренный, СР — сильная]. Далее указывается, что стандартная тройная схема с ИПП и кларитромицином не должна назначаться без определения чувствительности к последнему, если частота устойчивости к препарату в регионе превышает 15% [УД — очень низкий, СР — слабая].
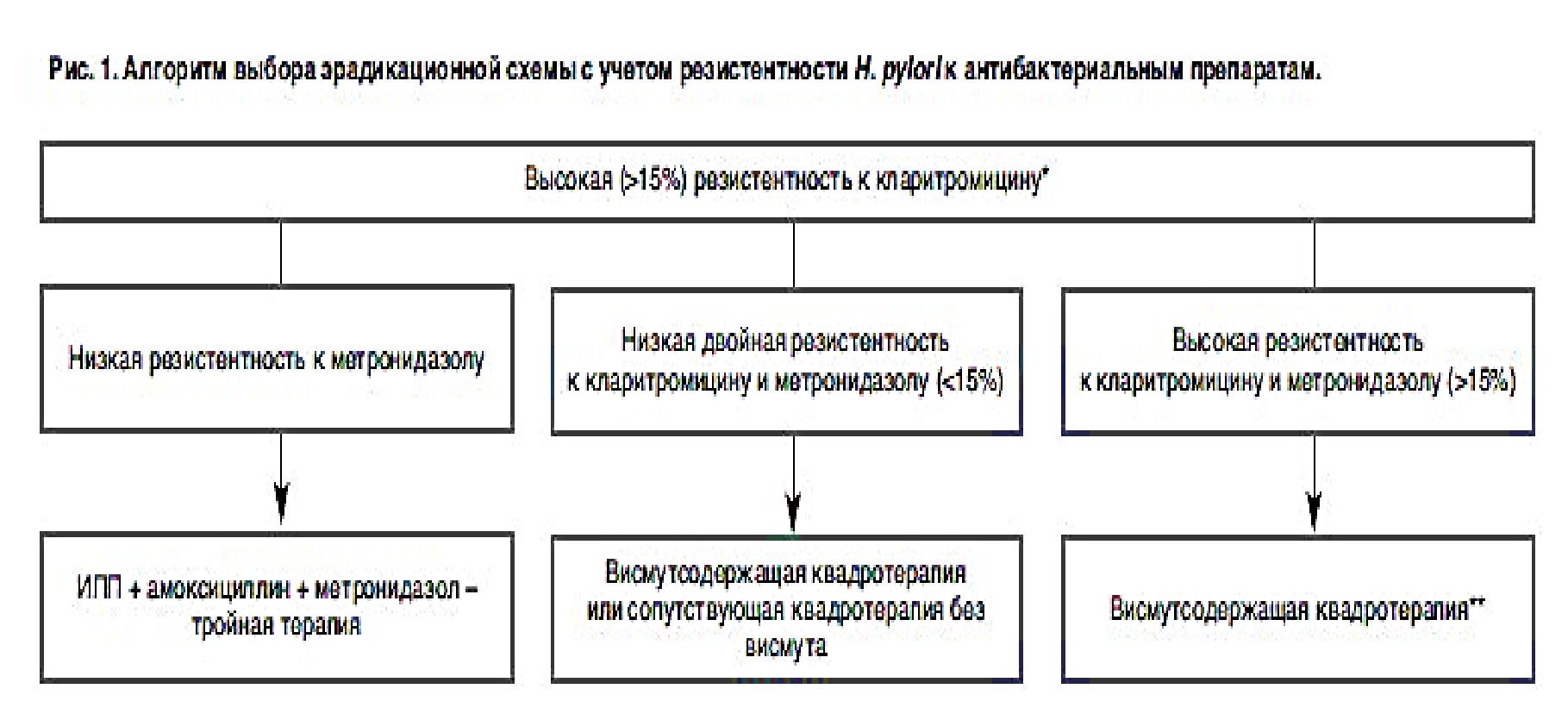
В регионах с низкой (<15%) устойчивостью к кларитромицину в качестве терапии 1-й линии рекомендуется стандартная тройная терапия (ИПП, амоксициллин, кларитромицин); при этом альтернативой может служить назначение квадротерапии с препаратами висмута [УД — высокий, СР — сильная] (рис1).
Резистентность к кларитромицину достигла примерно 30% в Италии и Японии, 40% в Турции, 50% в Китае, хотя в Швеции и на Тайване составляет около 15%.
Существует несколько объяснений снижения эффективности стандартной тройной терапии (ингибитор протонной помпы – ИПП + кларитромицин + амоксициллин или метронидазол): комплаенс, высокаякислотопродукция, высокое бактериальное обсеменение, особенности штаммов, однако самым важным фактором считается рост резистентности H. pylori к кларитромицину. По рекомендациям Европейского медицинского агенства по чувствительности микроорганизмов к антибиотикам различают следующие варианты: обычно чувствительную (0–10% резистентность), непостоянно чувствительную (10–50% резистентность) и обычно резистентную (>50% резистентность).
Председательствовавший на этом симпозиуме P. Malfertheiner (Германия) [7] в своем вступительном слове напомнил, что еще в XIX веке известный немецкий терапевт А. Куссмауль успешно применял субнитрат висмута для лечения заболеваний желудка и высоко оценил эффективность квадротерапии с солями висмута, образно назвав входящие в эту схему препараты «Д'Артаньяном и тремя мушкетерами».F. Megraud (Франция) [8] отметил, что добавление препаратов висмута к тройной терапии повышает частоту эрадикации у больных, резистентных к кларитромицину, с 38 до 84%. F. Bazzoli (Италия) [9] подчеркнул, что назначение квадротерапии с препаратами висмута особенно показано в регионах с высокой резистентностью к метронидазолу.
Наиболее популярным из висмутсодержащих препаратов в настоящее время является висмута трикалиядицитрат (Де-Нол), который образует комплекс с белками стенки бактерий и вызывает их деградацию за счет окислительного стресса, препятствует адгезии H. pyloriкэпителиоцитам, блокирует подвижность бактерий, подавляет активность вырабатываемых ими ферментов, а также обладает цитопротективными свойствами.
4-й раздел согласительного документа «Маастрихт V» посвящен связи H. pyloriи рака желудка. Подтверждено, что наличие этой инфекции является главным этиологическим фактором развития рака желудка [УД — высокий, СР — сильная], причем не только дистального, но и (в случае надежного исключения аденокарцино-мы гастроэзофагеального перехода) проксимального отдела [УД — умеренный, СР — умеренная]. Другие факторы риска (например, курение, избыточное употребление соли) играют по отношению к H. pyloriвторостепенную роль.
Эрадикация инфекции приводит к быстрому уменьшению активности воспаления слизистой оболочки желудка, замедляет прогрессирование гастритических изменений [УД - высокий, СР - умеренная] и вызывает у части больных - при отсутствии кишечной метаплазии - обратное развитие атрофии [УД-высокий, СР-сильная][11]. При этом риск возникновения рака снижается более эффективно, если эрадикация проводится до развития выраженной атрофии и кишечной метаплазии [УД - умеренный, СР- умеренная]. Эрадикационная терапия несет и другие преимущества в виде уменьшения риска возникновения язвенной болезни, рецидивов язвенных кровотечений, а также НПВП-гастропатии.
5-й раздел согласительного документа содержит положения, касающиеся взаимоотношений H. pyloriимикробиоты желудка и кишечника. Указывается, что микробиота желудка включает в себя и другие микроорганизмы помимо H. pylori, в частности представителей фирмикутов, бактероидов и актинобактерий [УД-умеренный, СР-умеренная]. При этом отмечается, что состав желудочной микрофлоры у здорового человека и влияние на него H. pyloriизучены еще недостаточно, хотя полагают, что наличие данного микроорганизма суживает спектр других бактерий в желудке, которые, в свою очередь, также могут играть определенную роль в развитии осложнений гастрита, ассоциирован-ного с инфекцией H. pylori[УД- низкий, СР-слабая][12]. К развитию заболеваний желудка (гастрита, язвенной болезни, рака, MALT-лимфомы) могут быть причастны и другие виды бактерий, входящих в род Helicobacter,-H. heilmannii, H. bizzozeronii, H. felisи др. [УД - умеренный, СР-умеренная].
Выводы
- Тактика выбора режимов эрадикации H. pylori должна определяться региональной (популяционной) резистентностью микроорганизма к кларитромицину, метронидазолу и фторхинолонам. Кроме того, следует учитывать индивидуальный анамнез применения этих антибактериальных препаратов.
- В случае высокой резистентности H. pylori к кларитромицину в популяции использование стандартной тройной терапии не рекомендуется. Порог высокой резистентности микроорганизма к антибиотикам составляет 15%. Начинать эрадикационную терапию в таких случаях следует с висмут содержащей квадротерапии или безвисмутовой квадротерапии без кларитромицина. При неэффективности 1-й линии лечения используют протокол с левофлоксацином.
- Стандартная тройная и висмутсодержащаяквадротерапия должны иметь длительность лечения, равную 14 дням. Рекомендуется увеличить продолжительность последовательной и сопутствующей терапии до 14 дней.
- Почти все новые варианты эрадикационных протоколов предполагают использование двойной дозы ИПП 2 раз в день, чаще применяется эзомепразол 40 мг 2 раза в день.
- Большинство положений Маастрихт V/Флорентийский консенсуса, касающихся эрадикационной терапии, имеют низкий или очень низкий уровень доказательности и слабую степень рекомендаций.
ЛИТЕРАТУРА
- Исаева Г.Ш. Резистентность H. pylori к антибактериальным препаратам и методы ее определения. Клин.микробиология и антимикробная химиотерапия. 2012;
- КорниенкоЕ.А., СуворовА.Н., ТкаченкоЕ.И. идр. Критический рост резистентности Helicobacterpylоri к кларитромицину и педиатрической и взрослой гастроэнтерологической практике. Справочник поликлинического врача 2014;
- Дехнич Н. Н., Костякова Е. А., Пунин А. А. и др. Антибиотикорезистентность H. pylori: результаты микробиологического регионального исследования. Росжурнгастроэнтеролгепатол 2012;
- Miiller A. Debate: H. pylori has protective potential. Pro.EHMSGXXIXth International Workshop. Magdeburg, 2016.- Oralpresentation.
- Labenz J. Debate: H. pylori has protective potential. Pro.EHMSGXXIXth International Workshop. Magdeburg, 2016.- Oralpresentation.
- ПимановС.И., МакаренкоЕ.В. Анализ эффективности протоколов эрадикации инфекций Helicobacterpylori. Рецепт. 2005;
- Megraud F. Overcoming Helicobacter pylori antibiotic resistance in Europe with bismuth.c Satellite Symposium «What's new in Helicobacter pylori eradication. The renaissance of bismuth».EHMSGXXIXth International Workshop.Magdeburg, 2016. — Oral presentation.
- Пиманов С.И., Макаренко Е.В., Овчинников В.В. и др. Эрадикация инфекции Helicobacterpylori при использовании тройной терапии первого выбора. Мед.панорама. 2008; 88 (5): 46–8.
- Bazzoli F. Update on management of Helicobacter pylori infection and the role of bismuth. Satellite Symposium «What's new in Helicobacter pylori eradication.The renaissance of bismuth».EHMSGXXIXth International Workshop.Magdeburg, 2016- Oralpresentation.
- Горгун Ю.В., МараховскийЮ.Х., Пиманов С.И. идр. Диагностика и лечение пациентов с заболеваниями органов пищеварения: клинический протокол. Минск: Профессиональные издания, 2016.
- Янович О.О., Носова Е.С., Титов Л.П., Дорошко М.В. Оценка резистентности Helicobacterpylori к кларитромицину методом ПЦР у больных хеликобактериозом. Здравоохранение. 2011
- Нижевич А. А. Клинико-морфологическая характеристика, генетические маркеры, диагностика и лечение НР-ассоциированных заболеваний, 2013