Резюме
Природные соединения, глицирризиновая кислота (ГК) и её производные широко применяются в медицинской практике из-за универсального спектра биологической активности и малой токсичности. В связи с этим целью данной работы явилось разработка метода количественного определения Глилагина в составе гемостатического геля-Глилагеля. В результате проведенных экспериментов подобрана оптимальная концентрация стандартного вещества глицирризиновой кислоты. При этом оптимальной оказалась концентрация от 0,0030%г/мл до 0,005%г/мл. Разработан УФ спектроскопический метод количественного определения действующего начала состава гемостатического геля- Глилагель.
Ключевые слова: Глицирризиновая кислота, супрамолекулярные комплексы, критическая концентрация мицеллообразования, поверхностно-активные вещества.
Введение. Глицирризиновая кислота (ГК) и её производные широко применяются в медицинской практике из за универсального спектра биоактивности и малой токсичности, а также биосовместимости с живым организмом. Большое значение имеет изучение поведения супрамолекулярных комплексов полученных на основе производных ГК с лекарственными средствами в различных растворителях и средах.
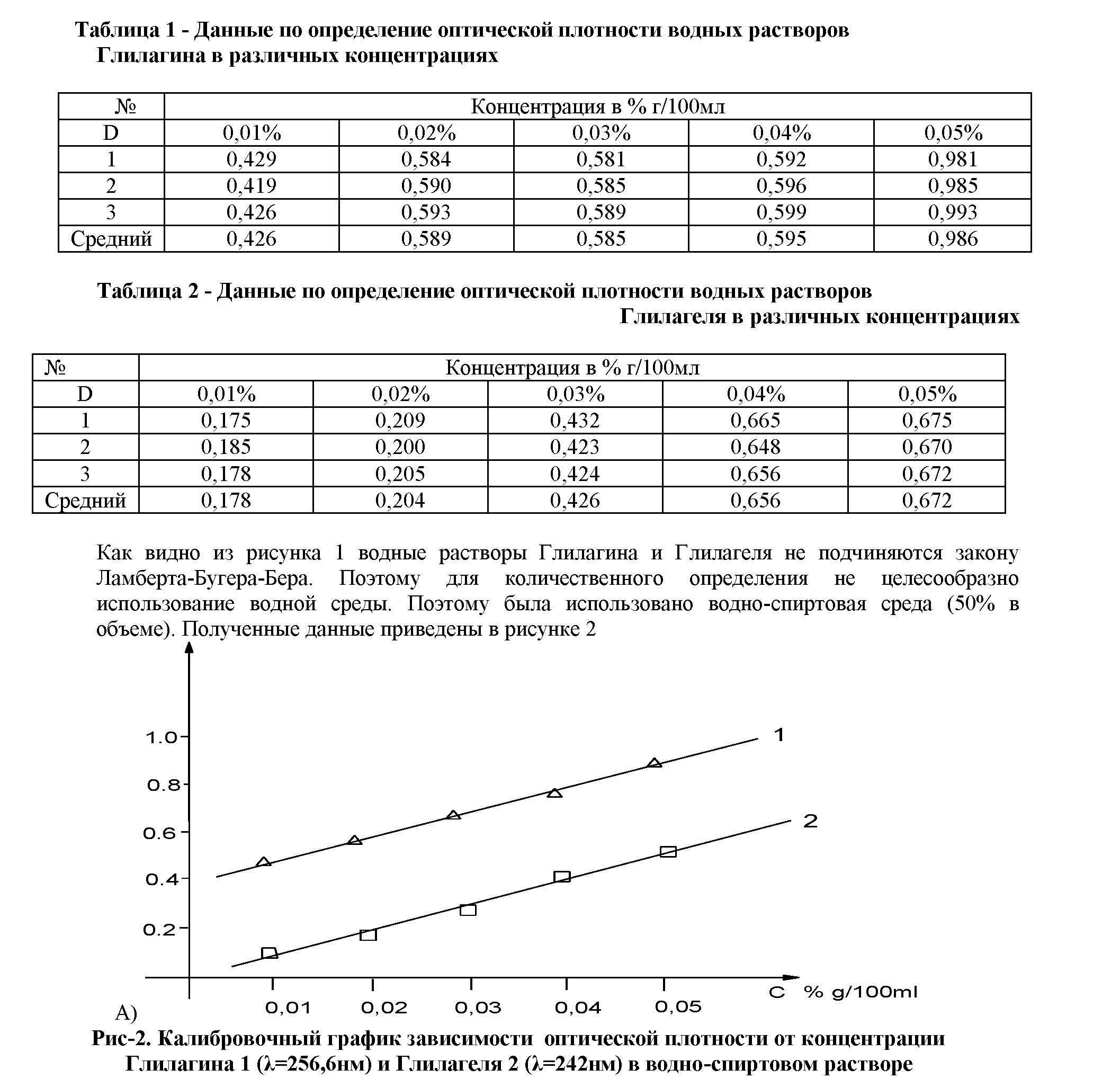
Изучение вязкостных свойств водных растворов ГК показало, что наименьшие значения критической концентрации мицеллообразования (ККМ) показывают моноаммониевая и монокалиевая соль ГК [1]. ККМ характеризует поверхностно-активные (ПАВ) свойства, указывая ту концентрацию ПАВ, при которой в растворе начинается образование мицелл. Возникновение мицелл в растворе является решающим фактором процесса солюбилизации. ККМ определяется измерением объемных или поверхностных свойств растворов, содержащих различные количества ПАВ. В результате исследований было показано, что мицеллообразование возникает в растворе моноаммониевой соли глицирризиновой кислоты (МАСГК) при концентрации МАСГК - 2.12540-3 моль/литр, что составляет 0,2%. [2]. Поэтому водные растворы Глилагина и Глилагеля
отклоняются от законов светопоглощения.
Уникальная способность 18в—Н—ГК и её производных к гелеобразованию связана с особенностями ее строения. Методом 13C-HMP была показана циклическая конформация ГК. Ранее считалось, что в мицеллярном состоянии, стабильность обусловлена за счет внутримолекулярного взаимодействия карбоксильных групп агликона и глюкуроновой кислоты, расположенной в конце углеводного фрагмента [3].
Однако, дальнейшие исследования показали, что ГК и её соли образует мицеллы характерные для ПАВ, где молекулы ГК гидрофобной частью повернуты во внутрь мицеллы [4].
В литературе имеются данные, в которых добавление спиртов к водным растворам ГК её производных приводить увеличению ККМ и тем самым в меньших концентрациях, что соответствует закономерностям Ньютоновских растворов.
В работе [5] были изучены реологические особенности водных и водно-этанольных растворов с содержанием в них ГК от 1» 10-5 до 1х 10—4 моль/л и выше (10 и 20 об. % этанола), при температуре 273 - 333 0K на модифицированном вискозиметре «Rheotest-2,1» с коаксиальными цилиндрами. Как известно [6] в области малых концентраций мицеллы ПАВ обычно симметричны, сохраняют сфероидальную форму и равномерно покрыты с поверхности гидратированными полярными группами. Это означает, что мицеллы вполне стабилизированы. Они не образуют анизометрические цепочки или пространственные сетки, что легко обнаруживается реологическими методами. Вязкость таких систем остается практически постоянной (ньютоновской). Концентрация ГК ниже 3*10-5 моль/л недостаточна для образования устойчивых ассоциатов. При добавлении в раствор этилового спирта (до 10 об. %) число ассоциатов уменьшается и значение ККМ при этом увеличивается до 4-5*10-5 моль/л. При содержании этанола в водном растворе до 20 об. % ККМ достигает 1*10-4 моль/л [7].
Цель исследования. Целью данной работы явилось разработка метода количественного определения Глилагина в составе гемостатического геля-Глилагеля.
Результаты и обсуждение. В результате проведенных экспериментов была подобрана оптимальная концентрация стандартного вещества, при котором точность определения была максимальной. При этом оптимальной оказалась концентрация от 0,0030%г/мл до 0,005% г/мл.
Определение максимума поглощения Z нм моноаммониевой соли ГК, стандартного образца Глилагина, основания геля «Полижель» и Глилагеля изучали при длине волн от 200нм до 400нм в средней ультрафиолетовой зоне, в водно спиртовых растворах показали, соответственно 251 нм, 257,2 нм, 256 нм и 259,2 нм. В полижеле сильное гипсохромное перемещение максимума поглощения на 63 нм, это свидетельствует на то, что полижел сильно взаимодействует с молекулами этанола. Гемостатической гели в водно-спиртовом растворе максимум поглощения наблюдается батахромный сдвиг отличается на 13-15 нм по сравнению - Глилагином.
Определение концентрации веществ в по оптической плотности рассчитывали по следующей формуле:
131
D X 50 x 50
X =
135.4 x 2 x a
где а-навеска в г.
135,4-удельное поглощение
Е-1%
D-оптическая плотность
Расчеты показали, что количественное содержание Глилагина в Глилагеле 83±7% относительно стандартного образца. Полученные данные были статистической обработаны и метрологические характеристики приведены ниже в таблице 5 по ГФ [8] .
Таблица 3 - Метрологическая характеристика количественного определения
Глилагина из состава Глилагеля
|
P |
F |
X |
di |
S2 |
S |
P |
Ax |
е |
S |
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
5 |
4 |
4,14 |
0.15 |
0,0156 |
0,125 |
95% |
0,35 |
8.45 |
2,49 |
Выводы. Таким образом, разработан УФ спектроскопический метод количественного определения действующего начала состава гемостатического геля- Глилагель.
Литература
- Колядина О.А., Муринов Ю.И. Парциальные мольные объемы глицирризиновой кислоты в этаноле и диметилформамиде. - Журн. Физ. Хим. 1997, Т 71, №3, с. 460-463.
- Муравьев И.А., Башура Г.С., Красова Т.Г. Получение некоторых препаратов солодкового корня и изучение их поверхностно-активных свойств. - Фармация. 1974, №4, с. 14-18.
- Азимов М.М. Противовоспалительная активность производных глицирретовой кислоты. Доктр. дисс. Ташкент. 350 с.
- Абдушукурова С.Э., Мухамедиев М.Г., Далимов Д.Н., Мусаев У.Н., Гафуров М.Б. Вязкость водних растворов образцов моноаммониевой соли глицирризиновой кислоты, содержащих различное количество основного вещества // Узб. хим. журнал.-2005.-№2.-С.18-22.
- Давыдова В.А., Балтина Л.А., Рыжова С.А., Толстиков Г.А. Фармакологические свойства новых гликопептидов глицирризиновой кислоты. - Хим. фарм. журн. 1995, №1, с. 41-44.
- Baltina L.A., Tolstikov G.A. chemical modification of glycyrrhizic acid in relation to the biological actives. - Book abstr. Int. Conf. On Natural product and physiologically active substances. Novosibirsk. 1998, 28 p.
- Романенко Т.В., Муринов Ю.И. Некоторые особенности течения разбавленных растворов глицирризиновой кислоты. - Журн. Физ. Хим. 2001, Т 75, №9, с. 1601-1604.
- ГФ XI. выпуск 1 М.Медицина.1987.с208-216.