Необходимостью создания препарата на основе лекарственного растительного сырья для негормональной терапии климактерического синдрома является малое количество на рынке Украины лекарственных препаратов, обладающих широким спектром действия на климактерический синдром. Целью исследований стало изучение влияния фармацевтических факторов на получение водных вытяжек из лекарственного растительного сбора для негормональной терапии климактерического синдрома.
Ключевые слова: лекарственный растительный сбор, технология, климакс.
Дисбаланс гормонов и резкое снижение количества эстрогенов негативно влияют на самочувствие и общее состояние, вызывая массу неприятных ощущений и обострение некоторых хронических заболеваний. Именно по этой причине врачи часто назначают разные препараты при климаксе, чтобы облегчить симптомы и улучшить качество жизни женщины в этот непростой период. Учитывая, что заместительная гормональная терапия продолжает оставаться основным методом лечения вазомоторных и урогенитальных симптомов в пред- и постменопаузе, некоторое количество женщин имеет противопоказания или личные предубеждения к применению гормональных препаратов. Негормональные лекарственные средства при климактерическом синдроме назначаются тогда, когда симптомы его незначительны, а также, когда женщина находится в группе риска и заместительногормональная терапия ей противопоказана [2].
В связи с этим актуальным является поиск альтернативных методов лечения климактерического синдрома, в том числе препаратов растительного происхождения. Препараты, в состав которых входит лекарственное растительное сырьё, имеют широкий спектр фармакологической активности за счёт сочетания в их составе различных групп биологически активных веществ, незначительный риск возникновения аллергических реакций, мягкое действие, небольшой спектр побочных явлений и обладают более низкой токсичностью на органы выделительной системы в сравнении с препаратами микробного, гормонального и химического синтеза. Не случайно в настоящее время лекарственные вещества природного происхождения, особенно растительного, составляют около трети всех препаратов, применяемых в современной медицине [3].
На украинском фармацевтическом рынке биологически активных веществ, применяемых для негормональной терапии климактерического синдрома препаратов украинского производства очень мало, что делает изготовление биологически активных веществ украинского происхождения актуальным и перспективным. К преимуществам отечественного производства лекарственных средств в форме сборов можно отнести: наличие достаточной сырьевой базы, несложного технологического процесса, легко воспроизводимого на фармацевтических предприятиях Украины, пациент имеет возможность получить препарат по приемлемой цене [2,3].
Одним из важных этапов в комплексе исследований при создании новых лекарственных препаратов является обоснование рациональной технологии. Поскольку лекарственное средство в форме сбора является твёрдой лекарственной формой, а его применение в медицинской практике целесообразно в виде настоев и отваров, то обоснование оптимальных условий изготовления, как самого сбора, так и водных извлечений из него должно базироваться на комплексе фармако-технологических исследований.
Процесс получения водной вытяжки из растительного лекарственного сбора ориентирован на максимальный выход биологически активных веществ. Поскольку извлечение БАВ из клеток ЛРС происходит за счет экстракции, целесообразно было изучить влияние различных фармацевтических факторов на выход экстрактивных веществ. Существует зависимость этих показателей от степени дисперсности частиц ЛРС, характеризующих поверхность экстрагирования. Кроме того, установленная степень измельчения частиц растительного сырья необходимо учитывать на стадии смешивания компонентов при приготовлении сбора.
На полноту выхода БАВ при приготовлении водных вытяжек влияют и другие факторы, среди которых важную роль играет режим экстракции. Поэтому при разработке рациональной технологии получения водных вытяжек необходимо обосновать продолжительность настаивания на водяной бане и последующее настаивание при комнатной температуре после снятия с бани. [2]
Цель исследования. Изучение факторов, влияющих на оптимизацию высвобождения БАВ при получении водных вытяжек из лекарственного растительного сбора.
Материалы и методы. С целью изучения влияния различных фармацевтических факторов исследовали три фракции сбора, одинаковых по составу, но разных по степени измельчения частиц компонентов, которые подбирали с помощью просеивания через сита № 1, 2, 3. Лекарственное сырьё измельчали траворезкой. Размер частиц первой фракции составлял 1-2 мм, второй фракции - 2-4 мм, третьей - 4-6 мм [1].
Согласно фармакопейным методикам, в подогретую инфундирку помещали сырье, заливали водой очищенной комнатной температуры в соотношении 1:10 (сбор не содержит ЛРС, требующего другого соотношения с экстрагентом), учитывая коэффициент водопоглощения, настаивали на кипящей водяной бане, оставляли для дальнейшего охлаждения при комнатной температуре. Затем полученный настой процеживали, доводя общий объем водной вытяжки из ЛРС водой очищенной до необходимого объема [1].
Для каждой из указанных фракций сбора изучали по 20 вариантов режима экстракции. Для каждого образца настаивание на водяной бане проводили в течение 2, 8,5, 15, 21,5 и 28 мин (с шагом 6,5 мин). Выбирая временные интервалы, настаивания при комнатной температуре руководствовались общеизвестными правилами охлаждения настоя ЛРС 15, 30, 45 и 60 мин (с шагом 15 мин). Таким образом, для 60 различных вариантов настоев сбора с заданными значениями степени измельчения при определенных режимах настаивания определяли содержание экстрактивных веществ, проводя эксперимент трижды и обрабатывая полученные данные.
В таблице 1 представлены временные режимы приготовления настоев (время настаивания на водяной бане и время охлаждения при комнатной температуре) с указанием степени измельчения лекарственного сбора.
Таблица 1 - Режимы получения выдержек из собрания с разной степенью измельчения
|
№ |
Переменные факторы |
№ |
Переменные факторы |
№ |
Переменные факторы |
|
1 |
2 |
3 |
4 |
5 |
6 |
|
1 |
С(1-2)Н(2)О(15) |
21 |
С(2-4)Н(2)О(15) |
41 |
С(4-6)Н(2)О(15) |
|
2 |
С(1-2)Н(2)О(30) |
22 |
С2-4)Н(2)О(30) |
42 |
С(4-6)Н(2)О(30) |
|
3 |
С(1-2)Н(2)О(45) |
23 |
С(2-4)Н(2)О(45) |
43 |
С(4-6)Н(2)О(45) |
|
4 |
С(1-2)Н(2)О(60) |
24 |
С(2-4)Н(2)О(60) |
44 |
С(4-6)Н(2)О(60) |
|
5 |
С(1-2)Н(8,5)О(15) |
25 |
С(2-4)Н(8,5)О(15) |
45 |
С4-6)Н(8,5)О(15) |
|
6 |
С(1-2)Н(8,5)О(30) |
26 |
С(2-4)Н(8,5)О(30) |
46 |
С(4-6)Н(8,5)О(30) |
|
7 |
С(1-2)Н(8,5)О(45) |
27 |
С(2-4)Н(8,5)О(45) |
47 |
С(4-6)Н(8,5)О(45) |
|
8 |
С(1-2)Н(8,5)О(60) |
28 |
С(2-4)Н(8,5)О(60) |
48 |
С(4-6)Н(8,5)О(60) |
|
9 |
С(1-2)Н(15)О(15) |
29 |
С(2-4)Н(15)О(15) |
49 |
С(4-6)Н(15)О(15) |
|
10 |
С(1-2)Н(15)О(30) |
30 |
С(2-4)Н(15)О(30) |
50 |
С(4-6)Н(15)О(30) |
|
11 |
С(1-2)Н(15)О(45) |
31 |
С(2-4)Н(15)О(45) |
51 |
С(4-6)Н(15)О(45) |
|
12 |
С(1-2)Н(15)О(60) |
32 |
С(2-4)Н(15)О(60) |
52 |
С(4-6)Н(15)О(60) |
|
13 |
С(1-2)Н(21,5)О(15) |
33 |
С(2-4)Н(21,5)О(15) |
53 |
С(4-6)Н(21,5)О(15) |
|
14 |
С(1-2)Н(21,5)О(30) |
34 |
С(2-4)Н(21,5)О(30) |
54 |
С(4-6)Н(21,5)О(30) |
|
15 |
С(1-2)Н(21,5)О(45) |
35 |
С(2-4)Н(21,5)О(45) |
55 |
С(4-6)Н(21,5)О(45) |
|
16 |
С(1-2)Н(21,5)О(60) |
36 |
С(2-4)Н(21,5)О(60) |
56 |
С(4-6)Н(21,5)О(60) |
|
17 |
С(1-2)Н(28)О(15) |
37 |
С(2-4)Н(28)О(15) |
57 |
С(4-6)Н(28)О(15) |
|
18 |
С(1-2)Н(28)О(30) |
38 |
С(2-4)Н(28)О(30) |
58 |
С(4-6)Н(28)О(30) |
|
19 |
С(1-2)Н(28)О(45) |
39 |
С(2-4)Н(28)О(45) |
59 |
С(4-6)Н(28)О(45) |
|
20 |
С(1-2)Н(28)О(60) |
40 |
С(2-4)Н(28)О(60) |
60 |
С(4-6)Н(28)О(60) |
Примечания: С - степень измельчения ЛРС, мм; Н - время настаивания на водяной бане, мин; В - время охлаждения при комнатной температуре, мин.
В ходе эксперимента, было получено 60 настоев, для которых определяли содержание экстрактивных веществ в процентном выражении, руководствуясь фармакопейной методикой:
X = m * 200*100
m1 *100 *W
где: m - масса сухого остатка, в граммах;
m1 - масса навески сырья, в граммах;
W - потеря в массе при высушивании, в процентах.
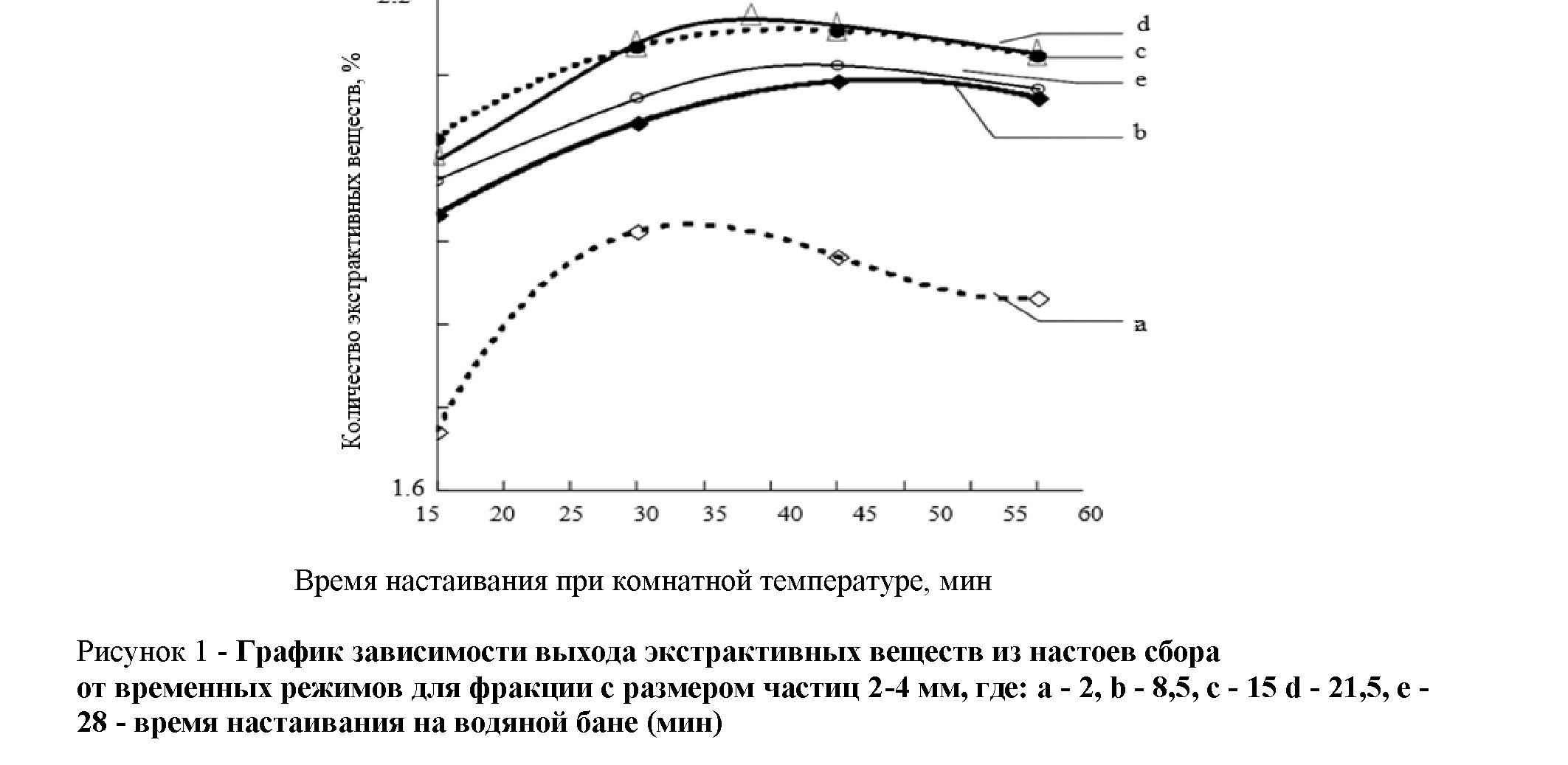
Результаты обсуждения. При заданных значениях степени измельчения и режимах настаивания было рассчитано содержание количества экстрактивных веществ, полученных из водных извлечений растительного сбора, представленных в виде кривых на рисунке. В результате проведённых исследований доказана обратная зависимость выхода экстрактивных веществ из лекарственного растительного сбора для лечения климактерических расстройств от степени дисперсности сырья. При измельчении сырья до размера частиц 2-4 мм наблюдали более высокое высвобождение экстрактивных веществ из-за разрушения клеток ЛРС. При размерах частиц 3-4 и 4-6 мм происходит уменьшение значений сухого остатка. Оптимальным режимом экстракции является настаивание на водяной бане на протяжении 15 минут с последующим охлаждением при комнатной температуре 3035 минут.
Выводы. 1. Изучили влияние различных фармацевтических факторов на выход экстрактивных веществ. 2. Определили зависимость выхода экстрактивных веществ из лекарственного сбора при различной степени дисперсности сырья - при измельчении сырья до размера частиц 2-4 мм наблюдали более высокие показатели высвобождения экстрактивных веществ, чем в образцах с размером частиц 1-2 и 4-6 мм. 3. Оптимальным режимом экстракции выбрано настаивание на водяной бане на протяжении 15 минут с последующим охлаждением при комнатной температуре - 30-35 минут.
Литература
- Державна Фармакопея Украіни: в 3 т. / Державне підприемство «Украінський науковий фармакопейний центр якості лікарських засобів» - 2-е вид. - Харків: Державне підприемство «Украінський науковий фармакопейний центр якості лікарських засобів», 2014. - Т. 3. - 734 с.
- Коноваленко И.С. Изучение технологических свойств сбора для лечения климактерического синдрома / И.С. Коноваленко, Н.П. Половко // Сучасні досягнення фармацевтичноі технологи та біотехнологіі: збірник наукових праць. - X.: Вид -во НФаУ, 2016. - 318-320 с.
- Перспективы использования шалфея лекарственного при негормональной терапии климактерического синдрома/ И.С. Коноваленко, Н.П. Половко // Сучасні теоретичні та практичні аспекти клінічноі медицини :наук.-практ. конф. з міжнар.участю, Одеса, 27-28 квітня 2017 року : тези доп. - Одеса:ОНМедУ, 2017. - 60 с.