АННОТАЦИЯ
Применение Цераксона у больных с транзиторными ишемическими атаками приводит к улучшению состояния пациентов и уменьшению выраженности наиболее часто встречающихся клинических проявлений данной патологии. При комплексном лечении, включающем Цераксон у больных с транзиторной ишемической атакой, происходит снижение показателей СРОЛ и повышение антиоксидантных механизмов в биосредах организма. В комплексное лечение больных транзиторной ишемической атакой включать Цераксон, обладающего антирадикальным, антиоксидантным и нейропротективным действием. Полученные данные демонстрируют перспективу применения Цераксона в качестве нейропротектора при сосудистых заболеваниях головного мозга.
Ключевые слова: транзиторная ишемическая атака, ишемический инсульт, перекисное окисление липидов, свободно-радикальное окисление липидов, антирадикальная активность.
Стратегия лечения ишемического инсульта наряду с реперфузией, направленной на восстановление кровотока в очаге ишемии, включает и осуществление нейропротекции, основной целью которой является поддержание жизнеспособности мозговой ткани для последующего восстановления нарушенных церебральных функций. Теоретической предпосылкой использования различных цитопротекторов служит установленная последовательность патологических событий (так называемый «ишемический каскад»), в результате которой развивается необратимое поражение - инфаркт мозга [11]. С другой стороны, реперфузионные мозговые изменения, т.е. протекающие в условиях восстановленного кровотока, сопряжены с теми же механизмами. Другими словами, даже в случае спонтанного восстановления кровотока, что наблюдается при ТИА, утрата нейронов представляется реальной проблемой. Клиническим подтверждением такой ситуации может служить развитие диффузной неврологической симптоматики у больных с «безынсультным» течением хронического цереброваскулярного заболевания, в анамнезе которых можно обнаружить указания на кратковременные эпизоды нарушений чувствительности, координации, нечеткости речи и т.п. В связи с этим вопросы использования цитопротекторов при ТИА приобретают актуальность, и наиболее перспективными являются средства, способные блокировать как наиболее ранние, так и отсроченные реакции, приводящие к гибели нейронов.
Одним из основных механизмов повреждения клеток служит оксидативный стресс. Ишемия оказывает повреждающее действие на антиоксидантные системы, приводя к образованию активных форм кислорода. Эти процессы инициируют глутаматную эксайтотоксичность, накопление ионов кальция, некроз и апоптоз клеток головного мозга [11, 12]. Оксидативный стресс реализуется как в условиях недостатка, так и избытка
кислорода, и развивается уже в первые часы ишемии, а спонтанная или индуцированная реперфузия вызывает вторую волну церебрального повреждения. Поэтому в существующей клинической практике наиболее востребованными средствами с нейропротективными свойствами остаются антиоксиданты и антигипоксанты. Другое перспективное направление - разработка препаратов, нормализующих функции митохондрий и энергообеспечение клетки. Еще одна возможность нейропротекции связана с предотвращением либо уменьшением токсического действия глутамата, выделяемого в межклеточное пространство.
Основными принципами врачебной тактики при ТИА являются экстренная госпитализация и обследование больного, многокомпонентная консервативная терапия с использованием антитромботических, антигипертензивных, гиполипидемических препаратов и антиоксидантов. При наличии показаний к проведению каротидной эндартерэктомии операция должна выполняться как можно раньше - в пределах первой недели после ТИА. Неотложная тактика позволяет реально уменьшить риск инсульта, предупредить смерть или инвалидность пациента, и этот шанс нужно максимально использовать. Наряду с совершенствованием организационных мероприятий, в последние десятилетия интенсивно разрабатываются методы метаболической коррекции патобиохимических нарушений, обусловленных ишемией и реперфузией, медикаментозной защиты нейронов и восстановления функции пораженной ткани мозга, то есть методы, направленные на предупреждение распространения деструктивных процессов вследствие активации ишемического каскада и провоспалительных реакций. Комплексная фармакологическая нейропротекция путем воздействия на взаимосвязанные патобиохимические и молекулярные механизмы, за счет процессов компенсации, нейрональной пластичности, формирования новых проводников, установления новых синаптических связей, несомненно, должна способствовать более значительному восстановлению структуры и функции поврежденной нервной системы.
В настоящее время появились новые фармакологические препараты, эффекты которых связаны с комплексным нейропротекторным действием на нейроны ишемизированной ткани головного мозга, обладающие свойствами мембранопротекторов и антиоксидантов. К таким средствам относится цитиколин (цитидин-5‘-дифосфохолин; ЦДФ-холин) производства компании «Ferrer International» (Испания), зарегистрированный в Украине в 2006 г. компанией «Nycomed» (Австрия) под названием Цераксон. Цитиколин имеет широкий спектр нейропротекторного действия: уменьшает выброс с аксональных терминалей глутамата, стимулирует обратный внутриклеточный захват нейромедиаторных аминокислот; тормозит процесс разрушения мембран ишемизированных нейронов путем ингибирования активности фосфолипазы А2, восстанавливает их структуру и функцию за счет стимуляции биосинтеза фосфатидилхолина — одного из структурных элементов клеточных мембран; нормализует энергетику митохондрий, восстанавливает функционирование №1+/1<+-АТФазы, сниженный уровень АТФ в ткани головного мозга, энергетические процессы в нейронах; ослабляет свободнорадикальное окисление и ПОЛ, снижает окислительный стресс после ишемии/реперфузии, повышает активность эндогенной антиоксидантной системы защиты клеток за счет стимуляции синтеза глутатиона —неферментного фактора внутриклеточной антиоксидантной защиты — и повышения активности фермента глутатионредуктазы; предотвращает гибель нейронов путем торможения выброса глутамата и подавления экспрессии белков.
Целью нашей работы явилось проведение комплексного клинико-биохимического исследования эффективности Цераксона у больных с транзиторными ишемическими атаками, с детальным анализом взаимосвязи между клинической эффективностью препарата и количественными характеристиками окислительного стресса. Соответственно, в задачи нашего исследования входили:
- оценка динамики основных клинических синдромов у больных с транзиторными ишемическими атаками на фоне лечения Цераксоном.
- оценка влияния терапии Цераксоном на состояние процессов перекисного окисления липидов (ПОЛ) и антиоксидантной защиты, характеризующих степень выраженности окислительного стресса.
- проведение сопоставления между вышеуказанными параметрами окислительного стресса и клиническими характеристиками заболевания (в том числе их динамикой) на фоне терапии Цераксоном.
Клиническая характеристика больных и методы исследования.В исследование были включены 45 пациента (19 мужчин и 26 женщин), средний возраст составил 58 лет, с диагнозом транзиторная ишемическая атака. Основными сосудистыми заболеваниями, обусловившими развитие неврологических расстройств у обследованных больных, были артериальная гипертония и атеросклероз. Эффективность Цераксона исследовалась открытым способом. 25 пациентов получали препарат в суточной дозе 1000 мг в сутки (на 200,0 мл физиологического раствора внутривенно капельно) в течение 10 дней. При необходимости больные получали базовую гипотензивную, антиагрегантную, антикоагулянтную, кардиальную и антидиабетическую терапию. Группу сравнения составили 20 пациентов, сопоставимых по полу, возрасту и характеру заболевания, получавших в течение 10 дней лишь вышеуказанную базовую терапию. На протяжении всего курса лечения пациентам обеих групп не назначались вазоактивные, ноотропные, психотропные препараты.
Для оценки эффективности терапии до начала лечения и после его окончания определяли выраженность основных субъективных проявлений заболевания (слабость рук, ассиметрия лица, чувство онемения конечностей и лица, головной боли, головокружения, шума в голове, нарушение речи, снижения памяти, эмоциональной лабильности), а также показателей неврологического статуса (вестибуло-мозжечковых, двигательных, чувствительных, менингеальных, вегетативных, речевых и бульбарных расстройств) с помощью 5-балльной рейтинговой шкалы со стандартизированными критериями оценки выраженности каждого симптома (0 - симптом отсутствует, 1 - легкие проявления, 2 - умеренные проявления, 3 - значительные проявления, 4 - грубые проявления). Общая эффективность лечения оценивалась исследователем и пациентом по 5-ступенчатой шкале: 0 - ухудшение, 1 -без динамики, 2 - удовлетворительно (небольшое улучшение), 3 - хорошо (заметное улучшение), 4 - отлично (исчезновение симптомов).
Количественную характеристику окислительного стресса в динамике до и после курса лечения осуществляли с помощью изучения содержания диеновых конюъгатов, гидроперекиси липидов и малонового диальдегида в крови.
Одновременно у обследуемых лиц изучено состояние антиоксидантной системы. Для этого определялось содержание естественного антиоксиданта а-токоферола в эритроцитах, а также содержание SH- групп в цельной крови. Из энзимных антиоксидантов изучали активность ключевого фермента- супероксиддисмутазы, глютатион пероксидазы и глютатион-редуктазы. Полученные результаты подвергались статистической обработке на основе пакета программ Statistica 99 (StatSoft, США).
Результаты исследования и их обсуждение. При общей оценке эффекта лечения было выявлено четкое превалирование положительных результатов при использовании Цераксона (95,7%) по сравнению с группой сравнения (65%) (табл. 1).
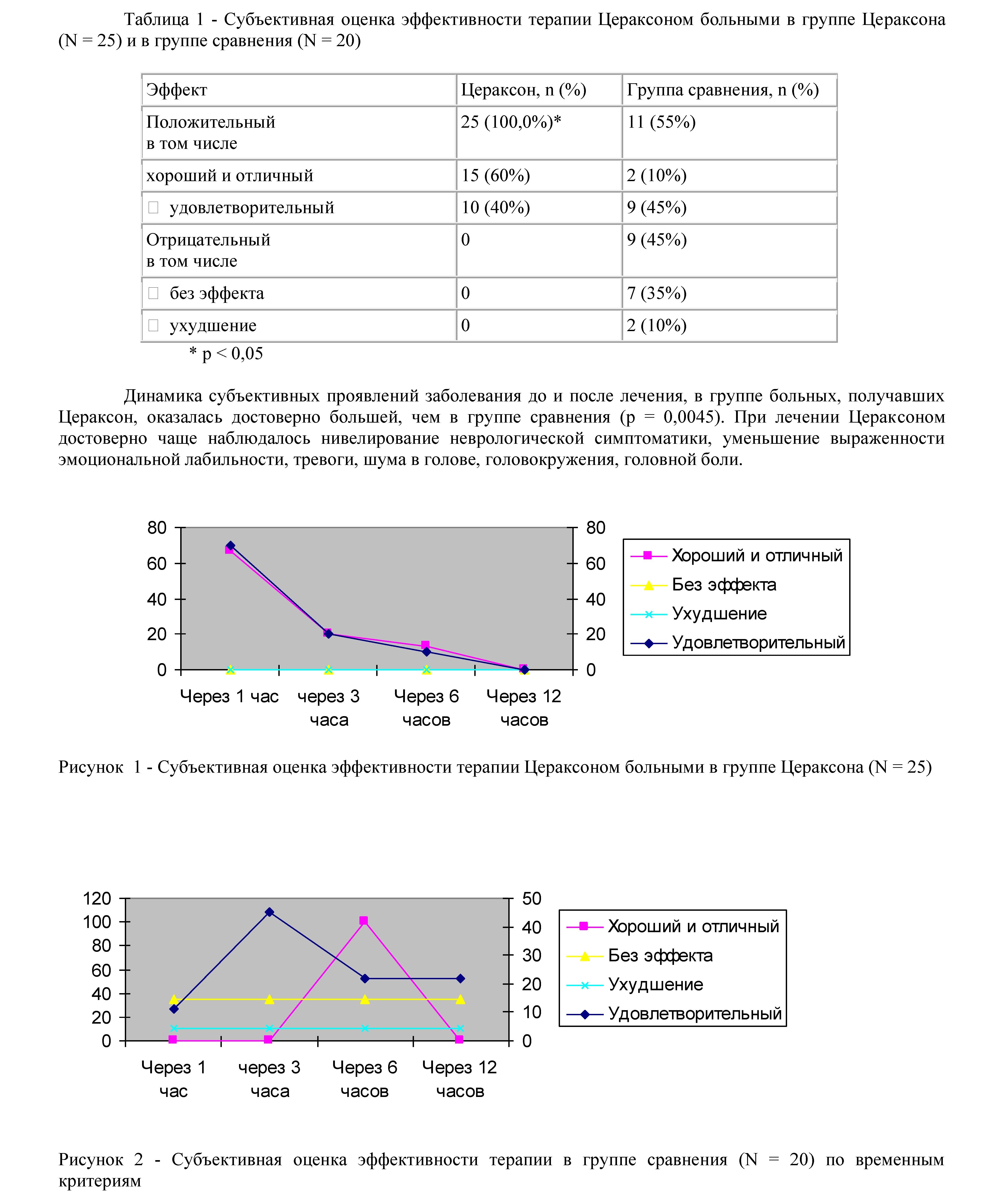
В группе больных принимавших Цераксон положительный эффект наблюдался в первые 3 часа транзиторной ишемической атаки, а в группе сравнения положительный эффект наблюдался только через 6 часов после ТИА, также в группе сравнения наблюдался отрицательный эффект, который проявлялся отсутствием эффекта (35%), и у 2 больных транзиторная ишемическая атака осложнилась ишемическим инсультом рис1,2.
Результаты изучения показателей гиперпероксидации до и после терапии Цераксоном больных транзиторной ишемической атакой показали однонаправленные сдвиги изученных параметров. Под влиянием комплексного лечения включающего Цераксон содержание ДК, ГЛ и МДА в эритроцитах крови снизилась на 30%, 24% и 50% по сравнению с началом лечения, в контрольной группе содоржание ДК, ГЛ и МДА в эритроцитах крови снизилось всего на 17%, 14% и 13% по сравнению с началом лечения (таблица 2).
Таблица 2 - Динамика содержания продуктов ПОЛ в эритроцитах у больных транзиторной ишемической атакой в процессе лечения
|
Показатели Группы |
ДК в эритроцитах ДД232/мг на липид |
ГПЛ в эритроцитах ДД480/мг на липид |
МДА в эритро-цитах нмоль/мг на липид |
|
|
Контрольная группа до лечения |
0,35±0,008 |
2,79±0,02 |
79,3±0,61 |
|
|
Контрольная после лечения |
группа |
0,29±0,01 P>0,05; P1<0,05 |
2,41±0,14 P<0,05; P1<0,05 |
69,3±3,4 P<0,05; P1<0,01 |
|
До лечения Цераксоном |
0,34±0,016 P<0,05 |
2,78±0,13 P<0,01 |
80,6±0,8 P<0,01 |
|
|
После Цераксоном |
лечения |
0,24±0,01 P>0,05; P1<0,01 РФ<О,О5 |
2,1±0,12 P>0,05; P1<0,01 РФ<О,О5 |
39,6±2,4 P>0,05; P1<0,01 РФ<О,О5 |
Для подтверждения наличия антирадикальной и антиоксидантных свойств Цераксона в соответствии с задачами исследования проведено изучение состояния антиоксидантных систем до и после лечения. В результате проведенного лечения, включающего в состав традиционной терапии Цераксон происходят позитивные сдвиги со стороны показателей АОС крови. АРА и АОА плазмы крови после терапии Цераксоном увеличились на 51% и 18% по сравнению с началом лечения (таблица 3).
Таблица 3 - Состояние антиоксидантной системы крови у больных транзиторной ишемической атакой в результате терапии Цераксоном
|
Группы Показатели |
Контрольная группа |
До лечения Цераксоном |
Контр группа после лечения |
После лечения Цераксоном |
|
АРА |
28,5±2,1 P<0,001 |
27,5±2,1 P<0,001 |
33,9±1,3 P<0,01 P1<0,05 |
56,4±2,1 P>0,05 P1<0,01 P2<0,05 |
|
АОА |
25,7±2,1 р<0,001 |
26,7±2,1 р<0,001 |
30±0,9 P<0,05 P1<0,05 |
37,1±1,6 P>0,05 P1<0,01 P2<0,05 |
Таким образом, положительная динамика всех клинических проявлений транзиторной ишемической атаки, параллельно с нормализацией показателей СРОЛ и антиоксидантных механизмов защиты крови, позволяет положительно оценить комплексную терапию, включающую Цераксон, и показывает её несомненное преимущество перед другими лечебными комплексами. На основании полученных данных можно заключить, что Цераксон обладает выраженной антиоксидантной активностью, существенно увеличивает резистентность липопротеиновых структур к окислению, проявляя таким образом у больных с цереброваскулярными заболеваниями свойства мембранопротектора.
Выводы. Применение Цераксона у больных с транзиторными ишемическими атаками приводит к улучшению состояния пациентов и уменьшению выраженности наиболее часто встречающихся клинических проявлений данной патологии. При комплексном лечении, включающем Цераксон у больных с транзиторной ишемической атакой, происходит снижение показателей СРОЛ и повышение антиоксидантных механизмов в биосредах организма. В комплексное лечение больных транзиторной ишемической атакой включать Цераксон, обладающего антирадикальным, антиоксидантным и нейропротективным действием. Полученные данные демонстрируют перспективу применения Цераксона в качестве нейропротектора при сосудистых заболеваниях головного мозга.
СПИСОК ЛИТЕРАТУРЫ
- Віничук С.М., Мохнач В.О., Прокопів М.М. та співавт. Нейропротекторна терапія в гострий період ішемічного інсульту. Міжнар. неврол. журн., №4(20). - 2008. - С. 42-48.
- Пирадов М.А. Интенсивная терапия инсульта: взгляд на проблему. Анналы клин. и эксперим. неврологии, №1(1) - 2007. - С.17-22.
- Фишер М., Шебитц В. Обзор подходов к терапии острого инсульта: прошлое, настоящее и будущее. Журн. неврологии и психиатрии им. С.С. Корсакова. Инсульт (приложение), - №1.- 2001.- С. 21-33.
- Adibhatla R.M., Hatcher J.F. Cytidine 5’-diphosphocholine (CDP-choline) in stroke and other CNS disorders. Neurochem. Res., №30(1). - 2005.-С.15-23.
- Adibhatla R.M., Hatcher J.F., Dempsey R.J. Citicoline: neuroprotective mechanisms in cerebral ischemia. J. Neurochem., 80(1).- 2002.- 12-23.
- Alonso de Lecinana M., Gutierrez M., Roda J.M. et al. Effect of combined therapy with thrombolysis and citicoline in a rat model of embolic stroke. J. Neurol. Sci., 247(2).- 2006.- 121-129,
- Andersen M., Overgaard K., Meden P. et al. Effects of citicoline combined with thrombolytic therapy in a rat embolic stroke model. Stroke, 30(7).- 1999. - 1464-1471.
- Arakawa S., Perera N., Donnan G.A. Neuroprotection in stroke. ACNR, 5(5). - 2005.-10-11.