В статье приведены данные компьютерного прогнозирования спектра биологической активности для природных соединений и их производных с применением компьютерной системы PASS online. Представлены результаты биологических исследований в тест-системах in vivo по выявлению противовоспалительного и анальгетического действия нового индивидуального стероидного соединения акантостерона, которые проведены на основании данных компьютерного прогнозирования.
В настоящее время по данным Chemical Abstract Service известно более 65 млн структур химических соединений, а количество виртуальных структур, т.е. структур, сгенерированных in silico, но еще не синтезированных, превысило 165 млрд [1]. Несмотря на широкое применение методов высокопроизводительного скрининга, экспериментально протестировать действие миллионов соединений для определения их спектров биологической активности не представляется возможным. С этим связана одна из фундаментальных проблем современной химии — исследование соотношений «структура–активность» физиологически активных соединений [2, 3].
Поэтому необходима помощь специальных компьютерных систем в получении оценок по возможным видам биологической активности для различных классов соединений. Реальную возможность комплексного исследования биологической активности веществ могут обеспечить развитие новых технологий компьютерного прогнозирования и их применение для оценки вероятных видов активности химических соединений, с последующим тестированием изучаемых веществ в соответствии с результатами прогноза [4].
Достаточно быстрым и эффективным методом поиска фармакологически активных соединений является использование баз данных, на основе которых возможен предварительный прогноз структурных аналогов с заданной фармакологической активностью. При этом чаще всего для отображения структур молекул прогнозируемых соединений в плоскости 2D используются такие программы, как ISIS/Draw, ChemDraw, ChemScetch и др. Процесс поиска перспективных соединений осуществляется при помощи виртуального скрининга. По такому принципу работает программа компьютерного прогнозирования спектра биологической активности органических соединений PASS (Prediction of Activity Spectra for Substances) [5].
Программа PASS online разработана под руководством В.В.Поройкова, Д.А.Филимонова Институтом биомедицинской химии имени В.Н.Ореховича. Для описания структуры органических соединений в PASS выбрана в качестве основы структурная формула. Программа позволяет осуществить прогноз спектра биологической активности органических соединений на основе их двумерной структурной формулы, представленной в формате mol-файла через интернет, в режиме реального времени [6].
Результат прогноза спектра биологической активности представлен в PASS в виде упорядоченного списка названий соответствующих активностей и вероятностей Pa — «быть активным» и Pi — «быть неактивным» для прогнозируемого соединения. Это позволяет объединять в одной обучающей выборке информацию о биологически активных соединениях, собранную из многочисленных источников. Упорядочение списка выполнено по убыванию разности Pa–Pi, соответственно более вероятные виды активности находятся в начале спрогнозированного спектра [7, 8].
Целью исследования являлось экспериментальное подтверждение результатов PASS-прогнозирования спектра биологической активности для нового стероидного соединения акантостерона (1), выделенного из сырья колючелистника качимовидного (Acantophillum gypsophylloides Rgl.), произрастающего на территории Республики Казахстан.
Материалы и методы
Для прогнозирования спектра биологической активности индивидуальных соединений на основе их структурной формулы использовалась компьютерная система PASS online, разработанная В.В.Поройковым, Д.А.Филимоновым и предсказывающая спектр биологической активности по структурной формуле (http://pharmaexpert.ru/passonline) [9]. Так как в качестве основы для описания структур органических соединений в программе PASS выбрана двумерная структурная формула, был использован профессиональный редактор химической графики — программа ChemDraw Ultra 10.0 от компании-разработчика CambridgeSoft [10].
Благодаря использованию программы PASS online был осуществлен предварительный фармакологический скрининг природных соединений, выделенных из растений, произрастающих на территории Республики Казахстан. Прогнозирование спектра биологической активности было проведено для трёх индивидуальных соединений: новое стероидное соединение акантостерон (1) (3α,14α,22R,25тетрагидрокси-5α(Н)-холест-7-ен-6-он), выделенное из сырья колючелистника качимовидного (Acantophillum gypsophylloides Rgl.); химически модифицированное производное сесквитерпенового лактона арглабина — гидрохлорид диметиламиноарглабина (2), полученного из сырья полыни гладкой (Artemisia glabella Kar. et Kir.); а также сесквитерпеновый лактон — фуроэремофилан-14b-6aолид (3), выделенный из бузульника крупнолистного (Ligularia macrophylla). Структурные формулы соединений представлены на рисунке.
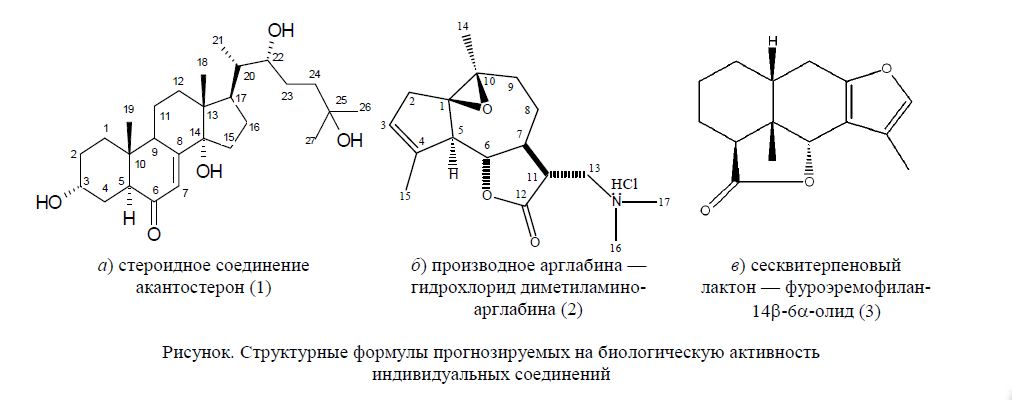
Рисунок. Структурные формулы прогнозируемых на биологическую активность индивидуальных соединений
Противовоспалительное действие нового стероидного соединения акантостерона (1) изучали на модели острой экссудативной реакции (перитонит), которую вызывали внутрибрюшинным введением 1 %-ного раствора уксусной кислоты в объеме 1 мл на 100 г массы тела крыс. Через 3 ч животных забивали, вскрывали брюшную полость, собирали экссудат и оценивали его объем [11]. Исследуемый образец изучали в дозе 50 мг/кг при пероральном введении в виде крахмальной слизи. Препарат сравнения «Диклофенак натрия» изучали в дозе 50 мг/кг. Контрольные животные получали эквиобъемное количество крахмальной слизи. Исследуемое соединение вводили однократно в дозе 50 мг/кг за 1 ч до введения 1 %-ного раствора уксусной кислоты. Статистическая обработка результатов проводилась с использованием пакета программ «Statistica 6.0». Полученные результаты представлены как «среднее значение ± стандартная ошибка среднего значения». Достоверными считались различия при достигнутом уровне значимости p < 0,05.
Анальгетическое действие нового стероидного соединения акантостерона (1) изучали в тесте химического раздражения брюшины (тест «уксусные корчи») на белых беспородных мышах. 0,75 %-ный раствор уксусной кислоты вводили внутрибрюшинно в количестве 0,1 мл на 10 г массы животного. За 30 мин до введения уксусной кислоты внутрижелудочно вводили исследуемый образец в дозе 50 мг/кг. Сразу после введения раздражителя проводили подсчет корчей в течение 30 минут [12]. Анальгетическое действие образца определяли по способности уменьшать количество «корчей», подсчитанных в течение 10, 15, 20 и 30 мин, по сравнению с соответствующими показателями у животных в контрольной группе. Препарат сравнения «Диклофенак натрия» изучали в дозе 50 мг/кг. Контрольные животные получали эквиобъемное количество крахмальной слизи. Статистическая обработка результатов проводилась с использованием пакета программ «Statistica 6.0». Полученные результаты представлены как «среднее значение ± стандартная ошибка среднего значения». Достоверными считались различия при достигнутом уровне значимости p < 0,05.
Результаты и их обсуждение
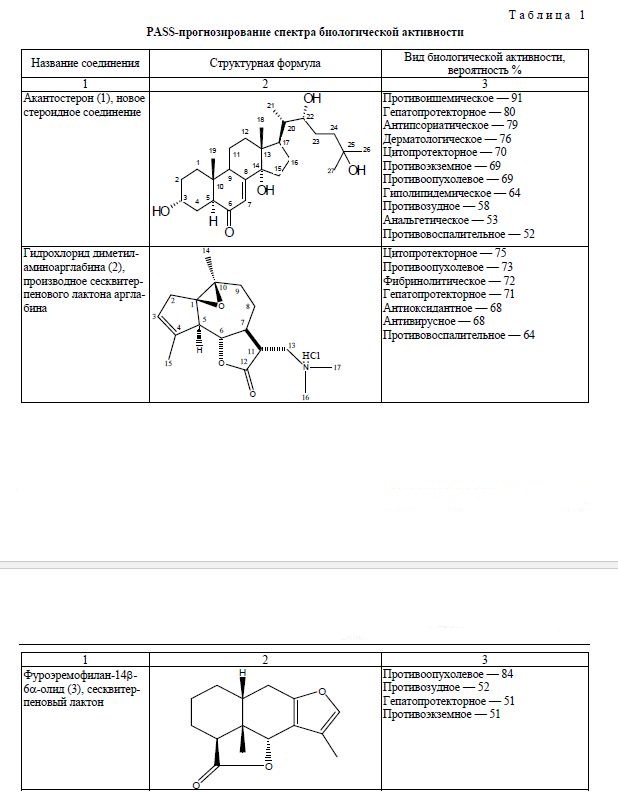
В результате прогнозирования спектра биологической активности в системе PASS online было выявлено, что для нового стероидного соединения акантостерона (1) с высокой вероятностью экспериментального подтверждения прогнозируется наличие гепатопротекторного (80 %), цитопротекторного (70 %), противоопухолевого (69 %), гиполипидемического (64 %) действия. Также для соединения прогнозируется противовоспалительное действие, вероятность экспериментального подтверждения которого составляет 52 %.
Для гидрохлорида диметиламиноарглабина (2) прогнозируется наличие противоопухолевого действия в отношении множественной миеломы (76 %), рака легких (75 %), рака поджелудочной железы (58 %), а также противометастатическое (58 %), противолейкемическое (51 %), аналептическое (50 %) действия.
В то же время для сесквитерпенового лактона — фуроэремофилан-14b-6a-олида (3) система PASS online прогнозирует противоопухолевое (84 %), гепатопротекторное (51 %), противоэкземное (51 %) действия (табл. 1).
PASS-прогнозирование спектра биологической активности
Т а б л и ц а 1
По результатам PASS-прогнозирования было проведено исследование противовоспалительного действия нового стероидного соединения акантостерона (1), выделенного из сырья Acanthophillum gypsophylloides Rgl. В эксперименте использовались беспородные белые крысы средней массой 207– 250 г, полученные из вивария лабораторных животных АО «МНПХ «Фитохимия». Животные находились на обычном рационе питания. Были сформированы 3 группы животных (первая группа — контроль, вторая — вводился препарат сравнения «Диклофенак натрия» в дозе 50 мг/кг, третья — вводилось исследуемое вещество акантостерон (1) в дозе 50 мг/кг). Каждая группа состояла из 6 особей подопытных животных, всего исследовано 18 крыс.
Результаты исследования противовоспалительного действия нового стероидного соединения акантостерона (1) на модели острой экссудативной реакции на белых беспородных крысах представлены в таблице 2.
Т а б л и ц а 2
Противовоспалительное действие нового стероидного соединения акантостерона (1)
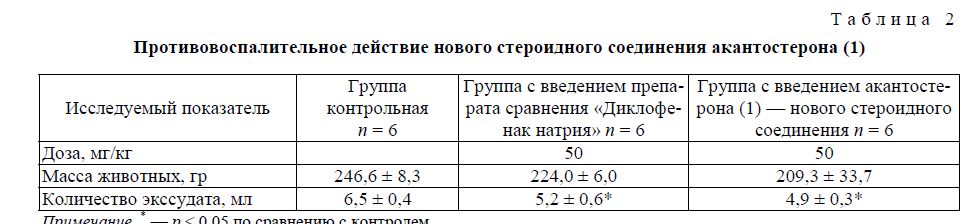
Примечание. * — р < 0,05 по сравнению с контролем.
В ходе изучения противовоспалительного действия отмечено, что под влиянием стероидного соединения акантостерона (1) проявляется выраженное снижение количества экссудата в брюшной полости крыс. При этом противовоспалительное действие исследуемого соединения (1) по своим показателям превосходит препарат сравнения «Диклофенак натрия» в дозе 50 мг/кг на 4,6 %. Данные исследования имеют достоверный характер.
Также изучены анальгетические свойства нового стероидного соединения акантостерона (1) в тесте химического раздражения брюшины (тест «уксусные корчи») на белых беспородных мышах. В эксперименте использовались беспородные белые мыши, полученные из вивария лабораторных животных АО «МНПХ «Фитохимия». Животные находились на обычном рационе питания. Были сформированы 3 группы животных (первая группа — контроль, вторая — с введением препарата сравнения «Диклофенак натрия» в дозе 50 мг/кг, третья — с введением исследуемого вещества акантостерона (1) в дозе 50 мг/кг). Каждая группа состояла из 6 особей подопытных животных, всего исследовано 18 мышей. Результаты исследования приведены в таблице 3.
Т а б л и ц а 3
Анальгетическое действие нового стероидного соединения акантостерона (1)
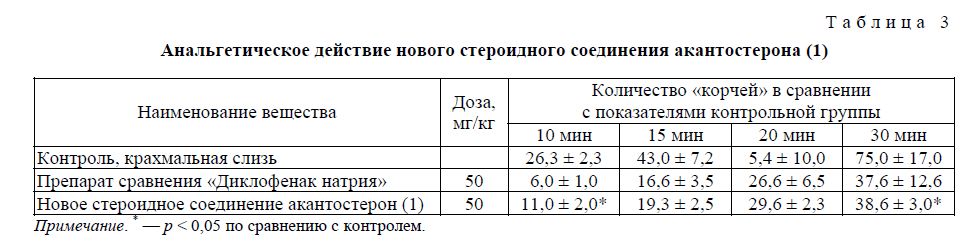
Примечание. * — р < 0,05 по сравнению с контролем.
В результате проведения исследования установлено, что акантостерон (1) обладает достоверным анальгетическим действием, что способствует уменьшению числа специфического ответа (корчи) на химический раздражитель в сравнении с контролем на 48,5 %. При этом исследованный образец (1) незначительно уступает показателям препарата сравнения «Диклофенак натрия» в дозе 50 мг/кг на 1,6 %.
Данные PASS-прогнозирования биологической активности для производного сесквитерпенового лактона арглабина гидрохлорид диметиламинопроизводного (2) были сопоставлены с результатами ранее проведенных исследований. Так, гидрохлорид диметиламиноарглабина (2) проявил высокую противоопухолевую активность в отношении саркомы М-1, карциносаркомы Уокера, саркомы 45, карциносаркомы Герена, альвеолярного слизистого рака печени РС-1 и лимфосаркомы Плисса, лейкоза Р-388 в тестах in vivo на белых беспородных крысах с перевиваемыми опухолями мышей и крыс [13]. Таким образом, проведенный сравнительный анализ данных компьютерного прогнозирования с результатами ранее проведенных биологических исследований для производного арглабина (2) позволяет отметить достоверность и перспективность применения PASS-прогнозирования в предварительной оценке биологической активности.
Заключение
- Новое стероидное соединение акантостерон (1) на модели острой экссудативной реакции (перитонит) тормозит развитие острого экссудативного воспаления на 24,6 % в сравнении с контролем. В свою очередь акантостерон (1) превосходит показатели препарата сравнения, нестероидного противовоспалительного препарата «Диклофенак натрия» в дозе 50 мг/кг на 5,1 %. Таким образом, можно констатировать, что новое стероидное соединение акантостерон (1), выделенный из Acantophillum gypsophylloides Rgl., обладает выраженным противовоспалительным действием.
- Новое стероидное соединение акантостерон (1) обладает достоверным анальгетическим действием в тесте химического раздражения брюшины (тест «уксусные корчи») на белых беспородных мышах, что способствует уменьшению числа специфического ответа (корчи) на химический раздражитель относительно контроля на 48,5 %.
- Данные компьютерного прогнозирования спектра биологической активности для производного сесквитерпенового лактона арглабина гидрохлорид диметиламинопроизводного (2) были подтверждены результатами ранее проведенных исследований на противоопухолевую активность в тестсистемах in vivo на белых беспородных крысах с перевиваемыми опухолями мышей и крыс. Таким образом, отмечены достоверность данных компьютерного прогнозирования спектра биологической активности и перспективность дальнейшего использования компьютерной системы PASS online в целенаправленном поиске природных соединений и их производных с желаемыми видами биологической активности.
- Данные компьютерного прогнозирования спектра биологической активности компьютерной системой PASS online требуют дальнейших экспериментальных исследований и подтверждений, но предоставляют возможность целенаправленно проводить исследования на конкретные виды биологической активности, вероятность экспериментального проявления которых довольно высока. Таким образом, данные прогноза можно учитывать при планировании дальнейших экспериментальных исследований в тест-системах in vitro и in vivo.
Список литературы
- Лагунин А.А. Компьютерная оценка плейотропного действия фармакологических веществ: Дис. … д-ра биол. наук.— М., 2012. — С. 1–2.
- Поройков В.В., Лагунин А.А., Глориозова Т.А. Лекарство, действующее на несколько молекулярных мишеней в организме: исключительная ситуация или будущее фармакотерапии? // Биологические мишени для действия лекарственных препаратов нового поколения. Перспективы интеграции российских ученых в международную кооперацию: Материалы междунар. конф. — Химки, 2006. — С. 20–21.
- Поройков В.В., Лагунин А.А., Коборова О.Н., Захаров А.В., Филимонов Д.А. Роль биои хемоинформатики в создании лекарств, действующих на множественные мишени // Биотехнология: состояние и перспективы развития: Материалы IV Моск. междунар. конгресса. — М., 2007. — 396 с.
- Зефирова О.Н., Палюлин В.А. История QSAR. Ранние исследования количественной связи между структурой и биологической активностью органических соединений. — М.: Изд. МГУ, 2001. — С. 60–73, 74–81.
- Филимонов Д.А., Поройков В.В. Прогноз спектров биологической активности органических соединений // Российский химический журн. — 2006. — № 2(50). — С. 66–75.
- Арчаков А.И., Поройков В.В. Биоинформатика. Новые биомедицинские технологии. Обзор. — М.: РАМН, — 47 с.
- Филимонов Д.А., Поройков В.В., Караичева Е.И. и др. Компьютерное прогнозирование спектра биологической активности химических соединений по их структурной формуле: система PASS // Экспериментальная клиническая фармакология.— 1995. — № 2(58). — С. 56–62.
- Поройков В.В., Филимонов Д.А., Лагунин А.А. и др. Компьютерная оценка спектра биологической активности химических соединений с целью минимизации рисков их применения в медицине // Проблемы оценки риска здоровью населения от воздействия факторов окружающей среды. — М., 2004. — C. 167–169.
- [ЭР]. Режим доступа: http://www.pharmaexpert.ru/passonline.
- Мартынова Н.Б., Филимонов Д.А., Поройков В.В. Компьютерное прогнозирование спектра биологической активности низкомолекулярных пептидов и пептидомиметиков // Биоорганическая химия. — 2000. — № 5(26). — С. 330–339.
- Хабриев Р.У. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ.— 2-е изд. — М.: Медицина, 2005. — 700 с.
- Миронов А.Н. Руководство по проведению доклинических исследований лекарственных средств. — Ч. — М.: Гриф и К, 2012. — 752 с.
- Адекенов С.М. Сесквитерпеновые лактоны растений Казахстана. Строение, свойства и применение: Дис. … д-ра хим. наук. — М.: Ин-т биоорганич. химии РАН, 1992. — С. 377–381.