Статистические данные последних лет свидетельствуют о неуклонном, интенсивном росте заболеваемости и смертности от рака молочной железы в различных странах. Усилия онкологов, направленные на борьбу с раком молочной железы, еще не дают ожидаемого эффекта. Наиболее критическим фактором, определяющим успех лечения рака молочной железы, является степень распространенности опухолевого процесса в период постановки диагноза. Однако не менее чем у 50 % больных раком молочной железы при первом обращении у врачу обнаруживается инвазивный локальный рост опухоли или метастазы в отдаленные органы. В связи с этим актуальную проблему представляет разработка методов раннего выявления злокачественных опухолей молочной железы. Раннее обнаружение метастаз позволит своевременно проводить радикальное лечение и повышать его эффективность. При неопластической трансформации в клетке происходят значительные изменения, позволяющие ей приобрести такие свойства, которые предопределяют ее возможность образовывать злокачественную опухоль. Эти события выражаются в становлении новых антигенных свойств малигнизированных клеток, которые в значительной степени определяются антигенами клеточной поверхности. Антигенные отличия злокачественно трансформированной клетки от нормальной — ключевой вопрос иммунологии опухолей. Исследования в этом направлении позволяют выяснить не только механизмы малигнизации клетки, прогрессии опухоли и ускользания ее от иммунного надзора организма, но и вносят существенный вклад в клиническую онкологию. Многочисленные исследования выявили ряд специфических антигенов на поверхностной мембране и в цитоплазме опухолевых клеток, ассоциированных с раком молочной железы человека — антигены эпителиальных мембран [СА15–3, СА15–5, СА19–9], муциноподобный ассциированный антиген [МСА], тканевой полипептидный антиген [ТПА], гликопротеидный антиген [ЛСА] и т.д. Динамика уровня других онкомаркеров (онкофетальные антигены — РЭА, α-фетопротеин, метаболические маркеры — ферритин, микроглобулин; гормонов — ХГЧ и АКТГ и ферментов — фосфатазы, лактатдегидрогеназы) также позволяет сделать заключение о природе прогрессирования данного онкозаболевания [1–6].
До настоящего времени уже накоплен достаточный фактический материал о поверхностных антигенах, ассоциированных с лейкозами, меланомами и другими опухолями, позволившие усовершенствовать диагностику данных злокачественных заболеваний. Таким образом, наши исследования обусловлены необходимостью поиска специфических антигенов опухолевых клеток рака молочной железы, представляющих диагностический интерес, к которому в дальнейшем необходимо получать моноклональные антитела.
С того момента, как в работе Келера и Мильстейна (1975) [7] было описано получение гибридом способных в фактически неограниченных количествах продуцировать однородные популяции молекул антител (благодаря чему препараты антител смогли получить статус химически чистых реактивов), для иммунодиагностики открылась буквально новая эра. Моноклональные антитела, благодаря таким свойствам, как химическая гомогенность, высокая аффинность и доступность в больших количествах, могут весьма эффективно использоваться для разработки иммунодиагностических тестов. Благодаря развитию гибридомной технологии появилась возможность идентифицировать моноклональные антитела, узнающие уникальные антигенные детерминанты опухолевых клеток [2–8].
Для иммунодиагностики рака молочной железы (РМЖ) известны работы по моноклональным антителам, полученным при иммунизации различным антигенным материалом: постоянные клеточные линии (Soule et.al., 1983), мембраны метастатических клеток (Colher et.al., 1981), мембраны жировых глобул женского молока (Taylor, Papadimitrou, 1981; Ceriani; 1983; Foster et.al., 1983; Hilkers et.al., 1984), очищенные белки (Thor et.al., 1986; Jacobelli et.al., 1986). В последние годы в связи с совершенствованием методики получения моноклональных антител проводится интенсивный поиск онкоантигенов, ассоциированных со структурами поверхностных мембран опухолевых клеток рака молочной железы. Опубликованы сообщения о диагностическом значении карбогидратного антигена СА15–3, ассоциированного с клеточной фракцией карциномы молочной железы; высокомолекулярного гликопротеина МСА, ассоциированного с соединениями с муциноподобной характеристикой; тканевого полипептидного антигена ТПА, полидисперсного соединения, связанного с промежуточными волокнами тканей (S.Kumar et al.1987; L.Repetto et al.1993; E.Seregni et al 1998; и др.) [1,2,5,6,8].
Самым известным препаратом моноклональных антител, результаты применения которого при раке молочной железы стали сенсацией, является герсептин — моноклональное антитело против белковых трансмембранных рецепторов фактора роста Her2. M.Cobleigh et. al., (1998) были представлены результаты лечения 213 больных раком молочной железы, резистентным к стандартной терапии. У всех больных была повышенная экспрессия Her2-neu. В результате лечения герсептином у 44 больных (21 %) были зарегистрированы объективные лечебные эффекты, в том числе у 8 больных (4 %) полный регресс опухоли и у 36 больных (17 %) — частичный, с уменьшением размеров метастазов более 50 %.[1].
Современные тест-системы на опухолевые маркеры производятся ведущими фармацевтическими компаниями мира и составляют солидную отрасль фармацевтической промышленности (Organtec (Германия), DSL (США), Monobind (США), BCM Diagnostics (США), Bender MedSystem (Австрия), CanAg (Швеция), IDL (Швеция)).
В России также проводятся широкомасштабные работы по получению моноклональных антител к маркерным антигенам опухолевых клеток и разработке высокоэффективных и высокочувствительных диагностических тест-систем. С 2001 г. ЗАО «Вектор-Бест» (Россия) приступил к выпуску наборов реагентов для количественного иммуноферментного определения онкомаркеров РЭА, ХГЧ, АФП, СА 125, СА19–3 в сыворотке крови человека — «ИФА-БЕСТ».
Ценность применения этих наборов в медицине достаточно широка. На борьбу с онкологическими заболеваниями поставлены новейшие научные достижения — компьютерная томография, ультразвуковое сканирование, радиоизотопные методы, но они достигают успеха лишь на достаточно далеко зашедших стадиях этого заболевания. Наиболее ранняя информация может быть получена при определении белков-онкомаркеров, концентрация которых начинает изменяться задолго до того, как опухоль обнаруживается другими методами. Кроме того, постоянное определение концентраций раковых маркеров в организме больных (мониторинг) позволяет оценивать эффективность проводимого лечения, а также обнаруживать рецидивы рака.
Моноклональные антитела сегодня — необходимый атрибут лаборатории, производящей современные диагностические тест-системы. Применение моноклональных антител в диагностике онкозаболеваний позволит значительно увеличить специфичность и чувствительность тест-систем. Современные тест-системы на опухолевые маркеры производятся ведущими фармацевтическими компаниями мира и составляют солидную отрасль промышленной биотехнологии. При этом иммунодиагностика онкозаболеваний открыта для поиска новых маркеров и разработки новых методов их определения.
В настоящее время моноклональные антитела к поверхностным дифференцировочным антигенам лимфоцитов (CD) широко используют для определения их фенотипа при иммунодефицитных состояниях, лимфопролиферативных состояниях или иммунологической недостаточности методом проточной цитометрии [9, 10].
В Республике Казахстан аналогичных данному направлению исследований и планируемых прикладных результатов нет. Впервые в Национальном центре биотехнологии РК получены моноклональные антитела к поверхностным антигенам опухолевых клеток рака молочной железы, которые могут быть использованы как высокочувствительные и специфичные реагенты для диагностики онкозаболеваний. Штамм гибридных культивируемых клеток животных Mus Musculus L. «Mab/MCF — 3Д4» депонирован в ДГП «Республиканская коллекция микроорганизмов» РГП «НЦБ » МОН РК как продуцент моноклональных антител к белковому антигену (молекулярная масса 200 кДа) опухолевых клеток аденокарциномы молочной железы MCF-7. и подана заявка на инновационный патент.
Основной целью наших исследований являлась отработка метода применения полученных моноклональных антител (МКА) в непрямом варианте иммуноферментного анализа (ИФА).
Материалы и методы
Для постановки непрямого варианта твердофазного иммуноферментного анализа иммунологические полистироловые планшеты («Nunc» Дания и «Sarstedt» США) иммобилизовывали интактными клетками культивируемых опухолевых клеток линии аденокарциномы молочной железы MCF-7 и карциномы молочной железы ZR-75 в концентрации 20–25 тыс.клеток/мл в питательной среде
DMEM (HiMedia, Индия) при продолжительности инкубации 24 часа в СО2-инкубаторе при температуре 37 0С. Клетки культивировали при температуре 37°С в атмосфере 5 % СО2 на питательной среде ДМЕМ («HiMedia», Индия) с добавлением 50 мкг/мл гентамицина и 10 % фетальной сыворотки крупного рогатого скота. Для снятия монослоя клеток использовали 0,25 %-ный раствор трипсина и 0,02 %-ный раствор версена («HiMedia», Индия). Подсчет клеток и морфологический анализ культур проводили при помощи инвертированного микроскопа. Концентрацию клеток в суспензии, а также число жизнеспособных клеток подсчитывали в камере Горяева с применением 0,4 %-ного раствора трипановой сини.
После инкубации планшеты отмывали три раза ЗФР рН 7,2 с 0,05 % твин-20 и три раза ЗФР без твина и производят фиксацию клеток 70 %-ным спиртом в течение 10 минут. Планшет отмывают четырехкратно ЗФР, содержащим 0,1 % тритона Х-100 (ЗФР-Т), и в каждую лунку вносят по 0,1 см³ 1 %-ного раствора бычьего сывороточного альбумина на ЗФР-Т для блокировки свободных поверхностей твердой фазы при 370С в течение 1 часа. Для определения диагностического титра моноклональных антител в непрямом ИФА проводили исследование образцов позитивных (специфических МКА) и отрицательных (контрольных — неспецифических МКА) антител в разведениях от 1:100 до 1:12800. В качестве специфических продуцентов моноклональных антител к поверхностным антигенам опухолевых клеток использовали штаммы гибридных культивируемых клеток 3D4 и 2A8. В качестве неспецифических антител использовали моноклональные антитела, специфичные к полисахаридным антигенам бруцелл, и микобактерии, продуцируемые штаммами гибридом 7F10 и 4G8. После инкубирования при 370С в течение 1,5 часа планшет в лунки планшета вносили кроличьи антитела к иммуноглобулинам мыши, меченные пероксидазой хрена (антивидовой конъюгатSigma, Германия) в объеме 0,1 мл и инкубировали в течение 1 часа. Для проявления реакции в лунки вносили по 0,1 мл раствора субстрата фермента, который готовили путем растворения 0,01 г ортофенилендиамина (Sigma, США) в 10 мл 1 %-ного раствора лимонной кислоты с рН 4,5 и добавления 0,005 мл 30 %-ной перекиси водорода. Реакцию останавливали добавлением в лунки планшет раствора 2М серной кислоты. Результаты ИФА учитывали с помощью спектрофотометра с вертикальным потоком света при длине волны 492 нм.
Результаты исследований
Первичным процессом в любом иммунохимическом анализе является стадия «узнавания» анализируемого соединения специфическим к нему антителом. Процесс образования иммунохимического комплекса «антиген – антитело» происходит в строго количественном соотношении, обусловленном аффиностью, концентрациями компонентов и условиями реакции. В этой связи нами изучалось влияние временного фактора и температурного режима на прочность образования иммунного комплекса «антиген – антитело» (рис.1).
Изучение кинетики образования иммунного комплекса «антиген – антитело» при температуре +4 °С показало, что полное насыщение твердой фазы иммунным комплексом происходит через 14–18 часов. При этом значения оптической плотности достигали 1,042–1,062 о.е. Оценку кинетики соединения моноклинальных антител с адсорбированным на поверхности твердой фазы специфическим антигеном также проводили при температуре +37 0С в течение 30 минут, 1, 2, 3 и 4 часов. Согласно полученным результатам равновесие в реакции антиген – антитело наступает через 2 часа инкубирования, со значением оптической плотности 0,980–1,044 о.е. Увеличение экстинции ведет к повышению «фонового» показателя на 20–40 % из-за неспецифического связывания белка с поверхностью твердой фазы. Дальнейшая экспозиция не приводила к увеличению концентрации иммунного комплекса, поскольку показатель оптической плотности реакционной жидкости оставался на одном уровне.
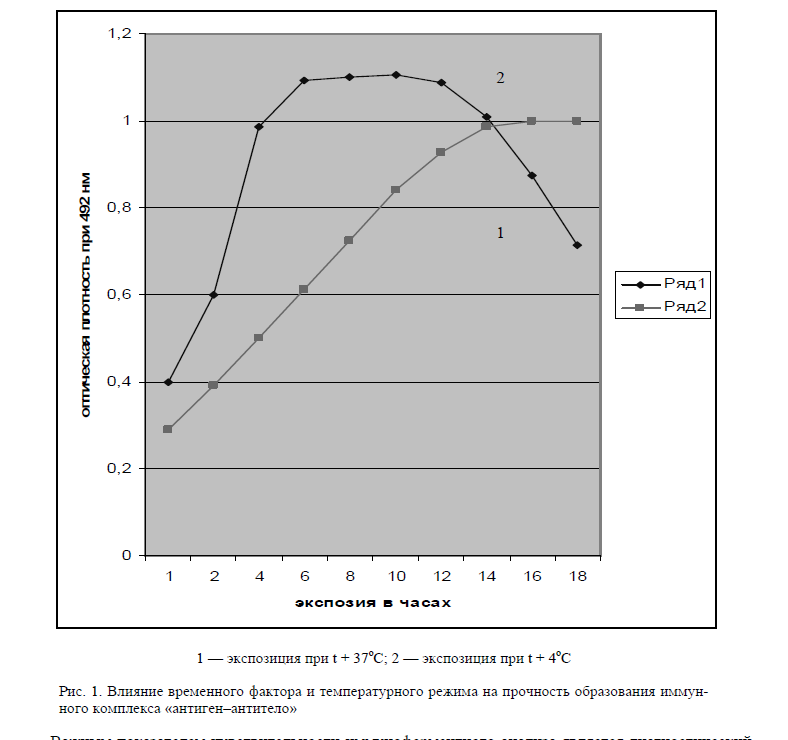
Рис. 1. Влияние временного фактора и температурного режима на прочность образования иммунного комплекса «антиген–антитело»
Важным показателем чувствительности иммуноферментного анализа является диагностический титр моноклональных антител по отношению к используемому антигену. Для определения диагностического титра моноклональных антител в непрямом ИФА провели исследование образцов позитивных (специфических МКА) и отрицательных (контрольной — неспецифических МКА) антител в разведении от 1:100 до 1:12800.
Согласно полученным результатам в качестве диагностического титра моноклональных антител в непрямом ИФА можно принять разведение 1:200 и выше. Начиная с этого разведения наблюдается неизменность максимальной разности в 2 и более раза между экстинциями (ОП + 492) позитивного и негативного контролей. Титры специфических МКА в непрямом ИФА обнаруживались до разведения 1 : 51200.
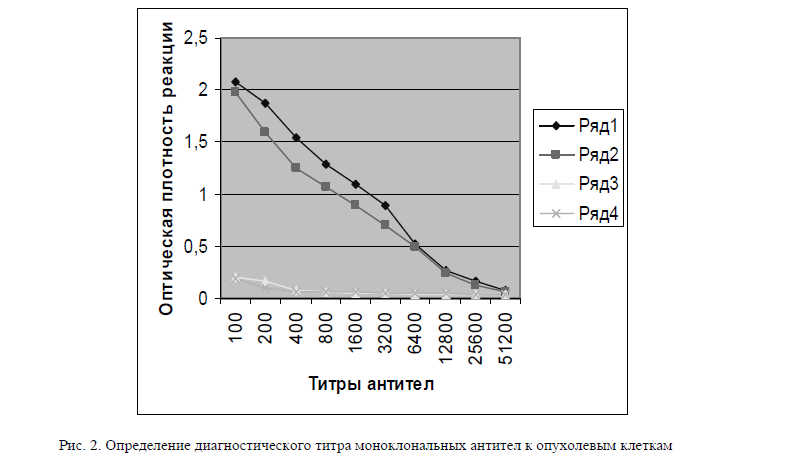
Рис. 2. Определение диагностического титра моноклональных антител к опухолевым клеткам
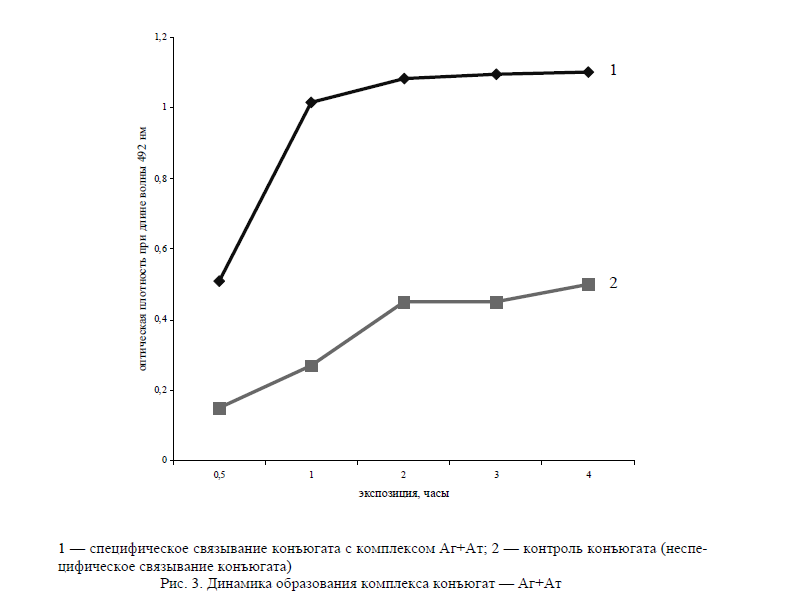
Рис. 3. Динамика образования комплекса конъюгат — Аг+Ат
На следующем этапе исследований предсматривалось оценка кинетики соединения иммунопероксидазного конъюгата с комплексом «антиген–антитело».
Установление константы равновесия между иммунным комплексом «антиген-антитело» и антивидовым иммунопероксидазным конъюгатом осуществляли стандартизацией рабочего разведения конъюгата исходя из условий минимальной фоновой реакции и наибольшей оптической плотности. При инкубации иммунопероксидазного конъюгата в пяти различных разведениях (1:1000, 1:2500, 1:5000, 1:10000, 1:20000) оптимальное изменение субстрата наблюдалось лишь для одного разведения — 1:5000 (чувствительность — 1 нг). Повышение концентрации конъюгата приводило к увеличению степени его связывания и соответственно к росту наблюдаемой ферментативной активности. При слишком низкой концентрации конъюгата в результате низкой скорости превращения субстрата заметно снижалась чувствительность анализа (до 500 нг).
На следующем этапе нами изучалось влияние продолжительности и режима инкубирования антивидового конъюгата на кинетику связывания с комплексом «антиген–антитело» (рис. 3.).
Согласно полученным результатам наиболее оптимальными параметрами длительности и режима инкубации для иммунопероксидазного конъюгата являются 1 час при 37 °С. Величина оптической плотности при этом составила 1,015 о.е. Инкубирование более 1 часа сопровождалось незначительным увеличением величин оптической плотности. Уменьшение времени инкубации в обоих случаях сопровождалось практически ослаблением окраски в ходе ферментативной реакции превращения субстрата. Увеличение экспозиции, наоборот, сопровождалось повышением «фонового» показателя на 40–60 % из-за наличия примеси свободного фермента пероксидазы.
Таким образом, нами изучены условия постановки непрямого варианта ИФА на основе полученных МКА, который включает определение оптимальной концентрации антигена для сенсибилизации твердой фазы, установление константы равновесия иммунного комплекса «антиген–антитело» и оценку кинетики соединения с коммерческим конъюгатом.
Список литературы
- Канцерогенез / Под ред. Д.Г.Заридзе. — М.: Медицина, 2004. — 576 с.
- Абелев Г.И. Принципы иммунодиагностики опухолей // Иммунология. — 1982. — № 4. — С. 5–12.
- Таранов А.Г. Лабораторная диагностика опухолевых заболеваний (радиоиммунный и иммуноферментный методы анализа) // Новосибирск: Наука, 1995. — 123 с.
- Зорин Н.А. Новые подходы к диагностике онкозаболеваний // Новости «Вектор-Бест». — 1997. — № 2. — С. 45–56.
- Lioyd O. Human tumor antigens: Detection and characterization with monoclonal antibodies. In: Basis and clinical Tumor immunology. R.B.Herberman{ed}. — Boston. — 1983. — Р. 159–214.
- Neville M., Gusterson B.A. Monoclonal antibodies and human tumors. Eur.J.Cancer Clin.Oncol. — 1985. — V. 21. — Р. 355–369.
- Kohler , Milstein C. Continuous cultures of fused cells secreting antibody of predefined specificity. Nature. — 1975. — V. 275. — Р. 485–497.
- Klug L., Bast R.C., Niloff Y.M. Monoclonal antibody immunonassay for an antigenic determinant. Cancer Rec. — 1984. — V. 44. — Р. 1048–1053.
- Петров Р.В. Иммунология / Под ред. И.А.Кондратьевой, В.Д.Самуилова. — М.: Изд-во МГУ, 2001. — 350 с.
- Хаитов Р.М., Игнатьева Г.А., Сидорович И.Г. Иммунология. — М.: Медицина, 2000. — 275 с.