На сегодняшний день внутримозговые кровоизлияния являются важной проблемой общественного здравоохранения, которые приводят к высоким показателям летальности и инвалидизации взрослых пациентов. Не смотря на значительное улучшение диагностики внутримозговых кровоизлияний во всем мире за последние 10 лет, показатели летальных исходов не снижаются. Результаты проведенных клинических исследований показывают, что скоординированная работа скорой и специализированной медицинской помощи населению, позволяет достичь более низкой летальности. Разработка протоколов лечения для оказания неотложной помощи, а также новых рекомендаций по ведению пациентов в специализированных учреждениях, могут улучшить исходы лечения пациентов с внутримозговыми кровоизлияниями. Специализированный подход в лечении внутримозговых кровоизлияний включает в себя: раннюю диагностику и остановку продолжающегося кровотечения, постоянный контроль артериального давления, хирургические методы удаления внутримозговых гематом, методики устранения последствий внутрижелудочковых кровоизлияний, а также лечение внутричерепного давления. Данные подходы улучшают клиническое течение заболевания у пациентов с внутримозговыми кровоизлияниями и способствуют снижению показателей летальных исходов и улучшению функциональных исходов заболевания.
Введение. Нетравматические внутримозговые кровоизлияния (ВМК) возникают в результате разрыва кровеносных сосудов головного мозга, которые приводят к высоким показателям летальности и инвалидизации. Это очень серьезная проблема общественного здравоохранения, при показателях заболеваемости 10-30 на 100 тыс. населения в год [1]. Количество госпитализаций пациентов с ВМК увеличилось на 18% за последние 10 лет, вероятно, изза увеличения количества пожилых людей, многие из которых не получают адекватной терапии по поводу артериальной гипертензии и все более широкого использования антикоагулянтов, тромболитиков и антиагрегантов [2]. Азиаты, латиноамериканцы, афроамериканцы имеют более высокие показатели заболеваемости, чем лица европеоидной расы [3]. Различия в основном заметны в распространенности глубинных ВМК и наиболее заметны у пациентов молодого и среднего возраста. Снижение показателей заболеваемости в некоторых популяциях, возможно, связано как с доступностью специализированной медицинской помощи, так и с более качественным контролем артериального давления.
Первичные и вторичные (в том числе индуцированные антикоагулянтами) внутричерепные кровоизлияния имеют сходные патологические изменения [4]. ВМК чаще происходят в полушариях головного мозга, базальных ганглиях, таламусе, стволе мозга (преимущественно в мосту) и мозжечке в результате разрыва сосудов, имеющих дегенеративные изменения вследствие артериальной гипертензии и церебральной амилоидной ангиопатии. Большинство кровотечений при ВМК связанных с гипертензией, локализуются вблизи бифуркаций небольших пенетрирующих артерий, которые ответвляются от базилярной артерии или передней, средней или задней мозговых артерий головного мозга [5]. Малые ветви диаметром 50-700 мкм часто имеют несколько мест разрывов; некоторые из них частично затромбированы. Помимо этого, происходит повреждение эластической мембраны, атрофия и фрагментация мышечного слоя сосудов, диссекция, а также гранулярная или везикулярная клеточная дегенерация [6]. Атеросклероз, включая липидную инфильтрацию, может влиять, в частности, на пожилых пациентов. Фибриноидный некроз субэндотелия с последующими очаговыми дилатациями (микроаневризмами) приводит к кровоизлиянию у небольшой части пациентов. Церебральная амилоидная ангиопатия характеризуется отложением в-амилоидного пептида и дегенеративными изменениями (образование микроаневризм, хронические воспалительные инфильтраты и фибриноидный некроз) в капиллярах, артериолах и артериях малого и среднего калибра коры головного мозга, мягкой мозговой оболочки, и мозжечка [7]. ВМК, связанные с приемом пероральных антикоагулянтов, обычно возникают у пациентов с васкулопатиями, хронической гипертензией или церебральной амилоидной ангиопатией, что может значительно ухудшать течение заболевания [8]. Патофизиология. Область, вокруг гематомы, характеризуется наличием отека, апоптоза и некроза, а также инфильтрацией воспалительными клетками. Гематома вызывает разрушение нейронов и клеток глии (Рисунок 1), которое приводит к высвобождению нейромедиаторов, митохондриальной дисфункции и деполяризации мембран [9]. В зависимости от тяжести митохондриальной дисфункции исходы повреждения варьируются от временной метаболической супрессии (фаза гибернации) до клеточного отека и некроза. Вторичные повреждения провоцируются продуктами распада гемоглобина и факторами коагуляции, в частности тромбином, которые приводят к активации микроглии (макрофагов) через 4 часа после кровоизлияния [10]. Активированные продукты реакции микроглии (воспалительные цитокины), вызывают разрушение гематоэнцефалического барьера, возникновение вазогенного отека и апоптоза в нейронах и клетках глии [11].
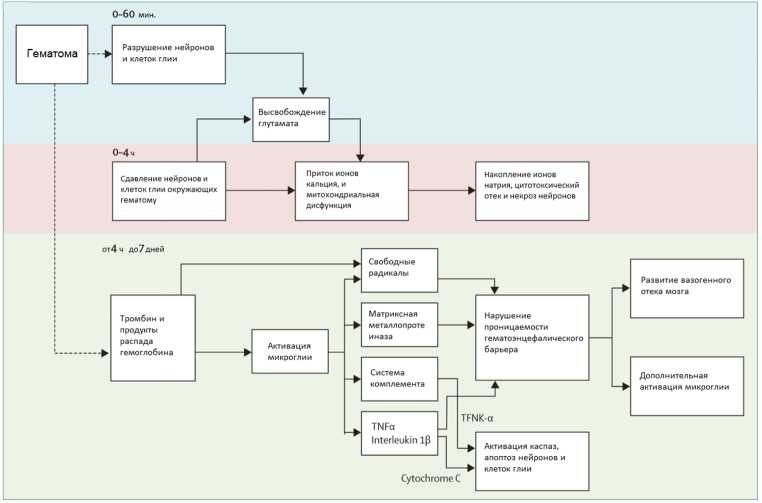 Гемостаз активизируется локальной активацией факторов коагуляции и механической тампонадой. Однако около 73% пациентов, осмотренных в течение 3 часов с момента начала симптомов, имеют некоторую степень увеличения размеров гематомы и до 35% имеют клинически выраженное увеличение. Увеличение размеров гематомы происходит в течение 3 часов, хотя оно может продолжиться и до 12 ч после возникновения кровоизлияния [12]. Отек паренхимы мозга увеличивается примерно на 75% в первые 24 часа после ВМК, пик приходится на 5-6 сутки и длится до 14 дней. Раннее увеличение объема отека относительно объема гематомы вносит наибольший вклад в исход заболевания. Тем не менее, отек, который первоначально не так выражен, может увеличиться в объеме в первые 24 часа после кровоизлияния. В развитии отека важную роль играют гипоперфузинные и метаболические нарушения [13]. Региональная гипоперфузия в клинических и экспериментальных исследованиях не всегда является настолько серьезной, чтобы вызвать ишемию и может быть вторичной по отношению к нарушению метаболизма клеток и тканей мозга. В результате очень высокого внутричерепного давления и низкого перфузионного давления головного мозга риск глобальной ишемии очень высок. Фаза реперфузии длится от 2 до 14 дней, после 14 дней начинается фаза нормализации кровообращения, с восстановлением нормального церебрального кровотока во всех жизнеспособных зонах головного мозга [14].
Гемостаз активизируется локальной активацией факторов коагуляции и механической тампонадой. Однако около 73% пациентов, осмотренных в течение 3 часов с момента начала симптомов, имеют некоторую степень увеличения размеров гематомы и до 35% имеют клинически выраженное увеличение. Увеличение размеров гематомы происходит в течение 3 часов, хотя оно может продолжиться и до 12 ч после возникновения кровоизлияния [12]. Отек паренхимы мозга увеличивается примерно на 75% в первые 24 часа после ВМК, пик приходится на 5-6 сутки и длится до 14 дней. Раннее увеличение объема отека относительно объема гематомы вносит наибольший вклад в исход заболевания. Тем не менее, отек, который первоначально не так выражен, может увеличиться в объеме в первые 24 часа после кровоизлияния. В развитии отека важную роль играют гипоперфузинные и метаболические нарушения [13]. Региональная гипоперфузия в клинических и экспериментальных исследованиях не всегда является настолько серьезной, чтобы вызвать ишемию и может быть вторичной по отношению к нарушению метаболизма клеток и тканей мозга. В результате очень высокого внутричерепного давления и низкого перфузионного давления головного мозга риск глобальной ишемии очень высок. Фаза реперфузии длится от 2 до 14 дней, после 14 дней начинается фаза нормализации кровообращения, с восстановлением нормального церебрального кровотока во всех жизнеспособных зонах головного мозга [14].
Рисунок 1 - Патофизиология внутримозгового кровоизлияния
(Qureshi AIet. al. Intracerebral haemorrhage, Lancet. 2009 May 9; 373)
Диагностика, клиника и исходы.
Несмотря на то, что компьютерная томография (КТ) является методом выбора для первоначальной оценки состояния головного мозга при ВМК, такие режимы магнитно-резонансной томографии (МРТ), как градиентное эхо и Т2 SWI, столь же чувствительны, как и КТ и подходят для выявления острого ВМК и более эффективны при обнаружении мелких очагов кровоизлияния. Экстравазация контраста при КТ-ангиографии может помочь в выявлении продолжающегося кровотечения. Для диагностики причин вторичных ВМК, таких как аневризмы, артериовенозные мальформации, тромбоз венозных синусов и васкулитов необходимо проведение селективной церебральной ангиографии (Рисунок 2). МРТ и МР-ангиография могут также идентифицировать вторичные причины ВМК, такие как кавернозные ангиомы, хотя их чувствительность полностью не доказана [15, 16]. Классические симптомы, такие как внезапное начало, очаговый неврологический дефицит, угнетение сознания и признаки сдавления ствола мозга, напрямую связаны с размером и локализацией гематомы. Нарастание неврологической симптоматики впервые 24 часа связано с ранним увеличением гематомы и немного более поздним развитием отека головного мозга. Прогностическими факторами тяжелого течения заболевания и возможного раннего летального исхода являются: возраст старше 70 лет, исходный балл по шкале комы Глазго ниже 8 баллов, первоначальный объем гематомы, объем внутрижелудочкового кровоизлияния (ВЖК) и увеличение размеров гематомы в динамике [17]. По результатам исследования летальность в течение первых 3х месяцев составила 34% среди 586 пациентов с ВМК [18]. В других исследованиях летальность составляла 31% в течении первых 7-ми дней, 59% через 1 год, 82% через 10 лет и более 90% через 16 лет после кровоизлияния [19]. У пациентов с лобарными кровоизлияниями наблюдалась высокая частота рецидивов (4% в течении одного года). Риск повторного кровотечения может быть значительно снижен при проведении адекватной антигипертензивной терапии [20].
Лечение.
Общие принципы лечения.
В исследовании по течению заболевания, у 1421 пациентов с ВМК, наиболее распространенными причинами летальных исходов (в 68%) являлись недостаток должного ухода или неадекватный контроль за показателями жизненно важных функций [21]. Общенациональное исследование в США показало, что более высокая летальность наблюдается при лечении и ведении пациентов вне условий отделения интенсивной терапии [22]. Другое исследование показало, что внутрибольничная летальность была ниже у пациентов, получавших лечение в отделении нейрореанимации [23]. Эти исследования свидетельствуют о том, что госпитализация в отделение интенсивной терапии может улучшить исход заболевания у пациентов с ВМК. К лечению ВМК необходим единый подход, а именно организованная терапия, которая направлена на уменьшение объема гематомы, удаление ВЖК и борьбу с увеличением гематомы [24].
Ранняя оценка состояния и лечение.
Поддержка адекватного дыхания, контроль артериального и внутричерепного давления обычно начинается в приемном отделении, где пациент с ВМК также может получить первичную консультацию нейрохирурга. Исследования показывают, что около 30% пациентов с супратенториальной локализацией гематомы и почти все пациенты с субтенториальными кровоизлияниями нуждаются в интубации трахеи [25]. Быстрое ухудшение
состояния, признаки дислокации головного мозга, массэффект, окклюзия путей оттока ликвора, являются несомненными показаниями для нейрохирургической консультации и возможной установки внутрижелудочкового дренажа или хирургического удаления гематомы при сопутствующем использовании гипервентиляции и внутривенного введения противоотечных препаратов. Риск нарастания неврологической симптоматики и сердечно-сосудистой недостаточности является наибольшим в первые 24 часа с момента начала симптомов, поэтому необходима частая оценка неврологического статуса пациентов и гемодинамических показателей в специализированных отделениях интенсивной терапии [26].
Срочная гемостатическая терапия.
Активированный рекомбинантный фактор VII (fVIIa) способствует гемостазу в местах повреждения сосудов и препятствует увеличению гематомы в результате ВМК. Проведенные исследования fVIIa не подтвердили вероятность улучшения исходов заболевания, несмотря на значительное снижение скорости увеличения гематомы в объеме [27]. Отсутствие значительного преимущества fVIIa, несмотря на его способности остановки кровотечения, предполагает, необходимость дополнительных методов лечения, таких как хирургическое удаление. Анализ исследуемой подгруппы показал потенциальную выгоду применения fVIIa у пациентов моложе 70 лет, с исходным объемом гематомы менее 60 мл и объема ВЖК менее 5 мл, а также времени от начала не более 2,5 ч [28].
Лечение масс-эффекта, приводящего к развитию внутричерепной гипертензии.
Масс-эффект, вызванный гематомой, а также отеком окружающих тканей и окклюзионной гидроцефалией с последующей дислокацией головного мозга, является основной причиной смерти в первые несколько дней после ВМК. Мониторинг внутричерепного давления (ВЧД), и проведение интенсивной терапии, направленной на контроль церебрального перфузионного давления (ЦПД) на уровне 50-70 мм рт. ст., может приводить к улучшению исходов заболевания [29]. Проведенные исследования с болюсным введением маннитола с целью улучшения регионального церебрального кровотока, не показали положительных результатов [30]. Таким образом, только краткосрочное использование маннитола считается рациональным у пациентов с ВМК при таких состояниях как нарастание масс-эффекта и развитие дислокационного синдрома. Рекомендации The American Stroke Association (ASA) и The European Stroke Initiative (EUSI) подтверждают необходимость в проведении мониторинга ВЧД у пациентов, получавших осмотические диуретики, эвакуацию цереброспинальной жидкости через внутрижелудочковый катетер и гипервентиляцию [31].
Контроль артериального давления.
Высокой распространенностью и неблагоприятным прогностическим значением характеризуется развитие гипертензионного синдрома при ВМК. При анализе 45 330 пациентов с ВМК 75% имели систолическое артериальное давление (САД) более 140 мм рт.ст. у 20% пациентов оно превышало 180 мм рт.ст [32]. Согласно рекомендациям ASA у пациентов с артериальной гипертонией рекомендуется снижение артериального давления (АД) и поддержание среднего АД менее 130 мм рт. ст. [31]. Проведенные исследования показывают, что пациенты с ВМК, получавшие внутривенную инфузию блокаторов кальциевых каналов в соответствии с рекомендациями ASA в течение 24 часов после появления симптомов, хорошо переносили лечение и имели более меньший неврологический дефицит, а болюсное введение антигипертензивных препаратов, оказывают более управляемый эффект в борьбе с высоким АД [33]. При проведении агрессивной терапии по снижению АД отмечается больший терапевтический эффект. В одном из исследований было показано, что увеличение объемов гематомы произошло у 9% пациентов с САД ниже 150 мм рт.ст., у 30% пациентов с САД на уровне 160 мм рт.ст. или выше [34]. Так же было показано, что агрессивное снижение АД до 140 мм.рт.ст. снижает вероятность увеличения объема гематомы [35].
Лечение внутрижелудочковых кровоизлияний и гидроцефалии.
Клинические исследования подтвердили, что ВЖК и нарастающая гидроцефалия являются независимыми показателями неблагоприятного исхода при спонтанном ВМК [36]. Образование кровяных сгустков и сдавление ликворопроводящих путей масс-эффектом приводят к развитию обструктивной гидроцефалии. Наложение вентрикулярного дренажа способствует снижению ВЧД, а также санации желудочков головного мозга от крови, но образование сгустков в катетере и его инфицирование может привести к неблагоприятным результатам [37]. ВЖК является последствием ВМК. В исследовании препарата fVIIa, у 45% из 374 пациентов с внутримозговыми гематомами (ВМГ) отмечалось наличие ВЖК [38]. Появление ВЖК наблюдалось у 17% пациентов, получавших плацебо, и у 10% пациентов, получавших fVIIa. Факторами риска при этом являлись: показатели среднего артериального давления более 120 мм рт.ст., большой объем ВМГ, наличие ВЖК, и отсутствие лечения с помощью fVIIa. При наличии ВЖК увеличилась вероятность летального исхода или тяжелой инвалидности в течении первых начала заболевания. С целью более эффективного лизирования кровяных желудочках головного мозга,
3-х месяцев от быстрого сгустков необходимо из гематомы самым избежать процессов. В тромболитических рандомизированное внутрижелудочковое введение препаратов [39]. Проведенное контролируемое исследование, показало более быстрое разрешение ВЖК, при интравентрикулярном введении тромболитических препаратов, проводимое каждые 12 часов. Систематические обзоры клинических исследований показывают снижение летальности на 30-50%, при интраветрикулярном введении тромболитиков [40]. Хорошего результата в лечении и более благоприятных исходов заболевания при ВЖК и обструктивной гидроцефалии можно достигнуть путем эндоскопического удаления гематомы [41,42].
Хирургическое удаление внутримозговой гематомы. Хирургическое удаление может предотвратить дальнейшее увеличение объема гематомы, уменьшить масс-эффект, а также блокировать высвобождение нейропатических продуктов и тем развитие цепочки патологических исследовании The Surgical Trialin Intracerebral Haemorrhage (STICH) авторы провели сравнение результатов раннего хирургического удаления ВМГ (в среднем через 20 часов после начала заболевания) с консервативными методами лечения у 1033 пациентов [43]. Через 6 месяцев, раннее хирургическое удаление не имело никаких преимуществ в сравнении с консервативным лечением: у 24% против 26% было хорошее восстановление функций или умеренное снижение функциональной активности. Неизбежное повреждение мозговой ткани и рецидивы кровотечения, особенно при ВМГ глубинных локализаций могут быть преимуществами открытого оперативного лечения. Также исследование STICH показало, что хирургическое удаление лобарных гематом и ВМГ в пределах 1 см от поверхности коры головного мозга, вероятнее всего принесет пользу пациенту. Еще одно исследование показало, что раннее нейрохирургическое вмешательство будет наиболее целесообразным у пациентов с исходным уровнем сознания по шкале комы Глазго не менее 8 баллов, или объемом внутримозговой гематомы не более 80 мл [44]. С целью минимизации рисков повреждения структур головного мозга и возможного рецидивирующего кровотечения, связанных с краниотомией, исследования в настоящее время сосредоточены на малоинвазивных методиках, таких как стереотаксическое и эндоскопическое удаление ВМГ с использованием тромболитических препаратов. Рандомизированное исследование показало, что стереотаксическая эвакуация путаменальных гематом характеризуется более низкой летальностью и лучшим восстановлением пациентов с угнетением сознания [45].
Согласно принципам ASA Stroke Council и EUSI рутинное удаление супратенториальных гематом со стандартной краниотомией в течение 96 ч. от начала заболевания не рекомендуются. Оба руководства рекомендуют открытое хирургическое вмешательство у пациентов с лобарными кровоизлияниями в пределах 1 см от поверхности мозга, особенно у пациентов с исходным хорошим неврологическим статусом, у которых отмечается клиническое ухудшение состояния. Хирургическое удаление ВМГ в течение 12 ч, особенно с использованием минимально-инвазивных методик, имеет более хороший эффект и может применяться при глубоких кровоизлияниях и при наличии масс-эффекта. Однако в тех же принципах руководств отмечается, что раннее хирургическое вмешательство может быть связано с повышенным риском рецидива кровотечения.
Операции на задней черепной ямке.
Своевременная декомпрессия при гематомах мозжечка может снизить летальность, связанную с компрессией ствола головного мозга. При анализе данных, у пациентов, которым было проведено хирургическое вмешательство, регресс неврологической симптоматики был значительно выше, чем у тех, кто получал консервативное лечение, независимо от возраста и исходного неврологического дефицита. В большинстве клиник нарастание неврологической симптоматики является показанием для хирургического удаления гематомы задней черепной ямки; но более эффективным, особенно при наличии компрессии четвертого желудочка, будет проведение хирургического вмешательства до развития ухудшения неврологической картины [46]. Эндоскопическое удаление гематомы мозжечка также может быть эффективным, с меньшей продолжительностью времени операции, чем при краниэктомии. ASA Stroke Council и EUSI рекомендуют срочное хирургическое удаление гематомы мозжечка, у пациентов с относительно хорошим неврологическим статусом или гематомой, превышающей 3 см, у которых отмечается ухудшение клинической картины, компрессия ствола головного мозга или обструктивная гидроцефалия. Допускается установка вентрикулярного дренажа, с обязательным мониторированием ВЧД и проведением КТконтроля.
Лечение нейропротекторами и антиконвульсантами.
У 8% пациентов с ВМК отмечаются случаи судорожных приступов в течение 1 месяца после начала симптомов, связанных с лобарной локализацией или увеличением гематомы. Непрерывный электроэнцефалографический мониторинг в одном из исследований показал, что 28% пациентов с ВМК имели (преимущественно субклинические) судороги в течение первых 72 ч после начала заболевания [47]. Судорожные приступы значительно ухудшали течение заболевания и приводили к неблагоприятным исходам. В другом исследовании, проведенном у 45 пациентов с ВМК, было обнаружено 126 субклинических припадков и случаи не судорожного эпилептического статуса у 13% и 9% пациентов соответственно [48]. Таким образом, пациентам с ВМК необходимо назначать противосудорожные препараты в течение 30 дней от начала заболевания.
Лечение осложнений.
Около 30% пациентов с ВМК имеют и желудочно-кишечные кровотечения. Назначение гастропротекторов поможет защитить слизистую оболочку желудка, и уменьшить количество подобных осложнений [49].
Тромбоз глубоких вен нижних конечностей обнаруживается с помощью методов ультрасонографии в первые 2 недели у 40% пациентов. Наибольшему риску подвергаются пациенты с выраженным неврологическим дефицитом и высокой концентрацией D-димера. Рандомизированное исследование показало, что интермиттирующая пневматическая компрессия уменьшает возникновение бессимптомной тромбоэмболии по сравнению с эластическим бинтованием и должно использоваться у всех пациентов [50].Пациентам со стабильным неврологическим статусом, также рекомендуется назначение небольших доз гепарина или низкомолекулярного гепарина на второй день после начала заболевания. При развитии тромбоза глубоких вен, рекомендуется установка кава-фильтра и 5-10-дневный курс низкомолекулярного гепарина, затем 3-месячный курс низкомолекулярного гепарина с меньшей дозировкой или назначение варфарина.
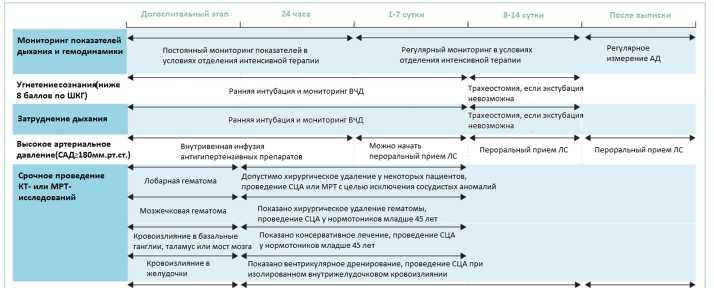
Раннее проведение трахеостомии может снизить риск аспирации и развития легочных осложнений у пациентов с ВМК. Также необходим контроль за гипертермией и гипергликемией с помощью жаропонижающих препаратов и, возможно, инфузий инсулина в остром периоде внутримозговой гематомы.
Высокий показатель МНО
Возобновление антикоагулянтной терапии у пациентов с высоким риском тромбозов и низким риском рецидива кровотечения
Мониторинг повышения показателя МНО
Введение свежезамороженной плазмы, тромбоконцентрата, фактора VII и вит.К
Уровень глюкозы>11ммоль/л
Гипертермия
Усиление неврологического дефицита
Признаки нарастания масс- эффекта и дислокационного синдрома
Судорожные припадки
Профилактика осложнений
Внутривенное введение инсулина
Прием парацетамола
Пероральный прием гипогликемических препаратов или подкожное введение инсулина
Физические методы снижения температуры тела
Повторить КТ-сканирование головного мозга, постоянный мониторинг ВЧД с определением показаний для оперативного вмешательства
Показана гипервентиляция, введение осмотических диуретиков с определением показаний для оперативного вмешательства
Введение антиконвульсантов
Продолжить прием антиконвульсантов
Назначение гастропротекторов, интермиттирующая пневматическая компрессия, назначение небольших доз гепарина или низкомолекулярного гепарина на второй день после начала заболевания
Установка кава-фильтра у пациентов с высоким риском тромбоэмболии.
Рисунок 2 - Алгоритм лечения пациентов с нетравматическим внутримозговым кровоизлияниием (Qureshi AI et. al. Intracerebral haemorrhage, Lancet. 2009 May 9; 373)
Выводы. Клинические данные свидетельствуют о необходимости организации лечения ВМК в трех основных направлениях: остановка продолжающегося кровотечения, удаление гематомы и контроль давления с целью поддержки перфузии головного мозга на приемлемом уровне. Данные подходы лечения могут значительно улучшить клиническое течение заболевания у пациентов с ВМК, способствовать снижению показателей летальных исходов и улучшению функциональных исходов заболевания. Еще одним приоритетом является использование МРТ в реальном времени с высоким разрешением и трехмерной визуализацией. Немаловажным является также изучение агрессивного метода лечения высокого артериального давления и коагулопатии, применение минимально-инвазивных хирургических методик, включая механические и фармакологические способы удаления гематомы. Разработка протоколов лечения для оказания неотложной помощи, а также новых рекомендаций по ведению пациентов в специализированных учреждениях, могут улучшить исходы лечения пациентов с ВМК.
СПИСОК ЛИТЕРАТУРЫ
- Qureshi AI, Tuhrim S, Broderick JP, Batjer HH, Hondo H, Hanley DF. Spontaneousintracerebralhemorrhage // N Engl J Med. 2001. - 1 №u344h. Р. 1T4u5h0-1460B. od k P B ondo n y F pon n ou n b h o h En d 2001
- Qureshi AI, Suri MFK, Nasar A, et al. Changes in cost and outcome among US patients with strokehospitalized in 1990 to 1991 and those hospitalized in 2000 to 2001 // Stroke. 2007. №38. Р. 2180-2184.
- Feigin VL, Lawes CMM, Bennett DA, Anderson CS. Stroke epidemiology: a review of populationbasedstudies of incidence, prevalence, and case-fatality in the late 20th century // Lancet Neurol. 2003. №2. Р. 43-53.
- Steiner T, Rosand J, Diringer M. Intracerebral hemorrhage associated with oral anticoagulanttherapy: current practices and unresolved questions // Stroke. 2006. №37. Р. 256-262.
- Takebayashi S, Kaneko M. Electron microscopic studies of ruptured arteries in hypertensiveintracerebral hemorrhage // Stroke. 1983. №14. Р. 28-36.
- Mizutani T, Kojima H, Miki Y. Arterial dissections of penetrating cerebral arteries causinghypertension-induced cerebral hemorrhage // J Neurosurg. 2000. №93. Р. 859-862.
- Rosand J, Hylek EM, O'Donnell HC, Greenberg SM. Warfarin-associated hemorrhage andcerebral amyloid angiopathy: a genetic and pathologic study // Neurology. 2000. №55. Р. 947-951.
- Hart RG. What causes intracerebral hemorrhage during warfarin therapy? // Neurology. 2000. №55. Р. 907-908.
- Qureshi AI, Suri MF, Ostrow PT, et al. Apoptosis as a form of cell death in intracerebralhemorrhage // Neurosurgery. 2003. №52. Р. 1041-1047.
- Nakamura T, Xi G, Park JW, Hua Y, Hoff JT, Keep RF. Holo-transferrin and thrombin can interactto cause brain damage // Stroke. 2005. №36. Р. 348-352.
- Xi G, Keep RF, Hoff JT. Mechanisms of brain injury after intracerebral haemorrhage // Lancet Neurol. 2006. №5. Р. 53-63.
- Broderick JP, Diringer MN, Hill MD, et al. Determinants of intracerebral hemorrhage growth: anexploratory analysis // Stroke. 2007. №38. Р. 1072-1075.
- Inaji M, Tomita H, Tone O, Tamaki M, Suzuki R, Ohno K. Chronological changes ofperihematomal edema of human intracerebral hematoma // Acta Neurochir Suppl. 2003. №86. Р. 445-448.
- Orakcioglu B, Fiebach JB, Steiner T, et al. Evolution of early perihemorrhagic changes—ischemiavs edema: an MRI study in rats // Exp Neurol. 2005. №193. Р. 369-376.
- Fiebach JB, Schellinger PD, Gass A, et al. Stroke magnetic resonance imaging is accurate inhyperacute intracerebral hemorrhage: a multicenter study on the validity of stroke imaging // Stroke. 2004. №35. Р. 502-506.
- Kidwell CS, Chalela JA, Saver JL, et al. Comparison of MRI and CT for detection of acuteintracerebral hemorrhage // JAMA. 2004. №292. Р. 1823-1830.
- Leira R, Davalos A, Silva Y, et al. Early neurologic deterioration in intracerebral hemorrhage:predictors and associated factors // Neurology. 2004. №63. Р. 461-467.
- Weimar C, Weber C, Wagner M, et al. Management patterns and health care use after intracerebralhemorrhage. a cost-of-illness study from a societal perspective in Germany // Cerebrovasc Dis. 2003. №15. Р. 29-36.
- Flaherty ML, Haverbusch M, Sekar P, et al. Long-term mortality after intracerebral hemorrhage // Neurology. 2006. №66. Р. 11821186.
- PROGRESS Collaborative Group. Randomised trial of a perindopril-based blood-pressureloweringregimen among 6105 individuals with previous stroke or transient ischaemic attack // Lancet. 2001. №358. Р. 1033-1041.
- Zurasky JA, Aiyagari V, Zazulia AR, Shackelford A, Diringer MN. Early mortality followingspontaneous intracerebral hemorrhage // Neurology. 2005. №64. Р. 725-727.
- Hemphill JC 3rd, Newman J, Zhao S, Johnston SC. Hospital usage of early do-not-resuscitate orders and outcome after intracerebral hemorrhage // Stroke. 2004. №35. Р. 1130-1134.
- Diringer MN, Edwards DF. Admission to a neurologic/neurosurgical intensive care unit isassociated with reduced mortality rate after intracerebral hemorrhage // Crit Care Med. 2001. №29. Р. 635-640.
- Tuhrim S. Intracerebral hemorrhage—improving outcome by reducing volume? // N Engl J Med. 2008. №358. Р. 2174-2176.
- Gujjar AR, Deibert E, Manno EM, Duff S, Diringer MN. Mechanical ventilation for ischemicstroke and intracerebral hemorrhage: indications, timing, and outcome // Neurology. 1998. №51. Р. 447-451.
- Naff NJ, Tuhrim S. Intraventricular hemorrhage in adults: complications and treatment // NewHorizons. 1997. №5. Р. 359-363.
- Mayer SA, Brun NC, Begtrup K, et al. Recombinant activated factor VII for acute intracerebral hemorrhage // N Engl J Med. 2005. №352. Р. 777-785.
- Mayer SA, Davis SM, Begtrup K, et al. Subgroup analysis in the FAST trial: a subset ofintracerebral hemorrhage patients that benefit from recombinant activated factor VII // Stroke. 2008. №39. Р. 528-533.
- Fernandes HM, Siddique S, Banister K, et al. Continuous monitoring of ICP and CPP followingICH and its relationship to clinical, radiological and surgical parameters // Acta Neurochir Suppl. 2000. №76. Р. 463-466.
- Misra UK, Kalita J, Ranjan P, Mandal SK. Mannitol in intracerebral hemorrhage: a randomizedcontrolled study // J Neurol Sci. 2005. №234. Р. 41-45.
- Broderick J, Connolly S, Feldmann E, et al. Guidelines for the management of spontaneousintracerebral hemorrhage in adults: 2007 update: a guideline from the American HeartAssociation/American Stroke Association Stroke Council, High Blood Pressure Research Council,and the Quality of Care and Outcomes in Research Interdisciplinary Working Group // Stroke. 2007. №38. Р. 2001-2023.
- Qureshi AI, Ezzeddine MA, Nasar A, et al. Prevalence of elevated blood pressure in 563,704 adultpatients with stroke presenting to the ED in the United States // Am J Emerg Med. 2007. №25. Р. 32-38.
- Qureshi AI, Mohammad YM, Yahia AM, et al. A prospective multicenter study to evaluate thefeasibility and safety of aggressive antihypertensive treatment in patients with acute intracerebralhemorrhage // J Intensive Care Med. 2005. №20. Р. 34-42.
- Ohwaki K, Yano E, Nagashima H, Hirata M, Nakagomi T, Tamura A. Blood pressure managementin acute intracerebral hemorrhage: relationship between elevated blood pressure and hematomaenlargement // Stroke. 2004. №35. Р. 1364-1367.
- Qureshi, AI. Antihypertensive Treatment of Acute Cerebral Hemorrhage (ATACH) trial // International Stroke Conference. New Orleans, LA.: 2008. Р. 52-56.
- Bhattathiri PS, Gregson B, Prasad KS, Mendelow AD. Intraventricular hemorrhage andhydrocephalus after spontaneous intracerebral hemorrhage: results from the STICH trial // ActaNeurochir Suppl. 2006. №96. Р. 65-68.
- Hanley DF. Intraventricular hemorrhage and ICH outcomes: severity factor and treatment target // Stroke. 2009. №2. Р. 358-364.
- Steiner T, Diringer MN, Schneider D, et al. Dynamics of intraventricular hemorrhage in patientswith spontaneous intracerebral hemorrhage: risk factors, clinical impact, and effect of hemostatictherapy with recombinant activated factor VII // Neurosurgery. 2006. №59. Р. 767-773.
- Huttner HB, Tognoni E, Bardutzky J, et al. Influence of intraventricular fibrinolytic therapy withrt-PA on the long-term outcome of treated patients with spontaneous basal ganglia hemorrhage: acase-control study // Eur J Neurol. 2008. №15. Р. 342-349.
- Nieuwkamp DJ, de Gans K, Rinkel GJ, Algra A. Treatment and outcome of severeintraventricular extension in patients with subarachnoid or intracerebral hemorrhage: a systematicreview of the literature // J Neurol. 2000. №247. Р. 117-121.
- Yadav YR, Mukerji G, Shenoy R, Basoor A, Jain G, Nelson A. Endoscopic management ofhypertensive intraventricular haemorrhage with obstructive hydrocephalus // BMC Neurol. 2007. №7. Р. 1-5.
- Zhang Z, Li X, Liu Y, Shao Y, Xu S, Yang Y. Application of neuroendoscopy in the treatment ofintraventricular hemorrhage // Cerebrovasc Dis. 2007. №24. Р. 91-96.
- Mendelow AD, Gregson BA, Fernandes HM, et al. Early surgery versus initial conservativetreatment in patients with spontaneous supratentorial intracerebral haematomas in the International Surgical Trial in Intracerebral Haemorrhage (STICH): a randomised trial // Lancet. 2005. №365. Р. 387-397.
- Pantazis G, Tsitsopoulos P, Mihas C, Katsiva V, Stavrianos V, Zymaris S. Early surgicaltreatment vs conservative management for spontaneous supratentorial intracerebral hematomas:aprospective randomized study // Surg Neurol. 2006. №66. Р. 492-501.
- Hattori N, Katayama Y, Maya Y, Gatherer A. Impact of stereotactic hematoma evacuation on activities of daily living during the chronic period following spontaneous putaminal hemorrhage:a randomized study // J Neurosurg. 2004. №101. Р. 417-420.
- Morioka J, Fujii M, Kato S, et al. Surgery for spontaneous intracerebral hemorrhage has greaterremedial value than conservative therapy // Surg Neurol. 2006. №65. Р. 67-72.
- Vespa PM, O'Phelan K, Shah M, et al. Acute seizures after intracerebral hemorrhage: a factor inprogressive midline shift and outcome // Neurology. 2003. №60. Р. 1441-1446.
- Claassen J, Mayer SA, Kowalski RG, Emerson RG, Hirsch LJ. Detection of electrographicseizures with continuous EEG monitoring in critically ill patients // Neurology. 2004. №62. Р. 1743-1748.
- Misra UK, Kalita J, Pandey S, Mandal SK, Srivastava M. A randomized placebo controlled trialof ranitidine versus sucralfate in patients with spontaneous intracerebral hemorrhage forprevention of gastric hemorrhage // J Neurol Sci. 2005. №239. Р. 5-10.
- Lacut K, Bressollette L, Le Gal G, et al. Prevention of venous thrombosis in patients with acuteintracerebral hemorrhage // Neurology. 2005. №65. Р. 865-869.