Одной из значимых проблем хирургической стоматологии и челюстно-лицевой хирургии является проблема регенерации костной ткани при заполнении дефектов. Впервые будет разработаны композиционные трансплантационные материалы на основе отечественного нанокристаллического гидроксилапатита, костного коллагена, замешанных на плазме, обогащенной тромбоцитами и отечественного нанокристаллического гидроксилапатита, костного коллагена, замешанных на плазме крови кролика. Впервые будет дано экспериментальное обоснование эффективности разработанного нами нового трансплантационного композитного материала на основе нанокристаллического гидроксилапатита, обогащенной тромбоцитами плазмы и костного коллагена при пластике созданного сквозного дефекта в области угла нижней челюсти кролика с помощью морфологических исследований.
Современное состояние применения биосовместимых материалов. Биосовместимость предмет, который исследуется и анализируется более 50 лет. В последние годы четко прослеживается рост исследований о биоматериалах из предмета, который почти исключительно касался медицинских имплантатов, к исследованиям о биоматериалах, используемых в процессах доставки генов и лекарств, в клеточной терапии и тканевой инженерии, а также в различных системах визуализации и диагностики. Существенный прогресс в вопросе регенерации костных полостей может быть достигнут благодаря разработке новых научных технологий. В последние годы на лидирующие позиции в современной регенеративной медицине выходят нанотехнологии. Из различных наночастиц, используемых в настоящее время (фуллерены, наноалмазы и др.), существенная роль в практической медицине может принадлежать нанокристаллическому гидроксиапатиту: обладает высокой сорбционной и адгезивной активностью по отношению к белкам; быстро реагирует на изменение биохимической среды в ткани. С помощью наногидроксилапатита, легко воспринимаемого и адаптируемого организмом, можно восстановить различные костные полости В Республике Казахстан учеными из Института проблем горения Казахского национального университета им. аль-Фараби был синтезирован нанокристаллический гидроксиапатит кальция различными методами химического осаждения с использованием биологического источника — яичной скорлупы птиц, которая на 94% состоит из карбоната кальция. Полученный порошкообразный материал представляет собой мелкодисперсный порошок микронных размеров (4—5 |im). Новая рецептура в наногидроксилапатитной смеси как основного компонента неорганических материалов кости, повышает биосовместимость и биоактивность соединения, давая возможность организму восстанавливаться много быстрее.
В доступной нам литературе не обнаружено каких-либо опытов использования нанокристаллического гидроксиапатита, как костнозамещающего материала (НГАП) (Темирбаев М.А., 2015).
Состав и выбор биоматериала зависят от его конкретного применения [5]. Биосовместимый материал, помимо того, что не должен индуцировать воспаления, токсические реакции и аллергенные симптомы в организме, должен быть биосовместимым, биофункциональным, биоактивным, биоинертным и стерилизуемыми, что в свою очередь означает, что процессы стерилизации не должны способствовать модификации свойств биоматериала, что является одним из важных условий, так как поверхность биоматериала, непосредственно воздействующая на живые клетки организма, играет решающую роль в отношении биосовместимости [6]. При рассмотрении этого вопроса, физические, морфологические и биологические характеристики могут быть адаптированы для улучшения взаимодействия биоматериалов и тканей [7].
В последние несколько лет концепция биосовместимости была глубоко изменена. Считалось, что материал биосовместим, будучи полностью инертным в организме человека, без какой-либо реакции от биологической среды к ее присутствию. Идея полностью инертного материала была отвергнута. После проведения исследований обнаружилось, что наличие какого-либо материала всегда влечет за собой некоторый отклик организма, изменяющийся в зависимости от вида применения и характеристик пациентов (возраст, пол и т. д.). Таким образом, понятие биосовместимости материала, в частности, взаимодействие с живыми тканями, можно определить только путем охвата различных форм взаимодействия органов с материалом [8]. Биоматериалы могут быть использованы для различных применений в множестве областей медицины. Однако для каждого из этих применений требуемой особенностью свойств биоматериалов является степень взаимодействия при контакте с органами и тканями.
Использование медицинских имплантатов увеличилось в последние десятилетия из-за старения населения, увеличения продолжительности жизни, стиля жизни и улучшения технологии имплантатов [9]. Разработка биоматериалов, обладающих необходимыми характеристиками для восстановления тканей, поврежденных в результате несчастных случаев или болезней, является одной из основных проблем в научной области, касающейся медицины и инженерии [10].
Биосовместимый материал, используемый в области медицины как для замены органа, так и для роста ткани или адресной доставки лекарственных препаратов, должен иметь определенные характеристики, чтобы не стимулировать или не вызывать каких-либо аллергенных или воспалительных реакций в организме человека. Характеристики, которые следует учитывать, когда речь идет о биоматериале, используемом для имплантата, включают биосовместимость, биофункциональность, химическую и механическую стабильность. Помимо этих характеристик материал должен быть стерилизован во избежание раздражения, отторжения и / или проблем в локусе имплантата [11, 12].
Биосовместимость материала, связана с различными свойствами материалов, такие как токсичность, совместимость с тканями, совместимость с кровью (гемосовместимость) и свойствами биологической функциональности [13]. Биофункциональность подразумевает собой то что материал эффективно выполняет определенные функции, в требуемый период времени.
Объем исследования: 24 кроликов породы «Шиншилла» весом 4000 4500 грамм обоего пола. Животные до и после операции будут содержаться в условиях вивария КазНМУ имени С.Д. Асфендиярова.
У кроликов будет проведено определение динамики восстановления костной ткани искусственно созданных костных дефектов челюстей у кроликов при помощи рентгенологических и морфологических методов исследования.
Животные обеих серий выводились из опыта путём передозировки введения в ушную вену наркотических веществ в сроки: 30, 60, 90 и 120 суток после проведённой операции. У выведенных из опыта животных вычленяется послеоперационная половина нижней, и проводится рентгенологическое исследование, а затем выпиливаются костные блоки со слизистой оболочкой в области оперативного вмешательства, фиксируются в 10% растворе нейтрального формалина, декальцинируются в азотной кислоте, обезвоживаются в спиртах, заливаются в парафин, готовятся серийные срезы толщиной 10-12 микрон и окрашиваются гематоксилин-эозином и по Вангизону.
Животные до и после содержались в условиях вивария НИИ ФПМ им. Б.Атчабарова, КазНМУ имени С.Д. Асфендиярова. Для экспериментов будут использоваться лабораторные животные (кролики), которые будут находиться в специализированном помещении с характеристикой их содержания согласно международным правилам по этическому обращению с животными. Все манипуляции, проводимые на лабораторных животных, будут проведены с обязательным соблюдением Хельсинской декларации защиты позвоночных животных, используемых для экспериментов и других научных целей (от 1975 года и ее пересмотренного варианта 2008 г.)
Критерии включения, исключения и выбытия животных:
- критерии включения здоровые, половозрелые животные обоего пола
- критерии исключения больные кролики (изменение покровов, глаз, состава мочи, экскрементов, наличие ран).
- критерии выбытия животных данные всех подопытных животных после начала эксперимента включаются в отчет. Основные изучаемые группы:
Экспериментальная часть работы на кроликах будет включать две серии:
серия эксперимента две группы животных по 12 кроликов. Под рометаровым наркозом и инфильтрационной анестезией 2% раствором лидокаина производится разрез в поднижнечелюстной области длиной 2 см. Скелетируется нижний край нижней челюсти, с помощью распатора отслаиваются мягкие ткани до кости и отводятся кверху. С помощью окончатой фрезы диаметром 1 см воспроизводится стандартный сквозной дефект нижнечелюстной кости в области её угла. Вместе с костным фрагментом резецируется и надкостница с обеих сторон челюсти. В контрольной группе животныхвоспроизведенные дефекты заполняются пастой из костного коллагена и кристаллического гидроксилапатита фирмы «ЮКОК» (Шымкент), замешанной на плазме, обогащенной тромбоцитами, в подопытной же группе полость заполняется композитом из костного коллагена, нанокристаллического гидроксилапатита, замешанного на плазме, обогащенной тромбоцитами. Введенный в послеоперационный дефект трансплантационный материал закрывается коллагеновой мембраной, фиксируется мышечно-кожным лоскутом, лоскут укладывается на место.
Послеоперационная рана мягких тканей послойно ушивается кетгутом и викрилом. Композит будет готовиться во время операции следующим образом: порошковый костный коллаген и нанокристаллический гидроксилапатит в равных весовых пропорциях смешивается на стерильном стекле, добавляется обогащенная тромбоцитами плазма, приготовленная из крови кролика и шпателем перемешивается с образованием густой смеси, с последующим введением в искусственно созданную полость в области угла нижней челюсти кролика.
Таблица 1 Описание распределения опытных и контрольных групп
|
Вид животных |
Кол-во |
Вес |
Серия эксперимента |
Характеристика модели |
Тип исследования |
|
Кролики породы «Шиншилла» |
24 |
4000 4500 гр |
1 серия -2 группы Кролики с созданным дефектом нижнечелюстной кости в области её угла. |
Использование костного коллагена и кристаллического гидроксилапатита фирмы «ЮКОК» (Шымкент), замешанной на плазме, обогащенной тромбоцитами в контрольной группе, использование костного коллагена, нанокристаллического гидроксилапатита, замешанного на плазме, обогащенной тромбоцитами в подопытной группе. |
Экспериментальная модель |
Результаты: Клинические наблюдения послеоперационного периода в обеих группах животных показали, что спустя сутки после оперативного вмешательства в области травмы определялся умеренный отек мягких тканей, который постепенно увеличивался и достигал максимальных размеров к третьим суткам. Затем послеоперационный отек мягких тканей постепенно уменьшался и полностью исчезал в контрольной группе к 9 суткам, в подопытной же группе к 6 суткам. Послеоперационные раны в контрольной группе животных зажили первичным натяжением на 11 сутки, а в подопытной группе на 8 сутки после операции.
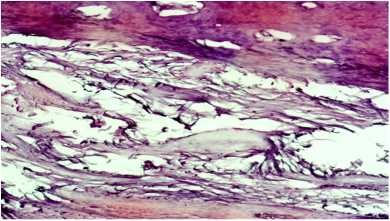
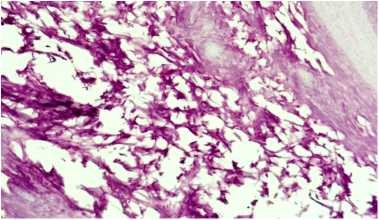
Морфологические исследования показали, что в контрольной группе животных на 15 сутки большая часть послеоперационного дефекта заполнена грануляционной тканью содержащей в свое составе многочисленные кровеносные сосуды , клеточные элементы. Среди клеток появляется тонкие коллагеновые волокна. (рисунок 1). В подопытеой группе начерез 15 суток послеоперационной дефект заполнен зрелой клеточно-волокнистой тканью, а на его переферии начинаются процессы формирования остеоидной ткани, местами появля ются нежные костные балочки и трабекулярные структуры (рисунок 2).
Рисунок 1
Рисунок 2
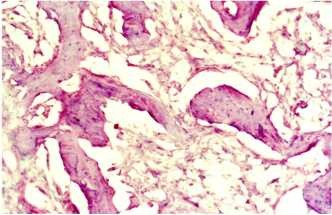
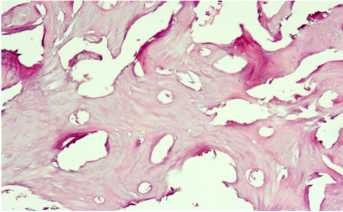
У контрольных животных на 30 сутки в центре костного дефекта выявляются крупные очаги разрастания грубой клеточно-волокнистой ткани. В периферических отделах костного дефекта появляются примитивные костные балочки, которые образуют трабекулярные структуры (рисунок 3). Через 30 суток в подопытной группе послеоперационный дефект практически полностью замещен новообразованной костной тканью. В периферической части костного дефекта регенерат становится более мощным, вокруг капилляров появляются концентрические фигуры в виде трубочек, формирующих компактные остеонные системы (рисунок 4).
Рисунок 3
Рисунок 4
У контрольных животных к 90 суткам костный дефект подопытной группе на 90 сутки определяется уже зрелая заполнен толстыми трабекулярными структурами и грубой новообразованная костная ткань, полностью сливающаяся с волокнистый соединительной тканью (рисунок 5). В материнской костной тканью по краю дефекта (рисунок 6).
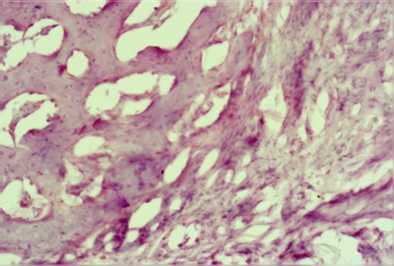
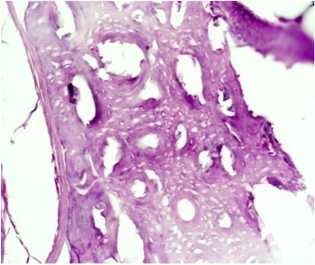
Рисунок 5
Рисунок 6
СПИСОК ЛИТЕРАТУРЫ
- Агентство маркетинговых и социологических исследований «damuresearch», отчет по результатам исследования Рынок стоматологических услуг Республики Казахстан
- Данильченко С..Н. Влияние биокомпозиционных материалов на регенерацию костной ткани при заполнении дефектов челюстных костей после удаления радикулярных кист челюстей: Дисс. ... канд.мед.наук М., 2005. 149 с.
- Murugan R., Ramakrishna S. Nanocrystallic hydroxyapatite from biological material for practical health care // American Journal of Biochemistry and Biotechnology. 2007. V.3., №3. С. 118-124.
- Prodana M., Bojin D., Ionita D. Obtaining nanocrystalline hydroxyapatitis method of chemical precipitation using a biological source calcium // U. P. B. Sci. Bull. 2009. V.71, №4. P. 1454-2331.
- Chen, Q., Thouas, G.A.: Metallic implant biomaterials // Mat. Sci. Eng. R. 2015. №87. Р. 51-57.
- Bauer, S., Schmuki, P., Von Der Mark, K., Park, Engineering biocompatible implant surfaces Part I: materials and surfaces // Prog. Mater Sci. 2013. №58. Р. 261-326.
- Domanska, A., Boczkowska, A.: Biodegradable polyurethanes from crystalline prepolymers // Polym. Degrad. Stab. 2014. №108. Р. 175-181.
- Orefice, R.L., Pereira, M. de. M., Mansur, H.S.: Biomateriais: fundamentos e eaplicafoes // Cultura Medica. Rio de Janeiro: 2006. №8. Р. 89-97.
- Holzapfel, B.M., Reichert, J.C., Schantz, J.T., Gbureck, U., Rackwitz, L., Noth, U., Jakob, F., Rudert, M., Groll, J., Hutmacher, D.W.: How smart do biomaterials need to be? A translational science and clinical point of view // Adv. Drug Deliv. Rev. 2013. №65. Р. 581-603.
- Lasprilla, A.J.R., Martinez, G.A.R., Lunelli, B.H., Jardini, A.L., MacielFilho, R.: Poly-lactic acid synthesis for application in biomedical devices: a review // Biotechnol. Adv. 2012. №30(1). Р. 321-328.
- Ravaglioli, A., Krajewski, A.: Bioceramics—Materials, Proprieties Applications // Chapman & Hall. Nova York: 1992. Р. 122-129.
- Silver, F., Doillon, C.: Biocompatibility: interactions of biological and implantable materials. VCH. New York: 1989. 371 р.
- Wang, Y.X., Robertson, J.L., Spillman Jr., W.B., Claus, R.O.: Effects of the chemical structure and the surface properties of polymeric biomaterials on their biocompatibility // Pharm. Res. 2004. №21(8). Р. 1362-1373.
- Hench, L.L., Wilson, J.: An Introduction to Bioceramics // World Scientific Publish. Singapore: 1999. Р. 51-57.
- Rai, R., Tallawi, M., Roether, J.A., Detsch, R., Barbani, N., Rosellini, E., Kaschta, J., Schubert, D.W., Boccaccini, A.R.: Sterilization effects on the physical properties and cytotoxicity of poly(glycerol sebacate) // Mater. Lett. 2013. №105. Р. 32-35.