В данной статье рассматривалась клиническая характеристика пациентов рассеянным склерозом в г. Алматы, как наличие активности заболевания, длительность заболевания, частота обострений, длительность первой ремиссии, выраженность неврологического дефицита по расширенной шкале инвалидности (EDSS) и выраженность дефицита по отдельным функциональным шкалам, симптоматика, с которой заболевание дебютировало, длительность заболевания до наступления прогредиентного течения и принимавшиеся ранее препараты для лечения РС.
Введение. Рассеянный склероз (РС) аутоиммунное заболевание центральной нервной системы, которое наиболее часто является причиной инвалидности у молодых людей. В основе заболевания лежат воспаление и нейродегенеративные изменения, которые могут привести к необратимому повреждению нейронов. Считается, что аксональная дегенерация в конечном счете несет ответственность за прогрессирующую неврологическую дисфункцию [1].
В 2008 году было подсчитано, что около 2,5 млн. человек страдали от РС по всему миру, что соответствует общей распространенности 120/100 000, ежегодная заболеваемость составляет 7/100 000 жителей [2]. Возраст начала заболевания приходится на 20-40 лет. Самые высокие показатели распространенности встречаются в населения североевропейского происхождения, особенно в Скандинавии, Великобритании, северные части США и Южной Канады [2, 3]. В Финляндии показатель распространенности РС оценивается приблизительно в 130/100 000, а ежегодная заболеваемость составляет 7/100 000 жителей [3, 4]. В некоторых исследованиях отмечают об увеличении уровня заболеваемости РС, за последнее столетие, особенно у женщин, что приводит к соотношению женщин и мужчин 3: 1 [4, 5].
Неравномерное распределение РС среди популяций объясняют различиями в генах и окружающей среде и их взаимодействии [5, 6, 7].
Согласно многочисленным исследованиям, был идентифицирован генетический компонент как фактор риска развития РС, при этом зарегистрировано около 110 генов. Различные комбинации генов взаимодействуют, чтобы влиять на риск. Генетическая восприимчивость к РС традиционно связывают с гаплотипами класса II человека с лейкоцитарным антигеном (HLA) HLA-DW2 и HLA-DR2.
Было проведено много исследований для определения факторов экологического риска, связанных с развитием РС. Факторы экологического риска для РС могут быть разделены на инфекционные и неинфекционные факторы. Что касается инфекционных факторов риска, то, более всего, придают значение вирусу Эпштейна-Барра (EBV) [7, 8]. Общеизвестные неинфекционные факторы риска включают низкое потребление D-витамина, а также низкий уровень воздействия солнечных лучей [8, 9].
Исследования также показали взаимосвязь даты рождения больных РС, так в северном полушарии наблюдается увеличение числа РС родившихся весной и уменьшение РС у пациентов, родившихся осенью; в южном полушариикартина меняется наоборот, с ростом в ноябре и уменьшением в апреле [8].
В патогенезе особое значение отводят иммунному механизму. Долгое время считалось, что только активированные Т-клетки пересекают гематоэнцефалический барьер и входят в центральную нервную систему, вызывая воспалительную реакцию, которая приводит к повреждению миелиновых и миелинобразующих клеток, называемых олигодендроцитами (этот процесс известен как демиелинизация) [8, 9].
Теперь В-клетки считаются центральным компонентом патологии РС. Дисфункция и аберрантная активность антигенпредставляющих клеток, Т-клеток и В-клеток являются частью патофизиологии заболевания [8, 9]. Вклетки способствуют прогрессированию болезни с помощью множества механизмов, включая секрецию цитокинов, продуцирование антител и представление антигена. Более поздние данные свидетельствуют о том, что В-клетки могут играть более значительную роль, чем считалось ранее в развитии острых эпизодов РС [8, 9]. Научные знания о роли В-клеток при РС существенно увеличились за последнее десятилетие, так в клинических исследованиях широко обсуждается анти-CD20-опосредованного истощения Вклеток. Помимо того, что В-клетки являются источником продуцирующих антитела плазматических клеток, они опосредованного истощения В-клеток в РС. Установлено, что популяция периферических CD20 + иммунных клеток участвует в воспалительной инфильтрации ЦНС, вызывая острые рецидивы РС [8-12]. Миелин это изоляционный материал, который покрывает аксоны нейронов в ЦНС и обеспечивает быстрое и эффективное передачу импульсов вдоль аксона. Когда это покрытие повреждено, передача импульсов вдоль аксона может быть отложена или нарушена, или полностью заблокирована. Особенностью РС является постоянная потеря аксонов и дегенерация нейронов, что приводит к более высокой частоте атрофии головного мозга, больше чем можно было бы ожидать в общей популяции [10, 11, 12]. Здоровые взрослые теряют 0,1-0,5% своих клеток головного мозга в год, тогда как люди с РС теряют 0,5-1,35% в год [13, 14]. Атрофия головного мозга начинается на ранних стадиях заболевания [14], часто даже до постановки диагноза, и продолжается на протяжении всей жизни, если у человека нет соответствующего модифицирующего лечения.
Клинически РС вызывает множество симптомов, которые влияют на физическую и когнитивную функцию, а также на настроение; симптомы различаются между людьми и для одного и того же человека. РС затрагивает каждый аспект жизни людей работу, семью, социальную жизнь и характеризуется непредсказуемостью и изменчивостью.
В большинстве случаев (85%) РС первоначально представляет собой рецидивирующую болезнь. Рецидивирующий ремиттирующий тип РС (РРРС) характеризуется рецидивами, которые определяются как атаки новых или рецидивирующих неврологических признаков или симптомами, согласующиеся с демиелинизирующим событием в ЦНС, продолжающимся не менее 24 часов и последующее полное или частичное восстановление. В зависимости от нейроанатомического расположения очага или очагов поражения в ЦНС, симптомы могут включать самые различные сенсорные, моторные дисфункции, когнитивные нарушения и т.д.
По мере прогрессирования заболевания восстановление после рецидивов остается неполным, и начинают накапливаться постоянные симптомы.
Примерно через 10-15 лет в 50-65% пациентов с РРРС, болезнь переходит во вторичную прогрессивную (ВПРС) форму, где постепенное прогрессирование заболевания приводит к увеличению инвалидности, и эта стадия может быть или не быть наложена с рецидивами. РС классифицируется по разным типам в зависимости от течения заболевания, но поскольку нет объективного диагностического теста, часто бывает сложно точно определить тип. Особенно трудно идентифицировать переход между рецидивирующим типом РС и вторично прогрессирующим РС.
Первый острый эпизод или рецидив называют клинически изолированный синдром (КИС), если диагностические критерии не всегда удовлетворены для РРРС [16]. Термин КИС обычно применяется к молодым людям с эпизодами острого или подострого начала, который достигает пика довольно быстро в течение 2-3 недель. У 85% молодых людей РС, зачастую КИС начинается с острого поражения зрительных нервов, мозгового ствола или спинного мозга [16].
Улучшенное понимание патофизиологии РС недавно привело к пересмотру способа описания РС, и неврологи все чаще классифицируют заболевание как рецидивирующие или прогрессивные, так и активные или неактивные [15]. Это особенно актуально при рассмотрении лечения препаратами изменяющими течение РС (ПИТРС). Назначение ПИТРС должно основываться на количестве рецидивов, наблюдавшихся за данный период времени, и на показателях активности болезни, проявляемых магнитно-резонансной томографией.
В меньшинства (10-20%) случаев, заболевание представляет собой первичную прогрессирующую (ППРС) где прогрессивное накопление инвалидности проявляется уже с самого наступление симптомов.
Диагностика и лечение рецидивов РС в клинической практике является сложной задачей, так как существует множество проявлений рецидива, таких как неврит зрительного нерва, пароксизмы и миелит, а симптомы рецидива могут варьироваться даже в каждом конкретном проявлении.
Не существует единого патогномоничного теста, который можно было бы использовать для диагностики РС. Диагноз обычно основывается на истории болезни, клинических проявлениях и подтверждается неврологическим исследованием и МРТ-исследованием головного и спинного мозга. Магнитно-резонансная томография (МРТ) считается стандартом в диагностике РС из-за высокой чувствительности в определении очагов демиелинизации в головном и спинном мозге.
Критерии McDonald 2005 г., 2010 г., 2017 г. основаны на диссеминации очагов в пространстве (ДВП) и во времени (ДВВ), при условии исключения других заболеваний ЦНС, которые имеют сходную радиологическую и клиническую картину с РС.
В 2010 году Международный комитет по диагностике РС (The International Panel on the Diagnosis of MS) пересмотрел критерии McDonald от 2005 года. Конкретизируются критерии ДВП необходимостью наличия очагов в двух из четырех типичных локализаций (субкортикальной, перивентрикулярной, инфратенториальной, спинальной). Подтверждением ДВВ служит одновременное наличие накапливающих и не накапливающих контрастное вещество очагов вне зависимости от времени исследования. Появление новых очагов на Т2-режиме или накапливающих контрастное вещество очагов при повторных исследованиях вне зависимости от времени проведения первого исследования.
В 2017 году состоялся очередной пересмотр критериев McDonald. В целом, критерии McDonald 2017 года представляют собой доработанный и улучшенный вариант согласно требованиям, к диагностике РС. Здесь соблюдаются клинические оценки и практические навыки и знания о болезнях, но с соответствующими уровнями специфичности и чувствительности. Пересмотры в 2017 году повысили роль результатов спинномозговой жидкости наличие или отсутствие специфических олигоклональных полос и повысилась ценность результатов визуализации путем включения кортикальных очагов поражения [17, 18].
Наиболее безопасными препаратами для лечения РС остаются интерферон-в (ИФН-в) и глатирамера ацетат (ГА), хотя их эффективность сильно варьирует у разных пациентов. Новые лекарства более эффективны, однако, чемэффективнее препарат, тем выше вероятность побочных эффектов и развития осложнений.
Цель. изучить клинические характеристики, особенности течения, вопросы диагностики и лечебной помощи больным с РС в Алматы.
Материалы и методы исследования. Клинический с применением расширенной шкалы оценки инвалидизации EDSS (Expanded Disability Status Scale) для объективизации степени выраженности имеющегося неврологического дефицита. Функциональная шкала MSFC (Multiple Sclerosis Functional Composite).
Инструментальные методы исследования. Всем обследуемым проводилась МРТ головного мозга, шейного отдела позвоночника и спинного мозга с введением контраста (результаты исследования, получаемые на МРТ с величиной магнитной индукции 1,5 Тесла и 3.0 Тесла). Критерием включения в группу пациентов с РС был диагноз «достоверный РС» согласно критериям McDonald (2017) и отсутствие других неврологических заболеваний.
В исследование были включены 250 пациентов с рассеянным склерозом, среди которых было 165 женщин и 85 мужчин (Таблица 1). Возраст пациентов с РС составлял от 18 до 64 лет (Рисунок 1).
Всем пациентам с РС проводился неврологический осмотр, сбор анамнеза, забор крови из кубитальной вены. При необходимости, проводились люмбальная пункция и МРТ спинного мозга.
Мы оценивали такие клинические характеристики, как наличие активности заболевания, длительность заболевания, частоту обострений, длительность первой ремиссии, выраженность неврологического дефицита по расширенной шкале инвалидности (EDSS) и выраженность дефицита по отдельным функциональным шкалам, симптоматика, с которой заболевание дебютировало, длительность заболевания до наступления прогредиентного течения и принимавшиеся ранее препараты для лечения РС.
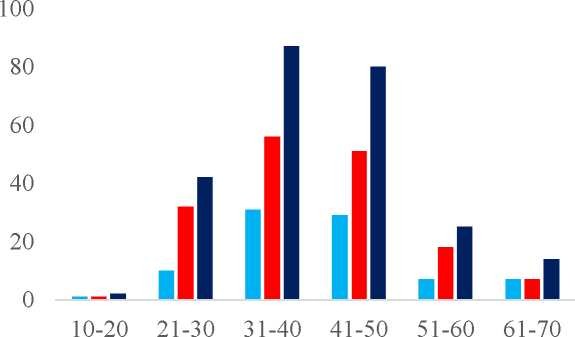
Таблица 1 Общая характеристика пациентов по полу и возрасту
|
Возраст |
10-20 |
21-30 |
31-40 |
41-50 |
51-60 |
61и старше |
|
Мужчины |
1 |
10 |
31 |
29 |
7 |
7 |
|
Женщины |
1 |
32 |
56 |
51 |
18 |
7 |
|
Всего |
2 |
42 |
87 |
80 |
25 |
14 |
■ мужчины ■ женщины ■ всего
Рисунок 1 Половозрастная характеристика больных
Таблица 2 Типы течения рассеянного склероза
|
№ |
Течение РС |
Количество пациентов |
|
1 |
Клинический изолированный синдром |
12 |
|
2 |
Рецидивирующе-ремиттирующее течение |
191 |
|
3 |
Вторично-прогрессирующее течение |
44 |
|
4 |
Первично-прогрессирующее течение |
15 |
Среди всех наблюдаемых пациентов было 76,4% (191) с с первично-прогрессирующим течением. 12 пациентов ремиттирующим течением заболевания, 17,6% (44) находятся под наблюдением с КИС (Рисунок 2).
пациента с вторично-прогрессирующим течением, 6,0% (15)
Течение рассеянного склероза
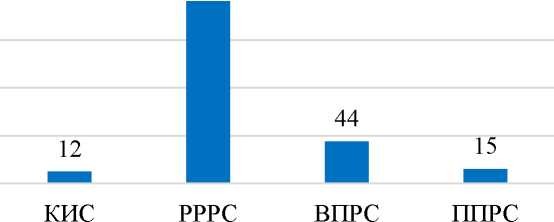
Рисунок 2 - Течение рассеянного склероза
У пациентов с РРРС частота обострений за предшествующие 2 года перед включением в исследование составляла менее 1 за год наблюдалось у 81,6% (156) больных, общее число обострений от 2 до 5 у 18,4% (35) больных.
Длительность первой ремиссии в среднем составила от 2 до 15 лет. Длительность заболевания в среднем составила от 6 до 25 лет. Балл по шкале EDSS - от 1,5 до 3,0 количество больных - 67,01% (128); от 3,0 до 8,0 количество больных - 32,9% (63).
При анализе дебюта неврологических проявлений больных с РРРС у 63 больных (33%) выявлялись признаки преимущественного поражения пирамидной системы, которые клинически характеризовались высокими коленными рефлексами с клонусом коленных чашечек и стоп. Снижение мышечной силы в конечностях и патологическими рефлексами.
Синдром зрительных расстройств был выявлен у 42 больных (22%) (снижением остроты зрения, атрофия зрительного нерва, сужение или выпадение полей зрения). Горизонтальный нистагм крупноамплитудного характера наблюдался у 9 больных (4,7%). Преимущественные чувствительные расстройства наблюдались у 25 больных (13,1%). Пациенты отмечали: парестезии, умеренное снижение болевой, температурной и проприоцептивной чувствительности. Симптомы преимущественного поражения функций мозжечка определялись у 27 больных (14,1%), статическая и локомоторная атаксия была выявлена у 8 больных (4,2%). Поражение спинного мозга выявлялось у 17 больных (8,9%).
У пациентов с прогрессирующим течением РС (59) частота обострений за предшествующие 2 года перед включением в исследование составляла менее 1 за год количество больных у 38,9% (23), общее число обострений от 2 до 5 - количество больных 61,1% (36).
Длительность первой ремиссии в среднем составила от 3-х до 5 лет. Длительность заболевания в среднем составила от 4-х до 28 лет.
Балл по шкале EDSS - от 1,5 до 3,0 больных составил 11,9% (7); от 3,0 до 8,0 у 88,1% (52) больных.
При анализе дебюта неврологических проявлений больных с ППРС преобладали симптомы поражения спинного мозга, которые выявлены почти у 27 больных (45,8%). Нижний спастический парапарез выявлен почти у 18 больных (30,5%). Нарушения функций тазовых органов в дебюте выявлены у 14 исследованных больных (23,7%).
Таблица 3 Данные препаратов и количество пациентов принимающих ПИТРС
Все наши пациенты принимали ПИТРС первой линии, из них интерфероны бета (1-b и 1-a) получают 88,0% больных; глатирамера ацетат получают 12,0% больных (Таблица 3). Учитывая, что пока в стране не зарегистрированы препараты второй линии нет возможности подбора терапии для пациентов в зависимости от степени активности течения болезни, сопутствующих заболеваний.
Заключение. В результате клинического исследования у больных РРРС неврологический статус характеризовался превалированием двигательных расстройств в виде центральных параличей и координаторных нарушений, таких как мозжечковая атаксия, мышечная гипотония, нарушения координации. У этих пациентов с РРРС случались обострения, но при этом между обострениями болезнь не прогрессировала в отличие от прогрессирующих форм. В редких случаях обострение завершалось ухудшением состояния пациента, но в период, когда обострений не было, прогрессирования заболевания не наблюдалось.
Прогрессирующие формы рассеянного склероза включительно вторично-прогрессирующий и первичнопрогрессирующий РС отличались более тяжелым течением, с преобладанием нижнего спастического парапареза. У нескольких больных ПП РС протекает агрессивно с частыми обострениями и с быстрым прогрессированием неврологической симптоматики. Эти пациенты чаще других получают курсы стационарного лечения для купирования обострений и проведения реабилитации. Все пациенты находятся под диспансерным наблюдением в кабинете рассеянного склероза, где проводится комплексная медикаментозная терапия.
|
№ |
Название препарата |
Количество пациентов |
|
1 |
Интерферон бета-П) (Бетаферон) 9,6 млн, через день, п/к. |
67 (26,8%) |
|
2 |
Интерферон бета-'к (Ребиф) 44 мкг, 3 раза в неделю, п/к. |
31 (12,4%) |
|
3 |
Интерферон бета-^ (СинноВекс) 30 мкг, 1 раз в неделю, в/м |
36 (14,4%) |
|
4 |
Глатирамера ацетат (Копаксон) 20 мг, ежедневно, п/к |
30 (12,0%) |
СПИСОК ЛИТЕРАТУРЫ
- World Health Organization. Atlas multiple sclerosis resources in the world 2008. Geneva: WHO Press, 2008. 29 р.
- Compston A, Coles A: Multiple sclerosis // Lancet. 2008. №372. Р. 1502-1517.
- Alonso A, Hernan MA. Temporal trends in the incidence of multiple sclerosis: a systematic review // Neurology. 2008. №71(2). Р. 129-135.
- Koch-Henriksen N, S0rensen PS. The changing demographic pattern of multiple sclerosis epidemiology // Lancet Neurol. 2010. №9. Р. 520-532.
- Orton SM, Herrera BM, Yee IM, et al: Sex ratio of multiple sclerosis in Canada: a longitudinal study // Lancet Neurol. 2006. №5. Р. 932-936
- Ramagopalan SV, Byrnes JK, Orton SM, Dyment DA, Guimond C, Yee IM, Ebers GC, Sadovnick AD. Sex ratio of multiple sclerosis and clinical phenotype // Eur J Neurol. 2010. №17(4). Р. 634-637.
- Trojano M, Lucchese G, Graziano G, Taylor BV, Simpson SJ, Lepore V, Grand'maison F, Duquette P, Izquierdo G, Grammond P. et al. Geographical variations in sex ratio trends over time in multiple sclerosis // PLoS One. 2012. №7(10). Р. 348-358.
- Willer CJ, Dyment DA, Sadovnick AD, Rothwell P.M, Murray CJ, Ebers GC: Timing of birth and risk of multiple sclerosis // BMJ. 2005. №330. Р. 120-128.
- Matsushita T, Yanaba K, Bouaziz JD, Fujimoto M, Tedder TF: Regulatory B cells inhibit EAE initiation in mice while other B cells promote disease progression // J Clin Invest. 2008. №118. Р. 3420-3430.
- Iwata Y, Matsushita T, Horikawa M, et al: Characterization of a rare IL-10-competent B-cell subset in humans that parallels mouse regulatory B10 cells // Blood. 2011. №117. Р. 530541.
- Yoshizaki A, Miyagaki T, DiLillo DJ, et al: Regulatory B cells control T-cell autoimmunity through IL-21-dependent cognate interactions // Nature. 2012. №491. Р. 264-268.
- Lehmann-Horn K, Schleich E, Hertzenberg D, et al: Anti-CD20 B-cell depletion enhances monocyte reactivity in neuroimmunological disorders // J Neuroinflammation. 2011. №8. Р. 146-152.
- Palanichamy A, Apeltsin L, Kuo TC, et al: Immunoglobulin class-switched B cells form an active immune axis between CNS and periphery in multiple sclerosis // Sci Transl Med. 2014. №6. Р. 248-256
- Lublin FD, Reingold SC, Cohen JA, et al. Defining the clinical course of multiple sclerosis: the 2013 revisions // Neurology. 2014. №83. Р. 278-286.
- Giovannoni G, Cook S, Rammohan K, et al. Sustained disease-activity-free status in patients with relapsing-remitting multiple sclerosis treated with cladribine tablets in the CLARITY study: A post-hoc and subgroup analysis // Lancet Neurol. 2011. №10. Р. 329-337.
- Miller DH, Chard DT, Ciccarelli O. Clinically isolated syndromes // Lancet Neurol. 2012. №11. Р. 157-169.
- Thompson, A, Banwell, B, Barkoff, F. Diagnosis of multiple sclerosis: 2017 revisions of the McDonald Criteria // Lancet Neurol. 2018. №17(2). Р. 162-173.
- Filippi, M, Rocca, MA, Ciccarelli, O. MRI criteria for the diagnosis of multiple sclerosis: MAGNIMS consensus guidelines // Lancet Neurol. 2016. №15(3). Р. 292-303.