КонДенсацией 1-метил-пипериДин-4-она c феноксипропаргилом в условиях реакции Фаворского в абсолютном бензоле в присутствии пятикратного избытка порошкообразного технического КОН при соотношении пипериДон-4:феноксипрорпаргил=1:1,5 получен соответствующий 4-(3-феноксипроп-1-ин-1-ил)пипериДин-4-ол. При ацилировании третичного феноксипропинилового пипериДола циклопропан-, циклобутан-, циклопентан-, циклогексанкарбонилхлориДами в Диоксане при комнатной температуре или нагревании образуются соответствующие гиДрохлориДы сложных эфиров. Строение синтезированных соеДинений поДтвержДены Данными спектроскопии ЯМР и ИКС.
По данным Министерства здравоохранения РК, в стране наблюдается рост числа заболеваний, сопровождающихся болевым синдромом (онкологические, сердечно-сосудистые и т.д.), растет число больных аллергией, туберкулезом и другими заболеваниями, связанными с загрязнением окружающей среды, что ведет к увеличению потребности в лекарственных средствах. В связи с этим одним из главных направлений синтетической органической химии остается целенаправленный поиск и создание высокоэффективных и безвредных лекарственных препаратов.
Поиск новых соединений c антимикробным и вирулицидным действием, в том числе обладающих способностью вызывать реверсию лекарственной чувствительности, относится к приоритетному направлению в области разработки новых противоинфекционных препаратов. Актуальность НИР, несмотря на большой ассортимент антибактериальных лекарственных средств, связан, в первую очередь, с высокой приспособляемостью патогенных организмов к ним, включая антибиотики [1].
Рациональным путем поиска эффективных биологически активных соединений (БАС) признано направленное конструирование новых молекул из фармакофорных структурных фрагментов, среди которых лидирующие позиции занимают насыщенные азотистые гетероциклы, являющиеся синтетическими аналогами природных алкалоидов. Разнообразные по строению алкилокси-, арилоксии гетераарилоксипропинилкарбинолы [2-5] зарекомендовали себя как удобные реакционноспособные «строительные» блоки в органическом синтезе в том числе и для БАС.
Текущая ситуация в органической химии отражает дефицит новых структур-лидеров, которые могут быть оптимизированы до терапевтически пригодных лекарств. Научные исследования, направленные на создание новых материалов для практической медицины и сельского хозяйства, являются актуальными и приоритетными во всем мире.
Основанием для проведения настоящих исследований явилась высокая биологическая активность синтезированных ранее сложных эфиров 1-(2-этоксиэтил)4-гидрокси-4-[3-(арилокси)пропин-1-ил]пиперидинов [6], а также пиперидинсодержащих сложных эфиров циклопропанкарбоновой кислоты [7-10].
Цель настоящей работы заключается в направленном синтезе новых феноксипропаргилпиперидинов с потенциальной биологической активностью варьированием природы ацилоксигруппы и введением в молекулы дополнительных фармакофоров, фрагментов малых циклов циклопропан-, циклобутан-, циклопентан-, циклогексанкарбонилов.
Конденсация 1-метил-4-оксопиперидина (1) с феноксипропаргилом в условиях реакции Фаворского [11] приводит к третичному феноксипропаргиловому спирту (2).
O
CH3
Ph
O
»
KOH, benzene
CH3
Ph
3-6
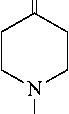
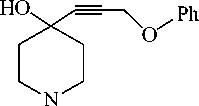
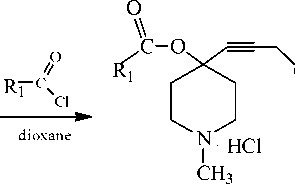
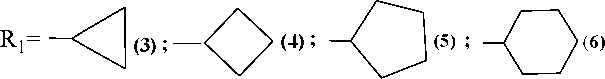
Рисунок 1
Оптимальными параметрами реакции оказались: соотношение пиперидон:фенилоксипропин =1:5, абсолютный бензол, пятикратный избыток технического едкого кали, при которых фенилоксипропинилпиперидол получен с хорошим выходом (таблица1).
Ацилирование феноксипропинилового пиперидола (2) взятыми в избытке циклопропан-, циклобутан-, циклопентан-, циклогексанкарбонилхлоридами проводят при комнатной температуре или нагревании в диоксане. Сложные эфиры циклопропан-, циклобутан-, циклопентан-, циклогексанкарбоновых кислот (3-6) представляют собой кристаллические порошки белого, кремового цвета, хорошо растворимые в воде, этаноле, ацетоне.
Состав и строение синтезированных соединений (2-6) подтверждены данными элементного анализа, ИК спектроскопии, спектроскопии ЯМР 13С, индивидуальность тонкослойной хроматографией (таблица 1).
Таблица 1 Выходы и физико-химические характеристики соединений 2-6
|
Соединени е |
Выход, % |
Rf |
Т.пл., оС |
ИК спектр, см-1 |
Брутто-формула |
|
|
OH |
С=О сл.эф. |
|||||
|
2 |
74,6 |
0,27 |
84-86 |
3414 |
- |
С1$Н^О2 |
|
3 |
66,4 |
0,83 |
181-183 |
- |
1738 |
С19Н24ЫО3СІ |
|
4 |
68,31 |
0,82 |
140-143 |
- |
1735 |
С20Н26ЫО3СІ |
|
5 |
72,1 |
0,91 |
163-165 |
- |
1736 |
С21Н28NОзCІ |
|
6 |
24,6 |
0,83 |
182-184 |
- |
1737 |
С22Нз0NОзCІ |
В ИК спектре пиперидола (2) проявляются полосы поглощения валентных колебаний гидроксильной группы в области 3414 см-1, ароматического кольца 617-774 см-1. Интенсивные полосы поглощения при 1735-1738 см-1, обусловленные колебаниями С=О сложноэфирной группы, свидетельствуют об образовании целевых эфиров 4феноксипропинил пиперидол-4-ов циклопропан-, циклобутан-, циклопентан-, циклогексанкарбоновых кислот (3-6).
В таблице 2 приведены значения химических сдвигов соответственно углеродов, которые полностью подтверждают углеродный состав сложных эфиров 4феноксипропинил пиперидол-4-ов циклопропан-, циклобутан-, циклопентан-, циклогексанкарбоновых кислот (3-6).
В спектрах ЯМР 13С (таблица 2) циклопропан-, циклобутан-, циклопентан-, циклогексан карбонилоксипроизводных (3-6) присутствуют синглетные сигналы атомов углерода сложноэфирного карбонилав области 173,22-174,36 м.д., синглетный сигнал С4 резонирует в области 71,22-80,04 м.д., атом углерода метиленовой группы пропинового фрагмента проявляется в области 56,01-61,02 м.д. Слабопольная область (115-157 м.д.) спектров «населена» сигналами ароматических углеродов. Сигналы при 18,22-29,83 м.д. и 42,35-50,83 м.д. отнесены к углеродам циклопропанового, циклобутанового, циклопентанового, циклогексанового колец. Кроме того, наблюдаются дублетный набор сигналов углеродов C3,5 и C2,6 соответственно при 33,80-36,54 м.д. и 48,69-56,16 м.д. пиперидинового цикла, связанных с замедленной инверсией последнего из-за объемных заместителей при С4.
Таблица 2 Значения химических сдвигов атомов углерода в спектрах ЯМР 13 С эфиров 4-феноксипропинил-пиперидин-4-олов циклопропан-, циклобутан-, циклопентан-, циклогексанкарбоновых кислот (3-6)
|
Соеди нение |
Химические сдвиги (CDCI3), 6, м.д. |
||||||||||
|
Сз,5 |
C2,6 |
C4 |
CH |
CH2 |
C=O |
=С-СН2 |
С,-С= |
O-CH2 |
OPh |
N-CH3 |
|
|
3 |
33,89 |
50,86 |
71,22 |
13,61 циклопропан |
8,99 циклопро пан |
172,62 |
81,80 |
85,97 |
56,06 |
115,5; 115,68;121,8; 129,9; 129,9; 157,7 |
42,24 |
|
4 |
33,83 |
48,69 |
72,35 |
42,35; циклобут ан |
18,22; 25,03 циклобут ан |
173,22 |
81,88 |
86,07 |
56,01 |
115,58; 121,86;129,98; 157,67 |
37,96 |
|
5 |
36,37; 36,54 |
56,03; 56,16 |
78,38 |
50,83 циклопен тан |
25,85; 29,83 циклопен тан |
174,36 |
81,72 |
91,16 |
61,02 |
115,47; 121,72;130,01; 157,89 |
48,85 |
|
6 |
33,15; 33,80 |
50,17; 50,84 |
80,04 |
42,76 циклогек сан |
25,31; 25,77; 28,85 циклогек сан |
174,36 |
70,84 |
81,74 |
56,03 |
115,48; 121,79;129,92; 157,59 |
48,85 |
Соединение (3) под шифром ПИП-36 изучен на противомикробную активность в отношении музейных штаммов микроорганизмов, оценены действия данных препаратов in vitro в отношении Escherichia coli ATCC 25922, Escherichia coli ATCC-BAA-196, Klebsiella pneumoniae ATCC 10031, Klebsiella pneumoniae ATCC 700603, Staphylococcus aureus ATCC 6538-P, Staphylococcus aureus ATCC-BAA-39, Candida albicans ATCC 10231. Модель исследования включает в себя необходимый минимум тестов с различной степенью чувствительности in vitro [12]. Схема исследования проводится в соответствии с действующими на территории Республики Казахстан методическими рекомендациями, утвержденными Государственным Фармакологическим комитетом Республики Казахстан [13].
На основании результато в изучения антимикробной активности показано, что гидрохлорид 1-метил-4-(3феноксипропин-1-ил)-4циклопропанкарбонилоксипиперидина под шифром ПИП-36 обладает антимикробной активностью ко всем семи взятым в эксперимент музейным штаммам микроорганизмов: Escherichia coli ATCC 25922, Klebsiella pneumoniae ATCC 10031, Candida albicans ATCC 10231 в концентрации (МИК 1000 мкг/мл), а в отношении Escherichia coli ATCC-BAA-196, Klebsiella pneumoniae ATCC 700603, Staphylococcus aureus ATCC 6538-P, Staphylococcus aureus ATCC-BAA-39 в концентрации (МИК 2000 мкг/мл) [14,15].
Таким образом направленное введение циклопропанкарбонльного фрагмента в структуру феноксипропинилпиперидина привело к соединениям с противоинфекционной активностью.
СПИСОК ЛИТЕРАТУРЫ
- Antimicrobial resistance surveillance in Europe 2012. Annual Report of the European Antimicrobial Resistance Surveillance Network (EARS-Net). European Centre for Disease Prevention and Control. Stockholm: 2013. 208 р.
- Шостаковский М.Ф., Власов В.М., Кузнецова Т.С., Сафронова Л.А. Новая область применения реакции А.Е. Фаворского // Ж. орган. хим. 1966. №2. С. 953-956.
- Азербаев И.Н., Ержанов К.Б., Садыков Т.С., Мусин М.А., Умарова З.Н. Взаимодействие бутоксипропаргилов с карбонильными соединениями // Изв. АН КазССР. Сер. хим. 1976. №1. С. 30-33.
- Иокубайтите С.П., Коудис З.П., Мозолис В.В. Синтез и свойства ацетиленовых производных на основе феноксипропаргила // Труды АН Лит. ССР. Сер. Б. 1980. №1. С. 116-119.
- Курбанов Ф.К., Кучкаров А.В., Агзамов К.А., Джуракуло в Г. Синтез ацетиленовых спиртов на основе пропаргилового эфира фенолов // Докл. АН Узб. ССР. 1972. №1. С. 38-39.
- Бажыкова К.Б., Пралиев К.Д., Поплавская И.А. Синтез и некоторые превращения 1-(2-этоксиэтил)-4-(3-арилоксипропин-1ил)пиперидинов // Изв. МН-АН РК.Сер. хим. -1998. №3. С. 112-120.
- Козловский В.И., Пралиев К.Д., Гончарук В.В., Заводник Л.Б., Ахметова Г.С., Искакова Т.К., Ю В.К. Анальгетическая активность оригинальных веществ пиперидинового ряда: экспериментальное исследование на модели термического раздражения // Журнал Гродненского медицинского университета. Беларусь. 2014.№3С.38-41.
- Ахметова Г.С., Садырбаева Ф.М., Ю В.К., Пралиев К.Д., Жилкибаев О.Т. Пичхадзе Г.М., Насырова С.Р., Имашова Ш.О., Амиркулова М.К. Пиперидинсодержащие производные циклопропанкарбоновой кислоты потенциальные ФАВ //Хим.журнал Казахстана 2012. №1. С.118-127.
- Садырбаева Ф.М., Оспанова С.И., Исаева У.Б., Ахметова Г.С., Ю В.К, Пралиев К.Д. Амиды циклопропанкарбоновой кислоты потенциальные БАВ // Кластер конференций по органической химии «ОргХим-2013. 17-21 июня 2013. СПб.: Репино, 2013. С. 248-249.
- Kumar K. Ajar. Brief review on cyclopropane analogs: synthesis and their pharmacological applications // Int. J. of Pharm. and Pharmac. Sc. -2012.№5(1) P. 467-472.
- Басымбеков М.Б., Садыков Т.С., Адильбеков С.Т. и др. Синтез замещенных феноксипропинилпиперидолов и влияние заместителей на строение продуктов, полученных в условиях реакции гидратации // Известия АН РК. Сер. Химия. 1992. №4. С. 50-56.
- Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ, Минздрав РФ, «ИИА Ремедиум» М.: 2000. 679 с.
- Доклинические испытания лекарственных средств (Методические рекомендации). Фарм. государственный комитет РК. Алматы: 1997. 22 с.
- Инновац. патент РК № 31047. Гидрохлорид 1-метил-4-(3-феноксипропин-1-ил)-4-циклопропанкарбонилоксипиперидина, обладающий антимикробной активностью/ Пралиев К.Д., Кулманов М.Е., Ильин А.И., Садырбаева Ф.М., Ахметова Г.С., Ю В.К., Исаева У.Б., Леонова Н.В., Сульжик О.А., Касымбекова С.С. Опубл. Бюл. №4 от 15.04.16 г.
- Садырбаева Ф.М., Ахметова Г.С., Ю В.К, Пірәлиев Қ.Ж., Сейлханов Т.М. Циклопропанкарбонқышқылының пиперидин туындылары эфирлерінің микробқа қарсы белсенділігі // Химический журнал Казахстана. 2017. №4С.73-82.