Введение. Повсеместный рост нейроонкологической заболеваемости, нерешенные вопросы лечения, удручающие показатели выживаемости обусловливают актуальность проблем исследования злокачественных глиом головного мозга (ЗГГМ) [1,2+. В Республике Казахстан заболеваемость злокачественными опухолями центральной нервной системы за последние десятилетие возросла на 70,0% с 362 (2,3%000) первично выявленных больных в 2000 г., до 641 (3,9%000) больных в 2011 г. *3,4+. При этом ЗГГМ являются наиболее часто встречающимися первичными опухолями ЦНС. Их частота среди всех опухолей головного мозга достигает 60-70% [5,6,7].
По действующей гистоморфологической классификации (WHO, 2007) выделены 4 формы ЗГГМ: астроцитомы I-II степени злокачественности (Grade I-II), анапластические астроцитомы, олигодендроглиомы, олигоастроцитомы степени злокачественности (Grade III), мультиформная глиобластома степень злокачественности (Grade IV) *8+. Применение данной классификации имеет огромное значение для выбора тактики лечения глиом.
В настоящее время современная стратегия лечения больных ЗГГМ основана на междисциплинарном подходе, который включает хирургическое вмешательство, лучевое, лекарственное и симптоматическое лечение.
Оперативное вмешательство остается ведущим методом лечения ЗГГМ. Нейрохирургическая операция приводит к уменьшению объема опухоли и разрешает проблемы, связанные с масс-эффектом, такие как симптомы внутричерепной гипертензии и неврологический дефицит, т.е. устраняет непосредственные причины угрозы жизни больного. Однако тотальное удаление глиомы затруднено вследствие глубокой микроинвазии опухоли в отделы мозга, где располагаются жизненно важные центры, При этом доля глубиннораспространенных опухолей достигает 65% *9,10+.
Лучевая терапия (ЛТ) по-прежнему остается единственным методом локального контроля роста глиальной опухоли после хирургического вмешательства. Однако ЗГГМ являются радиорезистентными опухолями, что, несомненно, снижает эффективность ЛТ, тем самым, ухудшая показатели выживаемости. Также следует учитывать инфильтративный рост злокачественной глиомы, при котором отсутствует более или менее четкая граница между опухолью и окружающим мозговым веществом.
При этом опухолевые клетки распространяются за пределы видимого на МРТ-, ПЭТ-, КТ-изображениях участка накопления контрастного вещества. Поэтому достаточно трудной задачей остается определение клинического и планируемого объема опухоли (CTV и PTV), что, несомненно, отражается на точности выбора мишени облучения, и тем самым отражается на результатах ЛТ *11,12,13+.
Одним из немногих способов улучшения результатов лечения ЗГГМ является включение в программы терапии цитостатиков. Химиотерапия (ХТ) является наиболее реальным вариантом повышения эффективности лечения ЗГГМ в ближайшей перспективе. Однако при выборе препаратов существенное значение имеет гематоэнцефалический барьер (ГЭБ) как фактор, влияющий на её эффективность, так как питание пограничных с окружающим мозгом участков опухоли осуществляется сосудами, имеющими нормальное для мозга строение *14,15+. При применении ХТ решаются следующие задачи: аддитивность и радиосенсибилизация, т.е. XT должна быть более агрессивна (применяют 2-3 компонентные схемы и более высокие дозы цитостатиков), а при радиосенсибилизации чаще используют меньшие дозы в режиме монохимиотерапии *16,17,18+.
Таким образом, проблема лечения ЗГГМ по-прежнему остается одной из острых в нейроонкологии. Несмотря на комплексный подход в лечении больных с данной патологией, прогноз для этой группы больных остается неблагоприятным. Так медиана общей выживаемости составляет менее одного года для мультиформной глиобластомы и два года для анапластической астроцитомы. Поэтому для этой группы больных Таблица 1 Распределение больных злокачественными глиомами головного мозга в испытуемых группах по возрасту, полу и объему необходим поиск новых терапевтических режимов, которые должны увеличивать частоту непосредственного ответа, выживаемость и качество жизни.
|
Группы |
Средний возраст (годы) |
Пол |
Объём операции |
||
|
Мужчины |
Женщины |
Тотальное удаление |
Субтотальное удаление |
||
|
1-я группа /п=45/ |
33,9±6,8 |
24 (53,3±7,4%) |
21 (46,7±7,4%) |
13 (28,9±6,7%) |
32 (71,1±6,7%) |
|
2-я группа /п=45/ |
35,2±7,1 |
23 (51,1±7,4%) |
22 (48,9±7,4%) |
14 (31,1±6,9%) |
31 (68,9±6,9%) |
|
Итого: /п=90/ |
34,5±6,9 |
47 (52,2±5,2%) |
43 (47,8±5,2%) |
27 (30,0±4,8%) |
63 (70,0±4,8%) |
Цель исследования - повышение эффективности лечения злокачественных глиом головного мозга за счет оптимизации методик послеоперационной химио- и лучевой терапии.
Материал и методы. Контролируемое исследование (01.2005 г. - 12.2011 г.) проведено на 90 больных ЗГГМ (С71 по МКБ-10), проходивших в послеоперационном периоде химио- и лучевое лечение. Мужчин было 47 (52,2%), женщин 43 (47,8%), средний возраст 34,5±6,7 лет. Оперативное лечение в объеме тотального удаления опухоли проведено у 27 (30,0%) больных. У 63 (70,0%) больных произведено субтотальное (частичное) удаление опухоли в пределах анатомической дозволенности. Мультиформная глиобластома (G4) отмечена у 42 (46,6%) больных, анапластическая астроцитома или олигодендроглиома (G3) у 33 (36,7%) больных, и, у 15 (16,7%) пациентов была диагностирована астроцитома (G1-G2) (рисунок 1).
В зависимости от методики лучевой терапии и химиотерапии больные были разделены на две группы: 1-я группа - 45 (50,0%) больных, здесь проведена одновременная конформная лучевая терапия (КФЛТ) и ХТ + 4 курса ХТ; 2-я группа - 45 (50,0%) больных, здесь проведена конвенциальная ЛТ в стандартном режиме + 4 курса ХТ (таблица 1).
КФЛТ проводилась РОД 2,5 Гр 28 фракций до СОД 70 Гр в сочетании с приемом темодала (TZM) 100 мг № 42-45 ежедневно на протяжении всего курса лечения. Первичная симуляция проводилась на рентгеновском симуляторе "Acuity CBCT" с КТ-приставкой или компьютерном томографе. План дозиметрического расчета осуществлялся в объемном 3-D режиме на системе компьютерного планирования "Eclipse 6-7" с выведением зон интереса и критических органов.
Верификация плана облучения реализовывалась вначале на симуляторе с использованием встроенных защитных лепестков, и, далее на линейных ускорителях "Clinac 600 C/D и 2100 C/D" с MLC. Контроль качества КФЛТ проводился с помощью портальной визуализации на системе "Portal vision". Динамическая оценка результатов лечения проводилась с помощью МРТ исследования головного мозга до, в процессе и после лечения.
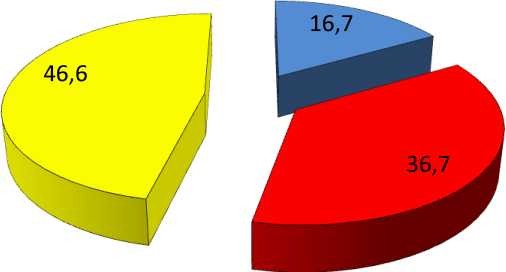
Распределение больных ЗГГМ по степени злокачественности
- G1-G2
- G3
- G4
Рисунок 1 Гистологический тип опухоли в испытуемых подгруппах
Непосредственную эффективность лечения анализировали согласно рекомендациям ВОЗ (1979) *19+, а отдаленные результаты с использованием актуриального моментного методу расчета по Kaplan E.L., Meier P. (1958) [20].
Результаты и обсуждение. В результате проведенной одновременной химиои лучевой терапии по методике конформного облучения были получены следующие результаты. Положительный объективный эффект (ОЭ) в 1-й группе был достигнут у 39 (86,7%) больных, что достоверно превышало на 31,1%, аналогичный показатель контрольной 2-й группы, где данный эффект был отмечен у 25 (55,6%) больных. При этом следует отметить, что количество полных ответов (ПО) на лечение в 1-й группе был выше на 17,8% в сравнении с таким же показателем 2-й группы, составляя 12 (26,7%) и 4 (8,9%) больных соответственно (p<0,05). Показатели частичного ответа (ЧО) были также выше в основной группе на 13,3%, составляя соответственно в 1-й группе 27 (60,0%) больных, а во 2-й группе 21 (46,7%). Следует отметить, что количество больных со стабилизацией процесса после проведенной конвенциальной лучевой терапии составило в контрольной группе 14 (31,1%) больных, в то время как в основной группе, полученный результат, оцененный как без эффекта был всего у 3 (6,7%) пациента. Прогрессирование (ПР) процесса отмечалось у 3 (6,7%) и 6 (13,3%) больных 1-й и 2-й групп (таблица 2).
В результате применения ЛТ у всех больных испытуемых групп отмечалось купирование таких тягостных симптомов, как головные боли, судорожные припадки и эпизоды симптоматической эпилепсии, регресс очаговых симптомов патологической неврологической симптоматики, соответствующей зонам поражения головного мозга, что, несомненно, свидетельствовало о полной или частичной регрессии процесса.
Таблица 2 Непосредственные результаты конформной лучевой терапии в комбинации с химиотерапией лучевой терапии при злокачественных глиомах головного мозга
При этом следует отметить, что исчезновение данных симптомов начиналось отмечаться при СОД 15-20 Гр, у больных получающих одновременное химио- и лучевое лечение, в то время как в контрольной 2-й группе эти явления начинали купироваться только после СОД 35-40 Гр, т.е. ближе к окончанию курса облучения. Это можно объяснить одновременным противоопухолевым воздействием химиотерапии и лучевой терапии.
Сравнительный анализ динамики общего состояния по шкале Карновского показал, что улучшение общего состояния или "качество жизни" после ЛТ наступило у большинства больных в обеих группах. Однако наибольшее количество больных отмечен в 1-й группе до 80 % у 27 (60,0%), до 90% у 18 (40,0%), в то время как во 2-й группе данные показатели были достигнуты у 18 (40,0%) и 9 (20,0%) больных соответственно (таблица 3).
|
Непосредственная эффективность |
Группы |
Вероятность ошибки р* |
|
|
1-я группа /п=45/ |
2-я группа /п=45/ |
||
|
ОЭ |
39 (86,7±5,0 ) |
25 (55,6±7,4 ) |
р<0,05 |
|
ПО |
12 (26,7±6,5 ) |
4 (8,9±4,2 ) |
р<0,05 |
|
ЧО |
27 (60,0±7,3 ) |
21 (46,7±7,4 ) |
р>0,05 |
|
БЭ |
3 (6,7±3,7 ) |
14 (31,1±6,9 ) |
р<0,05 |
|
ПР |
3 (6,7±3,7 ) |
6 (13,3±5,0 ) |
р>0,05 |
|
Примечание *р вероятность ошибки между 1-й и 2-й группами соответственно. |
|||
Таблица 3 Динамика показателей общего состояния по шкале Карновского до и после лучевой терапии у больных злокачественными глиомами головного мозга
|
Степень активности по шкале Карновского |
1-я группа /п=15/ |
2-я группа /п=15/ |
||
|
до ЛТ |
после ЛТ |
до ЛТ |
после ЛТ |
|
|
50% |
9 (20,0%) |
- |
9 (20,0%) |
- |
|
60% |
15 (33,3%) |
- |
12 (26,7%) |
3 (6,7%) |
|
70% |
18 (40,0%) |
- |
18 (40,0%) |
15 (33,3%) |
|
80% |
3 (6,7%) |
27 (60,0%) |
6 (13,3%) |
18 (40,0%) |
|
90% |
- |
18 (40,0%) |
- |
9 (20,0%) |
|
Примечания 90% способен продолжать нормальную активную жизнь; 80% умеренное снижение общей активности, имеются некоторые признаки заболевания; 70% общая активность значительная снижена, сам себя обслуживает, работать не может; 60% требует периодической помощи, сам себя обслуживать не может; 50% нуждается в значительной помощи и частом медицинском обслуживании. |
||||
Это объясняется, прежде всего, более высокими достигнутыми непосредственными результатами химиолучевой терапии с купированием основных клинических симптомов.
Следует отметить практически полное отсутствие общих лучевых реакций в испытуемых группах. Их проявления выражались в периодически проявляющемся гипертензионном синдромом, которые купировали дегидратационной терапией. Также нами не отмечено местных лучевых реакций со стороны кожных покровов, попадающих в зону облучения (эритема, сухой эпидермит).
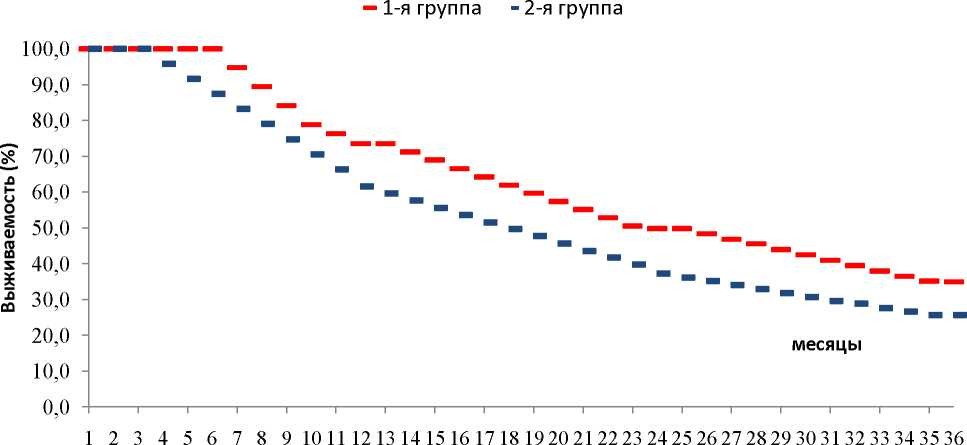
Проведенный анализ показал, что наблюдаемая общая 36-месячная выживаемость, рассчитанная одномоментным методом по Kaplan-Meier составила в 1-й группе 34,9±3,1%, что достоверно превышало аналогичные показатели 2-й группы на 9,2%, где они составили 25,7±2,1%, соответственно (p<0,05) (рисунок 2). Как видно из рисунка 2, одногодичная выживаемость составила 73,5±2,3% в 1-й группе и 61,6±2,1% во 2-й группе при статически значимой разнице в 11,9% (p<0,05). Показатели двухлетней выживаемости в 1-й группе также достоверно превышали на 12,6 % аналогичные показатели 2-й группы (p<0,05), составляя 49,8% и 37,2% соответственно.
Медиана общей наблюдаемой 3-летней выживаемости составила в 1-й и2-й группах 23,5±2,7 и 17,2±2,9 месяцев соответственно, при статически значимой разнице в 6,3 месяца (p<0,05).
Общая выживаемость по Kaplan-Meier у больных ЗГГМ
Рисунок 2 Общая наблюдаемая 3-х летняя выживаемость больных ЗГГМ в испытуемых группах
Заключение. КФЛТ в комбинации с ХТ обладает значительным преимуществом перед стандартной конвенциальной ЛТ, что отразилось на более высокой непосредственной эффективности, а также на ближайших результатов лечения. Следует также учесть, что радиобиологическое обоснование данных режимов, а также совершенствование цикла предлучевой подготовки, не только помогло повысить непосредственную эффективность лучевого лечения, но и максимально снизить побочные токсические проявления.
СПИСОК ЛИТЕРАТУРЫ
- American Cancer Society: Cancer Facts and Figures 2009.
- Parking D.M., Bray F., Pisani F., Pisani P. Global cancer statistics, 2005 //CA Cancer J. Clin. 2009. V. 59, № 2. P. 74 108.
- Абдрахманов Ж.Н., Позднякова А.П., Филиппенко В.И. Показатели онкологической службы Республики Казахстан за 1999 год (статистические материалы). Алматы, 2012. 108 с.
- Нургазиев К.Ш., Сейтказина Г.Д., Байпеисов Д.М. и др. Показатели онкологической службы Республики Казахстан за 2011 год (статистические материалы). Алматы, 2000. 78 с.
- Levin VA, Gutin PH, Leibel S. et. al Neoplasms of the central nervous system //Cancer Principles and Practice of Oncology, 4th Ed. Philadelphia, JB Lippin cott, 1992.
- Зозуля Ю. А., Пацко Я. В., Никифорова А. Н. //Вопр. Нейрохир. 1998. № 3. С. 50-54.
- Тиглиев Г.С., Олюшин В.Е. Злокачественные глиомы головного мозга. Проблемы диагностики и современные возможности комплексного лечения. Темодал новый противоопухолевый препарат для лечения злокачественных глиом // Мат. симп. СПб., 2002. С. 2-5.
- Louis D.N., Ohgaki H., Wiestler O.D., Cavenee W.K. WHO Classification of Tumours of the Central Nervous System.Lyon, 2007. 25 p.
- Олюшин В.Е. Глиальные опухоли головного мозга: краткий обзор литературы и протокол лечения больных // Нейрохирургия. 2005. № 4.-С.41 -47.
- Балканов А.С. Первые результаты лучевой терапии в режиме гиперфракционирования в сочетании с ломустином при глиомах III-IV степени злокачественности // Российский онкологический журнал. 2002. № 6. С. 24-26.
- Brada Michael, Sharpe Geoffrey, Rajan Balakrishman, Britton Juliet, Wilkins Peter R., Guerrero Douglas, Hines Frances. Traish Daphne, Ashley Susan. Modifying radical radiotherapy in high grade gliomas; shortening the treatment time trough acceleration //Int. J. Radiat., Oncol. Biol., Phys. 1999. Vol.43, № 2. С. 287-292.
- Ducci F., Fabrini M. G., Lutzemberg L., Cartei F., Silvano G., Laddaga M. Supratentorial malignant gliomas: results in 280 cases treated by post-operativ radiotherapy //Cancer J. 1995. Vol. 6, № 3. С. 163-170.
- Carlos A. Perez, Cuther W. Brady Principles and Practice of Radiation Oncology. 5-rd Edition, Lippincott-Roven, 2010. 2605 р.
- Кобяков Г.Л. Химиотерапия в лечении злокачественных внутримозговых опухолей //Современная онкология. 2002.Т.4, №1. С.1-10.
- Карахан В.Б. с соавт. Темодал в комплексном лечении глиобластом головного мозга //Матер. V съезда онкологов и радиологов СНГ. Ташкент, 2008.С. 430.
- Поддубная И.В. Новый век новые возможности химиотерапии: темодал в лечении злокачественных опухолей //Совр. онкология. 2002.Т. 4, №1.С. 1-10.
- Ruggiero A. Phase I stady of temozolomide combined with oral etoposide in children with recurrent of progressive medulloblastoma // EJC, Joint ECCO 15-34 ESMO Multidisciplinary congress, 2009.-Р.4103.
- Нечитайло М.Н., Иванов С.М., Желудкова В.М. Химиолучевая терапия злокачественных глиом // Мат. V съезда онкологов и радиологов СНГ.Ташкент, 2008.-С.434
- WHO Handbook for Reporting Results of cancer Treatment.WHO, Geneva, 1979.
- Kaplan E.L., Meier P. Nonparametric estimation from incomplete observations //J. Amer. Stat. Assoc. 1958.Vol. 53.P. 457481.