В данной статье представлен клинический случай доказывающий, что, если программный гемодиализ и постоянный амбулаторный перитонеальный диализ являются методами заместительной почечной терапии, то трансплантация почки это высокоэффективный метод лечения терминальной хронической почечной недостаточности и средство спасения жизни пациента. Перспективы развития заместительной почечной терапии и ее внедрение в клиническую практику зависят от улучшения всех этапов проведения трансплантации почки от законодательной базы До грамотного веДения пациента до и после операции.
Хроническая болезнь почек (ХБП) персистирующее нарушение функции почек, приводящее к повышению концентрации креатинина в сыворотке крови более 3-х месяцев, снижению скорости клубочковой фильтрации (СКФ) менее 60 мл в минуту. Прогрессирование почечной недостаточности приводит к необходимости начала заместительной почечной терапии (ЗПТ): диализу и трансплантации почки [1].
Ежегодно количество больных, требующие такой тактики терапии увеличивается на 1012%. Это связано, во-первых, с увеличением числа пациентов с патологией почек, во-вторых с распространенностью заболеваний, которые затрагивают почки и приводят к формированию ХБП, таких как системные заболевания, артериальная гипертензия, подагра, амилоидоз, мочекаменная болезнь, эндокринные заболевания, в частности, сахарный диабет [2]. ХБП, чаще встречается среди мужского населения, чем женского, такое гендерное неравенство распространяется и на терминальную почечную недостаточность (ТПН).
ХБП развивается у более 100 000 человек в год в Соединенных Штатах [3]. Количество больных с ХБП, прибегающие к различным видам заместительной почечной терапии (ЗПТ), колеблется в разных странах: от 90 человек на 1 млн. населения в Финляндии, до 410 человек на 1 млн. населения в Тайване. В Российской Федерации ежегодно поступает на ЗПТ около 110 человек на 1 млн. населения. Во многих странах СНГ обеспеченность ЗПТ находится на уровне 700-1000 больных на 1 млн. населения [4,5] .
Перспективным путем решения данной проблемы является трансплантация почки (ТП). За счёт своей физиологичности ТП является одним из самых эффективных, комплексных и единственным радикальным способом восстановления утраченной функции почек. ТП обеспечивает качество и продолжительность жизни пациентов.
В наше время выполняется более 30 тыс. ТП в год [3,6,7]. ТП во многих странах таких, как Норвегия, Швеция, Нидерланды, Финляндия, Испания, является основным видом ЗПТ больным с ХБП [3]. В настоящее время активно развивается ТП как от трупного донора, так и от живого родственного донора. По статистике доля таких операций от живого донора в России примерно 10%, на Кипре около 60, в США около 37% [8, 9].
Выживаемость пациентов, в течение последних 5 лет составляет более 90%, а приживаемость трансплантированной почки составляет более 80% [10-15].
Описание клинического случая.
Больная Н., женского пола, 16 лет с диагнозом хроническая почечная недостаточность терминальной стадии, хроническая болезнь почек 5 стадии (по K\DOQI), врожденный пузырно-мочеточниковый рефлюкс (ПМР) с обеих сторон. Осложнения: симптоматическая Артериальная гипертензия 2 степени, стабильная форма, Вторичная кардиопатия, СН ФК 3 степени. Неренальные состояния (НРС): Синусовая тахикардия, Ренальная анемия, скорригированая эритропоэтином,
Дисциркуляторная энцефалопатия, Цереброастенический синдром, адинамическая болезнь кости, в 2014 году была выполнена гетеротопическая трансплантация левой родственной почки в правую подвздошную область.
Анамнез заболевания. Больная Н., женского пола, 1998 г.р. В 2004 г, в возрасте 4-х лет, впервые был выявлен пузырномочеточниковый рефлюкс (ПМР), по поводу чего была проведена антирефлюксная пластическая операция с двух сторон. Катамнестическое наблюдение пациентки в динамике выявило прогрессирование хронической болезни почек.
С апреля 2009 г. года пациентка находилась на заместительной почечной терапии (ЗПТ), получала программный гемодиализ (ГД). Гемодиализу сопутствовала неконтролируемая агрессивная АГ 2 степени, по поводу которой пациентка получала лечение. В связи с этим в августе 2010 г. пациентка переведена на перитонеальный диализ (ПД). В апреле 2013 г. в связи с развитием кандидозной инфекции мочеиспускательного канала, резистентной к антимикотической терапии, было произведено удаление ПД-катетера. С 24 мая 2013 г. по 24 июня 2013 г. начала получать ГД через центральный венозный катетер (ЦВК). После этого в июле 2013 была проведена повторная имплантация ПД-катетера. В декабре 2013г. у пациентки развился диализный перитонит, и было получено лечение цефазолин и цефтриаксон в течение 21 дня, которое дало положительный эффект.
В январе 2014 г. на фоне mensis у пациентки отмечалось интенсивное окрашивание диализата в красный цвет, через 3 дня в динамке присоединился абдоминальный, болевой синдром, рвота, субфебрильная гипертермия, диализат мутный. После повторной антибиотикотерапии (цефазолин, цефтриаксон) положительного эффект не отмечено. В связи с клиникой разлитого резистентного перитонита, было произведено удаление ПД-катетера. В феврале 2014 г. была проведена лапароскопия, ревизия брюшной полости. После интраоперационной находки, конверсия, лапаротомия, холецистэктомия, дренирование брюшной полости. Диагноз после операции: калькулезный холецистит, водянка желчного пузыря, острый сепсис, септикопиемическая форма энтеробактерной этиологии, ДВС, I стадия, анемия тяжелой степени.
Начато лечение: цефепим 250мг/1л в ДР №4, цефепим 800мг/сут в/в 10 дней, флунол 150мг/сут, ревотаз 24 дня, метронидазол 10 дней, тиментин 10 дней.
Через 2 недели после проведенной операции у пациентки произошло профузное желудочнокишечное кровотечение (ЖКК). При обследовании на ФГДС обнаружены острые язвы желудка и ДПК на фоне анемизированной слизистой. Проведено противоязвенное лечение: де-нол+квамател в/в, затем нексиум. В марте 2014 г. при профилактическом осмотре был выявлен неревматический приобретенный инфекционный кардит с поражением аортального и митрального клапанов (вальвулит), подострое течение, СН ФК III. Симптоматическая артериальная гипертензия III ст., стабильная форма, синдром кардиалгии ишемического генеза. Получено лечение ципрофлоксацин 150мг/сут №30.
В июне 2014 г. поступила с жалобами на длительную лихорадку до высоких цифр. При обследовании СРБ 220мг/л. При исследовании крови на стерильность был высеян St. Aureus с чувствительностью к: оксациллину, ципрофлаксацину, доксациклину, гентамицину, линезолиду, тетрациклину, клиндомицину, ванкомицину, триметоприму. В лечении был назначен цефтазидим.
С учетом тяжести состояния пациентки вызванной ХПН: ренальная анемия (Hb 107 г/л), рекормон 4000МЕ/нед. Вторичная кардиомиопатия, СНФК 3 ст. Вторичная артериальная гипертензия (на терапии вальсакор 160мг/сут, бисопролол 2,5мг/сут, альдорон 50мг/сут АД 120/80 мм.рт.ст.) Адинамическая болезнь кости (фосфор 1,54, Ca/^24) 2,65/1,45, ПТГ88пг/мл. Отставание в физическом развитии, возраст 15 лет, рост 139 см, вес 32кг, S (1,1м2) ниже 5 перцентиля. Пациентке была рекомендована трансплантация почки.
Донорскую почку предоставил родственник пациентки. Исследование на гистологическую совместимость по HLA типированию несоответствие по 4 (А-2, В-2, DRB1-0, DRB-0), 3 совпадения из 7, что подтвердило допустимость пересадки почки. Кросс-матч отрицательно.
2 июля 2014 года 12:10-15:50 была проведена гетеротопическая трансплантация левой родственной почки, с учетом анатомических особенностей в правую подвздошную область, так же было проведено стентирование мочеточника. В день операции и на 4 день после нее, пациентке была проведена индукция Симулектом по 10мг. Девочка находилась в детском реанимационном отделении с 02.07.07.07.2014, затем была переведена в отделение уронефрологии для дальнейшего динамического наблюдения.
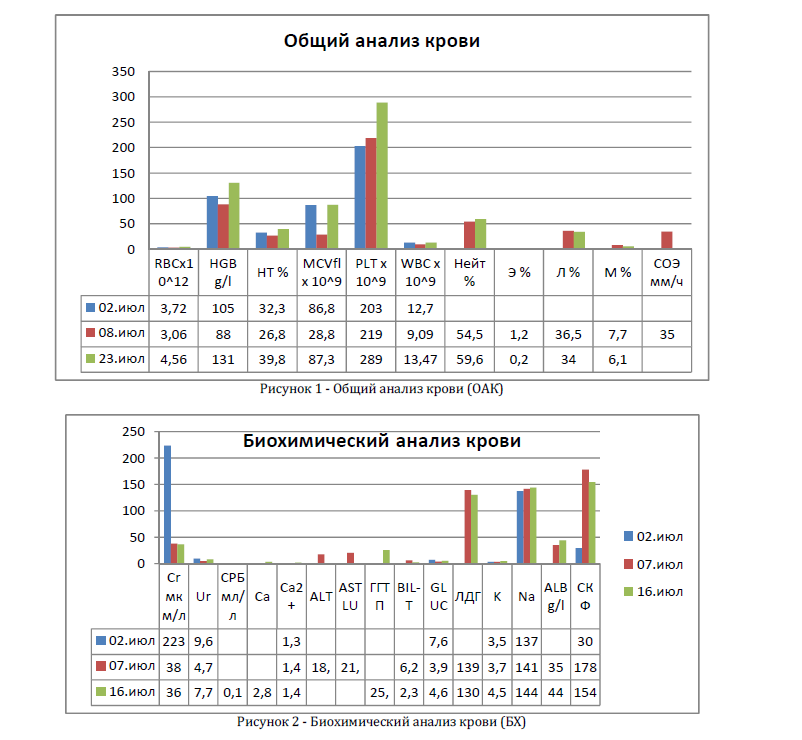
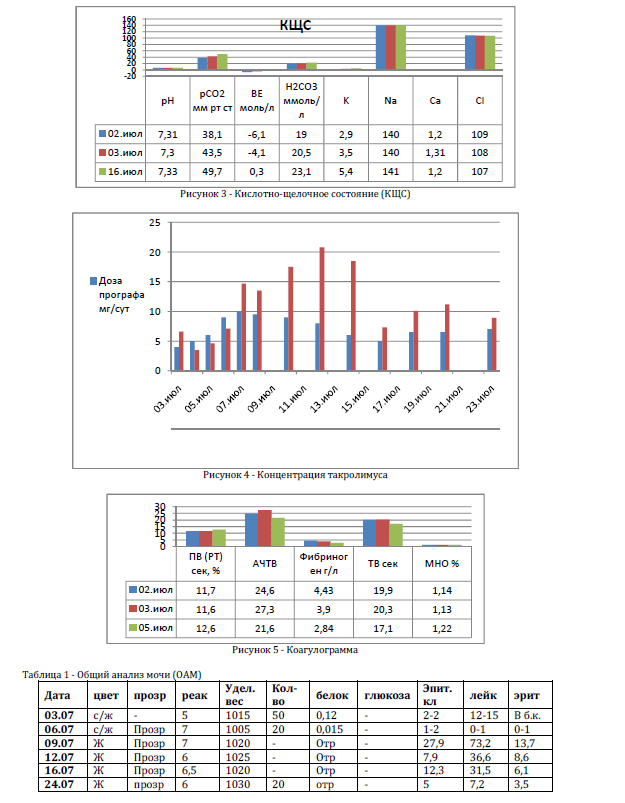
Результаты лабораторных обследований в динамике.
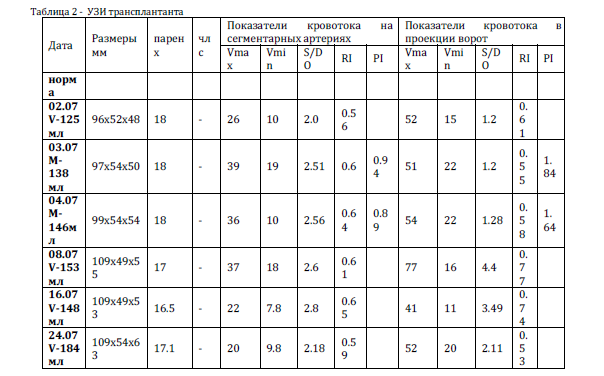
На УЗИ от 24.07.2014 не выявлено структурных изменений почечного трансплантата, кровоток удовлетворительный, наблюдается
незначительное количество жидкости у нижнего и верхнего полюсов трансплантата (объем 15 мл ).
Пациентка было проконсультирована кардиологом, подтверждены ранее диагностированные заболевания:
симптоматическая артериальная гипертензия 2 степени, стабильная форма, вторичная кардиопатия, СН ФК 3 степени. Неренальные состояния: синусовая тахикардия.
В послеоперационном периоде одной из основных проблем, которая развилась у пациентки, являлась артериальная гипертензия. По этому поводу больная Н. получила комбинированную гипотензивную терапию: бисопролол 2,5 мг/сут, зоксон 2мг/сут (амлодипин тахикардия). С 10 июля у пациентки отмечается стабилизация АД, на фоне терапии бисопрололом отмечалась брадикардия 55 в мин, поэтому доза была уменьшена до 1,25 мг/сут.
Клинический диагноз.
Основное заболевание. Хроническая почечная недостаточность терминальная стадия. Хроническая болезнь почек 5 стадия (по K\DOQI). Трансплантация почки от живого донора (02.07.2014).
Конкурирующее заболевание. Врожденный пузырно-мочеточниковый рефлюкс с обеих сторон. Состояние после антирефлюксной операции (2004г). Рефлюкс-нефропатия. Программный гемодиализ (04.2009-09.2010, 24.04.13-24.06.13, с 17.01.14). Перитонельный диализ (19.08.10-24.05.13г, 24.06.13-17.01.14). Осложнения основного заболевания. Симптоматическая артериальная гипертензия 2 степени, стабильная форма. Вторичная кардиопатия, СН ФК 3 степени. НРС: синусовая тахикардия. Ренальная анемия, скорригированная эритропоэтином.
Дисциркуляторная энцефалопатия, цереброастенический синдром. Адинамическая болезнь кости.
Проведенное лечение
В отделении было проведено следующее лечение:
- Поддерживающая иммуносупрессивная терапия (возраст 15 лет, вес 32 кг, рост 139см, площадь тела 1,1м2) :
- Програф коррекция дозы по концентрации препарата в крови 9.5 => 5.5 мг/сут => 7.0 мг/сут
- Селл Септ 750 мг/сут с 02.07.2014 (681мг/м2/ сут), 7:00 250 мг, 15:00 250мг, 23:00-250мг.
• Метипред 500 мг (02.07 в/в) => 250мг/сут (03.07 в/в) =>125 мг/сут (04.07 в/в) => с 3 дня Преднизолон (40мг/м2/сут) 44мг/сут или метилпреднизолон 36мг/сут с 05.07.2014 =>34мг/сут с 11.07.2014 => 32 мг/сут с 14.02.2014 =>30мг/сут с 17.07.2014 => 28мг/сут (30мг/м2/сут) с 20.07.2014
- Антибактериальная терапия: Фортум 1000мг 2 раза в день в/в с 02.07-08.07.2014г, заменен на меронем с 08.07-17.07.2014 в/в (в связи с нарастанием СРБ в динамике)
- Противогрибковая терапия: флуконазол 150мг/48час per os c 06.07-13.07.2014
- Профилактика инфекций: вальцит 0,45г/сут, ко-тримоксазол 360мг/сут, нистатин 250 000х3 раза в день с 03.07.2014.
- Профилактика тромботических осложнений: клексан 0,15 мл подкожно 14 дней, отменен с 17.07.2014, тромбо АСС 37,5мг/сут с 17.0722.07.2014
- Антисекреторная терапия: квамател
40мг/сут с 02.07-05.07.2014, омез 40мг/сут с 05.07.2014 г
- Гипотензивная терапия: бисопролол
2,5мг/сут => 1,25мг/сут с 18.07.2014, зоксон 2мг/сут => 1мг/сут с 23.07.2014
На 7 сутки после операции были удалены страховочный дренаж, уретральный катетер. По прошествии 23-х дней после операции под наркозом было произведено удаление мочеточникового стента, послеоперационный период проходил без осложнений.
Таким образом, на 23-ый день после пересадки донорской почки почечные функции полностью восстановились, диурез 1,5-2,0л/сут, нормализовались азотистые шлаки, на фоне комбинированной гипотензивной терапии АД достигло стабильных показателей 110/70 мм. рт.ст.
Рекомендации, данные при выписке на амбулаторное лечение:
- Диета с ограничением жирной, жареной, острой пищи, адекватный питьевой режим.
- Диспансерное наблюдение у нефролога, кардиолога, педиатра по месту жительства.
- Осмотр нефролога 1раз/месяц, ОАК, ОАМ 2 раза в месяц, биохимический анализ крови 1 раз в месяц.
- Определение базовой концентрации Такролимуса в крови (до приема препарата 9:00) 1 раз 15 дней.
- Определение ПТГ, ПЦР на ЦМВ, ВЭБ 1 раз/месяц. ИФА на ЦМВИ, ВПГ IgG, IgM 1 раз в месяц.
- Прививки противопоказаны (кроме вакцины от гриппа и только через 6 месяцев). Контроль АД и ЧСС 2-3 раза в день, учет выпитой, выделенной жидкости, измерение веса. Согласно перечню медицинских показаний имеет право на получение социального пособия и оформление инвалидности пожизненно.
- Селл септ 750мг/сут: 7:00 1 капсула, 15:00 1 капсула,23:00 1 капсула через рот, постоянно (при развитии лейкопении показано уменьшение дозы препарата)
- Програф 7,0 мг/сут: 2 раза по 3,5 мг
- ГКС: Метилпреднизолон 28мг/сут: 10:00 7 таблеток, через рот, ежедневно 25-30 июля Метилпреднизолон 26мг/сут: 10:00 6 таблеток +1/2 таблетки , через рот, 31 июля,1 августа Метилпреднизолон 24мг/сут: 10:00 6 таблеток, через рот, 2,3августа
Метилпреднизолон 22мг/сут: 10:00 5
таблеток+1/2 таблетки , через рот, 4,5 августа Метилпреднизолон 20мг/сут: 10:00 5 таблеток, через рот,6-7августа
Метилпреднизолон 18мг/сут: 10:00 4
таблеток+1/2 таблетки , через рот, 8-13августа Метилпреднизолон 16мг/сут: 10:00 4 таблеток, через рот, 14-15 августа
Метилпреднизолон 14мг/сут: 10:00 3
таблеток+1/2 таблетки , через рот, 16-17 августа
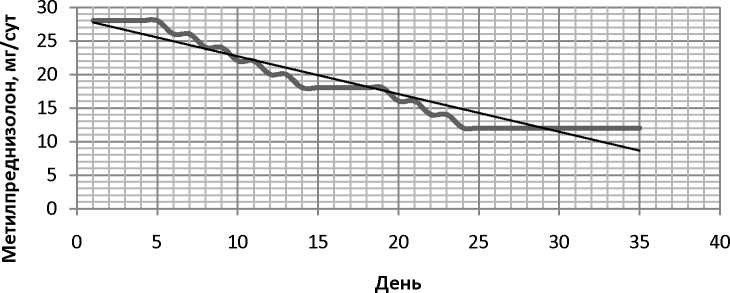
Метилпреднизолон 12мг/сут: 10:00 3 таблеток, через рот, 18-31 августа
Рисунок 6 Доза метилпреднизолона (мг/сут)
- Вальцит 0,45г/сут, 12:00 1 таблетка через рот, ежедневно до 9 октября 2014
- Бисептол 360мг/сут: 22:00 360 (2/3 таблетки), через рот, ежедневно до 9 октября 2014
- Фунгостатин 7:00,15:00,23:00 по 2,5 мл полоскание полости рта до 30 июля 2014
- Гипотензивная терапия:
Бисопролол 1,25мг/сут , 13:00 1,25мг ежедневно через рот, под контролем АД
Зоксон 1мг/сут, 22:00 1 мг через рот ежедневно постоянно через рот под контролем артериального давления
- Омез 40мг/сут,7:00, 22:00 по 1 капсуле 2 раза через рот ежедневно через рот
- Кровь на ВИЧ, вирусные гепатиты В,С 2 января 2015 года
- Наблюдение нефролога и кардиолога по месту жительства.
Заключение.
Данный клинический случай доказывает: если программный гемодиализ и постоянный амбулаторный перитонеальный диализ являются лишь методами ЗПТ, то ТП в наши дни это не только самый высокоэффективный метод лечения ТХПН, но и средство спасения жизни. При данном методе ЗПТ достигается модель гомеостаза, максимально приближена к функции здоровых почек.
Фосфорно-кальциевый обмен приходит в норму, уменьшается риск возникновения таких осложнений, как вторичный гиперпаратиреоз и почечная остеодистрофия. Восстанавливается секреция эритропоэтина , что способствует нормализации концентрации Hb, а также является прогностическим параметром для удовлетворительной функциональсти РТ.
После ТП обеспечивается эффективная реабилитация функции органа, организма, социально-трудовая адаптация. Повышается качественный уровень жизни больных. На данный момент ТП единственный радикальный метод лечения ТХПН [2, 13-15].
Перспективность развития ЗПТ и его внедрение в клиническую практику зависят от улучшения всех этапов проведения ТП от законодательной базы до грамотного ведения пациента до и после операции.
СПИСОК ЛИТЕРАТУРЫ
- Chertow GM, Burdick E, Honour M, Bonventre JV, Bates DW. Acute kidney injury, mortality, length of stay, and costs in hospitalized patients // J. Am. Soc. Nephrol. 2005. №16(11). Р. 3365-3370.
- Calderon-Margalit R, Golan E, Twig G, Leiba A, Tzur D, Afek A, Skorecki K, Vivante A. History of Childhood Kidney Disease and Risk of Adult End-Stage Renal Disease // N. Engl. J. Med. 2018. №378(5). Р. 428-438.
- Correa A, Patel A, Chauhan K, Shah H, Saha A, Dave M, Poojary P, Mishra A, Annapureddy N, Dalal S, Konstantinidis I, Nimma R, Agarwal SK, Chan L, Nadkarni G, Pinney S. National Trends and Outcomes in Dialysis-Requiring Acute Kidney Injury in Heart Failure: 2002-2013 // J. Card. Fail. 2018. №24(7). Р. 442-450.
- Хазов М.В., Романов С.В. Трансплантация почки в ФГУ «ПОМЦ Росздрава»: опыт и перспективы развития: Мат. II Междунар. конф. «Высокие технологии в медицине» // Мед. альманах. М.: 2008. С. 45-48.
- Knoll G. Trends in kidney transplantation over the past decade // Drugs. 2008. Vol. 68, suppl. 1. P. 3-10.
- Got'e SV, Khomyakov SM. Assessment of requirement of the population in the organ transplantation, the donor resource and planning of the effective network of the medical organizations (the centers of transplantation) // Vestnik transplantologii i iskusstvennykh organov. 2013. №15(3). Р. 45-57.
- Томилина Н.А., Бикбов Б.Т., Ким И.Г. и др. Сравнительный анализ эффективности разных видов заместительной почечной терапии в аспекте отдаленных результатов // Нефрология и диализ. 2009. Т. 11., №1. С. 12-18.
- Готье С.В., Мойсюк Я.Г., Хомяков С.М. и др. Развитие органного донорства и трансплантации в Российской Федерации в 2006-2010 гг. III сообщение регистра Российского трансплантологического общества // Вестн. трансплантол. искусств. органов. 2011. № 2. С. 6-20.
- Минина М.Г. О некоторых аспектах организации органного донорства // Вестн. трансплантол. искусств. органов. 2010. №3. С. 81-88.
- Grassmann S., Apelt J., Ligneau X. et al. Search for histamine H(3) receptor ligands with combined inhibitory potency at histamine N-methyltransferase: omega-piperidinoalkanamine derivatives // Arch. Pharm. 2004. Vol. 337(10). P. 533-545.
- Tsukamoto Y., Kajii T.S., Oonishi Y. et al. Growth and development of the cranial base in mice that spontaneously develop anterior transverse crossbite // Am J Orthod Dentofacial Orthop. 2008. Vol. 134(5). P. 676-683.
- Платонов B.C., Азаренкова О.В., Шаршаткин А.В. и др. Результаты трансплантации почки в зависимости от источника получения донорского органа / / Вестн. трансплантол. искусств. органов. 2009. №5. С. 48-56.
- Шамаева Е.Н., Шестакова М.В., Ким И.Г. и др. Трансплантация почки оптимальное лечение больных сахарным диабетом 1-го типа с терминальной хронической почечной недостаточностью // Тер. арх. 2007. № 6. С. 146-158.
- Muehrer R.J., Keller M.L., Powwattana A. et al. Sexuality among women recipients of a pancreas/kidney transplant // West J Nurs Res. 2006. Vol. 28. P. 137-150.