В статье представлено подробное описание таких инструментальных методов диагностики атеросклероза на субклинической стадии, как ультразвуковое исследование сосудов (дуплексное сканирование), компьютерная сфигмография, мультиспиральная компьютерная томография, магнитнорезонансная ангиография. Приведены возможности и ограничения каждого метода. Приоритетное значение при этом отдается дуплексному сканированию сонных артерий с обнаружением атеросклеротических бляшек. В конце статьи предложен, разработанный самими авторами, алгоритм диагностики субклинического атеросклероза.
В настоящее время среди всех возможных методов инструментальной и лабораторной оценки субклинических проявлений атеросклероза различных сосудистых бассейнов, особенно у лиц с суммарным риском 5-9 % по шкале SCORE, в стандарт обследования с позиций оценки уровня риска вошли три основных параметра [1, 2, 3]:
- . Признаки субклинического поражения сонных артерий (утолщение комплекса интима-медиа и наличие атеросклеротических бляшек);
- . Признаки поражения сосудов нижних конечностей (снижение лодыжечно-плечевого индекса -ЛПИ);
- . Скорость распространения пульсовой волны (СПВ), как интегральный показатель повышения сосудистой жесткости.
Все эти параметры являются независимыми прогностическими факторами и могут выступать в качестве суррогатной точки в процессе лечения сердечно-сосудистых заболеваний (ССЗ) и профилактики осложнений. В литературе обсуждается место дисфункции эндотелия в качестве ФР [4, 5]. Данный фактор не вошел пока еще в стандарты стратификации риска, но очевидно будет использоваться в качестве маркера сосудистого повреждения в ближайшем будущем.
Дуплексное сканирование брахиоцефальных сосудов. Поражение сосудов при атеросклерозе включает в себя ремоделирование стенки крупных артерий в виде утолщения комплекса «интима-медиа» (ТИМ), увеличение диаметра, наличие и прогрессирование атеросклеротических бляшек (АСБ), дисфункцию эндотелия и снижение эластических свойств артериальной стенки. Основным методом выявления этих изменений является ультразвуковое дуплексное сканирование. Оно на сегодняшний день является основным методом оценки состояния крупных сосудов в эпидемиологических и клинических исследованиях, благодаря тому, что обладает следующими преимуществами [6]:
- неинвазивность;
- количественный анализ и хорошая воспроизводимость;
- предоставляет информацию не только о просвете сосуда, но и о состоянии самой стенки.
Возможности, достоинства и ограничения метода ультразвукового дуплексного сканирования. Дуплексное сканирование высокоинформативный, широкодоступный, неинвазивный, не требующий дополнительной подготовки пациента метод исследования сосудистой системы [6,7]. Этот метод сочетает в себе визуализацию сосудов и тканей в В-режиме и допплеровскую оценку показателей кровотока (различные виды компьютерной обработки спектра доплеровского сдвига частот или «энергий»). Методика позволяет одновременно оценивать состояние сосуда (сосудистую геометрию, стенку и т.д.) и распределение потоков крови в сосуде в реальном режиме времени.К основным формам патологии, выявляемым при дуплексном сканировании, относятсяразличные виды окклюзирующих поражений атеросклероз, неспецифический аортоартериит и другие васкулиты, сопровождающиеся изменением комплекса интима-медиа, развитием стенозов и окклюзий; деформации врожденного и приобретенного характера, которые также играют существенную роль в развитии нарушений мозгового кровообращения (перегибы, извитости, петли); аномалии развития артерий (гипоплазии, аплазии, аномалии хода); аневризмы и псевдоаневризмы, ангиопатии.
Дуплексное сканирование позволяет выявлять как ранние доклинические формы патологии (дисфункцию эндотелия, снижение эластических свойств, утолщение артериальной стенки), так и выраженные формы в виде гемодинамически значимых стенозов артерий за счет АСБ. Очень важно, что ультразвуковое исследование предоставляет возможность качественной и количественной оценки патологических изменений (например, уплотнение стенки с утратой ее структуры с дифференциацией на слои), оценки структуры АСБ с выделением клинически значимых форм (мягкие АСБ, изъязвление поверхности с формированием кратеров, гетерогенные АСБ с гипоэхогенными компонентами). Отсутствие вредного воздействия на пациента при ультразвуковом исследовании позволяет проводить его так часто, как того требует клиническая ситуация. Следует подчеркнуть роль дуплексного сканирования в повышении приверженности пациентов рекомендациям по модификации факторов риска и лечению показано, что чаще бросали курить те пациенты, которым показывались фотокопии ультразвукового изображения их патологически измененных артерий[8].
В настоящее время с внедрением технологий высокочастотного сканирования (частота линейных датчиков от 10МГц и более) и углубленной обработке ультразвукового изображения значительно уменьшились ограничения исследования артерий шеи. Только тотальное кальцинирование всех стенок артерий не позволяет количественно оценить степень стенозирования. Однако результаты исследования и их интерпретация в значительной мере зависят не только от уровня подготовленности исследователя, но и от методических аспектов проведения исследования и интерпретации данных.
Для проведения дуплексного сканирования используются стандартные ультразвуковые системы, оснащенные ультразвуковым линейным датчиком с частотой не менее 7МГц, встроенным блоком ЭКГ и программным обеспечением для сосудистых исследований. Необходимо иметь возможность сохранения изображения в цифровом формате. Согласно Рекомендациям Американского общества эхокардиографии (ASE) необходимо дважды в год проводить профилактическое техническое обслуживание оборудования [9].
Роль параметра «наличие атеросклеротической бляшки (АСБ)» в стратификации сердечно-сосудистого риска (ССР). Применение параметра «наличие АСБ» позволяет провести переклассификацию степени риска по Фрамингемской шкале. В зарубежных исследованиях говорится, что до 38% популяции из низкого и среднего уровня риска были переведены в группу высокого риска [10]. По мнению некоторых авторов именно обнаружение АСБ, в противовес жёсткости артериальной стенки, является мощным предиктором развития сердечнососудистых заболеваний [11].В ряде клинических исследований показано, что прогностическая значимость ультразвуковых методов в обнаружении доклинического атеросклероза потенциально очень высока [1214]. В американских Рекомендациях 2011г. [15] по ведению пациентов с заболеваниями каротидных и позвоночных артерий указано, что проведение дуплексного сканирования сонных артерий в качестве рутинного обследования нецелесообразно у асимптомных пациентов без факторов риска (класс III, уровень доказательности: С). Однако проведение его необходимо у пациентов без клинических проявлений атеросклероза, но имеющих 1 или 2 ФР для диагностики стенозов сонных артерий (класс IIb, уровень доказательности: С). Кроме того, дуплексное сканирование сонных артерий рекомендовано в качестве первичного диагностического теста асимптомным пациентам с предполагаемым или известным стенозом сонных артерий (класс I, уровень доказательности: С).
Хотелось особо отметить, что по результатам мета-анализа 11 популяционных исследований, посвященных сравнению ТИМ и АСБ в прогнозе риска развития неблагоприятных сердечнососудистых событий, сделан вывод о том, что наличие АСБ в сонных артериях в большей степени, чем ТИМ обладает предсказательной способностью в отношении риска развития коронарной болезни сердца. Иными словами авторы утверждают, что прогностическая ценность параметра «наличие АСБ» в выявлении признаков субклинического атеросклероза выше, чем параметра ТИМ [16].
Лодыжечно-плечевой индекс систолического давления (ЛПИ).Измерение регионального артериального давления в артериях нижних конечностей введено в хирургическую практику T. Winsor в 1950г. и применяется при облитерирующих заболеваниях артерий для оценки состояния кровообращения нижних конечностей. Основным критерием является ЛПИ, который рассчитывается как отношение систолического давления на лодыжке и плече (давление определяется с помощью ультразвукового исследования). Впервые определение ЛПИ с помощью ультразвукового прибора было проведено CarterS. в 1968г.[17].
В Рекомендациях ACCF/AHA 2010 года по оценке ССР у бессимптомных лиц приведены данные о том, что значение ЛПИ ниже 0,9 является независимым прогностическим фактором развития сердечно-сосудистых событий, таких как инфаркт миокарда, внезапная сердечная смерть, нестабильная стенокардия [18]. Кроме того, он указывает на наличие гемодинамически значимой патологии артерий нижних конечностей, требующей агрессивной антиатеросклеротической терапии, и связано с увеличением сердечно-сосудистого риска независимо от других факторов. В рекомендациях Европейского общества кардиологов по артериальной гипертонии 2007г. впервые указывается на необходимость оценки субклинического поражения органовмишеней артерий нижних конечностей по параметру лодыжечно-плечевого индекса давления [19].
Уменьшение ЛПИ более чем на 0,15 демонстрирует сильную независимую связь с увеличением ССР [18-20], в том числе и у асимптомных лиц с промежуточным и низким риском по Фрамингемской шкале [21,22]. В настоящее время ЛПИ рассматривается как показатель генерализованного атеросклеротического поражения сосудистого русла. Значение ЛПИ позволяет судить о степени развития коллатерального кровообращения голени. Величина ЛПИ до 0,7 свидетельствует о компенсации кровообращения; снижение от 0,7 до 0,4 о субкомпенсации, при <0,4о декомпенсации. Однако в упомянутых Рекомендациях ACCF/AHA 2010 указано, что измерение ЛПИ целесообразно лишь для оценки ССР у лиц с умеренным риском (класс ІІа, уровень: В) [18]. Рогозой А.Н. и соавт.[23] предложен так называемый «компромиссный» вариант показаний для измерения ЛПИ:
- больные с АГ старше 45 лет;
- больные с симптомами напряжения со стороны конечности;
- больные в возрасте 50-69 лет с факторами риска развития ССЗ;
- больные старше 70 лет независимо от присутствия других ФР;
- больные со средним и высоким риском развития или осложнения ССЗ, выявленным согласно одной из современных шкал риска.
В связи с вышеизложенным не вызывает сомнений целесообразность внедрения методик определения ЛПИ в качестве скринингового метода для диагностики атеросклеротического поражения артерий нижних конечностей в учреждениях амбулаторно-поликлинического звена. Однако определение ЛПИ с помощью профессиональной ультразвуковой аппаратуры достаточно трудоемкий метод и выполняется на дорогостоящем оборудовании. Одним из методов, более доступным по цене и легко воспроизводимым в амбулаторных условиях, в том числе при массовых профилактических осмотрах, является ультразвуковая допплерография с помощью УЗ-индикатора кровотока.
Показатели ригидности (жесткости) магистральныхартерий. Жесткость сосудистой стенки свойство, зависящее от количества эластических элементов в сосудистой стенке[17]. Обратным понятием жесткости является термин податливости сосудистой стенки, характеризующий способность сосуда к увеличению объема в ответ на повышение АД. Золотой стандарт измерения жесткости оценка скорости распространения пульсовой волны (СПВ).Определение жесткости артериальной стенки с помощью параметра СПВ предложено для оценки ССР в 90-х годах прошлого столетия [24, 25]. Еще в 1929 году в лаборатории Г.Ф. Ланга было сделано заключение, что СПВ является наиболее обоснованным и надежным показателем эластичности аортальной стенки.СПВ зависит от ригидности сосудистой стенки, т.е. чем выше ригидность сосуда, толще стенка сосуда и меньше его диаметр, тем быстрее распространяется по нему пульсовая волна. Недостатком определения СПВ является ее зависимость не только от жесткости сосудистой стенки, обусловленной изменением ее структуры, но и от уровня среднего АД в артериальной системе во время определения СПВ (уровень растягивающего давления) [26].
Возрастание скорости пульсовой волны на 1 м/с относительно возраста, пола и традиционных факторов риска, увеличивает риск заболеваемости и смертности от ССЗ на 14% и 15% соответственно [27].
Многие исследования доказали высокую значимость этого параметра, как маркера поражения сосудистой стенки атеросклерозом и, следовательно, риска развития ССЗ и ССС [2730], в том числе и у пациентов с бессимптомным течением атеросклероза [31]. Все неинвазивные методы оценки сосудистой жесткости являются косвенными и оценивают некоторые суррогатные параметры, которые определяются жесткостью. Они включают три основных метода СПВ, анализ формы пульсовой волны на крупных артериях, а также прямое измерение взаимоотношений давления и диаметра сосуда.В клинике в основном используется два подхода, которые являются доступными и могут быть выполнены вне специализированной лаборатории:
- СПВ;
- анализ пульсовой волны центральных сосудов (сонных артерий, аорты или лучевой и других артерий с применением передаточной функции).
СПВ представляет собой региональный показатель сосудистой жесткости. Этот параметр зависит от эластического модуля стенки артерии, ее геометрии (радиус и толщина стенки), а также плотности крови и уровня давления [25].
Сердечно-лодыжечный сосудистый индекс (Индекс CAVI) .СПВ имеет существенный недостаток и соответственно определенные ограничения, он подвержен влиянию колебаний АД в течение измерения, то есть СПВ является параметром, зависимым от АД. В связи с чем японскими исследователями предложен другой индекс жесткости артериальной стенки, независимый от АД cardio-anklevascular index (CAVI) [32]. CAVI отражает жесткость стенки в аорте, бедренных и плечевых артериях. Вычисление его не требует специальной техники и измеряется на основе значений пл.СПВ и АД. Он позволяет оценить жесткость сосудов вне зависимости от уровня растягивающего АД, действующего на стенку артерии в момент регистрации пульсовой волны. Показано, что этот параметр ассоциируется с наличием и тяжестью коронарного атеросклероза, поэтому предлагается в качестве его предиктора [3335].САѴІполучил достаточно широкое распространение в последнее время ввиду того, что показал более достоверные и значимые результаты, чем ЛПИ, который был введён в практику несколько раньше.
Мультиспиральная компьютерная томография с определением коронарного кальция. Кальцификация коронарных артерий является неотъемлемой частью атеросклеротического процесса, т.е. кальцификация стенок артерий отражает развитие атеросклероза и не встречается в нормальных артериях. Другими словами, включения кальция обнаруживаются практически исключительно в пораженных атеросклерозом артериях и не встречаются в интактных сосудах. Небольшое количество коронарного кальция можно обнаружить уже на ранних стадиях атеросклеротического процесса, однако он наиболее характерен для сформировавшихся бляшек. Несмотря на то, что отмечается положительная корреляция между количеством коронарного кальция и степенью сужения просвета артерии, эта зависимость носит нелинейный характер [36]. Вследствие процесса ремоделирования артериальной стенки кальций не концентрируется исключительно в области значимого стенозирования.
В настоящее время основными методами оценки коронарного кальция являются электронно-лучевая компьютерная томография (ЭЛКТ) и МСКТ. Мульти-спиральная компьютерная томография (МСКТ) для диагностики атеросклеротического поражения сосудов стала использоваться c 90-х годов прошлого века [37]. Количественная оценка коронарного кальциноза основана на коэффициенте рентгеновского поглощения и площади кальцинатов [38]. Согласно этой шкале, коронарный кальциноз определяется как участок плотностью более 130 HU. Кальциевый индекс (КИ) по методу Агатстона, определяется как произведение площади кальцинированного поражения на фактор плотности. Было отмечено, что КИ отражает прогноз поражения сердечно-сосудистой системы и непосредственно коррелирует с частотой развития атеросклероза: чем выше показатель, тем больше риск атеросклеротического поражения. К примеру, при низком КИ от 10 ед. и ниже вероятность атеросклероза венечных артерий составляет не более 5-10%. При умеренном КИ от 11 до 100 ед., возможность наличия 50% сужения не более 20%, при КИ 101-400 ед. 75%, то есть умеренно высокий риск атеросклероза. А при высоком КИ, более 400 ед.- вероятность атеросклеротического поражения коронарных артерий около 90%.
На основании значения полученного в результате индекса кальцификациикоронар ных артерий (индекса Агатстона) пациенты могут быть разделены на следующие группы (таблица 1): менее 10 (соответствует минимальной кальцификации коронарных артерий), 11-99 (умеренная кальцификация), 100-400 (повышенная кальцификация) и более 400 (распространенная кальцификация) [38].Значения индекса Агатстона менее 100 ассоциируются с низкой (менее 3 %) вероятностью выявления значимого стенозирования коронарных артерий при ангиографии. Чувствительность коронарного кальция в отношении гемодинамически значимого атеросклероза очень высока (95-98 %), однако специфичность этой методики значительно ниже. Таким образом, МСКТ при условии синхронизации с ЭКГ, позволяют выявлять и количественно оценивать небольшие количества коронарного кальция и, соответственно, оценивать наличие и тяжесть коронарного атеросклероза.
Таблица 1 Основные указания к интерпретации индекса Agatston
|
Индекс кальция |
Выраженность бляшек |
Вероятность ИБС |
Кардиоваскуляр ный риск |
Рекомендации |
|
0 |
Нет бляшек |
Очень низкая |
Очень низкий |
Успокоить |
|
1-10 |
Минимальные бляшки |
Маловероятна |
Низкий |
Обсудить пути предупреждения ИБС |
|
11-100 |
Немного бляшек |
Вероятен минимальный или умеренный стеноз |
Умеренный |
Обсудить возможность воздействия на факторы риска |
|
101-400 |
Умеренное количество бляшек |
Высокая вероятность ИБС |
Умеренно высокий |
Рекомендовать воздействие на факторы риска |
|
Более 400 |
Распространенные бляшки |
Высокая вероятность значимого стеноза |
высокий |
Агрессивное воздействие на факторы риска, тесты с нагрузкой или фармакологическим стрессом |
Выявление коронарного кальция:
- Определяет наличие коронарного атеросклероза.
- Выраженность атеросклероза коррелирует со степенью кальциноза.
- Степень кальциноза является предиктором гемодинамического стеноза коронарных артерий.
- Степень кальциноза является предиктором развития осложнений ИБС.
Если коронарный кальций не выявлен:
- Это полностью не исключает наличия стенозов коронарных артерий.
- Имеется низкая вероятность гемодинамически значимого стеноза коронарных артерий.
- Низкий риск развития ИБС.
Основными показаниями к определению коронарного кальция в настоящее время являются необходимость исключения ИБС у пациентов с не вполне типичным болевым синдромом в грудной клетке и уточнение риска ССЗ у пациентов с промежуточным суммарным риском.С созданием 4-х в 1999 году [39], а затем 8-ми спиральных компьютерных томографов в 2001 появилась возможность диагностики не только статичных объектов c оценкой косвенных признаков атеросклеротического поражения, но и непосредственной визуализации состояния коронарного русла [37]. Развитие технологии шло очень быстро, и в конце 2001 года появились 16-ти, а затем и 32-х и 40спиральные КТ системы, но данная задача окончательно не была решена. Лишь на пороге 2005 года в арсенале врача появились неинвазивные 64-МСКТ, позволяющие еще быстрее получать изображение, с реконструкцией объемного изображения менее 0,5х0,5х0,6мм [40]. Высокоразрешающая способность 64 МСКТ позволяет:
- достоверно визуализировать коронарные артерии [40,41], с уточнением локализации атеросклеротического поражения, выявления аномалий развития венечных сосудов сердца;
- определять состоятельность аортокоронарных шунтов и внутрисосудистых эндопротезов (стентов)[41,42,43];
- проводить подсчет КИ [38], с целью уточнения прогноза заболевания;
- отмечать нарушения перфузии и жизнеспособности миокарда у больных в ранние и более поздние сроки инфаркта миокарда[44,45];
- оценивать сократительную способность сердца [44-46];
- изучать состояние перикарда, клапанов сердца [47,48].
Магнитно-резонансная ангиография.
Следующим "золотым" стандартом, но уже в диагностике глобальной и региональной функции левого желудочка, является МРТ. Проведенные исследования по прямому сравнению высокоразрешающей МРТ с 64-МСКТ, показали статистическое соответствие полученных данных по изучению состояния сердца у больных с перенесенным инфарктом миокарда [44]. В этой работе Baks T etal. показали, что 64 МСКТ достоверно определяет площадь зоны некроза миокарда в сравнении с 1,5 Т МРТ.
Магнитно-резонансная ангиография (МРА) это высокоинформативный и безопасный метод лучевой диагностики, позволяющий получить изображения кровеносных сосудов при помощи магнитно-резонансного томографа и оценить анатомические и функциональные особенности кровеносного русла. С помощью МР ангиографии можно выявить:
- аневризмы и патологические соустья;
- стенозы и окклюзии сосудов;
- сосудистые мальформации;
- атеросклеротические изменения.
Суть метода: под воздействием сильного магнитного поля спины протонов ядер водорода изменяют свое положение и располагаются вдоль оси магнитного поля [49]. Воздействие магнитного поля и радиочастотного излучения на протонынепостоянно, с заданными силой, частотой и временем, а протоны после воздействия на них радиочастотного сигнала вновь возвращаются в исходное положение — так называемое «время релаксации» (T1 и T2). Воздействие магнитного поля и радиочастотного импульса на протоны ядер водорода заставляет их вращаться относительно новых осей в течение очень короткого периода времени, что сопровождается выделением и поглощением энергии, формированием своего магнитного поля. Регистрация этих энергетических изменений и является основой МРТизображения. Метод магнитно-резонансной ангиографии позволяет получать изображения сосудов без использования каких-либо рентгеноконтрастных средств, хотя для получения еще более четкого изображения применяются особые контрастные вещества на основе гадолиния.
Для сосудов магистрального типа (грудная и брюшная аорта и их ветви, почечные артерии, чревный ствол, артерии нижних конечностей, воротная вена) целесообразно выполнение МР ангиографии с контрастным усилением [50]. Это необходимо для улучшения визуализации указанных сосудистых структур, а значит и большей информативности метода диагностики.
Следует отметить, что важным аспектом в обследовании асимптомных пациентов (на субклинической стадии заболевания) является соблюдение этапности, чтобы вовремя начать профилактические мероприятия по предупреждению прогрессирования заболевания и риска развития возможных осложнений. На рисунке 1 представленалгоритм поэтапной инструментальной диагностики данной категории пациентов.
Рисунок 1 Алгоритм поэтапной инструментальной диагностики атеросклеротического поражения сосудистой системы
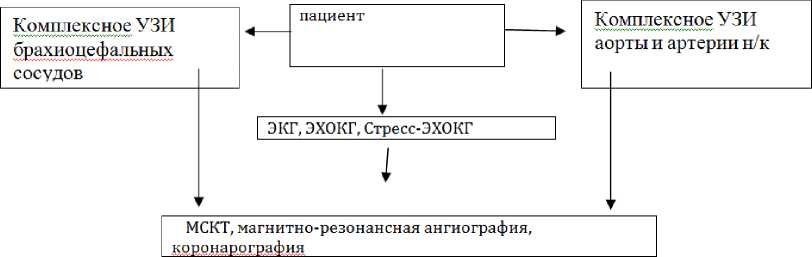
Заключение: Таким образом, приоритетным методом для ранней диагностики атеросклероза на субклинической его стадии является ультразвуковое исследование артерий. В дальнейшем по мере необходимости и возможности следует применять более дорогостоящие методы (МСКТ, магнитнорезонансную ангиографию).
Следует подчеркнуть, что несомненно широкое внедрение в медицинскую практику ультразвуковых методов исследования, в первую очередь дуплексного и триплексного сканирования, а также магнитно-резонансной ангиографии и мультиспиральной компьютерной томографии, улучшило идентификацию сердечно-сосудистой патологии.
СПИСОК ЛИТЕРАТУРЫ
- ConroyR.M., Pyorala K., Fitzgerald A.P. et al. Estimation of ten-year risk of fatal cardiovascular disease in Europe: the SCORE project / / Eur. Heart J. 2003. Vol. 24. P. 987-1003.
- MarmaK. Amanda, Donald M., LLoud-Jones.Sistematic examination of the updated Framingham HeartStudy general cardiovascular risk profile// Circulation. 2009. Vol. 120. P. 384-390.
- Lloyd-Jones, D. M. Cardiovascular risk prediction : Basic Concepts, current status, and future / / Circulation. 2010. Vol. 121. P. 1768-77.
- Greenland P., Smith J.S., Grundy S.M. Improving Coronary Heart Disease Risk Assessment in Asymptomatic People: Role of Traditional Risk Factors and Noninvasive
- Cardiovascular Tests // Circulation. 2001. Vol. 104. P. 1863-1867.
- Helfand M., Buckley D.I., Freeman M. et al. Emerging Risk Factors for Coronary Heart Disease : A Summary of Systematic Reviews Conducted for the U.S. Preventive Services Task Force / / Annals Internal Medicine. 2009. Vol. 151, N 7. P. 496-507.
- Цвибель В., Пеллерито Дж. Ультразвуковое исследование сосудов: [пер. с англ.]. М: Видар, 2008. 646 с.
- Лелюк В.Г., Лелюк С.Э. Ультразвуковая ангиология // М: Реальноевремя, 2011. 658с.
- M. KovaiteM., Petrulioniene Z., Ryliskyte L. et al. Relationship of arterial wall parameters to cardiovascular riskfactors and cardiovascular risk assessed by SCORE system / / Medicina (Kaunas). 2007. Vol. 43, N 7. P. 529-541.
- Roman M. J., Naqvi T.Z., Gardin J.M. et alClinical Application of Noninvasive Vascular Ultrasound in Cardiovascular Risk Stratification: A Report from the American Society of Echocardiography and the Society of Vascular Medicine and Biology / / Echocardiography. 2009. Vol. 19. P. 943-954.
- Belcaro G., Nicolaides A.N., RamaswamiG.etal.Carotid and femoral ultrasound morphology screening and cardiovascular events in low risk subjects: a 10-year follow-up study (the CAFES-CAVE study) / / Atherosclerosis. 2010.-Vol. 156, Iss. 2. P. 379-387.
- Sugioka K.,Hozumi T., Iwata S. et al Morphological but not functional changes of the carotid artery are associated with the extent of coronary artery disease in patients with preserved left ventricular function / / Stroke. 2008. Vol. 39, N 5. P. 1597-99.
- Chambless L. E., Folsom A.R., Sharrett et al.Coronary heart disease risk prediction in the atherosclerosis risk in communities (ARIC) study // J. Clinical Epidemiol. 2003. Vol. 56, N 9. P. 880-890.
- IreneM.,Bots M., Hofman A. et al Predictive value of noninvasive measures of atherosclerosis forincident myocardial infarction / / Circulation. 2004. Vol. 109. P. 1089-1094.
- Kitamura A, . Hiroyasu I., Hironori L.et al. Carotid Intima-Media thickness and Plaque characteristics as a riskfactor for stroke Japanese elderly men / / Stroke. 2004. Vol. 35. P. 2788-2794.
- Thomas G. L., Jonathan Halperin, SahnyAbbara et al. 2011ASA/ACCF/AHA/AANN/AANS/ACR/ASNR Guideline onthe management of patients with extracranial carotid and vertebral artery disease // J. Am. Coll. Cardiol. 2011. Vol. 57, N 8. P. 1002-1044.
- Inaba Y., Chen S., Bergmann R.Carotid plaque, compared with intima -media thickness, more accurately predicts coronary artery disease events: a meta-analysis / / Atheroscl.2012. -Vol. 220, N 1. P. 122-133. Carter S. A. Indirect systolic pressures and pulses waves in arterial occlusive disease of the lower extremities // Circulation. 1968. Vol. 37. P. 624-637.
- Greenland P., Alpert J.S., Beller G.A. et al.2010 ACCF/AHA Guideline for Assessment of CardiovascularRisk in Asymptomatic Adults // J. Am. Coll. Cardiol. 2010. Vol. 56, N 25. P. 2182-2199.
- Mancia G.,Backer G., Dominiczak A. et al 2007 Guidelines for the management of arterial hypertension: The Task Force for the Management of Arterial Hypertension of the EuropeanSociety оf Hypertension (ESH) and of the European Society of Cardiology (ESC) // J. ofHypertension. 2007. Vol.25, N 6. P. 1105-1187. Resnick H. E., Foster G.L. Prevalence of elevated ankle-brachial index in the USA: 1999-2002 / / Am. J. Medicine. 2005. Vol. 118. P. 676-679.
- Allison M. A.,Hiat W.R. et al. A high ankle-brachial index is associated with increased cardiovascular disease morbidity and lower quality of life // J. Am. Coll. Cardiol. 2008. Vol. 51. P. 12921298.
- Fowkes F. J., Murray G.D. et al. Ankle-brachial index combined with Framingham risk score topredict cardiovascular events and mortality: a meta-analysis / / JAMA. 2008. Vol. 300. P. 197-208.
- Рогоза А. Н. Роль и возможности лодыжечно-плечевого индекса систолического давления при профилактических обследованиях / / Российский медицинский журнал. 2011. № 2. С. 1-8. O’Rourke M. F.,Mancia G. Arterial stiffness // J. Hypertens. 1999. Vol. 17. P. 1-4.
- Arnett D. K., Evans G.W., Riley W.A.Arterial stiffness : a new cardiovascular risk factor?// Am. J. Epidemiol. 1994. Vol. 140. P. 669-682.
- МилягинВ. А.,Комиссаров В.Б.Современные методы определения жесткости сосудов / / Артериальная гипертензия. 2010. № 2. С. 134-143.
- Van Popele N. M., F.U. Mattace-Raso F.U., Vliegenthart R. et alAortic stiffness is associated with atherosclerosis of thecoronary arteries in older adults: the Rotterdam Study // J. Hypertenion. 2006. Vol. 24, N12. P. 23712376.
- Cecelja M.,Chowienczyk P.Dissociation of Aortic Pulse Wave Velocity with Risk Factors forCardiovascular Disease Other Than Hypertension: A Systematic Review / / Hypertension. 2009. Vol. 54. P. 1328-1336.
- Tomiyama H.,Koij Y. et al. Brachial-ankle pulse wave velocity is a simple and independentpredictor of prognosis in patients with acute coronary syndrome // Circulation. 2005. Vol. 69. P. 815-822.
- Yufu K.,Takahashi N., Anan F. et al. Brachial arterial stiffness predicts coronary atherosclerosis in patientsat risk for cardiovascular diseases //Japanese Heart J. 2004. Vol. 45, N 2. P. 231242.
- Liu C. S., Li C.I., Shih C.M. et al. Arterial stiffness measured as Pulse Wave Velocity is highlycorrelated with coronary atherosclerosis in asymptomatic patients// J. Atherosclerosis and Thrombosis. 2011. -Vol. 18, N 8. P. 652-658.
- Kohgi S.,Jungi U., Otsuka K. et al.A novel blood pressure independent arterial wall stiffnessparameter; cardio-ankle vascular index (CAVI)// J.Atheroscleros.and Thrombosis. 2003. Vol. 13.P. 101-107.
- Shirai K., Utino J., Otsuka K. et al. A novel blood pressure-independent arterial wall stiffness parameter: Cardio-Ankle Vascular Index (CAVI) // J. Atherosclerosis and Thrombosis. 2006. Vol. 13, N 2. P. 101-107.
- Takaki A.,Ogawa H., Wakeyama T. et al Cardio-ankle vascular index is a new noninvasive parameter of Arterial stiffness / / Circulation.2007. Vol. 71, N 11. P. 1710-1714.
- Nakamura K., Tomaru T., Yamamura S. et al. Cardio-Ankle Vascular Index is a Candidate Predictor of Coronary Atherosclerosis / / Circulation 2008. Vol. 72. P. 598-604.
- Оганов Р. Г., БойцовС.А. и др. Методы доклинической неинвазивной диагностики атеросклероза / / Кардиоваскулярнаятерапия и профилактика. 2011. №10(6). -С. 1-64.
- Терновой С.К., Синицин В.Е. и др. Неинвазивная диагностика атеросклероза и кальцинозакоронарных артерий. М: Атмосфера, 2003. 144с.
- AgatstonA. et al. Quantificationofcoronary artery calcium using ultrafast computed tomography //J. Am. Coll. Cardiol. 1990. -Vol.15. P. 827-832.
- Rumberger J.A. et al. Electron beam computed tomography coronary calcium scanning: a review and guidelines for use in asymptomatic persons / / Mayo Clin Proc. 1999. Vol. 74. P. 243-252.
- Fishman E.K. Introduction to 64-slice CT and its role in coronary imaging / / Suppl. Applied Radiol. 2005. S. 8-13.
- Anders K. et al.Coronary artery bypass graft (CABG) patency: assessment with high-resolution submillimeter 16-slice (MDCT) versus coronary angiography// Eur. J. Radiol. 2006. Vol. 57(3). P. 336-344.
- Kopp A.F.,Heuschmid M. et al. Evaluation of cardiac function and myocardial viability with 16and64slice multidetector / / Eur. Radiol. -2005. Vol. 15 (4). P. 15-20.
- Rychter K.et al.Multifocal coronary artery myocardial bridging involving the right coronary and left anterior descending arteries detected by ECG-gated 64 slice multidetector CT coronary angiography / / Int. J. Cardiovasc. Imaging. 2006. Vol.20. P. 234-240.
- Baks T. Multislice computed tomography and magnetic resonance imaging for the assessment of reperfused acute myocardial infarction // J. Am. Coll. Cardiol. 2006. Vol.48. P. 144-152.
- Lardo A.C. et al. Contrast-enhanced multidetector computed tomography viability imaging after myocardial infarction: characterization of myocyte death, microvascular obstruction, and chronic scar / / Circulation. 2006. Vol. 113(3). P. 394-404.
- Funabashi N. et al. New acquisition method to exclusively enhance the left side of The heart by a small amount of contrast material achieved by multislicecomputed tomography with 64 data acquisition system / / Int. J. Cardiol. 2006. Vol. 116. P. 246-252.
- Pannu H.K et al. Gated cardiac imaging of the aortic valve on 64multidetectorrow computed tomography : preliminary observations // J. Comput. Assist. Tomogr. 2006. Vol. 309(3). P. 443-446.
- Alkadhi H. Aortic stenosis: comparative evaluation of 16-detector row CT and echocardiography// Radiology. 2006. Vol.240. P.47-55.
- Rothwell.P., Gibson R, Slattery R.Equivalence of measurements of carotid stenosis.A comparison ofthree methods on 1001 angiograms. European carotid surgery trialists'collaborative group / / Stroke. 1994. Vol. 25(12). P. 2435-2439.
- Бобрикова Е.Э., Усов В.Ю., Щербань Н.В. и др. Высокоразрешающая контрастированная МРангиография в дифференциальной диагностике каротидных бляшек и его взаимосвязь с ишемическим повреждением головного мозга / / Бюллетень сибирской медицины.2013; Том12.№3.С.97-105.