Соотношение межДу уровнями противовоспалительными и провоспалительными цитокинами - важный момент в регуляции возникновения и развития системного воспалительного ответа, лечение которого является актуальной проблемой в современной медицине. Исследования по эффективности ангиопротектора депротеинизированного гемодиализата из крови молочных телят у новорожденных с системным воспалительным ответом, перенесших тяжелую асфиксию при рождении, выявили его положительное влияние на биохимическую картину СВО в виде уменьшения выраженности воспаления за счет активации синтеза противовоспалительных цитокинов и угнетения синтеза провоспалительных цитокинов.
Актуальность. Метаболический пожар у новорожденных, перенесших тяжелую асфиксию при рождении, сопровождается дискоординацией жизненноважных функций организма: нарушениямидыхания, кровообращения, микроциркуляции и пр., что позволяет предполагать участие в патогенезе асфиксии и ее последствий системного воспалительного ответа (СВО). Доказана диагностическая ценность цитокинов в формировании СВО у новорожденных, перенесших тяжелую асфиксию при рождении [1]. Среди цитокиновесть те, которые способствуют (провоспалительные), и те, которые препятствуют развитию воспалительного процесса (противовоспалительные). Соотношение между противовоспалительными и провоспалительными цитокинами - важный момент в регуляции возникновения и развития воспалительного процесса. От этого баланса зависит течение и исход заболевания. Лечение СВО включает в себя три основных звена: влияние на уровни эндотоксина [2, 3, 4, 5, 6, 7], цитокинов [8, 9, 10] и состояние эндотелия [2, 11]. В настоящее время не разработан единый подход к решению данной проблемы, что и определяет актуальность темы.
Из препаратов, обладающих многогранным действием на гомеостаз, мы обратили внимание на препарат из группы вазопротекторов - депротеинизированный гемодиализат из крови молочных телят (ДГКМТ), который является ангиопротектором и представляет собой совокупность ряда физиологически активных ингредиентов, которые стимулируют утилизацию кислорода тканями в условиях гипоксии, обеспечивают усиление транспорта глюкозы через биологические мембраны, повышают синтез внутриклеточного АТФ и увеличивают долю аэробного гликолиза [12]. Стимуляция утилизации кислорода при гипоксии приводит к тому, что в эндотелии сосудов нормализуется анаэробный метаболизм, происходит высвобождение простациклина и оксида азота, обладающих вазодилатирующим эффектом [12,13].
Вышеперечисленными механизмами действия данного препарата и обосновано изучение его эффективности при СВО у новорожденных, перенесших тяжелую асфиксию при рождении.
Цель исследования - изучение эффективности ДГКМТ при СВО у новорожденных, перенесших тяжелую асфиксию при рождении.
Материалы и методы. Исследования проводили у 16 новорожденных, перенесших тяжелую асфиксию при рождении, в стандартную терапию которых с первых суток заболевания введен ДГКМТ в дозе 0,5 мл/кг в сутки (изучаемая группа), а для контроля эффективности терапии использовали результаты исследования у 26 выздоровевших новорожденных с аналогичной патологией, получавших стандартную терапию, соответствующую протоколам лечения тяжелой асфиксии и гипоксически- ишемического поражения центральной нервной системы (контрольная группа). Изучали динамику уровней интерлейкина-4 (ИЛ-4), интерлейкина-6 (ИЛ-6). За основу для достоверности результатов исследовали биохимические показатели у 16 здоровых доношенных новорожденных на третьи сутки жизни.
Для статистической обработки данных использовался пакет программ обработки данных общего назначения Statisticafor Windows версии 6.0.
На первом этапе расчета были получены дискриптивные (описательные) статистики для показателей, измеряемых в количественной шкале. Такими характеристиками являются: медиана и среднее значение как меры положения; стандартное отклонение и квартили как меры рассеивания; минимальное и максимальное значение как показатель размаха выборки.
Распределение всех анализируемых количественных показателей достоверно отличались от нормального (критерий Колмогорова-Смирнова), поэтому в тексте дальнейшего изложения для их характеристики преимущественно использовались медиана (50-й процентиль) и 25 и 75-й процентили (верхний и нижний квартили).
Для определения различий между группами применялись методы непараметрической статистики, так как если распределение далеко от нормального, то критерии, основанные на оценках среднего и дисперсии (параметрические критерии), дадут неверные результаты. Так, для связанных выборок (динамика лечения) использовались критерий знаков и критерий Вилкоксона; для несвязанных выборок (разбиение на подгруппы по признаку) - критерии Колмогорова-Смирнова и Манна-Уитни.
Для исследования влияния независимой переменной на зависимую применялись непараметрические аналоги дисперсионного анализа - критерий Краскела-Уоллиса и медианный тест.
Результаты и их обсуждение.
В таблице 1 представлены показатели ИЛ-4 и ИЛ-6 у доношенных новорожденных, перенесших тяжелую асфиксию при рождении, и у здоровых доношенных новорожденных на третьи сутки жизни.
Таблица 1 - Показателей цитокинов у здоровых новорожденных детей на третьи сутки жизни (р<0,05).
|
Показатели, ед. изм. |
Среднее |
Медиана |
Мин. |
Макс. |
Нижний квартиль |
Верхний квартиль |
Станд. отклон. |
|
|
ИЛ-4, пг/мл |
здоровые |
20,11 |
18,73 |
9,62 |
32,07 |
16,71 |
22,90 |
5,886 |
|
контрольная группа |
24,73 |
22,89 |
13,05 |
42,25 |
17,16 |
29,25 |
9,056 |
|
|
изучаемая группа |
20,59 |
18,08 |
14,35 |
32,52 |
17,1 |
22,10 |
5,581 |
|
|
ИЛ-6, пг/мл |
здоровые |
131,21 |
104,85 |
71,81 |
224,75 |
91,22 |
158,46 |
54,748 |
|
контрольная группа |
116,08 |
116,47 |
28,58 |
204,47 |
91,69 |
138,64 |
38,494 |
|
|
изучаемая группа |
174,81 |
170,74 |
136,4 |
208,95 |
154,88 |
200,24 |
25,108 |
Из приведенных в таблице 1 данных видно, что уровень противовоспалительного цитокина ИЛ-4 у здоровых доношенных новорожденных на третьи сутки жизни 18,73 пг/мл. В группе новорожденных, перенесших тяжелую асфиксию при рождении и получавших стандартную терапию, уровень ИЛ-4 22,89 пг/мл, что выше, чем у здоровых новорожденных и выше, чем у новорожденных изучаемой группы, в комплекс терапии которых входил ДГКМТ (18,08 пг/мл).
Уровень провоспалительного цитокина ИЛ-6 у здоровых новорожденных 104,85 пг/мл, в группе больных, получавших стандартную терапию, уровень ИЛ-6 116 пг/мл, тогда как в группе больных, в комплекс терапии которых входил ДГКМТ, уровень ИЛ-6 выше - 170,74 пг/мл.
Динамика изучаемых показателей в группах больных, получавших стандартную терапию, и больных, в комплекс терапии которых входил ДГКМТ, представлена в таблице 2.
Таблица 2 - Сравнительная оценка динамического исследования показателей системного воспалительного ответа в группе выздоровевших новорожденных и в изучаемой группе (р<0,05)
|
Показатели, ед. изм. |
Сутки |
Группы больных |
Среднее |
Медиана |
Мин. |
Макс. |
Нижний квартиль |
Верхний квартиль |
Станд. отклон. |
|
ИЛ-4, пг/мл |
3 |
Контроль ная |
24,73 |
22,89 |
13,05 |
42,25 |
17,16 |
29,25 |
9,056 |
|
Изучаемая |
20,59 |
18,08 |
14,35 |
32,52 |
17,1 |
22,10 |
5,581 |
||
|
5 |
Контрольная |
27,90 |
26,92 |
16,54 |
39,16 |
21,60 |
36,23 |
8,986 |
|
|
Изучаемая |
21,29 |
19,01 |
14,87 |
36,75 |
16,09 |
22,05 |
7,494 |
||
|
7 |
Контрольная |
28,36 |
30,32 |
18,06 |
37,47 |
18,85 |
35,16 |
8,283 |
|
|
Изучаемая |
20,65 |
20,43 |
13,20 |
28,42 |
19,73 |
21,47 |
4,972 |
||
|
ИЛ-6, пг/мл |
3 |
Контрольная |
116,08 |
116,47 |
28,58 |
204,47 |
91,69 |
138,64 |
38,494 |
|
Изучаемая |
174,81 |
170,74 |
136,4 |
208,95 |
154,88 |
200,24 |
25,108 |
||
|
5 |
Контрольная |
139,43 |
118,89 |
75,90 |
222,47 |
91,62 |
208,83 |
61,456 |
|
|
Изучаемая |
143,35 |
149,00 |
113,9 |
171,64 |
121,94 |
154,56 |
20,214 |
||
|
7 |
Контрольная |
110,86 |
112,98 |
78,59 |
157,72 |
81,34 |
121,58 |
29,206 |
|
|
Изучаемая |
120,70 |
116,99 |
89,90 |
159,50 |
109,29 |
127,85 |
23,616 |
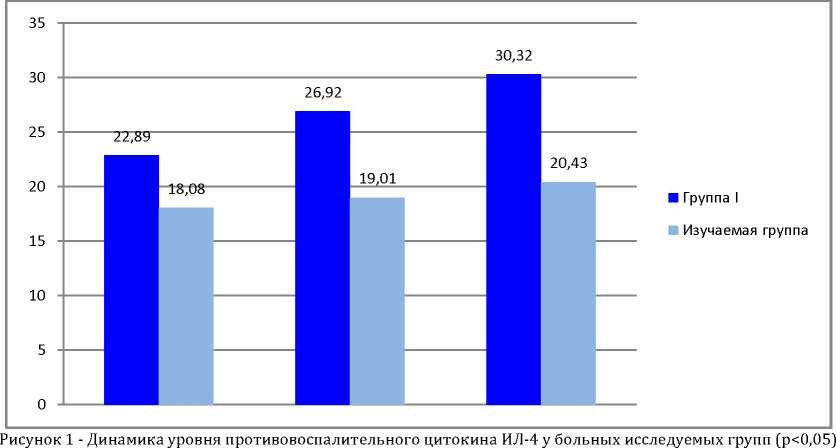
Из представленных данных видно, что в изучаемой группе уровень противовоспалительного цитокина ИЛ-4 стабильный (18,08, 19,01 и 20,43 пг/мл), он достоверно ниже, чем в группе новорожденных, получавших стандартную терапию, (22,89, 26,92 и 30,32 пг/мл) на 3,5-е и 7-е сутки соответственно. Кроме того в этой группе просматривается тенденция к его нарастанию на протяжении всего исследования.
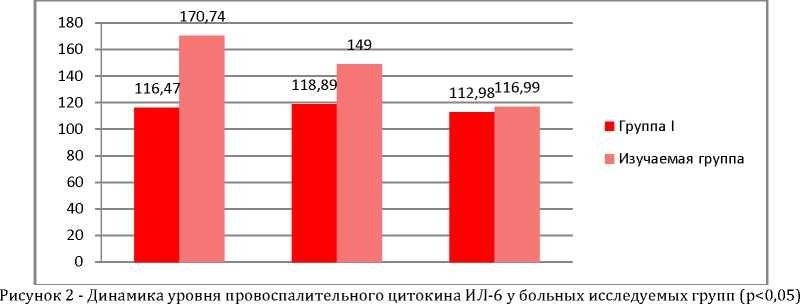
Уровень провоспалительного цитокина ИЛ-6 в изучаемой группе снижался на протяжении всего исследования с 170,74 пг/мл 3-и сутки до 149,00 пг/мл на 5-е и к седьмым суткам уровни ИЛ-6 существенно не различались в обеих группах (116,99 пг/мл в изучаемой группе и 112,98 пг/мл в контрольной).
Сравнительный анализ показателей противовоспалительного ИЛ-4 и провоспалительного цитокина ИЛ-6 в группе новорожденных, получавших стандартную терапию, и группе новорожденных, в комплекс терапии которых входил ДГКМТ, позволяет утверждать, что препарат ДГКМТ влияет на синтез цитокинов, так как в контрольной группе уровень противовоспалительного цитокина нарастает на протяжении всего исследования, угнетая синтез провоспалительного цитокина.
 Высокий уровень провоспалительного цитокина на третьи сутки связан с уменьшением угнетающего влияния противовоспалительных цитокинов, синтез которых тоже снижен, при этом за счет действия препарата ДГКМТ происходит и угнетение синтеза и провоспалительных цитокинов, подтверждением этому служит динамическое снижение уровня ИЛ-6 в группе новорожденных, в комплекс терапии которых был введен препарат ДГКМТ. К седьмым суткам уровни провоспалительного цитокина ИЛ-6 существенно не отличаются.
Высокий уровень провоспалительного цитокина на третьи сутки связан с уменьшением угнетающего влияния противовоспалительных цитокинов, синтез которых тоже снижен, при этом за счет действия препарата ДГКМТ происходит и угнетение синтеза и провоспалительных цитокинов, подтверждением этому служит динамическое снижение уровня ИЛ-6 в группе новорожденных, в комплекс терапии которых был введен препарат ДГКМТ. К седьмым суткам уровни провоспалительного цитокина ИЛ-6 существенно не отличаются.
Таким образом, анализ показателей воспаления противовоспалительного цитокина ИЛ-4 и провоспалительного цитокина ИЛ-6 позволяет считать, что препарат ДГКМТ оказывает влияние на биохимическую картину воспаления за счет угнетения синтеза цитокинов. Выводы. Применение ДГКМТ в лечении СВО у новорожденных, перенесших тяжелую асфиксию при рождении, оказывает влия ние на биохимическую картину СВО за счет уменьшения выраженности воспаления и снижения синтеза цитокинов.
СПИСОК ЛИТЕРАТУРЫ
- Овчаренко С.С. Оценка показателей активности эндотелия у новорожденных, перенесших тяжелую асфиксию при рождении. // Медицина неотложных состояний. - 2014. -№1(56). - С. 74-76.
- Козлов И.А. Метиленовый синий как ингибитор гиперпродукции эндогенного оксида азота при коррекции постперфузионной сосудистой недостаточности // Вестник интенсивной терапии. - 2002. - №2. - С. 7-12.
- М.Б. Ярустовский, М.В. Абрамян, Н.П. Кротенко Опыт применения селективной адсорбции эндотоксина у пациентов с тяжелым сепсисом после открытых операций на сердце // Анестезиология и реаниматология. - 2014. - № 3. - С. 39-46.
- М.Ш. Хубутия, М.М. Абакумов, И.В. Александрова и др. Селективная сорбция эндотоксина в комплексном лечении больных тяжелым сепсисом // Анестезиология и реаниматология. - 2010. - № 5. - С. 65-68.
- G. Novelli, G. Ferretti, L. Poli Clin^al results of treatment of postsurg^al endotoxin-mediated sepsis with polymyxin-B dirett hemoperfusion // Transplant. Proc - 2010. - Vol. 42 (4). - P. 1021-1024.
- Opal S. M. The host response to endotoxin, antilipopolysaccharide strategies, and the management of severe sepsis // Int. J. Med. M^ronot - 2007. - Vol. 297. - P. 365-377.
- S.E. Horoshilov, N. A. Karpun, S. G. Polovnikov. Selettive absorption of endotoxin in the treatment of abdominal sepsis // Obschajareanimatologija. - 2009. - Vol. 5 (6). - P. 83-87.
- Ашидкова Н.В. Эффективность препарата рекомбинантного интерлейкина-2 человека в терапии неонатального сепсиса и тяжелых неонатальных инфекций // Педиатрия. - 2009. - Т. 87, №3 - С. 80-86.
- Малыш И.Р. Влия ние анальгоседации на индуцированную продукцию цитокинов у пострадавших с тяжелойполитравмой // Біль, знеболювання, інтенсивна терапія. - 2003. - №2. - С. 67-70.
- Н.В.Ашиткова, Н.Н. Володин, М.В. Дегтярева Эффективность препарата рекомбинантного интерлейкина-2 человека в терапии неонатального сепсиса и тяжелых неонатальных инфекций // Педиатрия. - 2009. - Т. 87, №3. - С. 80-85.
- Клигуненко Е.Н. Влияние тромбопрофилактикибемипарином на маркеры воспаления // Біль, знеболювання і інтенсивна терапія. - 2013. - №3. - С. 9-12.
- Чуканова Е.И., Боголепова А.Н. Возможности использования солкосерила в терапии дисциркуляторной энцефвлопати // Инсульт. - 2007. - №21.- С.22-27.
- Yonekura M. Effects of solcoseryl on localized cerebral blood flow - clinical evaluation // Ther Res. - 1989. - №10. - Р. 137-145.