Синдром перекреста бронхиальной астмы и хронической обструктивной болезни легких (СПБАХ) в последние годы вызывает особый интерес у клиницистов и исследователей в связи с тяжелым течением, частыми обострениями и резистентностью к терапии. В обзоре представлено современное определение патологии, патогенез с характеристикой воспалительного процесса, новые биологические маркеры, лечебная тактика после установления трех фенотипов: бронхиальная астма с нейтрофильным воспалением дыхательных путей, хроническая обструктивная болезнь легких с преимущественно эозинофильным воспалением и бронхиальная астма с необратимой бронхиальной обструкцией и слабо выраженным воспалительным процессом.
Первоначально СПБАХ определялся как синдром повышенной сочетании с дыхательных
Бронхиальная астма (БА) и хроническая обструктивная болезнь легких (ХОБЛ) - широко распространенные глобальные заболевания, характеризующиеся обструкцией дыхательных путей, которая при БА имеет высокую вариабельность, а при ХОБЛ частично обратима и/или необратима. Наличие признаков обеих патологий у некоторых больных послужило основанием для выделения отдельного состояния - синдрома перекреста БА и ХОБЛ (СПБАХ) [1]. У больных с ранее поставленным диагнозом БА СПБАХ диагностируется в 29% случаев при наличии у них хронического бронхита и/или ухудшения диффузионной способности легких по моноокисиду углерода [2]. Распространенность СПБАХ у больных ХОБЛ варьирует в зависимости от диагностических критериев от 2,1 до 55% [3]. Больные с синдромом перекреста БА и ХОБЛ отличаются частыми обострениями, низким качеством жизни, быстрым ухудшением функции внешнего дыхания и высокой смертностью [4, 5, 6]. Для данной категории больных характерна высокая частота обращений за неотложной интенсивной терапии. Кроме того, расходы здравоохранения на таких больных почти вдвое превышают расходы на больных БА. Неблагоприятная динамика заболеваемости и тяжелые формы синдрома перекреста БА и ХОБЛ, нерешенная ситуация с его дифференциальной диагностикой, устойчивость к терапии, рост смертности обусловливают его медицинскую и социальную значимость [7].
Целью обзора является обобщение достижений в изучении механизмов развития синдрома перекреста БА и ХОБЛ с выделением диагностических маркеров и мишеней для целенаправленной терапии.
Определение.
В настоящее время нет четкого определения СПБАХ, поскольку неясно, является ли он отдельной нозологической единицей или все-таки это промежуточный фенотип, объединяющий два заболевания [8].
вариабельности воздушного потока в не полностью обратимой обструкцией путей [9]. При синдроме перекреста присутствует постоянное ограничение воздушного потока с наличием признаков, характерных и для БА, и для ХОБЛ [10]. Патогенез В 1961 году Орие и Шлютер [1] предложили парадигму, или, как позже ее стали называть, «голландскую гипотезу», в которой БА и ХОБЛ имеют общее происхождение с различиями, объясняемыми уникальными
индивидуальными особенностями, такими как генетические факторы, пол, возраст и воздействие окружающей среды, включающее табакокурение, загрязнение воздуха поллютантами, использование биомассы для отапливания помещений, сопутствующие заболевания легких и инфекции. Несмотря на длительность существования этой парадигмы, она продолжает активно оспариваться [10, 11]. В целом, «голландская гипотеза» утверждает, что БА и ХОБЛ являются одним заболеванием с диффузной обструкцией дыхательных путей, называемым авторами гипотезы «хронической неспецифической болезнью легких». С другой стороны, «британская гипотеза» поддерживает разное происхождение БА и ХОБЛ, подтверждаемое различиями в воспалительном профиле, генетическом полиморфизме, клиническом течении и ответе на терапию [10, 11].
В настоящее время предполагается, что синдром перекреста БА и ХОБЛ возникает в результате взаимодействия генетических, патологических и функциональных эффектов БА и ХОБЛ [5].
В патогенезе ХОБЛ особое внимание уделяется ^1-типу иммунного ответа и активации нейтрофильного воспалительного процесса в дыхательных путях [12]. Недавно Кристенсен и коллеги обнаружили экспрессию 100 ключевых генов, ответственных за Th2-воспалительный ответ, в эпителиальных клетках дыхательных путей больных ХОБЛ [13]. Примерно у 5% курильщиков с ХОБЛ выявлена высокая степень экспрессии генов Th2, которая была связана с увеличением количества эозинофилов в сыворотке и тканях, повышением ответа на бронходилататоры и значительным уменьшением легочной гипервентиляции после лечения ингаляционными кортикостероидами. Высокий уровень экспрессии генов ^2-типа иммунного ответа также в значительной степени коррелировал с генной экспрессией маркера тучных клеток CPA3 и эозинофильной хемотаксической молекулой CCL [14]. Соответствует ли это уникальному эндотипу ХОБЛ или генной экспрессии СПБАХ пока неясно.
Гебре и коллеги продемонстрировали возможность определения разных типов воспаления у больных БА и ХОБЛ при исследовании мокроты. У больных тяжелой БА и ХОБЛ были идентифицированы три кластера цитокинов: БА с высоким Th2- и эозинофильным воспалением, БА и ХОБЛ с преобладанием нейтрофилов в мокроте и ХОБЛ с преимущественно эозинофильным воспалением [15].
Известно, что табакокурение у больных ХОБЛ встречается в 80-90% случаев. Среди больных БА курильщиков около 25% [16] и по сравнению с не курящими больными БА они имеют значительно больший риск развития персистирующей обструкции дыхательных путей и СПБАХ [17, 18].
Взаимодействие хронического воздействия сигаретного дыма или продуктов сгорания биомассы и наличие БА способствуют выраженной обструкции дыхательных путей [19] - важной особенности СПБАХ. Курение сигарет может изменить воспаление дыхательных путей при БА с эозинофильного на нейтрофильное с повышением CD8+- клеток, наблюдаемое при ХОБЛ [20]. Этот процесс, возможно, опосредован IL-6, IL-8 и IL-17A, которые вовлечены в хемотаксис нейтрофилов у курильщиков с БА [21]. Кроме того, курение может индуцировать пролиферацию CD8+-клеток в дыхательных путях астматиков [22]. Исследования показали, что количество нейтрофилов и CD8+-клеток хорошо коррелирует с увеличением обструкции дыхательных путей [23]. Повышение CD8+-T-клеток, в частности, может привести к более быстрому снижению функции легких [23], а также к неполной обратимости обструкции воздушного потока [24]. У курильщиков с БА наблюдается большее количество бокаловидных и тучных клеток, меньшее количество эозинофилов и более выраженный эпителиальный слой, по сравнению c некурящими астматиками [25]. Кроме того, известно, что СПБАХ чаще встречается у пожилых людей [8]. Это может быть связано с более длительным воздействием экологических факторов, таких как загрязнение атмосферы и табачный дым, антигены или с возрастными физиологическими изменениями легких [26].
Ранее существовало мнение, что нижние дыхательные пути у астматиков стерильные. В последние годы по этому вопросу получены противоречивые данные. [27]. В нижних дыхательных путях больных БА была обнаружена Moraxella catarrhalis, а также представители рода Haemophilus и Streptococcus [28]. Колонизация этими видами бактерий была ассоциирована с изменением содержания нейтрофилов в мокроте и ухудшением состояния больных. Обнаружено, что сочетание инфицированности H. influenza с аллергическими заболеваниями дыхательных путей может активировать ТҺ17-иммунный ответ, который стимулирует развитие БА c нейтрофильным воспалением [29]. Кроме того, инфекционные факторы и курение вызывают повышение нейтрофилов в бронхо-альвеолярном лаваже больных БА за счет активации фосфатидилинозитол-3- киназы (PI3K) [30], играющей важную роль в хемотаксисе нейтрофилов [31]. Таким образом, предполагается, что персистирующая инфекция дыхательных путей способствует формированию «нейтрофильной» бронхиальной астмы [32].
Установлено, что патологические структурные изменения в мелких дыхательных путях способствуют фенотипическому перекресту между БА и ХОБЛ [33]. Эмфизема, гипервентиляция и потеря эластичности легочной ткани - основные проявления ХОБЛ, но они также могут встречаться и при поздних стадиях тяжелой БА.
БА и ХОБЛ имеют общие особенности морфологии эпителиального слоя: метаплазию кубических клеток и плоскоклеточную метаплазию. Ретикулярный базальный слой у больных ХОБЛ с астмаподобными симптомами имеет более толстую основную мембрану, чем больные ХОБЛ без этих признаков. При ХОБЛ увеличено количество гладких мышц дыхательных путей, но оно менее выражено, чем при БА. [34] Повторяющиеся обострения БА индуцируют бронхиальное воспаление с активацией протеаз, таких как нейтрофильная эластаза, катепсин G и матричные металлопротеазы (ММП), которые разрушают легочную паренхиму [35]. Исследование in vitro показало действие IL- 13 в качестве мощного супрессора экспрессии мРНК эластина через путь, включающий секрецию ММП-1 и ММП- 2 [36]. В более поздних стадиях БА, таким образом, начинает формироваться эмфизема, трансформирующая БА в СПБАХ. Диагностика.
Клинически СПБАХ обычно соответствует астматикам- курильщикам, у которых развивается не полностью обратимая обструкция дыхательных путей, однако, если в анамнезе нет БА, диагноз СПБАХ может быть затруднен из- за отсутствия конкретных биомаркеров. Во многих случаях постановка диагноза СПБАХ требует комплексного подхода, включающего анализ клинических проявлений, спирометрию с проведением бронходилатационного теста, идентификацию эозинофильного воспаления, определение легочных объемов, оценку диффузионной способности монооксида углерода и, в некоторых случаях, компьютерную томографию [37].
Многие исследования определяют СПБАХ как фенотип ХОБЛ. Повышенная обратимость дыхательных путей у больных ХОБЛ является одним из ключевых дифференциальных аспектов индивидуумов со СПБАХ, но он может ввести в заблуждение, если принимать во внимание только этот признак. У более 50% больных ХОБЛ от средней до крайне тяжелой степени тяжести в клинических испытаниях UPLIFT этот критерий часто встречался при проведении бронходилатационного теста [38]. Кроме того, бронхиальная гиперреактивность наблюдается примерно в 10-20% случаев от общей популяции и показано, что она является фактором риска развития БА и ХОБЛ [39]. У больных БА или ХОБЛ более тяжелая бронхиальная гиперреактивность была связана с более тяжелыми симптомами и более быстрым снижением ОФВ1 (объем форсированного выдоха за 1 секунду) [40]. Однако больные ХОБЛ без значимых сопутствующих заболеваний с высоким уровнем обратимости бронхов показали более лучшие клинические показатели в долгосрочном периоде [41]. Эти противоречивые результаты подчеркивают необходимость специализированного подхода к диагностике и оценке больных СПБАХ.
Возможно, наиболее важной диагностической особенностью СПБАХ при ХОБЛ является наличие эозинофилии мокроты. Воспаление у больных БА считается преимущественно эозинофильным и опосредуется CD4+-Т-лимфоцитами, тогда как при ХОБЛ оно нейтрофильное и связано с CD8+- клетками. Папи и коллеги [42] наблюдали, что содержание эозинофилов в крови и мокроте было значительно выше у больных со стабильной ХОБЛ с частичной обратимостью ограничения воздушного потока по сравнению с больными ХОБЛ без бронхиальной обратимости. Поскольку исследование эозинофилии мокроты обычно не проводится в клинической практике, были определены косвенные маркеры этого типа воспаления. Чоу и коллеги [43] продемонстрировали более высокие уровни выдыхаемой окиси азота (NO) у больных ХОБЛ и эозинофильным воспалением дыхательных путей (> 3% эозинофилов в индуцированной мокроте). Интересно, что у больных ХОБЛ с периферическим эозинофильным воспалением, получающими ингаляционные глюкокортикостероиды (ИГКС), наблюдается менее выраженное обострение, чем у больных с низким уровнем эозинофилии крови [44].
В настоящее время при СПБАХ изучаются возможные биомаркеры плазмы и мокроты. Ивамото и коллеги [45] исследовали четыре потенциальных биомаркера ХОБЛ (белок поверхностного активного вещества A (surfactant protein A - SP-A), растворимый рецептор для конечных продуктов гликирования (the soluble form of receptor for advanced glycation end - sRAGE), миелопероксидаза (myeloperoxidase - MPO) и липокалин, связанный с нейрофильной желатиназой (neutrophil gelatinase-associated lipocalin - NGAL)). По сравнению с больными БА MPO мокроты и SP-A плазмы были значительно повышены при СПБАХ, тогда как NGAL мокроты был увеличен у больных СПБАХ по сравнению с больными ХОБЛ. Фу и коллеги [46] исследовали уровни системных маркеров воспаления и IL-6 у больных БА, ХОБЛ и СПБАХ и выявили потенциальные клинические характеристики, которые были связаны с этими биомаркерами. Они обнаружили высокую распространенность системного воспаления у пожилых людей со СПБАХ и повышенный IL-6 по сравнению с больными БА. Было показано, что возраст, коморбидный индекс Чарлсона и IL-6 независимо были связаны со СПБАХ, тогда как IL-6 ассоциировался с обструкцией воздушного потока и сердечно-сосудистыми заболеваниями, предполагая, что он может участвовать в этих двух процессах и поэтому может быть независимой целью лечения [46].
Наследственные детерминанты также активно изучаются при СПБАХ. Генетический анализ больных ХОБЛ выявил несколько вариантов, связанных со СПБАХ, которые могут рассматриваться как факторы риска заболевания [47]. Как было сказано выше, Кристенсен и коллеги [13] исследовалиэкспрессию генов, ассоциированных с БА, в подгруппе больных ХОБЛ. Экспрессия генов ТҺ2-иммунного ответа, которые коррелировали с клиническими характеристиками ТҺ2-воспаления у больных БА, обнаружена приблизительно у 20% больных ХОБЛ. Затем была изучена связь исследуемых генов с клиническими параметрами в группе GLUCOLD (Groningen and Leiden Universities Corticosteroids in Obstructive Lung Disease) больных ХОБЛ. Экспрессия генов, ассоциированных с ТҺ2-ответом, была в значительной степени связана с увеличением количества эозинофилов в тканях, повышением процента сывороточных эозинофилов и повышением бронхолитического ответа. Интересно, что более высокая экспрессия была связана с большим снижением гипервентиляции после лечения ИГКС (с или без в2-агонистов длительного действия) по сравнению с плацебо в течение 30 месяцев [13]. Однако, хотя и были получены многообещающие результаты, на сегодняшний день эти методы пока не используются в качестве диагностического инструмента в лечебных учреждениях и не нашли своего широкого применения в клинической практике.
Возможные терапевтические подходы
В совместном проекте GINA и GOLD «Диагностика заболеваний с хронической обструкцией дыхательных путей: бронхиальная астма, ХОБЛ и БА-ХОБЛ перекрестный синдром» [9] предлагается начинать лечение СПБАХ как БА. Этот подход включает ИГКС (в низких или средних дозах в зависимости от симптомов). Обычно так же добавляются в2- агонисты длительного действия и/или пролонгированные антагонисты мускариновых рецепторов или их сочетание с ИГКС. Следует отметить, если имеются признаки БА, не рекомендуется лечение в2-агонистами без ИГКС. Всем больным с хронической бронхиальной обструкцией рекомендуется отказ от курения, лечение коморбидных состояний, физическая активность, пульмонологическая реабилитация и вакцинация.
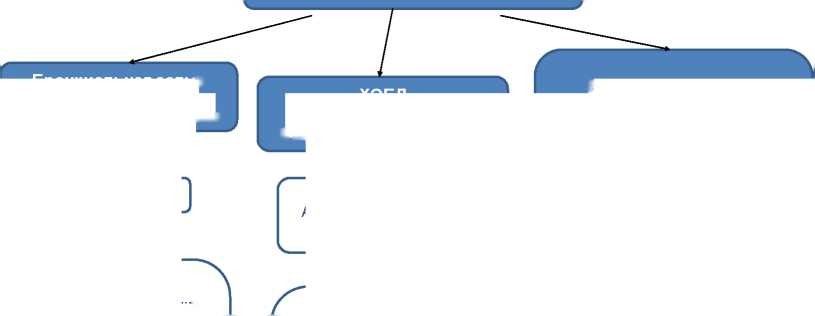
Гетерогенность СПБАХ, связанная с его патофизиологией, подразумевает, что один терапевтический подход нельзя применять ко всем больным СПБАХ. В частности, было предложено три фенотипа СПБАХ [48], которые необходимо установить перед началом терапии: «эозинофильная» ХОБЛ (высокое ТҺ2-воспаление), «нейтрофильная» БА (низкое ТҺ2-воспаление) и «невоспалительная» БА с необратимой бронхиальной обструкцией. Необходимым условием реализации этой стратегии является совершенствование методологии и стандартизация цитологического анализа мокроты. На рисунке 1 представлены терапевтические подходы к лечению СПБАХ в зависимости от трех возможных фенотипов. Эти варианты терапии могли бы обеспечить алгоритм таргетного лечения СПБАХ, связанного с патофизиологией заболевания.
Синдром перекреста бронхиальной
астмыи ХОБЛ




I
Макролиды
Ғ
I
г
л
Бронхиальная астма
ХОБЛ
Без выраженного воспаления
Необратимая обструкция дыхательных путей
Пролонгированные мускариновые антагонисты (тиотропиум)
ИГКС
Анти-ІдЕ-препараты (омализумаб)
Нейтрофильное воспаление
Эозинофильное воспаление
Анти-IL-I терапия,
ингибиторы воспаления
AH™-IL-17/IL-17Ra
препараты (иксекизумаб,
бродалумаб)
Анти-Ш-23, анти-р40
терапия (гуселькумаб)
Антагонисты CXCR2
Ингибиторы p38
MAPK/ингибиторы JAK
Ингибиторы PDE4
(рофлумиласт)
AK^-IL^/IL^Ra препараты
(меполизумаб, реслизумаб,
бенрализумаб),
An^-IL^/IL^Ra
препараты (лебрикизумаб,
тралокинаб, дипилумаб),
Анти-Ш-33^Т2 терапия,
Анти-^-25 терапия,
Анти-TSLP терапия,
Ингибиторы GATA3
(SB010),
Антагонисты CRTH2
Пролонгированные в2-агонисты и
мускариновые антагонисты
(индатерол/гликопирониум,
вилантерол/умеклидиниум)
Бронхиальная термопластика
Тройные ингаляторы
(кортикостероиды/пролонгирован
ные в2-агонисты и мускариновые
антагонисты)
Рисунок 1 - Подходы к терапии различных фенотипов СПБАХ [48]
Ингаляционные кортикостероиды.
Предиктором клинического ответа на ингаляционные кортикостероиды у больных СПБАХ и эозинофильного варианта ХОБЛ может быть повышение количества эозинофилов в мокроте (>3%) или крови (>400/дл), и эти больные могут иметь повышенную обратимость дыхательных путей [42]. Терапия таких больных проводится бронходилататорами и ИГКС. Кроме того, комбинации ингаляционных кортикостероидов и бронходилататоров рекомендуются как при БА, так и при ХОБЛ, что делает их использование при СПБАХ привлекательным. Однако даже высокие дозы пероральных кортикостероидов могут не подавлять маркеры активации эозинофилов и сами эозинофилы у больных ХОБЛ [49]. Это свидетельствует о том, что более специфическая антиэозинофильная терапия может быть более эффективной при резистентности к кортикостероидам.
Анти-IL-5/IL-5Ra терапия
IL-5 стимулирует дифференцировку и созревание эозинофилов в костном мозге, а также их миграцию из крови в ткани [50]. У больных эозинофильной ХОБЛ наблюдается повышение концентрации IL-5 в мокроте, в связи с чем, таргетирование IL-5 может иметь положительный эффект у этих больных. Применение моноклональных антител к IL-5 (меполизумаб и реслизумаб) при тяжелой БА с эозинофилией мокроты, не поддающейся лечению высокими дозами ИГКС или пероральными кортикостероидами, показали сокращение обострений у этих больных [48]. Назначение моноклональных антител к рецептору IL-5 (бенрализумаб) больным с эозинофильной ХОБЛ не привело к значительному уменьшению обострений и симптомов или улучшению функции легких, что, возможно, связано с недостаточно высокой степенью эозинофилии [51]. Таким образом, роль моноклональных антител против IL-5 и IL-5Ra в лечении СПБАХ не достаточно ясна, и в дальнейшем имеется потребность в проведении крупных рандомизированных контролируемых исследований с дифференцированным отбором больных.
Анти-IgE терапия.
Анти-IgE препараты, такие как омализумаб, вызывают блокирование связывания IgE со своим рецептором FccR1 на базофилах и тучных клетках, инициирующее опосредованное цитокинами эозинофильное воспаление. Омализумаб назначается при тяжелой персистирующей, плохо поддающейся лечению БА, и, как было показано, сокращает частоту обострений, госпитализаций, посещений отделений неотложной помощи, уменьшает использование ИГКС и ингаляционных препаратов короткого действия больными БА [1].
Ahtu-IL-ІЗ терапия.
IL-13 - цитокин, секретируемый Т^2-клетками, натуральными киллерами, тучными клетками, базофилами и эозинофилами. Его вторичная структура аналогична структуре IL-4, однако он имеет только 25% гомологичных последовательностей с IL-4 и способен к независимой сигнализации [52]. Его роль в патогенезе БА связана с регуляцией эозинофилов, продукцией слизи, гиперплазией кубического эпителия, сокращением гладкой мускулатуры бронхов и ремоделированием дыхательных путей [53]. Применение моноклональных антител против IL-13 (лебрикизумаба и тралокинаба) при тяжелой персистирующей БА показало улучшение функции легких и снижение частоты обострений [54, 55]. Отмечена высокая эффективность этих препаратов у больных с повышенной концентрацией в сыворотке крови белка внеклеточного матрикса периостина, который депонируется в базальной мембране дыхательных путей астматиков и отражает Th2- воспаление [56]. Роль IL-13 в развитии ХОБЛ в настоящее время не определена, несмотря на то, что он может стимулировать гиперсекрецию слизи и фиброз дыхательных путей, а также индуцировать кортикостероидную резистентность [48].
Лечение антителами, направленными против тимического стромального лимфопоэтина
Тимический стромальный лимфопоэтин (TSLP) - цитокин, высоко экспрессирующийся в эпителиальных клетках дыхательных путей больных БА и стимулирующий дендритные клетки к привлечению Th-2-клеток. Применение блокирующих антител у больных БА способствует защите от аллергенов и уменьшению эозинофилии [57]. У больных ХОБЛ также обнаружена высокая степень экспрессии TSLP в эпителиальных клетках дыхательных путей, но не совсем понятно, как это относится к эозинофильному воспалению [58].
Бронходилататоры.
Ингаляционные бронходилататоры длительного действия, такие как пролонгированные в2-агонисты и мускариновые антагонисты, являются основой лечения больных ХОБЛ [48]. Их действие связано с улучшением бронхиальной проходимости за счет уменьшения тонуса бронхов и снижения динамической гипервентиляции. Больным СПБАХ без явных признаков воспаления рекомендуется назначать бронходилататоры длительного действия на начальных этапах возникновения заболевания [1]. Пролонгированные в2-агонисты обычно оказывают более выраженное бронхолитическое действие на больных БА и СПБАХ, чем на больных ХОБЛ [42]. Это может быть связано с выпускаемыми эозинофилами бронхоконстрикторами, такими как cys-LTs и PGD2, а также с активацией тучных клеток, не характерной для больных с изолированной ХОБЛ. Несколько крупных контролируемых исследований продемонстрировали улучшение ОФВ1 у больных БА как у детей, так и у взрослых при добавлении тиотропия к лечению ингаляционными кортикостероидами и комбинацией ИГКС с пролонгированными антагонистами мускариновых рецепторов [59-61].
Таким образом, исследования показали эффективность применения в2-агонистов длительного действия при ХОБЛ и БА, и это свидетельствует о том, что пролонгированные в2-агонисты могут быть препаратами выбора при лечении больных СПБАХ. Возможность применения других бронхолитиков длительного действия, таких как пролонгированные антагонисты мускариновых рецепторов при СПБАХ требует дальнейших исследований.
Макролиды.
Плейотропные свойства макролидов, которые используются одновременно как антибактериальные, иммуномодулирующие и противовоспалительные препараты, привели к широкому применению их при нейтрофильных респираторных заболеваниях, таких как ХОБЛ, кистозный фиброз и бронхоэктатическая болезнь. Макролиды, по-видимому, ослабляют действие IL-8 и CXCL1, что приводит к апоптозу нейтрофилов и уменьшению окислительного стресса. Отмечено, что длительное применение эритромицина и азитромицина при ХОБЛ уменьшает частоту обострений заболевания [62, 63].
Назначение кларитромицина больным тяжелой БА, носителям Mycoplasma pneumoniae и Chlamydia pneumoniae, приводило к значительному улучшению ОФВ1. Однако другое, более крупное исследование применения кларитромицина при плохо контролируемой БА не показало клинически значимого улучшения состояния больных, хотя обнаруживалось значительное снижение гиперреактивности дыхательных путей [64].
Заключение.
На современном этапе СПБАХ рассматривается как отдельный клинический фенотип, включающий БА и ХОБЛ, характеризующийся выраженными респираторными симптомами и частыми эпизодами обострений и госпитализаций. Диагноз СПБАХ рекомендуется предполагать у всех пациентов в возрасте старше 40 лет с персистирующей обструкцией дыхательных путей, историей табакокурения или воздействия продуктов сгорания биотоплива, а также с наличием БА или выраженной обратимости дыхательных путей в ответ на бронходилятаторы при спирометрии [1]. Хотя механизмы развития СПБАХ еще полностью не выяснены, вероятно, существуют несколько путей, при которых у больных ХОБЛ может возникнуть обструкция с эозинофильным воспалением дыхательных путей, у больных БА может развиться нейтрофильная дыхательная обструкция, а у некоторых больных БА может сформироваться необратимая обструкция с отсутствием выраженного воспаления. Интерес к стратификации таких пациентов заключается в их дифференцированном ответе на разные группы лекарственных препаратов. Более глубокое изучение синдрома перекреста БА и ХОБЛ с исследованием его патогенетических механизмов, особенностей воспалительного процесса, клинического течения, ответа на медикаментозную терапию будет способствовать прояснению многих вопросов его дифференциальной диагностики и таргетной терапии.
СПИСОК ЛИТЕРАТУРЫ
- Leung J. M, Sin D. D. Asthma-COPD overlap syndrome: pathogenesis, clinical features, and therapeutic targets // BMJ. - 2017. - №358(3772). - P. 1-14.
- Tho N. V., Park H. Y. and Nakano Y. Asthma-COPD overlap syndrome (ACOS): A diagnostic challenge // Respirology. - 2016. - №21. - Р. 410-418.
- GIFA URL: http://ginasthma.org/asthma-copd-and-asthma-copd-overlap-svndrome-ACOS
- Nielsen M., Barnes C.B., Ulrik C.S. Clinical characteristics of the asthma-COPD overlap syndrome - a systematic review // International Journal of Chronic Obstructive Pulmonary Disease. - 2015. - Vol.10. - P.1443-1454.
- Rhee C.K., Yoon H.K., Yoo K.H., et al. Medical utilization and cost in patients with overlap syndrome of chronic obstructive pulmonary disease and asthma // COPD. - 2014. - Vol.11(2). - P. 163-170.
- Kauppi P., Kupiainen H., Lindqvist A., Tammilehto L., Kilpelainen M., Kinnula V.L., Haahtela T. Overlap syndrome of asthma and COPD predicts low quality of life // JAsthma. - 2011. - Vol.48(3). - P. 279-285.
- Woodruff P.G., van den Berge M., Boucher R.C., et al. American Thoracic Society/National Heart, Lung, and Blood Institute AsthmaChronic Obstructive Pulmonary Disease Overlap Workshop Report // Am J Respir Crit Care Med. - 2017. - №196. - Р. 375-381.
- Barrecheguren M., Esquinas C. and Miravitlles M. The asthma-COPD overlap syndrome: a new entity? // COPD Research and Practice. - 2015. - №1. - Р. 8-16.
- Barnes P.J. Against the Dutch hypothesis: asthma and chronic obstructive pulmonary disease are distinct diseases // Am J Respir Crit Care Med. -2006. -№174. - Р. 240-243.
- Kraft M. Asthma and chronic obstructive pulmonary disease exhibit common origins in any country // Am J Respir Crit Care Med. - 2006. - №174. - Р. 238-240.
- Hodge G., Nairn J., Holmes M., Reynolds P.N., Hodge S. Increased intracellular T helper 1 proinflammatory cytokine production in peripheral blood, bronchoalveolar lavage and intraepithelial T cells of COPD subjects // Clin Exp Immunol. - 2007. - №150. - Р. 22-29.
- Christenson S.A., Steiling K., van den Berge M., et al. Asthma-COPD overlap. Clinical relevance of genomic signatures of type 2 inflammation in chronic obstructive pulmonary disease // Am J Respir Crit Care Med. - 2015. - №191. - Р. 758-766.
- Bafadhel M., McKenna S., Terry S., et al. Blood eosinophils to direct corticosteroid treatment of exacerbations of chronic obstructive pulmonary disease: a randomized placebo-controlled trial // Am J Respir Crit Care Med. - 2012. - №186. - Р. 48-55.
- Ghebre M.A., Bafadhel M., Desai D., et al. Biological clustering supports both “Dutch” and “British” hypotheses of asthma and chronic obstructive pulmonary disease // J Allergy Clin Immunol. -2015. - №135. - Р. 63-72.
- Thomson N.C., Chaudhuri R., Livingston E. Asthma and cigarette smoking // Eur Respir J. - 2004. - №24. - Р. 822-833.
- Chung J.W., Kong K.A., Lee J.H., Lee S.J., Ryu Y.J., Chang J.H. Characteristics and self-rated health of overlap syndrome // Int J Chron Obstruct Pulmon Dis. - 2014. - №9. - Р. 795-804.
- Kumbhare S., Pleasants R., Ohar J.A., Strange C.. Characteristics and Prevalence of Asthma/Chronic Obstructive Pulmonary Disease Overlap in the United States // Ann Am Thorac Soc. - 2016. - №13. - Р. 803-810.
- Aanerud M., Carsin A.E., Sunyer J., Dratva J., Gislason T., Jarvis D., de Marco R., Raherison C., Wjst M., Dharmage S.C. et al. Interaction between asthma and smoking increases the risk of adult airway obstruction // Eur. Respir. J. - 2015. - №45. - Р. 635-643.
- Tamimi A., Serdarevic D., Hanania N.A. The effects of cigarette smoke on airway inflammation in asthma and COPD: therapeutic implications // Respir. Med. - 2012. - №106. - Р. 319-328.
- Siew LQC, Wu S.Y., Ying S., Corrigan C.J. Cigarette smoking increases bronchial mucosal IL-17A expression in asthmatics, which acts in concert with environmental aeroallergens to engender neutrophilic inflammation // Clin Exp Allergy. .- 2017. - №47. - Р. 740-750.
- Ravensberg A.J., Slats A.M., van Wetering S., et al. CD8(+) T cells characterize early smoking-related airway pathology in patients with asthma // Respir Med. - 2013. - №107. - Р. 959-966.
- den Otter I., Willems L.N., van Schadewijk A., et al. Lung function decline in asthma patients with elevated bronchial CD8, CD4 and CD3 cells // Eur Respir J. - 2016. - №48. - Р. 393-402.
- Boulet L.P., Turcotte H., Turcot O., Chakir J. Airway inflammation in asthma with incomplete reversibility of airflow obstruction // Respir Med. - 2003. - №97. - Р. 739-744.
- Broekema M., ten Hacken N.H., Volbeda F., Lodewijk M.E., Hylkema M.N., Postma D.S., Timens W. Airway epithelial changes in smokers but not in ex-smokers with asthma // Am. J. Respir. Crit. Care Med. - 2009. - №180. - Р. 1170-1178.
- Gibson P.G., McDonald V.M., Marks G.B. Asthma in older adults. Lancet. - 2010. - №376. - Р. 803-813.
- Beigelman A., Weinstock G. M., and Bacharier L. B. The relationships between environmental bacterial exposure, airway bacterial colonization, and asthma // Current Opinion in Allergy and Clinical Immunology. - 2014. - Vol. 14. - № 2. - P. 137-142.
- Green B. J., Wiriyachaiporn S., Grainge C. et al.,“Potentially pathogenic airway bacteria and neutrophilic inflammation in treatment resistant severe asthma // PloS One. - 2014. - vol. 9, №6. - Р. 104-113.
- Essilfie A. T., Simpson J. L., Horvat J. C. et al. Haemophilus influenzae infection drives IL-17-mediated neutrophilic allergic airways disease // PLoS Pathogens. - 2011. - Vol. 7., №10. - Р. 45-52.
- Kobayashi Y., Wada H., Rossios C. et al. A novel macrolide/fluoroketolide, solithromycin (CEM-101), reverses corticosteroid insensitivity via phosphoinositide 3-kinase pathway inhibition // British Journal of Pharmacology. - 2013. - Vol. 169., №5. - P. 1024-1034.
- Xu X., Gera N., Li H. et al. GPCR-mediated PLCbetagamma/PKCbeta/PKD signaling pathway regulates the cofilin phosphatase slingshot 2 in neutrophil chemotaxis // Molecular Biology of the Cell. -2015. - Vol. 26. -№ 5. - Р. 874-886.
- Alam R., Good J., Rollins D. et al. Airway and serum biochemical correlates of refractory neutrophilic asthma // The Journal of Allergy and Clinical Immunology. - 2017. - №9. - Р. 369-378.
- Mauad T., Dolhnikoff M. Pathologic similarities and differences between asthma and chronic obstructive pulmonary disease // Curr. Opin. Pulm. Med. - 2008. - №14. - Р. 31-38.
- Gelb A.F., Yamamoto A., Verbeken E.K., Nadel J.A. Unraveling the Pathophysiology of the Asthma-COPD Overlap Syndrome: Unsuspected Mild Centrilobular Emphysema Is Responsible for Loss of Lung Elastic Recoil in Never Smokers With Asthma With Persistent Expiratory Airflow Limitation // Chest. - 2015. - №148. - Р. 313-320.
- Ingram J.L., Slade D., Church T.D., et al. Role of Matrix Metalloproteinases-1 and -2 in Interleukin-13-Suppressed Elastin in Airway Fibroblasts in Asthma // Am J Respir Cell Mol Biol. - 2016. - №54. - Р. 41-50.
- McDonough J.E., Yuan R., Suzuki M., et al. Small-airway obstruction and emphysema in chronic obstructive pulmonary disease // N Engl J Med. - 2011. - №365. - Р. 1567-1575.
- Barrecheguren M., Esquinas C. and Miravitlles M. The asthma-COPD overlap syndrome: a new entity? // COPD Research and Practice. - 2015. - №1. - Р. 8-16.
- Tashkin D.P., Celli B., Decramer M., Liu D., Burkhart D., Cassino C., et al. Bronchodilator responsiveness in patients with COPD // Eur Respir J. - 2008. - №31. - Р. 742-750.
- Louie S., Zeki A.A., Schivo M., Chan A.L., Yoneda K.Y., Avdalovic M., et al. The asthma-chronic obstructive pulmonary disease overlap syndrome: pharmacotherapeutic considerations // Expert Rev Clin Pharmacol. - 2013. - №6. - Р. 197-219.
- Papaiwannou A., Zarogoulidis P., Porpodis K., Spyratos D., Kioumis I., Pitsiou G., et al. Asthma-chronic obstructive pulmonary disease overlap syndrome (ACOS): current literature review // J Thorac Dis. - 2014. - №6. - Р. 146-151.
- Marin J.M., Ciudad M., Moya V., Carrizo S., Bello S., Piras B., et al. Airflow reversibility and long-term outcomes in patients with COPD without comorbidities // Respir Med. - 2014. - №108. - Р. 1180-1188.
- Papi A., Romagnoli M., Baraldo S., Braccioni F., Guzzinati I., Saetta M., et al. Partial reversibility of airflow limitation and increased exhaled NO and sputum eosinophilia in chronic obstructive pulmonary disease // AM J Respir Crit Care Med. - 2000. - №162. - Р. 1773-1777.
- Chou K.T., Su K.C., Huang S.F., Hsiao Y.H., Tseng C.M., Su V.Y., et al. Exhaled nitric oxide predicts eosinophilic airway inflammation in COPD // Lung. - 2014. - №192. - Р. 499-504.
- Pascoe S., Locantore N., Dransfield M., Barnes N.C., Pavord I.D. Blood eosinophil counts, exacerbations and response to the addition of inhaled fluticasone furoate to vilanterol in patients with chronic obstructive pulmonary disease: a secondary analysis of data from two parallel randomized controlled trials // Lancet Respir Med. - 2015. - №7. - Р. 634-643.
- Iwamoto H., Gao J., Koskela J., Kinnula V., Kobayashi H., Laitinen T., et al. Differences in plasma and sputum biomarkers between COPD and COPDasthma overlap // Eur Respir J. - 2014. - №43. - Р. 421-429.
- Fu J.J., McDonald V., Gibson P., Simpson J.L. Systemic inflammation in older adults with Asthma-COPD overlap syndrome // Allergy Asthma Immunol Res. - 2014. - №6(4). - Р. 316-324.
- Hardin M., Cho M., McDonald M-L, Beaty T., Ramsdell J., Bhatt S., et al. The clinical and genetic features of COPD-asthma overlap syndrome // Eur Respir J. - 2014. - №44. - Р. 341-350.
- Barnes P. J. Therapeutic approaches to asthma-chronic obstructive pulmonary disease overlap syndromes // J Allergy Clin Immunol. - 2015. - V. 136., №3. - Р. 45-57.
- Keatings V.M., Jatakanon A., Worsdell Y.M., Barnes P.J. Effects of inhaled and oral glucocorticoids on inflammatory indices in asthma and COPD // Am J Respir Crit Care Med. - 1997. - №155. - Р. 542-548.
- Varricchi G., Bagnasco D., Borriello F., Heffler E., Canonica G.W. Interleukin-5 pathway inhibition in the treatment of eosinophilic respiratory disorders: evidence and unmet needs // Curr Opin Allergy Clin Immunol. -2016. - №16. - Р. 186-200.
- Brightling C.E., Bleecker E.R., Panettieri R.A Jr, Bafadhel M., She D., Ward C.K., et al. Benralizumab for chronic obstructive pulmonary disease and sputum eosinophilia: a randomised, double-blind, placebo-controlled, phase 2a study // Lancet Respir Med. - 2014. - №2. - Р. 891-901.
- Rael E.L., Lockey R.F. Interleukin-13 signaling and its role in asthma // The World Allergy Organization Journal. - 2011. - №4 (3). - Р. 5464.
- Nixon J., Newbold P., Mustelin T., Anderson G.P., Kolbeck R. Monoclonal antibody therapy for the treatment of asthma and chronic obstructive pulmonary disease with eosinophilic inflammation // Pharmacol Ther. - 2017. - №169. - Р. 57-77.
- Hanania N.A., Noonan M., Corren J., et al. Lebrikizumab in moderateto-severe asthma: pooled data from two randomised placebocontrolled studies // Thorax. - 2015. - №70. - Р. 748-756.
- Brightling C.E., Chanez P., Leigh R., et al. Efficacy and safety of tralokinumab in patients with severe uncontrolled asthma: a randomised, double-blind, placebo-controlled, phase 2b trial // Lancet Respir Med. - 2015. - №3. - Р. 692-701.
- Izuhara K., Ohta S., Ono J. Using Periostin as a Biomarker in the Treatment of Asthma // Allergy Asthma Immunol Res. - 2016. - №8. - Р. 491-498.
- Gauvreau G.M., O'Byrne P.M., Boulet L.P., Wang Y., Cockcroft D., Bigler J., et al. Effects of an anti-TSLP antibody on allergen-induced asthmatic responses // N Engl J Med. - 2014. - №370. - Р. 2102-2110.
- Ying S., O'Connor B., Ratoff J., Meng Q., Fang C., Cousins D., et al. Expression and cellular provenance of thymic stromal lymphopoietin and chemokines in patients with severe asthma and chronic obstructive pulmonary disease // J Immunol. - 2008. - №181. - Р. 2790-2798.
- Kerstjens H.A., Moroni-Zentgraf P., Tashkin D.P., et al. Tiotropium improves lung function, exacerbation rate, and asthma control, independent of baseline characteristics including age, degree of airway obstruction, and allergic status // Respir Med. - 2016. - №117. - Р. 198-206.
- Szefler S.J., Murphy K., Harper T. 3rd, et al. A phase III randomized controlled trial of tiotropium add-on therapy in children with severe symptomatic asthma // J Allergy Clin Immunol. - 2017. - №6749(17). - Р. 302-318.
- Hamelmann E., Bernstein J.A., Vandewalker M., et al. A randomized controlled trial of tiotropium in adolescents with severe symptomatic asthma // Eur Respir J. - 2017. - №49. - Р.160-175.
- Albert R.K., Connett J., Bailey W.C., et al. COPD Clinical Research Network. Azithromycin for prevention of exacerbations of COPD // N Engl J Med. - 2011. - №365. - Р. 689-698.
- Ni W., Shao X., Cai X., Wei C., Cui J., Wang R., et al. Prophylactic use of macrolide antibiotics for the prevention of chronic obstructive pulmonary disease exacerba- tion: a meta-analysis // PLoS One. - 2015. - №10. - Р. 96-105.
- Sutherland E.R., King T.S., Icitovic N., Ameredes B.T., Bleecker E., Boushey H.A., et al. A trial of clarithromycin for the treatment of suboptimally controlled asthma // J Allergy Clin Immunol. - 2010. - №126. - Р. 747-753.