В статье предоставлен аналитический обзор современной литературы о старении и возможности его замедления. В качестве мишени для снижения рискавозраст-ассоциированной патологии был описан процесс аутофагии. Собраны и описаны основные существующие геропротекторы. Так же рассказывается о полифенольных соединениях, которые могут использоваться как потенциальные геропротекторы. Описываются наиболее перспективные препараты, воздействующие на процессы аутофагии, рапамицин и метформин.
Программированная клеточная гибель - это активная форма клеточной смерти, являющаяся результатом реализации ее генетической программы или ответом на внешние сигналы и требующая затрат энергии и синтеза макромолекул denovo в составе программированной клеточной гибели (ПКГ) выделяют несколько типов: апоптоз, аутофагическая гибель (аутофагия) и программированный некроз [1].Аутофагия в нормальной клетке - способ обновления органелл [2].
Термин аутофагия происходит от греческого слова, означающего «самопоедание». Аутофагия является высококонсервативным катаболическим механизмом, который опосредует деградацию поврежденных клеточных компонентов, индуцируя их слияние с лизосомами. Этот процесс обеспечивает клетки альтернативным источником энергии для синтеза новых белков и поддержания метаболического гомеостаза в стрессовых ситуациях. Естественно, что аутофагия представляет собой сложный и строго регулируемый процесс, который доставляет клеточный материал в лизосомы для деградации, последующей рециркуляции и появлению новой генерации молекул, которые способствуют клеточному метаболизму. При аутофагической гибели деятельность аутофагосом и лизосом ведет к тому, что в клетке перевариваются практически все мембранные органеллы. Активированные нуклеазы фрагментируют ДНК ядра, но не на олигонуклеосомные фрагменты, как это происходит при апоптозе. Аутофагический тип гибели называют также лизосомной клеточной смертью. Аутофагическая гибель отличается следующими признаками: 1) частичная конденсация хроматина; 2) иногда пикноз ядра; 3) отсутствие фрагментации ядра и клетки на поздних стадиях гибели; 4) отсутствие деградации ДНК до нуклеосомного уровня; 5) увеличение числа аутофагосом и аутофаголизосом; 6) увеличение лизосомной активности; 7) увеличение протяженности аппарата Гольджи и иногда расширение цистерн эндоплазматического ретикулума; 8) длительная сохранность микротрубочек и промежуточных филаментов; 9) иногда возрастание проницаемости митохондрий; 10) отсутствие активации каспаз. В конечном итоге остается клеточный дебрис - остаток клетки, окруженный плазматической мембраной, который фагоцитируется макрофагами [3].
|
Органеллы |
Тип I (апоптотический) |
Тип II (аутофагический) |
|
Ядро |
Конденсация хроматина Пикноз ядра Ядерная фрагментация |
Частичная конденсация хроматина. Иногда пикноз ядра. Ядро остается неизменным до поздних стадий |
|
Цитоплазма |
Цитоплазма конденсирована Потеря рибосомы из эндоплазматического ретикулума Фрагментация на апоптотические тела Вероятно, выделение лизосомальных протеаз в цитозоль Часто признаки увеличения митохондриальной проницаемости Каспазы активны. |
Увеличенное число аутофагических везикул Увеличенное число автолизосом. Повышенная лизосомальная активность. Увеличение Гольджи, иногда дилатация эндоплазматического ретикулума Может быть увеличена митохондриальная проницаемость. Каспазы не реагируют. |
|
Клеточная мембрана |
Пузырчатая |
Пузырчатая |
|
Клеточный клиренс |
Гетерофагия другими клетками |
Поздняя и случайная гетерофагия другими клетками |
|
Методы исследования |
Электронная микроскопия Определение наличия Ядерной / клеточной фрагментации. Тесты активации каспазы Тесты на расщепление субстрата каспазы Определение ДНК-лестницы Окрашивание TUNEL) Увеличение популяции клеток подгруппы G1, оцененное при FACS Анализе Annexin V тест |
Электронная микроскопия Тест на увеличение деградации белка Тест на наличие повышенной лизосомальной активности (MDC, окрашивание акридином оранжевым или лизотреккерокрашивание и т. д.) Тест на усиление секвестрации цитоплазмы (LDH или тесты на секвестрацию сахарозы). Обнаружение рекрутирования LC3 в аутофагические мембраны (сдвиг полосы белка или изменение внутриклеточной локализации). |
Taблица 1 -
й клеточной гибели
типов п
м
Аутофагия и апоптоз при клеточном старении. В большинстве случаев, аутофагия способствует выживанию клеток путем адаптации клеток к условиям стресса. В этом контексте парадоксально, что механизм аутофагиипредставляет из себя также не-апоптотическую программу клеточной гибели, которую называют "autophagic"или" тип-II' клеточной смертью. Это основано на том, что некоторые случаи гибели клеток сопровождаются массовой аутофаговойвакуолязацией. Тем не менее, эти морфологические наблюдения не могут показать, сопровождается ли смерть клетки формированием аутофаговых вакуолей или клеточная гибель действительно осуществляется путём аутофагии.
В самом деле, отношения между аутофагией и апоптозом являются сложными, и именно то, что определяет, погибнет ли клетка путем апоптоза или по другому механизму по- прежнему остаётся неясным. В некоторых клеточных системах, аутофагия является единственным механизмом гибели, действуя в качестве резервного механизма исполнение смертного приговора, когда апоптоз в клетке просто заингибирован. И наоборот, если в процессе клеточного голодания заблокировать процесс аутофагии (например, припомощи малых интерферирующих РНК), то инициируется программа апоптоза. В опухолевых клетках клеточных линий при воздействии на них цитотоксическими веществами, клетки предпочитают аутофагию, избегая апоптоз и клеточное старения [4].
Опять же, белок p53 был определен в качестве одного из главных регуляторов определяющего направление, по которому пойдёт клетка. В стареющих и постмитотических клетках, аутофагия служит в качестве механизма адаптации к стрессу. Было показано, что аутофагосомы накапливаются в стареющих фибробластах в целях содействия обновлению веществ цитоплазмы и её органелл. Точно так же в кардиомиоцитах, оптимальное функционирование митохондрий зависит от макро-аутофагии. Работа одного типа аутофагии - CMA - снижается с возрастом, что увеличивает риск дегенерации нейронов, связанный с накоплением подверженных к аггрегации мутантных белков. Следует отметить, что нейродегенеративные заболевания, связанные с возрастом, имеют схожие характеристики с патологиями, вызванных нокаутом генов, связанных с аутофагией (atg) в головном мозге, такими как накопление убиквитинированных белков и телец включения в цитоплазме, увеличение апоптоза в нейронах и постепенная потеря нейрональных клеток.
Недостаток питательных веществ является наиболее часто используемым способом индуцированияаутофагии в культивируемых клетках, и действительно аутофагия это механизм, с помощью которого одноклеточные организмы (например, дрожжевые клетки), а также клетки млекопитающих могут адаптироваться к истощающимся ресурсам. В ходе деградации макромолекул высвобождается АТФ, что позволяет скомпенсировать отсутствие внешних источников питания. Важно отметить, что эта способность аутофагии может участвовать в продлении жизни организма за счёт ограничения в калорийности питания. Голодание или диетическое ограничение являются одним из сильнейших стимулов для запуска аутофагии по всему организму у мышей и нематод C.elegans. В интересном исследовании было показано, что выключение atg генов в C. elegansотмeнили эффекты противостарения, которые наблюдались у особей в ходе ограничения калорий. Точный механизм, посредством которого аутофагия уменьшает старение, далеко не ясен. Тем не менее, можно предположить, что регулярное обновление цитоплазматических структур и молекул "очищает" и тем самым омолаживает клетки. Кроме того, аутофагия играет важную роль в поддержании стабильности генома посредством механизмов, которые еще не изучены. Таким образом, общее увеличение уровня аутофагии может помочь избежать долгосрочных последствий повреждений ДНК, гипотеза, которая требует дальнейшего изучения [5].
Аутофагия важна для нормальной физиологии клеток и организма, а как увеличение, так и уменьшение аутофагии связано с отклонением от состояния нормального течения гомеостатических процессов [6]. В частности,интенсивность течения аутофагии меняется в процессе старения клеток и организма [7]. Есть предположения, что аутофагия защищает от возраст-ассоциированных болезней, таких как диабет типа 2 или метаболический синдром, нейродегенеративные расстройства, типа болезни Альцгеймера, болезни Паркинсона или болезни Хантингтона, иммунных/воспалительных заболеваний, и наконец, - от рака, опосредуя свое влияние через как врожденные, так и адаптивные иммунные ответы [8].Соответственно, есть основания полагать, что модуляция аутофагии может иметь терапевтический потенциал при таких нарушениях и состояниях [9].В то же время если, как признано, аутофагия полноценно регулирует клеточный гомеостаз во время развития и в молодости, то появляется все больше свидетельств того, что аутофагия становится дисфункциональной в позднем возрасте [10]. Так, результаты работ на Caenorhabditiselegans даже дают основания предполагать, что дисфункциональная аутофагия в позднем возрасте имеет пагубные последствия, которые и приводят собственно к процессу ускорения старения [11, 12]. Другие исследования связывают повышенную аутофагию с долголетием и отсутствием возраст- ассоциированных болезней[13].
Нобелевская премия профессору YoshinoriOhsumiв 2016 году за работу по пониманию механизмов аутофагииподчеркивает признание этого процесса для физиологии и медицины. Действительно, преднамеренное манипулирование аутофагами (стимуляция и подавление), было предложено для многих различных заболеваний [14,15,16,17], а продолжающиеся клинические испытания (более 50 клинических исследований) в основном сосредоточенны на попытке воздействия на аутофагию при лечении рака [16].
Кроме того, известно, что многие из препаратов, которые используются всовременной фармакотерапии, могут влиять на аутофагию, индуцируя или ингибируя течение аутофагии [18].
Все это значит, что принципиально имеется возможность манипулировать течением аутофагии.
В данном обзоре обсуждаются некоторые важные проблемы, которые необходимо решить в процессе дальнейших исследований аутофагии в экспериментальных условиях, например при скрининге anti-aging потенциала биологически активных субстанций по способности активировать и/или ингибировать аутофагию.
Схематически классический вид аутофагии представлен на рисунке в соответствии с публикацией Zhi X и соавт [19].
Рассматривая вводные общие положения относительно аутофагии, считаем нужным указать, что аутофагия считается эволюционно закрепленным клеточным катаболическим процессом, который облегчает рециркуляцию поврежденных белков и органелл [20]. Во времяаутофагии, дисфункциональный белок или органеллы секвестрируются в двух мембранный везикул, известных как аутофагосомы. Аутофагомы, называемые фагофорами или изолирующими мембранами, могут быть получены из плазматических мембран, аппарата гольджи, митохондрий и эндоплазматического ретикулума. Классически аутофагия индуцируется ситуацией отсутствия или снижения поступления питательных веществ к клетке, что сопровождается торможением у млекопитающих mTOR, которой обеспечивает набор UNC-51-подобного киназного комплекса (ULK) из цитозоля в изолирующую мембрану. Это приводит к накоплению на мембране комплекса ATG14, белков Beclin 1 и VPS15, III phosphatidylinositol-3-OH киназ (PI(3)K) и VPS34 комплексов. Дополнительно такие белки как Ambra 1, DFCP, ATG9, WIPI также поступают в аутофагосомы [20].
ER membrane Phagophore Autophagosome
Рисунок 1 - Схематическое изображение аутофагического процесса
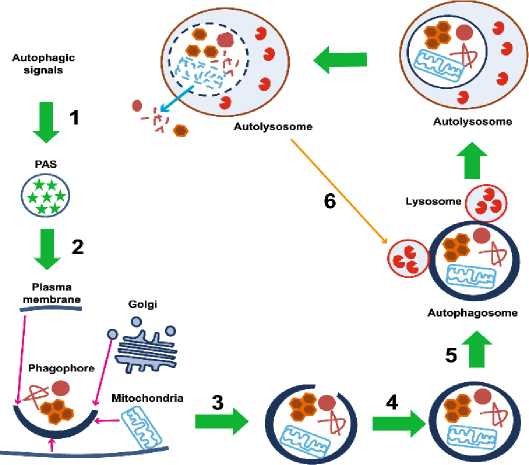
Как следует из рисунка 1, как только аутофагосома сформирована, она должна доставить свой груз к лизосоме. По достижении цели, наружная мембрана аутофагосомы будет сливаться с лизосомальной мембраной. Продукт слияния аутофагосом и лизосом в клетках млекопитающих называется аутолисосомой [21]. Под воздействием кислого содержимого и резидентных гидролаз лизосомы содержимое аутолисосом деградирует и составные части экспортируются обратно в цитоплазму с помощью лизосомныхпермеаз [22,23].
Вообще для клеток млекопитающих выделяют три основных типа аутофагии: микроаутофагия, макроаутофагия и опосредованная шаперонами аутофагия [24]. В то время как каждый из указанных типов морфологически специфичен, все три завершаются доставкой субстрата (избыточно присутствующих в клетке органелл и их продуктов) в лизосому для деградации и после рециркуляции расщепленных компонентов, что и представлено схематично на рисунке 1 в соответствии с данными работы [25].Макроаутофагия приводит к деградации долгоживущих цитозольных белков и органелл после их слияния с лизосомой и аутофагосом, которая поглощает субстрат. В микроаутофагии субстраты непосредственно поглощаются вакуольной мембраной и затем деградируют. Микроатофагия может наблюдаться у некоторых видов растений во время прорастания семян для деградации крахмальных гранул и хранения белков. Во время опосредованной шаперонамиаутофагии целевые субстраты отбираются в зависимости от шаперона и переносятся на лизосому для деградации.
Из трех типов аутофагии наиболее хорошо изучена макроавтофагия. Макроаутофагия происходит на относительно низком уровне рутинно, но может быть дополнительно индуцирована в условиях стресса, таких как питательное или энергетическое голодание, для деградации цитоплазматического материала в метаболиты, которые могут быть использованы в процессах биосинтеза или производства энергии, что позволяет выживать клеткам [26].
При нормальных условиях роста макроаутофагия помогает в поддержании стабильного состояния клетки, разрушая поврежденные или лишние органеллы [27]. Таким образом, макроаутофагия является прежде всего цитопротективныммеханизмом, однако чрезмерная активность или угасание активности аутофагии может быть связано с различной патологией человека, включая возраст- ассоциированные болезни и собственно процесс старения [28].Основным негативным регулятором макроаутофагии является киназаmTOR, которая, как правило, запускает базовое образование аутофагосом, но ее ингибирование (например, при помощи рапамицина при отсутствии питательных веществ - состояние сниженной калорийности - CR) запускает макроаутофагию. Подавление mTOR активности способствует ферментативной активации мультипротеинового комплекса, который формируется из III phosphatidylinositol 3-киназы (PI3K), белка вакуолярной сортировки 34 (Vps34), Beclin 1, белка вакуолярной сортировки 15 (Vps15), белка резистентности к УФ- излучению (UVRAG), endophilin B1 (Bif-1), молекулы активации Beclin-1-зависимой аутофагии (Ambra 1) и, возможно, другие белки. Этот комплекс негативно регулируются белками Bcl-2 / X L. Vps34 производит фосфатидилинозитол - 3-фосфат, молекулярный сигнал для сборки аутофаговых комплексов формирующим удлинение и закрытие везикул. Процесс макроаутофагии можно заингибировать по пути insulin/IGF-1, где PI3K продуцируют phosphatidylinositol - 3,4,5-trisphosphate, которые стимулируют функцию mTOR.
Возможное интегративное значение аутофагии в процессах старения, воспаления и накопления свободных радикалов (ROS) кажется вполне вероятным. Предполагается, что в молодом возрасте поддержание врожденной физиологической продолжительности жизни происходит через различные механизмы: в первую очередь, - посредством аутофагии, связывания в митохондриях свободных радикалов (mROS) и угнетения предиктора воспаления NLRP3 что приводит к уменьшению воспаления, тогда как снижение аутофагии во время старения приводит к увеличению биомаркеров воспаления и накоплению mROS [20].
Имеются достаточно указаний на то, что аутофагическая способность дисфункциональна при возрастных заболеваниях. Особенно важно подчеркнуть, что интенсивность аутофагии снижается со старением, при этом активируется NLRP3 и усиливается процесс воспаления. Соответственно можно сделать логическое заключение, что снижение активности NLRP3 и увеличение активности аутофагии могут продлить срок жизни. Например, повышение эффективности функция аутофагического поглощения и переваривания дисфункциональных митохондрий приводит к уменьшению окислительного стресса, а снижение активности NLRP3, имеет решающее значение для поддержания клеточного гомеостаза. Можно видеть растущее число доказательств того, что некоторые продукты, содержащие природные соединения, такие как ресвератрол, катехины, EGCG, экстракты прополиса, креозол и лютеолозиддействуют как анти-aging молекулы [29]. Существует предположение, что диетическое потребление этих соединений может способствовать здоровью и продлевать продолжительность жизни с помощью множества механизмов, включая снижение окислительного стресса, индукцию аутофагии и подавление активации NLRP3.
Микроаутофагия относится к процессу, посредством которого цитоплазматическое содержимое входит в лизосому через инвагинацию или деформацию лизосомной мембраны [30]. Показано, что с помощью микроаутофагиипроисходит перенос растворимых цитозольных белков в лизосомы с помощью эндосомных мультивезикулярных тел [31].
Шаперон-опосредованный тип аутофагиидо сих пор был описан только в клетках млекопитающих. В отличие от микроаутофагии и макроаутофагии, при которых может происходить неспецифическое объемное поглощение цитоплазмы, этот тип имеет высокую специфичность. Субстраты шаперон-опосредованного типа аутофагии представляют собой пентапептид, биохимически связанный с KFERQ [32]. Считается, что ~ 30% цитозольных белков содержат такую последовательность [33]. Целевые белки, содержащие консенсусный мотив KFERQ, разворачиваются посредством действия цитозольныхшаперонов и транслоцируются непосредственно через лизосомальную мембрану, а деградируют в просвете лизосомы [34].
Заявление о том, что стимуляцияаутофагии замедляет старение и увеличивает продолжительность жизни зиждется на экспериментальных доказательствах. Первое указание на то, что стимуляция аутофагии может способствовать удлинению жизни было получено из наблюдения за C. elegans, у которых ингибирование инсулиноподобного фактора роста, сопровождающееся повышением активности аутофагии, приводит к увеличению продолжительности жизни [35].
Феномен, известный как снижение калорийности - CR,можно считать наиболее физиологическим индуктором аутофагии [36], а ингибирование аутофагии предотвращает эффект анти-старения CR у всех исследованных видов. Предполагается, что CR индуцирует аутофагию через активацию AMPK [37,38] и Sirtuin 1 (SIRT1), которые сопряжены и участвуют в так называемой положительной петле взаимной активации [39]. Кроме того, установлено того, CR может индуцировать аутофагию посредством ингибирования передачи сигналов по пути инсулина / инсулиноподобного фактора роста (IGF), в этом случае параллельно также происходит торможение TOR [40].
Как SIRT1 запускает аутофагию, не совсем ясно. SIRT1 является NAD + -зависимой деацетилазой, действующей как в ядре, так и в цитоплазме [41]. Цитоплазматический вариант SIRT1 столь же эффективен, как и SIRT1 ядра, это объясняет, например,индуцированиеаутофагии с помощью ресвератрола в условиях энуклеации клеток, [42]. Соответственно, если SIRT1 деацетилирует несколько белковых продуктов гена (ATG5, ATG7 иATG8 / LC3) [43], то и ресвератрол индуцирует деацетилирование более чем десятка цитоплазматических белков. SIRT1 также деацетилирует транскрипционные факторы р53, NF-kB, HSF1, FOXO1, -3, -4 и PGC1a, для которых известны эффекты в регулировании продолжительности жизни [44].
Аутофагия играет важную роль в гомеостазе протеинов органелл. Эта роль особенно важна в непролиферирующих клетках, потому что в отличие от клеток в фазе митоза не существует «разбавления» внутриклеточного мусора при делении. Кроме того, антивозрастные эффекты цитопротекции особенно важны для клеток, которые не являются мишенями стволовых клеток. Агрегация внутриклеточных белков является кардинальными особенности многих нейродегенеративных заболеваний, называемых протеопатиями. К ним относятся, например, болезнь Альцгеймера или болезнь Паркинсона. Известно, что ряд экспериментальных индукторов аутофагии, включая рапамицин, рапалоги, вальпроат и литий, могут ослаблять накопление мутированного белка и снижать гибель клеток.
Аутофагия может повысить жизнеспособность организма путем ингибирования гибели клеток, снижения риска онкогенной трансформации или увеличения гормезиса, как в покоящихся, так и делящихся клетках. Кроме того, аутофагия может способствовать увеличению продолжительности жизни через различные механизмы в постмитотических и пролиферирующих клетках [45]. Соответственно, можно предполагать, что стимуляция
аутофагии может быть инструментом лечения ряда внутриклеточных протеопатий. Улучшенние функций митохондрий также вероятно с помощью аутофагии. Сообщается, что деление митохондрий может возникать в асимметричном варианте, дающем одну функционально полноценную митохондрию (которая претерпевает последовательные раунды слияния и деления) и одну дисфункциональную митохондрию с низким мембранным потенциалом (DJm), которая предназначается для аутофагического разрушения [46]. Этот механизм демонстрирует важность аутофагиально-митохондриального контроля качества клетки. Одна из видных гипотез старения постулирует накопление митохондриальных повреждений, приводящее к прогрессирующей биоэнергетической недостаточности с увеличением производства реактивных форм кислорода (ROS) [47]. Известно, что ингибирование аутофагии приводит к ухудшению функции митохондрий в клетках модельных организмов и у мышей. Например, в митохондриях, изолированных из ATG-дефицитных постмитотических клеток (например, скелетные мышцы без экспрессии Atg7) обнаруживают дефектный тип окислительного фосфорилирования с переключением клеточного метаболизма от дыхания к гликолизу [48].
|
Тип полифенола |
Молекулярный механизм |
Ссылки |
|
Стильбеноиды |
||
|
Ресвератрол |
Блокада активации NLRP3. Нарушение экспрессии генов каспазы- 1 и IL-1e. Снижение ацетилирования цитоплазматических белков. |
[49] |
|
Флавоноиды |
||
|
ФлавонолыКверцетин |
Подавление активации NLRP3. Ингибиция экспрессии генов каспазы-1 и IL-1e. |
[50] |
|
Флавон Лютеолозид |
Подавление активации NLRP3. Угнетение накопления ROS. Нарушение экспрессии генов каспазы-1 и IL-1e. |
[51] |
|
Флавонолы Катехин |
Ингибирование активации NLRP3. Нарушение экспрессии генов каспазы-1 и IL-1e. Усиленное экспрессии Beclin 1 |
[52,53,54,55,56] |
|
EGCG |
NF-kB активация. Усиление аутофагии. Ингибирование активации NLRP3. Нарушение экспрессии генов каспазы-1 и IL-1e. |
|
|
Другие фенольные компоненты из экстракта прополиса |
Подавление активации NLRP3. Снижение секреции IL-1e |
[57] |
Таблица 2 -
^енолы, для
отмечен э
ект и
агии
или
ния
Таким образом, можно считать, что функциональная аутофагия жизненно важна для здорового организма, но при старении аутофагическая активность уменьшается [58]. Это может привести к нейродегенерации, раку, снижению иммунного ответа и, возможно, способствует развитию диабета II типа. Различные исследования мутантных организмов показывают, что активация аутофагии может продлить срок жизни, например, дрозофил, нематод или мышей [59, 60]. Стимуляция аутофагии у мышей с моделью болезни Паркинсона или Альцгеймера приводит к регрессу нейродегенерации[61].
Полифенолы хорошо известны своими антиоксидантными свойствами за счет активации антиоксидантного транскрипционного фактора Nrf2. Таким образом, полифенолы ослабляют окислительный стресс с помощью различных механизмов включая транскрипцию генов, кодирующих антиоксидантную функцию белков [62]. Хотя есть единичное свидетельство того, что полифенолы также могут ингибировать аутофагию[63], в последнее время все большее число исследований показывает про - аутофагический потенциал полифенолов [64]. Известны, например, полифенольные индукторы аутофагии, такие как кверцетин и ресвератрол [65], есть сообщения относительно активации аутофагиикуркумином и эпигаллокатехином[66]. Значимость аутофагии в отношении отдельных аспектов патофизиологии старения и возраст-ассоциированной патологии только начинает осознаваться научным сообществом, растущее количество доказательств свидетельствует, что CR или CR-миметики оказывают свой эффект по обеспечению здорового старения хотя бы частично через стимуляцию аутофагии уменьшая клеточные повреждения. Учитывая, что получены доказательства того, что полифенол ресвератрол индуцирует аутофагию и может частично имитировать полезный эффект CR [67], представляется правдоподобным, что и другие полифенолы, индуцирующие аутофагию, также могут способствовать здоровому долголетию.
СПИСОК ЛИТЕРАТУРЫ
- Boland B., Kumar A., Lee S., Platt F., Wegiel J., Yu H. , Nixon R. J. Autophagy induction and autophagosome clearance in neurons: relationship to autophagic pathology in alzheimer's disease // Neurosci. - 2009. - Vol. 4(27). - P. 6926-6937.
- Zhi X., Feng W., Rong Y., Liu R. Anatomy of autophagy: from the beginning to the end // Cell Mol Life Sci. - 2018. - Vol. 75(5). - P. 815831.
- Скибо Ю.В., Абрамова З.И. Методы исследования программ ируемой клеточной гибели: Учебно- методическоепособиедлямагистровпокурсу «Теорияапоптоза». - Казань: ФГАОУВПОКФУ, 2011.-61 с.
- Hsiao Y.T., Kuo C.L., Chueh F.S., Liu K.C., Bau D.T., Chung J.G. Curcuminoids induce reactive oxygen species and autophagy to enhance apoptosis in human oral cancer cells // Am J Chin Med. - 2018. - Vol. 5. - P. 11-24.
- Zhang Z., Shen Y., Luo H., Zhang F., Jing L., Wu Y., Xia X., Song Y., Li W., Jin L. MANF protects dopamine neurons and locomotion defects from a human a-synuclein induced Parkinson's disease model in C. elegans by regulating ER stress and autophagy pathways // Exp. Neurol. -2018. - Vol. 308.- P. 59-71.
- Thorburn A. Autophagy and disease // J Biol Chem. - 2018. - №293(15). - Р. 5425-5430.
- Kim J, Lim YM, Lee MS. The Role of Autophagy in Systemic Metabolism and Human-Type Diabetes //Mol Cells.- 2018.-Vol. 41(1).- P. 1117.
- DeMartino GN. Introduction to the Thematic Minireview Series: Autophagy // J Biol Chem.- 2018.-Vol. 293(15).- P.5384-5385. Shoji-Kawata S, et al. Identification of a candidate therapeutic autophagy-inducing peptide // Nature.- 2013.- № 494(7436).- P. 201206.
- Wilhelm T, Richly H. Autophagy during ageing - from Dr Jekyll to Mr Hyde // FEBS J. - 2018. - №3. - P. 6-18.
- Hars ES, Qi H, Ryazanov AG, Jin S, Cai L, Hu C, Liu LF. Autophagy regulates ageing in C. elegans // Autophagy. - 2007. -Vol.3(2). - P. 93-95. Megalou EV, Tavernarakis N. Autophagy in Caenorhabditis elegans // BiochimBiophysActa.- 2009.- №1793(9). - P. 1444-1451.
- Lapierre LR, Melendez A, Hansen M. Autophagy links lipid metabolism to longevity in C. elegans // Autophagy. - 2012. -Vol.8(1). - P. 144-146.
- Rubinsztein, D. C., Codogno, P., and Levine, B. Autophagy modulation as a potential therapeutic target for diverse diseases // Nature reviews Drug discovery. - 2012.- Vol.11.-P. 709-730.
- Shehata M, Abdou K, Choko K, Matsuo M, Nishizono H, Inokuchi K. Autophagy Enhances Memory Erasure through Synaptic Destabilization // J Neurosci. - 2018. -Vol.38(15). - P.3809-3822.
- Marinkovic M, Sprung M, Buljubasic M, Novak I. Autophagy Modulation in Cancer: Current Knowledge on Action and Therapy // Oxid Med Cell Longev. - 2018. - Vol. 31. - P. 11-16.
- Rubinsztein, D. C., Bento, C. F., and Deretic, V. Therapeutic targeting of autophagy in neurodegenerative and infectious diseases // J Exp Med. - 2015. - Vol.212.- P. 979-990.
- Dikic I, Elazar Z. Mechanism and medical implications of mammalian autophagy // Nat Rev Mol Cell Biol.- 2018.-Vol.19(6).- P.349-364. Zhi X, Feng W, Rong Y, Liu R. Anatomy of autophagy: from the beginning to the end // Cell Mol Life Sci.- 2018.-Vol.75(5).- P. 815-831.
- Levine, N. Mizushima, H. W. Virgin Autophagy in immunity and inflammation // Nature.- 2011.-Vol. 469.-P. 323-335.
- Yang Z and Klionsky DJ. An overview of the molecular mechanism of autophagy // Curr Top MicrobiolImmunol. - 2009. - Vol.335. - P. 21-32.
- Tooze J, Hollinshead M, Ludwig T, Howell K, Hoflack B, and Kern H. In exocrine pancreas, the basolateral endocytic pathway converges with the autophagic pathway immediately after the early endosome // J Cell Biol.- 1990.- Vol.111.- P. 329-345.
- Berg TO, Fengsrud M, Stromhaug PE, Berg T, and Seglen PO. Isolation and characterization of rat liver amphisomes. Evidence for fusion of autophagosomeswith both early and late endosomes // J Biol Chem.- 1998.- Vol.273.- P.21883-21892.
- Parzych K.R., Klionsky D.J. An Overview of Autophagy: Morphology, Mechanism, and Regulation //Antioxid. Redox Signal. - 2014. - Vol.20. -P. 460-473.
- Yang Z., Klionsky DJ. Mammalian autophagy: core molecular machinery and signaling regulation // CurrOpin Cell Biol. - 2010. - Vol.22.- P. 124-131.
- Yorimitsu T.,Klionsky D.J. Autophagy: molecular machinery for self-eating // Cell Death Differ.-2005.- Vol.12.-P.1542-1552.
- Yokota S., DariushFahimi H. Degradation of excess peroxisomes in mammalian liver cells by autophagy and other mechanisms // Histochem Cell Biol.- 2009.- Vol.131.- P. 455-458.
- Wirawan E., VandenBerghe T., Lippens S., Agostinis P., Vandenabeele P. Autophagy: for better or for worse // Cell Res.- 2012.- Vol.22.- P. 43-61.
- Si H, Liu D. Dietary antiaging phytochemicals and mechanisms associated with prolonged survival // The Journal of Nutritional Biochemistry.- 2014.- Vol.25(6).- P.581-591.
- Marzella L., Ahlberg J., and Glaumann H. Autophagy, heterophagy, microautophagy and crinophagy as the means for intracellular degradation // Cell PatholInclMolPathol.- 1981.- Vol.36.- P. 219-234.
- Sahu R., Kaushik S., Clement C.C., Cannizzo E.S., Scharf B., Follenzi A., Potolicchio I., Nieves E., Cuervo A.M., and Santambrogio L. Microautophagy of cytosolic proteins by late endosomes // Dev Cell.- 2011.- Vol.20.- P. 131-139.
- Dice JF. Peptide sequences that target cytosolic proteins for lysosomal proteolysis // Trends Biochem Sci. - 1990. - Vol.15. - P. 305-309. Chiang H.L., Dice J.F. Peptide sequences that target proteins for enhanced degradation during serum withdrawal // J Biol Chem.- 1988.- Vol.263.- P. 6797-6805.
- Orenstein S.J.,Cuervo A.M. Chaperone-mediated autophagy: molecular mechanisms and physiological relevance // Semin Cell Dev Biol.- 2010.- Vol. 21.- P. 719-726.
- Melendez, A., Tallo' czy, Z., Seaman, M., Eskelinen, E.L., Hall, D.H., and Levine, B. Autophagy genes are essential for dauer development and life-span extension in C. elegans // Science. - 2003. - Vol.301. - P. 1387-1391.
- Levine, B., and Kroemer, G. Autophagy in the pathogenesis of disease // Cell. - 2008. - Vol.132. - P. 27-42.
- Egan, D.F., Shackelford, D.B., Mihaylova, M.M., Gelino, S., Kohnz, R.A., Mair, W., Vasquez, D.S., Joshi, A., Gwinn, D.M., Taylor, R. Phosphorylation of ULK1 (hATG1) by AMP-activated protein kinase connects energy sensing to mitophagy // Science.- 2011.- Vol.331.- P. 456-461.
- Kim, J., Kundu, M., Viollet, B., and Guan, K.L. AMPK and mTOR regulate autophagy through direct phosphorylation of Ulk1 // Nat. Cell Biol.- 2011.- Vol.13.- P. 132-141.
- Canto, C., Jiang, L.Q., Deshmukh, A.S., Mataki, C., Coste, A., Lagouge, M.,Zierath, J.R., and Auwerx, J. Interdependence of AMPK and SIRT1 for metabolic adaptation to fasting and exercise in skeletal muscle // Cell Metab.- 2011.- Vol.11.- P. 213-219.
- Kenyon, C.J. The genetics of ageing // Nature.- 2010.- Vol.464. - P. 504-512.
- Haigis, M.C., and Sinclair, D.A. Mammalian sirtuins: biological insights and disease relevance //Annu. Rev. Pathol. - 2010.- Vol.5.- P. 253295.
- Morselli, E., Marino, G., Bennetzen, M., Eisenberg, T., Megalou, E., Schroeder, S., Carbrera, S., Be' nit, P., Rustin, P., Criollo, A., Spermidine and resveratrol induce autophagy by distinct yet convergent pathways affecting the acetylproteome // J. Cell Biol.- 2011.- Vol.192.- P. 615-629.
- Lee, I.H., Cao, L., Mostoslavsky, R., Lombard, D.B., Liu, J., Bruns, N.E., Tsokos, M., Alt, F.W., and Finkel, T. A role for the NAD-dependent deacetylase Sirt1 in the regulation of autophagy // Proc. Natl. Acad. Sci.- 2008.- Vol.105.-P. 3374-3379.
- Saunders, L.R., and Verdin, E. Cell biology. Stress response and aging// Science.- 2009.- Vol.323.- P. 1021-1022.
- Ravikumar B, Sarkar S, Davies JE, Futter M, Garcia-Arencibia M, Green-Thompson ZW, Jimenez-Sanchez M, Korolchuk VI, Lichtenberg M, Luo S, Massey DC, Menzies FM, Moreau K, Narayanan U, Renna M, Siddiqi FH, Underwood BR, Winslow AR, Rubinsztein DC.Regulation of mammalian autophagy in physiology and pathophysiology // Physiol Rev.- 2010.- Vol.90(4).- P.1383-435.
- Twig, G., Elorza, A., Molina, A.J., Mohamed, H., Wikstrom, J.D., Walzer, G., Stiles, L., Haigh, S.E., Katz, S., Las, G. Fission and selective fusion govern mitochondrial segregation and elimination by autophagy // EMBO J.- 2008.- Vol.27.- P. 433-446.
- Vijg, J., and Campisi, J. Puzzles, promises and a cure for ageing // Nature.- 2008.- Vol.454.- P. 1065-1071.
- Wu, J.J., Quijano, C., Chen, E., Liu, H., Cao, L., Fergusson, M.M., Rovira, I.I., Gutkind, S., Daniels, M.P., Komatsu, M., and Finkel, T. Mitochondrial dysfunction and oxidative stress mediate the physiological impairment induced by the disruption of autophagy // Aging.- 2009.- Vol.1.- P. 425-437.
- Yang S. J., LimY.Resveratrol ameliorates hepatic metaflammation and inhibits NLRP3 inflammasome activation // Metabolism-Clinical and Experimenta.- 2014.- Vol.63.- P.693-701.
- WangC., PanY., ZhangQ.-Y., WangF.-M., KongL.-D. Quercetin and allopurinol ameliorate kidney injury in STZtreated rats with regulation of renal NLRP3 inflammasome activation and lipid accumulation // PLoS ONE.- 2012.- Vol. 7.- P. 382-389.
- FanS. H., WangY. Y., Lu J.Luteoloside suppresses proliferation and metastasis of hepatocellular carcinoma cells by inhibition of NLRP3 inflammasome // PLoS ONE.- 2014.- Vol.9.- P. 264-277.
- YangJ.-C., YangH.-C., ShunC.-T., WangT.-H., ChienC.-T., and KaoJ. Y.Catechins and sialic acid attenuate helicobacter pylori -triggered epithelial caspase-1 activity and eradicate helicobacter pylori infection // Evidence-Based Complementary and Alternative Medicine.- 2013.- Vol.5.- P. 1-13.
- YangJ. C., ShunC. T., ChienC. T., WangT. H.Effective prevention and treatment ofHelicobacter pylori infection using a combination of catechins and sialic acid in AGS cells and BALB/c mice // Journal of Nutrition.- 2008.- Vol.138. - P. 2084-2090.
- EllisL. Z., LiuW., Luo Y. Green tea polyphenol epigallocatechin-3-gallate suppresses melanoma growth by inhibiting inflammasome and IL-1^ secretion // Biochemical and Biophysical Research Communications.- 2011.- Vol. 414.- P. 551-556.
- TsaiP.-Y., KaS.-M., Chang J.-M. Epigallocatechin-3-gallate prevents lupus nephritis development in mice via enhancing the Nrf2 antioxidant pathway and inhibiting NLRP3 inflammasome activation // Free Radical Biology and Medicine.- 2011.- Vol. 51.-P. 744-754.
- LiW., ZhuS., Li J. EGCG stimulates autophagy and reduces cytoplasmic HMGB1 levels in endotoxin-stimulated macrophages // Biochemical Pharmacology.- 2011.- Vol.81.- P. 1152-1163.
- HoriJ. I.,ZamboniD. S.,CarraoD. B., GoldmanG.H., BerrettaA.A.The inhibition of inflammasomeby Brazilian propolis (EPP-AF) // EvidenceBased Complementary and Alternative Medicine.- 2013.- Vol.12.- P.1-11.
- Del Roso, A., Vittorini, S., Cavallini, G., Donati, A., Gori, Z., Masini, M., Pollera, M., Bergamini, E. Ageing-related changes in the in vivo function of rat liver macroautophagy and proteolysis // Experimental Gerontology.- 2003.- Vol.38.-P. 519-527.
- Bjedov, I., Toivonen, J.M., Kerr, F., Slack, C., Jacobson, J., Foley, A., Partridge, L., Mechanisms of life span extension by rapamycin in the fruit fly Drosophila melanogaster // Cell Metabolism.- 2010.- Vol.11.- P. 35-46.
- Harrison, D.E., Strong, R., Sharp, Z.D., Nelson, J.F., Astle, C.M., Flurkey, K., Nadon, N.L., Wilkinson, J.E., Frenkel, K., Carter, C.S., Pahor, M., Javors, M.A., Fernandez, E., Miller, R.A. Rapamycin fed late in life extends lifespan in genetically heterogeneous mice // Nature.- 2009. - Vol.460.- P. 392-395.
- Korolchuk, V.I., Mansilla, A., Menzies, F.M., Rubinsztein, D.C. Autophagy inhibition compromises degradation of ubiquitin-proteasome pathway substrates // Molecular Cell.- 2009.- Vol.33.- P. 517-527.
- Kaspar J.W., Niture S.K.,Jaiswal A.K. Nrf2:INrf2 (Keap1) signaling in oxidative stress// Free Radical Biology & Medicine.- 2009.- Vol.47.- P.1304-1309.
- Gordon P.B., Holen I., Seglen P.O. Protection by naringin and some other flavonoids of hepatocytic autophagy and endocytosis against inhibition by okadaic acid // The Journal of Biological Chemistry.- 1995.- Vol.270.- P. 5830-5838.
- Singletary K., Milner J., Diet, autophagy, and cancer: a review. Cancer Epidemiology, Biomarkers & Prevention // Publication of the American Association for Cancer Research, cosponsored by the American Society of Preventive Oncology.- 2008.- Vol.17.- P. 1596-1610.
- Howitz K.T., Bitterman K.J., Cohen H.Y., Lamming D.W., Lavu S. Wood J.G., Zipkin R.E., Chung P., Kisielewski A., Zhang L.L., Scherer B., Sinclair D.A. Small molecule activators of sirtuins extend Saccharomyces cerevisiae lifespan // Nature.- 2003.- Vol.425.- P.191-196.
- Wu J.C., Lai C.S., Badmaev V., Nagabhushanam K., Ho C.T., Pan M.H. Tetrahydrocurcumin, a major metabolite of curcumin, induced autophagic cell death through coordinative modulation of PI3K/Akt-mTOR and MAPK signaling pathways in human leukemia HL-60 cells // MolNutr Food Res. - 2011. - Vol. 55(11). - P. 1646-1654
- Baur, J.A., Pearson, K.J., Price, N.L., Jamieson, H.A., Lerin, C., Kalra, A., Prabhu, V.V., Allard, J.S., Lopez-Lluch, G., Lewis, K., Pistell, P.J., Poosala, S., Becker, K.G., Boss, O., Gwinn, D., Wang, M., Ramaswamy, S., Fishbein, K.W., Spencer, R.G., Lakatta, E.G., Le Couteur, D., Shaw, R.J., Navas, P., Puigserver, P., Ingram, D.K., de Cabo, R., Sinclair, D.A., Resveratrol improves health and survival of mice on a high-calorie diet // Nature.- 2006.- Vol.444.- P. 337-342.