Во время проведения операций на открытом сердце происходит нарушение барьерной функции воспаления и появление в системном кровотоке медиаторов воспаления и провоспалительных цитокинов, что реализуется в синдром системных проявлений воспаления. Для предупреждения развития данного состояния или для уменьшения выраженности его осложнений наиболее эффективным является механический метод удаления медиаторов воспаления и цитокинов из крови больного. Это объясняет большое количество исследований, направленных как на изучение патогенеза синдрома системных проявлений воспаления, так и на разработку новых методик борьбы с данным явлением и усовершенствование уже применяемых методик и технологий [1, 4]. Особое внимание уделяется изучению методов модифицированной ультрафильтрации и непрерывной вено-артериальнойгемофильтрации. Дальнейшее изучение методов ультрафильтрации у кардиохирургических пациентов при операциях на сердце с применением ИК необходимо для углубленного понимания физиологии и патофизиологии синдрома системного проявления воспаления, индуцированного проведением ИК, а также для последующей формулировки клинических рекомендаций для применения в кардиохирургической практике. В данной статье мы постарались рассмотреть наиболее значимые результаты подобных исследований.
О существования «отечного синдрома» при проведении ИК и осложнениях, связанных с экстравазальными отеками, написано достаточно много. Гораздо меньше работ посвящено профилактике и лечению такого состояния. Превентивные меры заключаются в усовершенствовании техники ИК: поддержании высоких скоростей перфузии, равномерному распределению перфузата по организму путем адекватной вазодилатации, снижению до минимума первичного объема заполнения и оптимизации его состава [1, 8]. Некоторые авторы используют намеренно высокий уровень интраоперационного гематокрита (до 35%) [2]. Появились работы об использовании, для снижения активности тромбоцитов во время ИК, различных препаратов, в частности, из группы простаноидов(PGEl; PG12). Применение же последних не получило распространения из-за выраженной системной гипотонии [3].
Для лечения «отечного синдрома» принято использовать медикаментозную стимуляцию диуреза, плазмаферез, перитонеальный диализ, метод CellSaverи ультрафильтрацию крови.
Медикаментозная стимуляция диуреза в детской практике, особенно у пациентов с малым весом, при лечении экстравазальных отеков не была успешной [4]. Применение же перитонеального диализа проблематично из-за инвазивности процедуры, хотя все авторы отмечали хороший лечебный эффект [5, 10].
Метод CellSaver(спасатель клеток) - интра- и постперфузионное центрифугирование крови с одновременным отмыванием эритроцитов физиологическим раствором в специальной центрифуге и возврашение полученного эритроцитарного концентрата больному. Основными недостатками метода являются применение дорогостоящего оборудования, неизбежный дефицит белка плазмы и тромбоцитопения, а также относительно низкая его эффективность [6, 9, 11].
Ультрафильтрация крови является наиболее предпочтительным в данном ряду методом. Ультрафильтрация - это процесс конвекции, при котором жидкость пропускают сквозь пористую мембрану, где за счет трансмембранной разницы давлений отфильтровываются соединения с молекулярной массой больше чем размер пор мембраны.
В зависимости от формы фильтрующей мембраны существуют пластинчатые и капиллярные
(половолоконные) фильтры. В качестве мембран используются полимеры синтетической природы (кополимер акрилонитрила металлилсульфоната натрия, полисульфон и др.), устойчивые к тромбообразованию и обладающие хорошей биосовместимостью [5]. Выяснено, что через 10-15 минут фильтрации крови фильтрующие свойства различных материалов не различаются [7, 9]. Ультрафильтры разделяются по размерам, объему заполнения, по площади фильтрующей поверхности и по размерам пор мембраны [8].
Кроме трансмембранного давления, скорость фильтрации определяют такие параметры как объемная скорость кровотока через ультрафильтр (должно быть на уровне 100-300 мл/мин) и коэффициент «просеивания» фильтра, т.е. размер пор. [12, 14]. При проведении ультрафильтрации отфильтрованный объем жидкости пациенту не возвращается [13].
Первый ультрафильтр был сконструирован Brüll в 1928 г. [15]. Однако практическое применение ультрафильтрации началось только в 1950 г. при лечении почечной недостаточности. С середины 70-х годов ультрафильтры стали использоваться для лечения недостаточности кровообращения [16]. В 1976 г. [17] впервые сообщили о применении УФ для сгущения крови, оставшейся в аппарате искусственного кровообращения. С тех пор вышло немалое число публикаций о преимуществах использования ультрафильтрации в сердечной хирургии.
Ультрафильтрацию (УФ) применяют для выведения жидкости у пациентов с резистентной сердечной недостаточностью для подготовки их к операции. [8]. Однако, такое применение УФ в клинике встречается редко. Чаще ультрафильтрация используется интраоперационно, как компонент искусственного кровообращения, а также в период интенсивной послеоперационной терапии. Основная цель УФ- коррекция жидкостного баланса. Ультрафильтрация так же успешна при лечении острой послеоперационной почечной недостаточности.
У взрослых пациентов применима классическая методика УФ, которая выполняется одновременно с искусственным кровообращением.
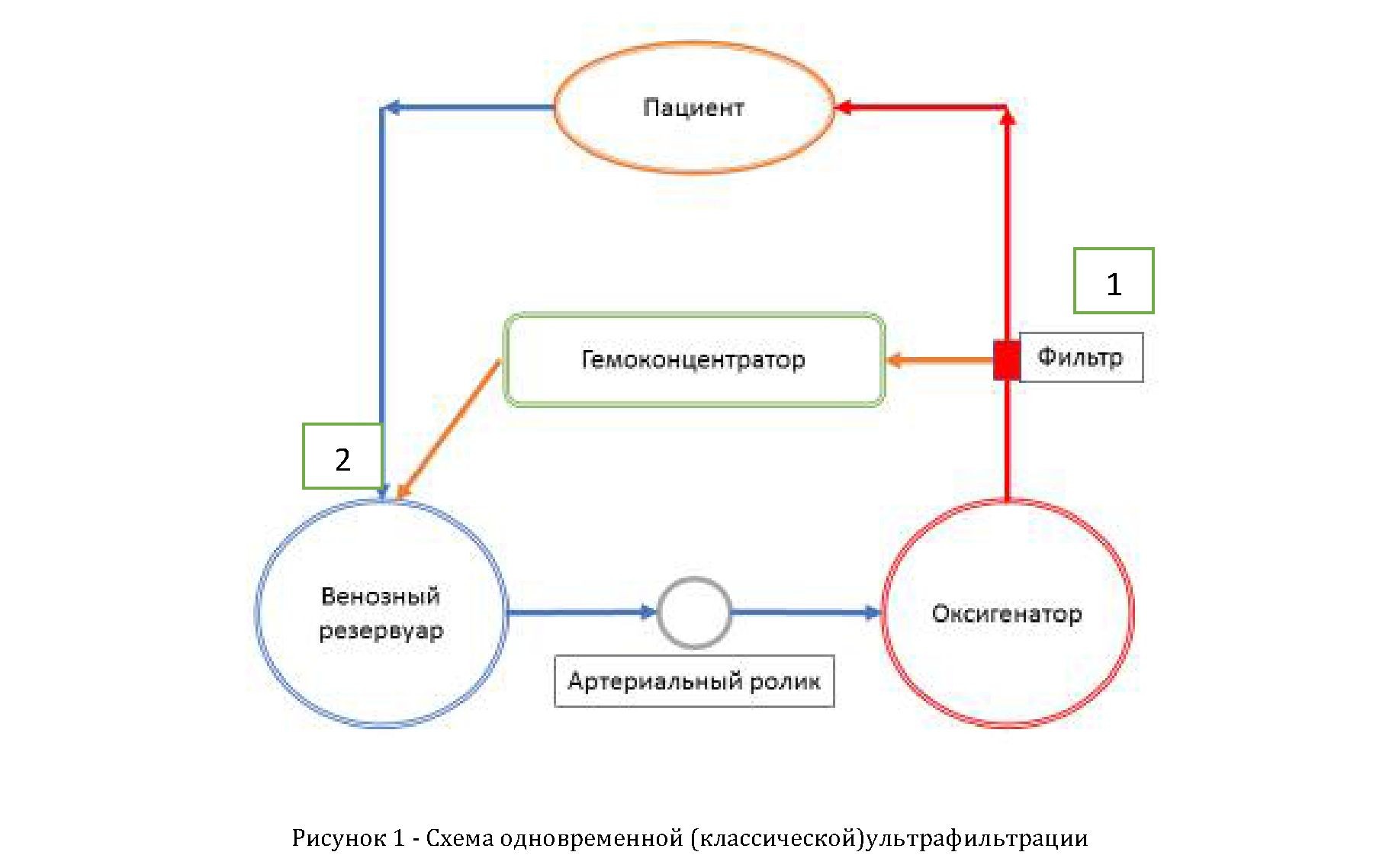
Схема одновременной (классической) ультрафильтрации изображена на рис. 1. Приточная магистраль (1) ультрафильтра соединена с артериальной магистралью системы ИК. Выход из ультрафильтра (2) осуществляется в венозный резервуар. [5]. Ультрафильтрация проводится в фазу согревания перед окончанием ИК. Гемоконцентрация, достигнутая в ходе УФ, способствует сохранению фибриногена и других факторов свертывания, а также поддержанию концентрации электролитов плазмы. [1].
Применение одновременной (классической) ультрафильтрации в детской кардиохирургии ограничено из-за гиповолемии. Скорость удаления жидкости через ультрафильтр у детей намного превышает скорость компенсаторного ее выделения в сосудистое русло из объема «третьего пространства». Проведение УФ одновременно с ИК ведет к критическому падению уровня жидкости в венозном резервуаре. Недостаток восполняется коллоидными и кристаллоидными растворами. Такое восполнение сводит эффект ультрафильтрации на нет.
При уменьшении же скорости фильтрации не удается достигнуть желаемого уровня гематокрита к концу ИК, а проведение классической УФ не предполагает ее использование после остановки искусственного кровообращения [15].
 В 1991 г. Naik и соавт. предложили новую схему подключения ультрафильтра, изменив при этом время проведения ультрафильтрации. Эта процедураполучила название модифицированной ультрафильтрации (МУФ) [1]. МУФ отличается от классической УФ расположением ультрафильтра в контуре ИК, проводится сразу после окончания ИК и позволяет под контролем концентрационных и гемодинамических показателей произвести оптимальную коррекцию гемогидробаланса. Эффективность УФ контролируется достижением желаемого уровня гематокрита (обычно36-42%) [2].
В 1991 г. Naik и соавт. предложили новую схему подключения ультрафильтра, изменив при этом время проведения ультрафильтрации. Эта процедураполучила название модифицированной ультрафильтрации (МУФ) [1]. МУФ отличается от классической УФ расположением ультрафильтра в контуре ИК, проводится сразу после окончания ИК и позволяет под контролем концентрационных и гемодинамических показателей произвести оптимальную коррекцию гемогидробаланса. Эффективность УФ контролируется достижением желаемого уровня гематокрита (обычно36-42%) [2].
Гиповолемия, возникающая при проведении МУФ, может быть компенсирована объемом, оставшимся в венозном резервуаре, т.е. параллельно осуществляется гемоконцентрация.В литературе встречаются упоминания о том, что модифицированная ультрафильтрация также снижает плазменную концентрацию интерлейкинов, продуктов перекисного окисления липидов и калия, способствуя, тем самым, улучшению сократительной способности миокарда после искусственного кровообращения [3].
В клинической практике МУФ используется совсем недавно и немногими центрами. В свете вышесказанного, изучение положительных клинических эффектов модифицированной ультрафильтрации и механизмов их возникновения - это вопрос интересный с научной точки зрения и практически весьма актуальный.
СПИСОК ЛИТЕРАТУРЫ
- Кирсанова В.Н., Мерунко А.А., Ковалев И.А. Влияние модифицированной ультрафильтрации на интенсивность перекисного окисления липидо // Грудная и сердечно-сосудистая хирургия. - 2000. - № 2. - С. 97-105.
- Allen M., Sundararajan S., Pathan N., Burmester M., Macrae D. Anti-inflammatory modalities: their current use in pediatric cardiac surgery in the United Kingdom and Ireland // Pediatr. Crit. Care Med. - 2009. - №10(3). - Р. 341-345. doi: 10.1097/PCC.0b013e3181a3105d
- Baizhigitov N. B., Ormantayev A. K., Sepbayevа A. D. Methods of modified ultrafiltration in the surgical correction of transposition of the great arteries in newbo // Original research. - 2017. - Р. 270-272. DOI - https://doi.org/10.14300/mnnc.2017.12073
- Draaisma A. M., Hazekamp M. G., Frank M., Anes N., Schoof P. H. [et al.] Modified ultrafiltration after cardiopulmonary bypass in pediatric cardiac surgery // Ann. Thorac. Surg. - 1997. - №64(2). - Р. 521-525. doi: 10.1016/S0003-4975(97)00522-5
- Francisco A. Portela, Alberto Pensado, Amelia Sánchez [et al.] A simple technique to perform combined ultrafiltration // Ann. Thorac. Surg. - 1999. - №3(67). - Р. 859-861. doi: org/10.1016/s0003-4975(98)01298-3
- Gaynor J. W. Use of ultrafiltration during and after cardiopulmonary bypass in children // J. Thorac Cardiovasc Surg. - 2001. - №122(2). - Р. 209-211. doi:10.1067/mtc.2001.115925
- Gaynor J. W. The effect of modified ultrafiltration on the postoperative course in patients with congenital heart disease // Semin. Thorac. Cardiovasc. Surg. Pediatr. Card. Surg. Ann. - 2003. - №6. - Р. 128-139. doi: 10.1053/pcsu.2003.50006
- Harig F., Meier C., Hakami L., Strasser R., Bretzger J. [et al.] Does the additional use of heparin-coated extracorporeal circuits (ECC) optimize the effect of modified ultrafiltration (MUF) in pediatric perfusion? // Thorac. Cardiovasc. Surg. 2006. - №54(3). - Р. 168-172. doi: 10.1055/s-2005-872863
- Keenan H. T., Thiagarajan R., Stephens K. E., Williams G., Ramamoorthy C. [et al.] Pulmonary function after modified venovenous ultrafiltration in infants: a prospective, randomized trial // The Journal of Thoracic and Cardiovascular Surgery. - 2000. - №119. - Р. 501-507. doi: 10.1067/mtc.2000.103602
- Magilligan D. J. Indications for ultrafiltration in the cardiac surgical patients // J. Thorac. Cardiovasc. Surgery. - 1985. - №89(2). - Р. 183189. PMID:3968903
- Mahmoud A. B., Burhani M. S., Hannef A. A., Jamjoom A. A., Al-Githmi I. S. [et al.] Effect of modified ultrafiltration on pulmonary function after cardiopulmonary bypass // Chest. - 2005. - №128(5). - Р. 3447-3453. doi: 10.1378/chest.128.5.3447
- Naik S. K., Knight A., Elliot M. J. A successful modification of ultrafiltration for cardiopulmonary bypass in children // Perfusion. - 1991. - №6(1). - Р. 41-50. doi:10.1177/026765 919100600106
- Onoe M., Oku H., Kitayama H. [et al.] Modified ultrafiltration may improve postoperative pulmonary function in children with a ventricular septal defect // Surgery Today. - 2001. - №31. - Р. 586-590. doi: 10.1007/s005950170091
- Ricci Z., Polito A., Netto R., De Razza F., Favia I. [et al.] Assessment of modified ultrafiltration hemodynamic impact by pressure recording analytical method during pediatric cardiac surgery // Pediatr. Crit. Care Med. - 2013. - №14(4). - Р. 390-395. doi: 10.1097/PCC.0b013e31828a7113
- Thompson L. D., McElhinney D. B., Findlay P., Miller-Hance W., Chen M. J. [et al.] A prospective randomized study comparing volume- standardized modified and conventional ultrafiltration in pediatric cardiac surgery // J. Thorac. Cardiovasc. Surg. - 2001. - №122(2). - Р. 220-228. doi: 10.1067/mtc.2001.114937
- Yokoyama K., Takabayashi S., Komada T., Onoda K., Mitani Y. [et al.] Removal of prostaglandin E2 and increased intraoperative blood pressure during modified ultrafiltration in pediatric cardiac surgery // J. Thorac. Cardiovasc. Surg. - 2009. - №137(3). - Р. 730-735. doi: 10.1016/j. jtcvs.2008.09.017
- Ziyaeifard M., Alizadehasl A., Massoumi G. Modified Ultrafiltration During Cardiopulmonary Bypass and Postoperative Course of Pediatric Cardiac Surgery // Res. Cardiovasc. Med. - 2014. - №3(2). - Р. 1783-1790. doi: 10.5812/cardiovascmed. 17830