Большим достижением восстановительной хирургии пищевода является разработка методов внутриплевральной толстокишечной эзофагопластики. Разработанные преимущественно для лечения рубцовых сужений пищевода эти операции иногда применяются и при лечении рака пищевода. В 1951 г. Orsoni и Lemaire предложили использовать для внутриплевральной пластики пищевода трансплантат из поперечной ободочной кишки. В клинике впервые успешную внутригрудную пластику пищевода толстой кишкой выполнил Lortat-Jacob (1951), использовав с этой целью часть правой и правую половину поперечной ободочной кишки. Внутриплевральную пластику пищевода при раке грудного отдела пищевода впервые успешно применили Nevilli и Gloves (1958) правой половиной толстой кишки. Целью исследования является освещение показаний и техники внутриплевральной пластики пищевода толстой кишкой на современном уровне.
Актуальность. Большим достижением восстановительной хирургии пищевода является разработка методов внутриплевральной толстокишечной эзофагопластики. Разработанные преимущественно для лечения рубцовых сужений пищевода эти операции иногда применяются и при лечении рака пищевода. В 1951 г. Orsoni и Lemaire предложили использовать для внутриплевральной пластики пищевода трансплантат из поперечной ободочной кишки. В клинике впервые успешную внутригрудную пластику пищевода толстой кишкой выполнил Lortat-Jacob (1951), использовав с этой целью часть правой и правую половину поперечной ободочной кишки с питающей восходящей ветвью левой ободочной артерии. Проксимальная часть трансплантата была соединена с пищеводом, а дистальная — с тощей кишкой. Внутриплевральную пластику пищевода при раке грудного отдела пищевода впервые успешно применили Nevilli и Gloves (1958). Техника операций, примененных Невиль и
Глоувз, следующая. При раке пищевода, располагающемся в средней трети и выше дуги аорты, применяются правосторонняя торакотомия и лапарото-мия. Операция выполняется одновременно двумя бригадами хирургов. Одна бригада мобилизует и удаляет пораженный участок пищевода. В это время другая бригада хирургов мобилизует правую половину толстой кишки, включая слепую кишку, аналогично методике Ройт, или сохраняя слепую кишку по методике А. А. Шалимова (рис. 265). При плохих анастомозах между средней и левой ободочной артериями вполне допустима мобилизация кишки по методике Лафарга (рис. 266). Через отверстие в диафрагме кишку проводят в правую плевральную полость, где первая бригада формирует пищеводно-кишечный анастомоз конец в конец. Вторая бригада в это время накладывает желудочнотолстокишечный анастомоз.
В США наиболее популярна пластика пищевода правой половиной толстой кишки. В Англии чаще для этих целей используется ее левая половина. Толстая кишка может быть перемещена как в антиперистальтическом направлении, так и изоперистальтически. Некоторые хирурги предпочитают
Все перечисленные показания относятся к случаям, когда для замещения пищевода нельзя использовать желудок.
Противопоказания: тяжелы есердечно- егочные заболевания, при ко торых проводить торакотомию опасно.
Специальная подготовка: как при суб- и тотальной шунтирующей пластике пищевода толстой кишкой.
Позиция больного: вначале лежа на спине, затем на левом боку с вали ком под грудной клеткой (стол поворачивают вместе с больным налево).
Анестезия: эндотрахеальный наркоз.
Доступ: широкая верхняя срединная лапаротомия с обходом пупка слева, затем переднебоковая торакотомия справа вIV—Vмежреберье.
Основные этапы операции:
- —лапаротомия, ревизия брюшной полости —формирование трансплантата и анастомозирование его с желудком, восстановление проходимости толстой кишки —диафрагмокруротомия
- —выведение трансплантата в плевральную полость; дренирование и ушивание брюшной полости
проведение трансплантата из поперечного отдела или левой половины толстой кишки внутриторакально позади корня легкого, не придавая особого значения при этом перистальтической ориентации трансплантата. При сравнительном изучении опыта операций пластики пищевода толстой кишкой отмечено, что в 70% случаев трансплантат был проведен позади корня легкого изоперистальтически и в 30% — ретростернально. В основном это были пациенты с атрезией пищевода и культей его дистального сегмента.
Целью исследования является освещение показаний и техники внутриплевральной пластики пищевода толстой кишкой на современном уровне.
Показания: 1) доброкачественные стриктуры пищевода, обычно локализующиеся в средне- и нижнегрудном отделах; 2) большие доброкачественные опухоли нижней трети пищевода при ситуациях, когда вылущивание невозможно; 3) рак нижней трети пищевода и рак кардии с переходом на пищевод;
- —торакотомия, ревизия пищевода
- —резекция пищевода или (при доброкачественных рубцовых стрик турах) соединение трансплантата с пищеводом по типу шунтирую щей пластики
- —проведение зонда в трансплантат для декомпрессии, дренирование и ушивание плевральной полости
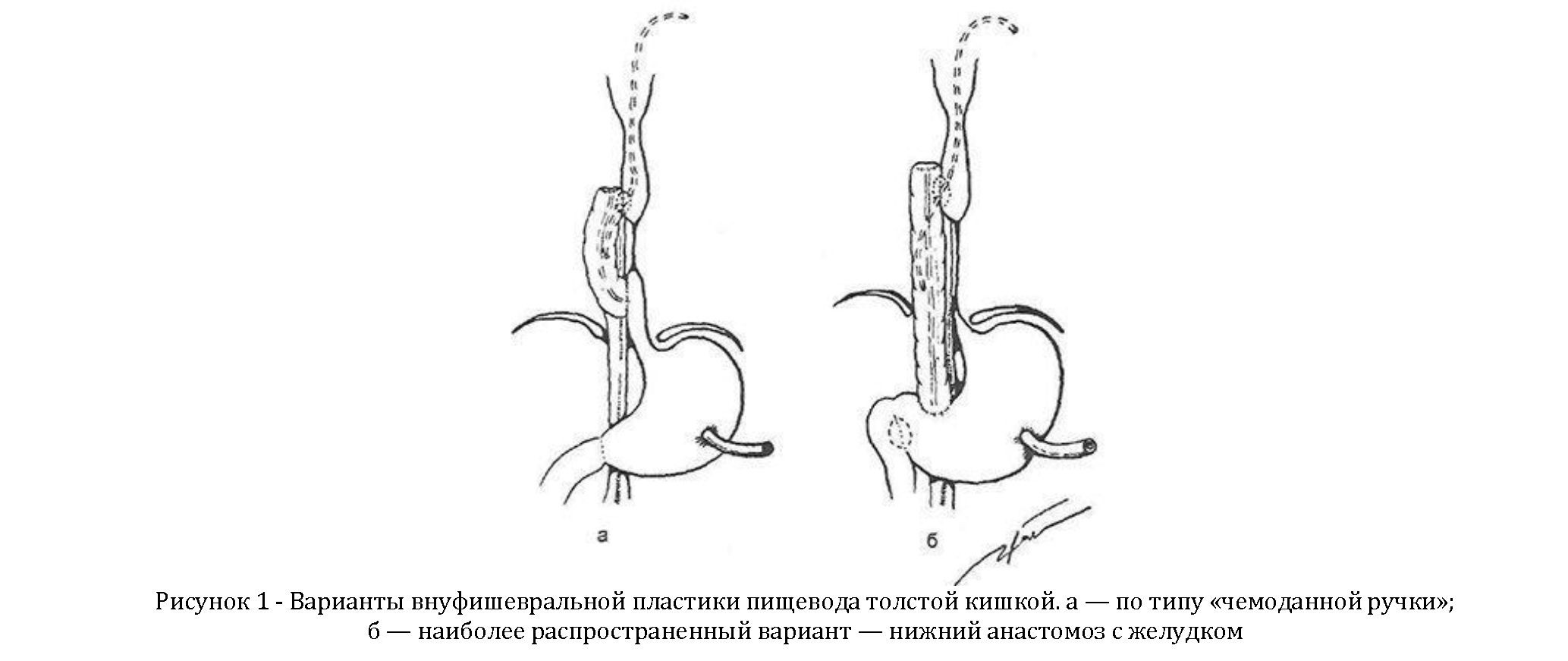
При рубцовых стриктурах пищевода применяют два основных вида шунтирующей пластики толстой кишкой. Первый — по типу «чемоданной ручки», когда оба анастомоза с пищеводом накладываются в плевральной полости выше и ниже стриктуры. Верхний анастомоз формируется по типу «бок в бок», нижний — «конец в бок». Преимуществом подобного вида пластики является сохранение кардиального сфинктера, основными недостатками — сложность и длительность операции, опасные осложнения. При втором виде внутриплевральной толстокишечной шунтирующей пластики один анастомоз накладывается в плевральной полости выше стриктуры, другой — с желудком — в брюшной полости (рисунок 1).
При более редких вариантах протяженных рубцовых стриктур шейного и верхнегрудного отделов пищевода анастомоз трансплантата с пищеводом в правой плевральной полости накладывают по типу «конец в бок», а на шее — с правым грушевидным синусом глотки — «бок в бок» (рисунок 2).
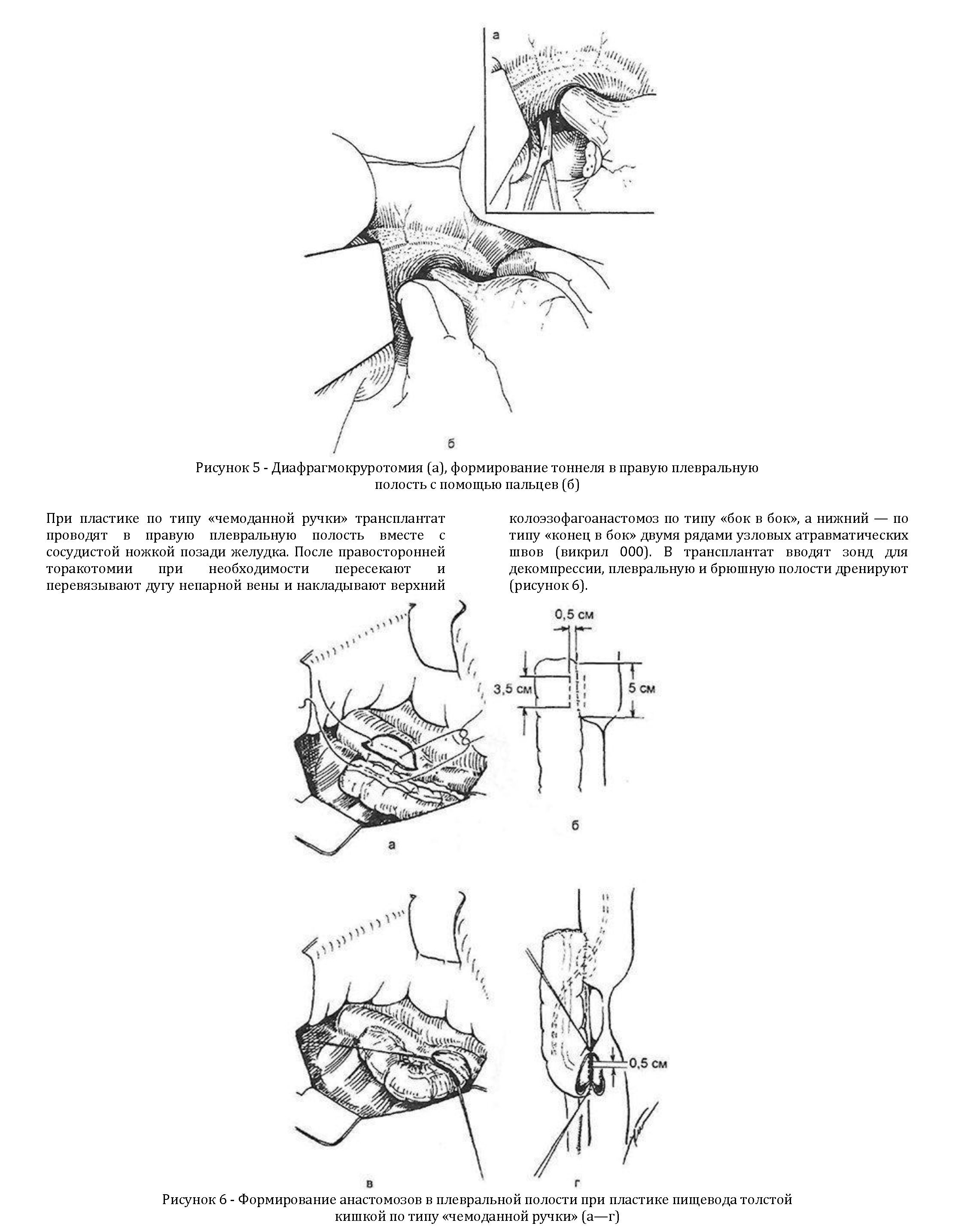
Далее мобилизуют левую долю печени рассечением треугольной связки и отводят ее вправо крючком Савиных. Мобилизуют абдоминальный отдел пищевода. Правую медиальную ножку диафрагмы рассекают ножницами, пальцами раздвигают ткани, создавая канал, идущий в правую плевральную полость (рисунок 5).

В типичных случаях сформированный для пластики средней и нижней третей пищевода трансплантат располагают за желудком и анастомозируют с антральным отделом в поперечном направлении. При необходимости к круротомии добавляют ограниченную (до нижней диафрагмальной вены) сагиттальную диафрагмотомию, чтобы избежать сдавления трансплантата (рисунок 7, а—в).
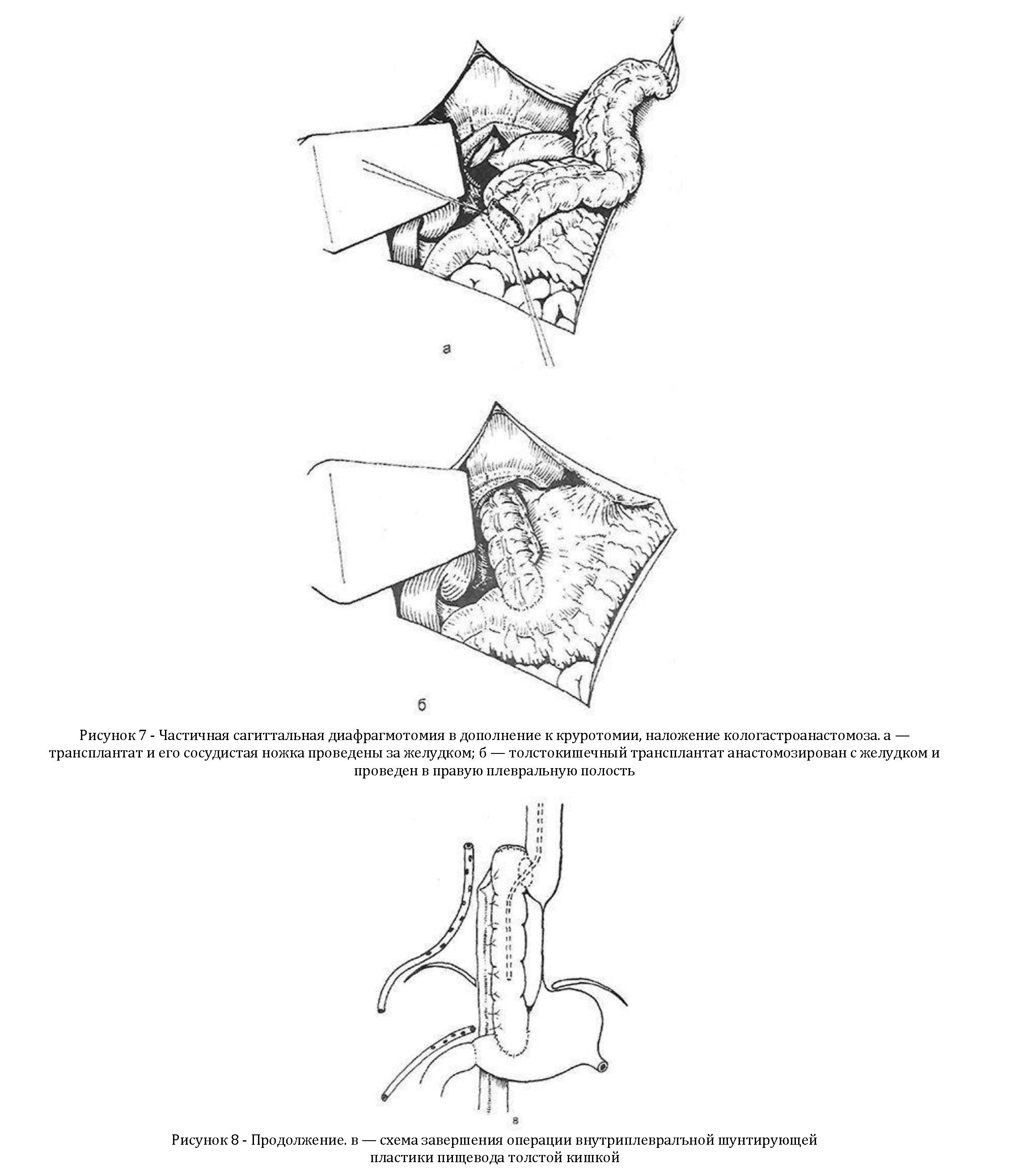
Проводят трансплантат в правую плевральную полость. Выполняют правостороннюю торакотомию, формируют колоэзофагоанастомоз по типу «бок в бок» таким же образом, как было описано выше. Для того чтобы избежать образования «слепого мешка» собственного пищевода, проксимальный анастомоз формируют как можно ближе к стриктуре. Так же проводят зонд в трансплантат для декомпрессии, плевральную и брюшную полость дренируют. Если есть гастростома, ее открывают на 2— 3 послеоперационных дня для декомпрессии желудка. В других случаях в желудок можно провести зонд через трансплантат.
Таким образом, все вышесказанное определяет актуальность и своевременность изучения внутриплевральной пластики пищевода толстой кишкой, основной целью которой — осветить на современном уровне проблемы показаний и техники внутриплевральной пластики пищевода толстой кишкой.
СПИСОК ЛИТЕРАТУРЫ
- Ванцян Э.Н., Черноусов А.Ф. Хирургия пищевода // Клинические аспекты хирургии. - М.: Медицина, 1978. - С.128-164.
- Матяшин М.М. Тотальная пластика пищевода толстой кишкой. — Киев: Здоровья, 1971. - 192 с.
- Черноусов А.Ф., Сильвестров B.C., Курбанов Ф.С. Пластика пищевода при раке и доброкачественных стриктурах. - М.: Медицина, 1990. - 142 с.
- Черноусов А.Ф., Андрианов В.А., Богопольский П.М., Воронов М.Е. Выбор метода пластики пищевода // Вестн. РАМН. - 1997. - № 9. - С. 21-25.
- Черноусов А.Ф., Андрианов В.А., Домрачее С.А., Богопольский П.М. Опыт 1100 плас тик пищевода // Хирургия. — 1998. — № 6. — С. 21 —25.
- Черноусов А.Ф., Богопольский П.М., Курбанов Ф.С. Хирургия пищевода. - М.: Медицина, 2000. - 349 с.
- Шалимов А.А., Саенко В.Ф., Шалимов С.А. Хирургия пищевода. — М.: Медицина, 1975. - 368 с.
- Cheng В., Lu S.Q., Gao S.Z., Tu Z.F., Lin DM, Wang T.S. Colon replacement of the esophagus. Clinical experience from 240 cases// Clin. Med. J. — 1994. — Vol. 107, №3. - P. 216-218.
- Cseke L., Horvath 0. Indications, new surgical technique and results of colon interposi tion or bypass in esophageal surgery // Acta chir. Hung. — 1997. — Vol. 36, №1. - P.49-50.