Статья посвящена сравнительному эпидемиологическому исследованию по изучению клинического применения реактогенности и заболеваемости гриппом у взрослых лиц привитых в один эпидемический сезон двумя вакцинами разных производителей – «Гриппол®плюс» (Россия) и «Инфлювак» (Нидерланды). В составе указанных вакцин содержались антигены три актуальных эпидемических штаммов вирусов гриппа типов А(H1N1), А(H3N2) и В. Эти препараты являются инактивированными субъединичными. Вакцина «Гриппол®плюс» имеет в составе инновационный иммуноадъювант «Полиоксидоний», способный дополнительно выступать как иммуномодулятор, обеспечивающий не только более эффективную защиту от гриппа, но и от других ОРВИ. Показано отсутствие статистически значимых различий реактогенности сравниваемых вакцин по общим и местным реакциям, за исключением более частого развития болезненности в месте инъекции на 2 и 3 дни после прививки вакцинной «Инфлювак» по сравнению с «Гриппол®плюс». Заболеваемость по истечении 6 месяцев после прививки в сравниваемых группах также были статистически не значимыми. Вакцину «Гриппол®плюс» можно рекомендовать как препарат выбора в рутинной практике иммунизации в Республике Казахстан, поскольку включенный в состав Полиоксидоний обладает антиинфекционной, противоопухолевой и детоксицирующей активностью. Аналогов такого адъюванта в мире не существует.
Грипп - чрезвычайно заразное массовые и наиболее динамичное острое вирусное заболевание. По данным ВОЗ в мире ежегодно заражаются приблизительно 1,2 млрд человек с риском серьезного течения инфекционного процесса, в том числе 350 млн пожилых людей старше 65 лет, 140 млн младенцев и 700 млн детей и взрослых с хроническими проблемами со здоровьем, а также 24 млн работников системы здравоохранения, имеющие тесный контакт заболевшими гриппом или ОРВИ пациентами во время сезонных эпидемий[1].
Необходимость борьбы с гриппом с помощью вакцинации обусловлена серьёзной медицинской значимостью, прежде всего, для предупреждения тяжелых форм осложнений в виде поражения органов дыхания, проявляющихся ярко выраженным нейтротоксикозом с гипертермическим и менингоэнцефалитическим синдромами, некротическим геморрагическим диатезом, вплоть до возникновения геморрагического отека легких, приводящих к летальному исходу [2, 4].
Также следует отменить и существующую социальную и экономическую значимость этой инфекций. По данным экспертов ВОЗ при ежегодных сезонных эпидемиях гриппа заболевают 5-10% взрослых и 20-30% детей (чаще младенческого возраста), ежегодная смертность от его осложненной формы составляет от 250 тысячи до 500 тысячи человек и приносят огромный экономический ущерб, составляющий 1-6 млн долларов США на 100 тысяч населения. Так, в США ущерб от ежегодных эпидемии гриппа составляет 10-15 млрд долларов; по расчетом ВОЗ в России даже при минимальных затратах (1 млн долларов США на 100 тысяч населении) ежегодный ущерб составляет около 1,5 млрд долларов США. Указанные выше медицинские проблемы и социальные и экономические потери этой инфекции могут многократно возрастать при переходе сезонных эпидемий в пандемию (обычно несколько раз в столетие), которая присуща только вирусу гриппа серотипа А [4].
Необходимо напомнить, что причины ежегодных эпидемии гриппа - быстрые и частые изменения антигенной специфичности гемагглютинина (Н) и нейраминидазы (N) и появление новых антигенных вариантов, «ускользающих» от антител, образовавших к предыдущему штамму вируса (дрейф). В то же время механизм возникновения вирусов, вызывающих пандемии происходит иначе. Они возникают в результате реассортации сегментов генов двух различных подтипов вирусов серотипа А гриппа, в результате чего появляются совершенно новый реассортант, содержащих сегменты генов, кодирующих гемаглютенина и нейраминидазы другого подтипа вируса. Зарождение нового подтипа вируса гриппа с новыми наружными белками (Н и N) одновременно и/или только гемаглютенина, легко распространяется и вызывает заболевание у огромного числа людей и, как следствие, высокую смертность, так как у заразившихся новым штаммом людей не успевает формироваться иммунитет, а производители также своевременно не могут создавать профилактические вакцины [4]. Еще один важный момент - невозможность прогнозировать появления пандемических штаммов, в отличие от эпидемических штаммов. Последних можно ежегодно отслеживать в базовых референтных вирусологических центрах, созданных ВОЗ и расположенных во всех континентах. Вакцинные препараты на
эпидемические штаммы создаются от актуальных в данный момент эпидемических штаммов гриппа.
Вышеприведенные данные о причинах возникновения эпидемических особенно пандемических штаммов гриппа, несвоевременности и опаздывания по созданию профилактических вакцин от пандемических вирусов для зашиты людей - это самые часто задаваемые вопросы со стороны большинства населения. Суть этих вопросов звучит примерно так: «Я прививалась от гриппа, но почему тогда заболел гриппом» или «Вакцина против гриппа не эффективна, поэтому люди часто повторно заболевают гриппом» и т.д [3,4]. К сожалению, не все практические врачи ПМСП могут ответить на подобные и другие вопросы простых обывателей. Отметим, что в возникновении таких ситуаций играют роль самые разнообразные причины, в частности, идентичность клинических проявлений гриппа и ОРВИ, поэтому люди зачастую путают обычный ОРВИ с гриппом; несовременность ежегодной вакцинации против сезонного гриппа, так как вирусу гриппа свойственна частые изменения антигенной структуры и сроки начала защитного иммунитета формируется только через 7-14 дней с момента заражения циркулирующим в данный момент возбудителя; состоянием коллективного иммунитета; уровнем высокой заболеваемости детей и именно они считаются основными распространителями гриппозной инфекции [3].
В Казахстане ежегодно вакцинируются более 400 тысяч человек за счет средств работодателей и личных средств населения. Вакцинация проводится в прививочных кабинетах поликлиник по месту жительства и в частных центрах вакцинации, имеющих соответствующие сертификаты для проведения подобной процедуры и прошедшие специальные курсы обучения по вакцинации, включая оказания квалифицированной медицинской помощи при возникновении нежелательных проявлений после прививки.
В данной статье рассматривается сравнительная оценка двух инактивированных гриппозных вакцин, из 5-ти зарегистрированных и разрешенных применению в Казахстане для ежегодной плановой вакцинации против гриппа - инактивированной субъеденичной (Инфлювак) вакциной и полимер-субъединичной вакциной («Гриппол®плюс») при проведении рутинной иммунизации взрослого населения в одном эпидемическом сезоне (20152016 гг.).
Цель исследования: оценить опыт клинического применения вакцины «Гриппол®плюс» в сравнении с «Инфлювак» в течение одного эпидемического сезона в рамках ежегодной вакцинации широко контингента лиц от гриппа в Республике Казахстана.
Задачи исследования:
- оценка местных и системных реакций после прививки инактивированными противогриппозными вакцинами «Гриппол®плюс» и «Инфлювак»;
- сравнительная оценка заболеваемости в течение 5-6 месяцев после вакцинации «Гриппол®плюс» и «Инфлювак».
Исследование проведено в трех клинических базах Казахстана, осуществляющих рутинную вакцинацию взрослых лиц (медицинский центр «САНА» и два клинические центры вакцинации ТОО «Фермаком»), с соблюдением всех необходимых требований, включая этических принципов Хельсинской декларации и Кодекса Республики Казахстан, «О здоровье народа и здравоохранения» от 18.09.2009 г. Вакцинация была проведена после письменного информированного согласия прививаемых, учтены противопоказания по применению изучаемых вакцин; в указанных выше клинических центрах имелись набор противошоковых средств и инструкций по их применению.
Всего в данном исследовательском проекте участвовали 1000 человек от 18 до 87 лет, которым в эпидемический сезон гриппа 2015/2016 гг были однократно введены испытуемые вакцины по 500 пациентов в каждой группе. Для оценки обычных и местных реакций на введение указанных гриппозных вакцин, заведена идентификационная регистрационная карта (ИРК) с закодированным номером в целях защиты личности пациента, который и использовался в документах исследования и проверялись на полноту и приемлемости в последующих анализах результатов.
Статический анализ данных проводился следующими методами: параметрические и непараметрические тесты, дисперсионный анализ, средние значения, стандартное отклонение, медиана, минимальные и максимальные значения, анализ различий с помощью t критерия Стьюдента или критерия Уилкоксона при параметрическом распределение данных, демографические данные с использованием таблиц частот, точного теста Фишера, критерия Х2 Пирсона, для описания категориалных данных - проценты или доли. Статистический анализ был выполнен с помощью специализированного программного обеспечения IBM SPSS Statistiсs (IBM Corporation, Armonk, New York, USA).
Оценка реактогенности прививаемых вакцин изучалась в течение 5 дней после введения на основании измерения температуры тела и оценки общих и местных проявлений на вакцину на протяжении всего периода наблюдения. Среди общих симптомов наиболее часто встречались недомогание (7,2% и 5,4%) и насморк (3,6% и 3,2%) в группах «Гриппол®плюс» и «Инфлювак». Реже всего у участников исследования выявлены миалгии/артралгии (0,4% и 1,0%) соответственно. Отметим, что статических различий между группами обнаружено не было. Среди местных реакций боль в месте инъекции наблюдались чаще всего и была выявлена у 2,8% участков в группе «Гриппол®плюс» и у 6,6% в группе «Инфлювак». Покраснение встречалась у 1,0% участков в обеих группах, зуд наблюдался у 0,4% и 0,2% участков соответственно в сравниваемых группах. Необходимо подчеркнуть, что увеличение регионарных лимфатических узлов не было зарегистрировано ни у одного из обследуемого в обеих группах. Припухлости/инфильтрата не обнаружено ни у одного из участников в группе «Гриппол®плюс», тогда как в группе «Инфлювак» данная реакция была выявлена у 0,8% участников исследования. Однако в сравниваемых группах участников статистически значимых различий выявлено не было.
Средние значения температуры тела вакцинируемых оставались в пределах 36,5-36,6°С на протяжении 5 дней, максимальные значения достигли 37,8°С в группе «Гриппол®плюс» в день введения вакцины и 38,0°С в группе «Инфлювак» во второй день. Различия статистически значимы при р<0,05. Динамика изменения температуры тела относительно исходного уровня была статистический значимой, кроме точки оценка «день 5» в группе «Инфлювак».
Таблица 1 - Температура тела: анализ различий в каждой точке исследования по сравнению с исходным значением (Критерии
|
Группа |
1 день |
0 день |
2 день - 0 день |
3 день - 0 день |
4 день - 0 день |
5 день - день |
0 |
|
|
Гриппол плюс |
Z* |
-8,236 |
-3,217 |
-5,144 |
-3,240 |
-2,414 |
||
|
Значение р** |
< 0,001 |
0,001 |
< 0,001 |
0,001 |
0,016 |
|||
|
Инфлювак |
Z* |
-9,197 |
-3,175 |
-3,199 |
-3,102 |
-1,297 |
||
|
Значение р** |
< 0,001 |
0,001 |
0,001 |
0,002 |
0,195 |
*Z - стандартизованное значение критерия Уилкоксона
**р - оценка значимости критерия Уилкоксона
Наиболее часто недомогание развивалось в 1, 2 и 3 дни после вакцинации. В день 1 частота развития недомогания составила 3,4% в группе «Гриппол®плюс» и 2,2 в группе «Инфлювак», в день 2 - 4,0% и 3,2% соответственно, в день 3 - 3,6% и 2,6%, соответственно (см. рисунок 1). Доля участников исследования с недомоганием статистически значима не различались между группами во все оцениваемые дни.
 Кашель развивался чаще всего на 2,3,4 и 5 день после вакцинации. На 2 день после вакцинации данный симптом отмечался у 0,2% участников в группе «Гриппол®плюс» и у 1,2% участников в группе «Инфлювак», на 3 день - у 0,4% и 1,2% участников соответственно, на 4 день - у 1,0% участников в обеих группах, на 5 день - у 1,0% участников в группе «Гриппол®плюс» и группе «Инфлювак» у 0,2% (рисунок 4).
Кашель развивался чаще всего на 2,3,4 и 5 день после вакцинации. На 2 день после вакцинации данный симптом отмечался у 0,2% участников в группе «Гриппол®плюс» и у 1,2% участников в группе «Инфлювак», на 3 день - у 0,4% и 1,2% участников соответственно, на 4 день - у 1,0% участников в обеих группах, на 5 день - у 1,0% участников в группе «Гриппол®плюс» и группе «Инфлювак» у 0,2% (рисунок 4).
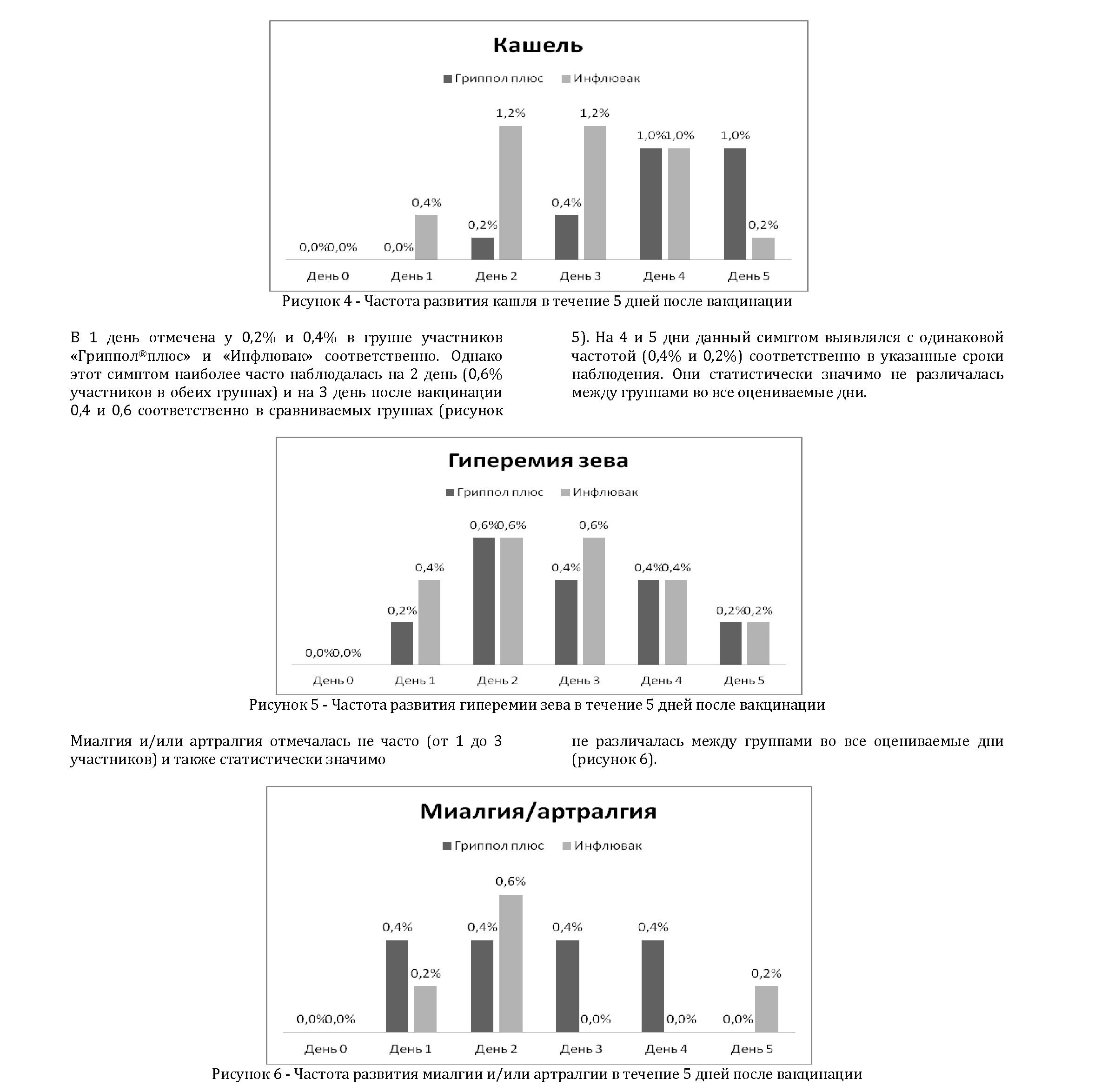 Боль в месте инъекции наиболее часто наблюдалась в 1, 2 и 3 день после вакцинации. В день 1 отмечалась у 2,6% и 3,4%, в день 2 - у 2,6% и 6,0%, (р=0,008) в день 3 - у 0,8% и 2,8% (р=0,08) участников в группах «Гриппол®плюс» и «Инфлювак», соответственно (рисунок 7). Эти данные статистически значимо ниже в группе «Гриппол®плюс», чем в группе «Инфлювак».
Боль в месте инъекции наиболее часто наблюдалась в 1, 2 и 3 день после вакцинации. В день 1 отмечалась у 2,6% и 3,4%, в день 2 - у 2,6% и 6,0%, (р=0,008) в день 3 - у 0,8% и 2,8% (р=0,08) участников в группах «Гриппол®плюс» и «Инфлювак», соответственно (рисунок 7). Эти данные статистически значимо ниже в группе «Гриппол®плюс», чем в группе «Инфлювак».
Зуд в месте инъекции отмечался в группе «Гриппол®плюс» у 1 участника (0,2%) в день 1 и день 2 и у 2 участников (0,4%) в день 3. В группе «Инфлювак» данный симптом отмечался у 1 человека (0,2%) в день 5 (рисунок 10). Эти данные между группами статистически значимо не различалась между группами во все оцениваемые дни (рисунок 10).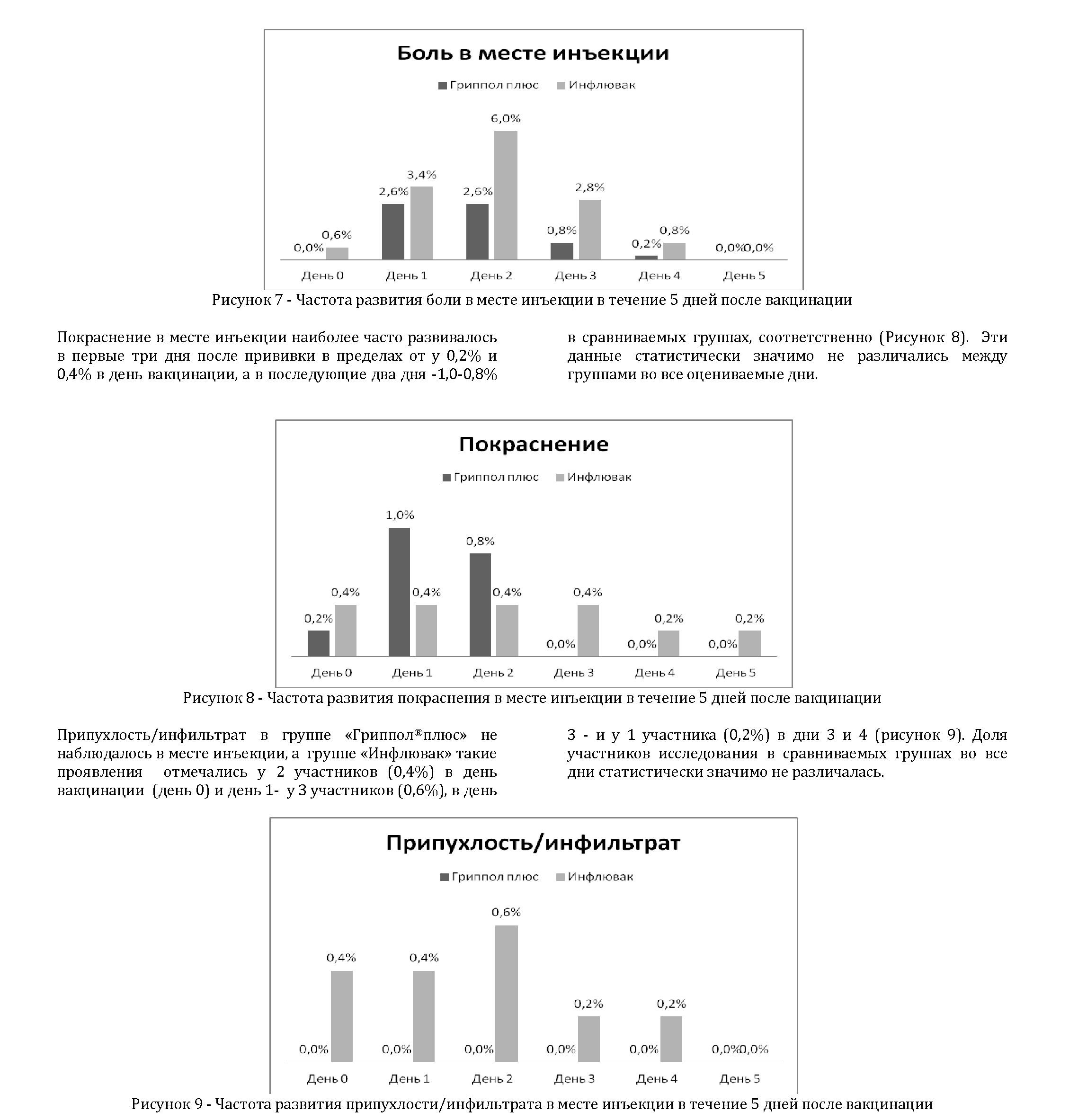
Увеличение регионарных лимфоузлов ни у кого из участников исследования не наблюдалось в течение 5 дней после прививки.
Общее заключение.
Оценка инфекционной заболеваемости за 6-месячный период после вакцинации показала, что ОРВИ или другие инфекций дыхательных путей развивались у 18,8% (94) участников, получивших вакцину «Гриппол®плюс», и у 17,2% (86) участников, получивших вакцину «Инфлювак» (различия не были статистически значимыми, р = 0,520).
При оценке реактогенности сравниваемых двух вакцин за время исследования среди общих симптомов у участников исследования наиболее часто встречалось недомогание (7,2% и 5,4% группах «Гриппол®плюс» и «Инфлювак») соответственно. Реже всего были выявлены миалгии/артралгии у 0,4% и 1,0% в сравниваемых группах соответственно. Статистических различий между группами ни по одной из общих реакции выявлено не было.
Среди системных реакций на вакцину наиболее часто наблюдалось недомогание, в первые три дня после прививки (4,0% и 3,2% в группах соответственно). Другие системные реакции включали головную боль с частотой в группах сравнения 1,2% и 0,8% соответственно, насморк (до 2,0% в обеих группах), кашель (от 1,0% до 1,2% в группе сравнения, соответственно), а также отдельные случаи гиперемии зева и миалгии/артралгии. Частота развития системных реакций между группами не различалась (p > 0,05).
Что касается исследования с местными проявлениями - наличие боли в месте инъекций значимо различалось между группами (р=0,004). Этот симптом встречался с частотой у 2,8% и у 6,6% участников в группах «Гриппол®плюс» и «Инфлювак» соответственно. Среди всех местных проявлений боль в месте инъекций являлась наиболее частой.. Стоит отметить отсутствие увеличение регионарных лимфатических узлов ни у одного из участников исследования. Припухлость/инфильтрат не были зафиксированы в группе «Гриппол®плюс», хотя в группе «Инфлювак» данная реакция выявлена у 0,8% участников (эти данные статистически не были значимы).
Наиболее часто местные реакции на вакцину наиболее часто проявлялись в виде болезненности в месте инъекции, которая преимущественно отмечалась в первые три дня после вакцинации. При этом в день 2 (р = 0,008) и день 3 (р = 0,018) различия между группами были статистически значимыми. Другие местные реакции включали в себя покраснение, припухлость/инфильтрат и зуд. Такие проявления между сравниваемыми группами статистически значимыми не были. Увеличения регионарных лимфоузлов не наблюдалось в обеих группах.
Результаты данного эпидемиологического исследования перекликаются с данными по безопасности, полученными в клинических исследованиях.
Выводы.
- Реактогенность изученных вакцин проявлялась в виде системных (недомогание, головная боль, повышенная температура тела) и местных реакций. Последние представляли собой боль и покраснение в месте инъекции, реже - припухлость/инфильтрат и зуд. Наиболее часто встречающимися общими реакциями были недомогание и насморк.
- Среди местных проявлений боль в месте инъекции была зафиксирована наиболее часто. Стоит отметить, что частота развития болезненности в месте инъекции на 2 и 3 дни после вакцинации у лиц, получивших «Гриппол®плюс», была статистически значимо ниже, чем у лиц, получивших «Инфлювак». По остальным, как общим, так и местным реакциям статистических различий выявлено не было.
- Инфекционная заболеваемость в течение 6 месяцев после вакцинации статистически значимо не различалась между группами и составила 18,8% среди участников, получивших вакцину «Гриппол®плюс», и 17,2% среди участников, получивших вакцину «Инфлювак».
- Результаты проведенного исследования позволили оценить опыт клинического применения вакцин «Гриппол®плюс» и «Инфлювак» у широкого контингента взрослого населения в рамках вакцинации от гриппа в эпидсезон 2015/2016 в Республике Казахстан.
- Учитывая равноценность сравниваемых вакцин по всем изучаемым параметрам реактогенности и заболеваемости в целом для рутинной практики иммунизации необходимо применять вакцину «Гриппол®плюс» с инновационным иммуноадъювантом «Полиоксидоний» - как препарата выбора из числа зарегистрированных и рекомендованных в Республике Казахстан. Полиоксидоний имеет сходство с биополимером (белком), имеет широкий спектр действий - стимулирует как клеточный, так и гуморальный иммунный ответ, обладает противоопухолевым, антиинфекционным, антиоксидантным свойствами и не имеет в мире аналогов как по структуре, так и разноплановым полезным действиям на организм прививаемого человека.
СПИСОК ЛИТЕРАТУРЫ
- Ю.В. Лобзин Вакцинопрофилактика. Лекции для практических врачей. - СПб.: 2012. - 285 с.
- Шамшева О.В, Учайкин В.Ф. Медуницын В.М. Клиническая вакцинология. - М.: ГЭТАР-Медиа, 2016. - 576 с.
- Амиреев С., Жаикбаев Н.Ж., Муминов Т.А. Қолданыстағы иммунизация. Ұлттық нұсқаулық. - Алматы: 2017. - 637 б.
- Гендон Ю.З. Грипозные вакцины. Вакцины и вакцинация: национальное руководство. - М.: ГЭТАР-Медиа, 2011. - 880 с.
- Ильина С.В., Намазова-Баранова Л.С. Баранов Вакцинация для всех: простые ответы на непростые вопросы. Руководство для врачей. - М.: 2016. - 204 с.
- 6. Beutler B.A. TLRs and innate immunity // Blood. — 2009. — Vol. 113. — P. 1399-1407.
- Rou X.E., Yersin A. Contribution { l'étude de la diphtérie // Amn. Inst. Pasteur. - Paris: 1888. — Vol. 2. — P. 629-661.