В статье представлены результаты многоцентрового кросс-секционного исследования пациентов с диагнозом функциональной диспепсии (ФД)и группы контроля, которым был проведен ИФА грелина и глюкагоноподобного пептида-1 (ГПП-1) в плазме крови. Согласно полученным результатам, очевидна связь между нейрогуморальной регуляцией и клинической симптоматикой ФД, уровнем pH желудочного сока, показателями аккомодационной и эвакуаторной функций желудка, инфекцией H.pylori. Не смотря на разнонаправленное физиологическое действие, между грелином и ГПП-1 выявлена положительная корреляционная связь (r=0,492, p<0,001).
Введение. По данным широкомасштабных исследований функциональная диспепсия (ФД) встречается у 10% - 30% населения в зависимости от популяции [1,2]. Нередко пациенты с ФД «замаскированы» под другими диагнозами, более привычными для клинициста, однако не отвечающими требованиям мирового научного сообщества. Так, терапевт и гастроэнтеролог зачастую некорректнообъясняют причины имеющихся у больных диспепсических расстройств, отождествляя морфологический диагноз «хронический гастрит» с клиническим, несмотря на то, что - «хронический гастрит» не имеет какого-либо клинического эквивалента и протекает чаще всего бессимптомно [3].
Как любое функциональное нарушение моторики органов пищеварения, ФД представляет собой заболевание, обусловленное нарушением нейрогуморальной регуляциижелудка и двенадцатиперстной кишки.В этом аспекте интерес представляют гормоны APUD-системы - глюкагоноподобный пептид 1 (ГПП-1) и грелин.
Грелин – полипептид, который вырабатывается, в основном, «Х/А-подобными» клетками слизистой оболочки фундального отдела желудка и в гипоталамусе, стимулируя синтез соматотропного гормона. Онвлияет на различные физиологические процессы: повышает аппетит, имея анаболическое действие;усиливает продукцию соляной кислоты и двигательной активности желудка. Низкие уровни грелина в плазме ассоциируются с инсулинорезистентностью, артериальной гипертензией и ожирением [4]. ГПП-1 продуцируется в L-клетках дистального отдела кишечника и стимулирует секрецию инсулина. ГПП-1 также способен вызывать несколько дополнительных эффектов - ингибирование секреции глюкагона и эвакуаторной функции желудка [5]. Следовательно, грелин и ГПП-1 оказывают противоположные воздействия на регуляцию аппетита и потребление пищи. Целью данной работы было установить роль гормонов APUD-системы – грелина и ГПП-1 в патогенезе функциональной диспепсии.
Материалы и методы
Протокол исследования
Исследование являлось многоцентровым, основной клинической базой было гастроэнтерологическое отделение центральной городской клинической больницы №3 г.Донецка. Протокол исследования был одобрен комиссией по биоэтике Донецкого национального медицинского университета им.М.Горького и полностью соответствует принципам Хельсинской декларации по правам человека. Дизайн исследования: кросс-секционное. В него были включены 70 пациентов с установленным диагнозом ФД согласно Римским критериям IVи 20 здоровых добровольцев, составивших группу контроля. При сравнении обследуемых не было выявлено статистически значимых отличий распределения по полу, возрасту, индексу массы тела, следовательно, эти группы можно считать идентичными (таблица 1).
Таблица 1 - Сравнительная характеристика основных параметров группы контроля и ФД
|
Параметры |
Группа контроля (N=20) |
ФД (N=70) |
p |
|
Мужчины/женщины |
5/15 |
8/27 |
0,889 |
|
Возраст, годы |
37,2±14,8 |
44,07±15,54 |
0,497 |
|
ИМТ, кг/м2 |
22,7±4,3 |
23,8±5,37 |
0,383 |
Критериями включения в исследование были пациенты, подписавшие информированное согласие на участие в исследовании, в возрасте от 18 до 75 лет, при наличии у них в соответствии с Римскими критериями IV как минимум одного из следующих длящихся не менее 3 последних месяцев и возникших впервые не менее 6 месяцев назад симптомов: чувства переполнения после еды; раннего насыщения; эпигастральной боли; эпигастрального жжения (чаще 1 раза в неделю). При этом обязательно должны были отсутствовать органические, системные или метаболические заболевания, которые могли бы сопровождаться аналогичными симптомами. Критериями исключения служили наличие любого симптома, указывающего на злокачественное заболевание; язвенная болезнь желудка в анамнезе; увеличение АСТ, АЛТ, креатинина более 1,5 норм; злоупотребление наркотиками или алкоголем; беременные или кормящие женщины; пациенты с индексом массы тела (ИМТ) более 30 кг/м2; прием препаратов, влияющих на моторику желудочнокишечного тракта и/или секреторную функцию желудка, а также центральную нервную систему в течение 4 недель до начала исследования.
Диагностические процедуры
Всем исследуемым была выполнена эзофагогастродуоденоскопия с уреазным тестом и внутрижелудочной эндоскопической pH-метрией. Для оценки моторики желудка и показателей висцеральной гиперчувствительности был разработан УЗИ тест с питьевой нагрузкой. Исследование аккомодационной и эвакуаторной функций осуществлялось путем измерения площади сечения свода желудка во время питьевой нагрузки и после ее окончания. Во время процедуры фиксировались ощущения дискомфорта или боли,интенсивность которых оценивалась по 5-балльной шкале Likert. Исследование уровня ацил-грелина и ГПП-1 в плазме крови проводили на автоматическом иммуноферментном анализаторе № АС-71АА1169 (США) с использованием тест-систем производства RayBio Human Ghrelin EIA Kit (США) и YK160 GLP-1 EIA Kit (Япония) в соответствии с инструкциями производителя. Учитывая, что по данным литературы [6,7] показатели содержания ацил-грелина и ГПП-1 в крови являются вариабельными, для оценки результатов анализа крови пациентов с ФД были использованы результаты группы контроля.
Статистический анализ
Характер распределения цифровых данных определяли с помощью критериев хи-квадрат (χ2), Стьюдента и Вилкоксона. Для оценки плотности корреляционной связи между признаками рассчитывали параметрический коэффициент Пирсона. Результаты, полученные при p<0,05, считались статистически значимыми. Формирование, хранение, анализ электронной базы данных, статистическая обработка и визуализация результатов исследований выполнены в лицензионных пакетах: MedStat v. 4 и NCSS (PASS 11).
Результаты и обсуждение.
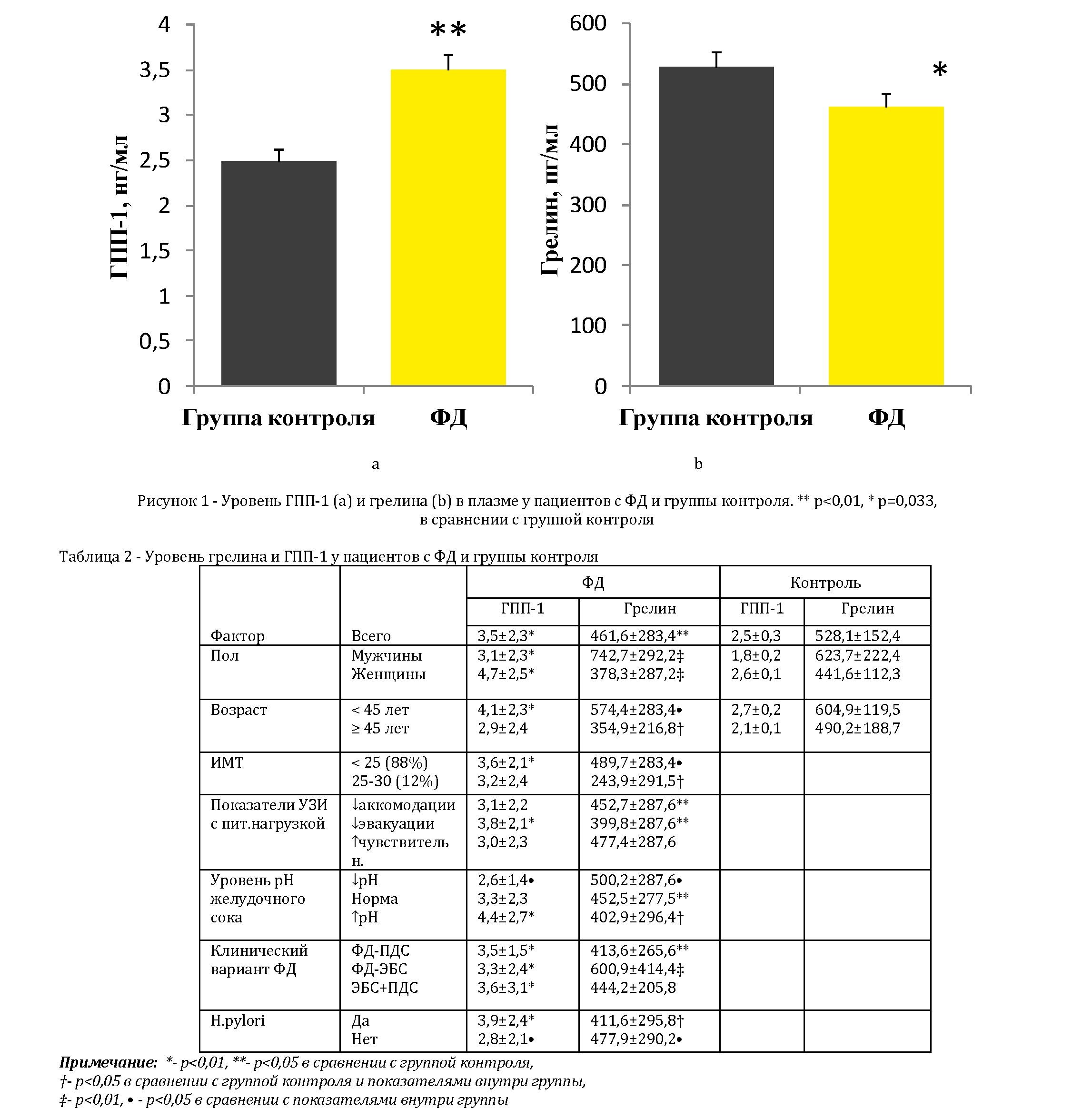
Результаты проведенного лабораторного исследования (рисунок 1) продемонстрировали достоверное повышение плазменного содержания ГПП-1 - 3,5±2,3 нг/мл (р<0,01) и снижения уровня грелина 461,6±283,4 пг/мл (р=0,033) в группе ФД (по сравнению со значениями группы контроля - 2,5±0,3 нг/мл и 528,1±152,4 пг/мл).
В качестве возможных предикторных факторов, определяющих выраженность секреторного ответа гастроинтестинальных гормонов, были изучены: гендерная принадлежность пациентов, возраст, ИМТ, показатели УЗИ желудка с питьевой нагрузкой, pH желудочного сока, клинический вариант ФД (эбигастральный болевой синдром (ЭБС), постпрандиальный дистресс-синдром (ПДС), overlap-вариант - ЭБС+ПДС) и наличие инфекции H.pylori (таблица 2).
В группе ФД у женщин был незначительно повышен уровень ГПП-1 и снижен уровень грелина, что по-видимому связано с гендерными различиями клинических вариантов заболевания (p=0,004).
 Содержание ГПП-1 в плазме крови больных ФД было незначительно выше в группе моложе 45 лет, чем у лиц старшего возраста (p=0,113), однако было значимо выше показателей группы контроля ≥ 45 лет (p=0,006). Некоторое снижение секреции ГПП-1 (ключевого гормона инкретинового ряда), может быть одной из причин увеличения распространенности СД 2 типа среди пожилых лиц. Уровень грелина у пациентов с ФД моложе 45 лет был выше, чем у лиц старшего возраста (p=0,029). При этом содержание плазменного грелина в группе ФД ≥45 лет было значимо ниже нормы (p=0,038). Учитывая, что грелин стимулирует секрецию соматотропина, можно предположить участие этого желудочного гормона в регуляции роста и развитии организма.
Содержание ГПП-1 в плазме крови больных ФД было незначительно выше в группе моложе 45 лет, чем у лиц старшего возраста (p=0,113), однако было значимо выше показателей группы контроля ≥ 45 лет (p=0,006). Некоторое снижение секреции ГПП-1 (ключевого гормона инкретинового ряда), может быть одной из причин увеличения распространенности СД 2 типа среди пожилых лиц. Уровень грелина у пациентов с ФД моложе 45 лет был выше, чем у лиц старшего возраста (p=0,029). При этом содержание плазменного грелина в группе ФД ≥45 лет было значимо ниже нормы (p=0,038). Учитывая, что грелин стимулирует секрецию соматотропина, можно предположить участие этого желудочного гормона в регуляции роста и развитии организма.
У лиц с повышенной массой тела отмечались сниженные показатели ГПП-1 и грелина (р=0,038), выявлено наличие отрицательной связи между ИМТ и уровнем ГПП-1 (r= -0,34, р=0,015) и грелина (r = -0650, р=0,03). Несмотря на то, что в данной работе нельзя было оценить причинноследственную связь между низким уровнем ГПП-1, грелина и наличием у пациента ИМТ 25-30 кг/м2, можно утверждать, что грелин и ГПП-1 участвуют в регуляции жирового обмена [8-10].
С возрастом концентрация обоих гормонов снижалась, однако влияние на секреторную и моторную активность желудка было противоположным: при повышении уровня ГПП-1 отмечалось снижение скорости опорожнения (p=0,007) и повышение pH желудочного сока, а при уменьшении содержания грелина было выявлено снижение способности желудка к растяжению и эвакуации (p<0,05). В группе с гиперацидностью определялось повышенное содержание грелина (p<0,05). Содержание ГПП-1 в плазме крови больных с ФД было повышено, в сравнении с группой контроля, независимо от клинического варианта. Понижение концентрации грелина было зафиксировано у пациентов с ПДС и сочетанным вариантом ФД, в сравнении с ЭБС (p<0,01). Также уровень грелина был статистически значимо ниже в группе ПДС, в сравнении со здоровыми добровольцами (p=0,041). Учитывая функции грелина, его роль больше выражена в патофизиологии ПДС, чем ЭБС. При изучении уровня ГПП-1 в группе Н. pylori-позитивных пациентов были получены значимо высокие результаты, в сравнении с нормой (p=0,007) и Н. pylori-негативными пациентами (p<0,05). У Н. pylori-позитивных пациентов уровень грелина был значительно ниже, чем у Н. pylori- негативных и группы контроля (p<0,05). Можно сделать заключение о том, что снижение уровня грелина имеет обусловленную инфекцией H.pylori связь с осью модуляции соматостатин — гастрин — кислота.
С помощью корреляционного анализа была выявлена положительная корреляционная связь между уровнем грелина и ГПП-1 в плазме больных ФД (r=0,492 на уровне значимости p<0,001), однако конечно он не учитывал влияние какого-либо еще фактора извне, поэтому на вопрос - является ли резкое повышение ГПП-1 компенсаторным в ответ на гипергрелинемию или наоборот - однозначного ответа пока нет.
Заключение.
Отсутствие морфологического субстрата делает весьма актуальной задачу поиска лабораторных и инструментальных маркеров функциональных заболеваний. Грелин и ГПП-1влияют на уровень секреторной и двигательной активности желудка, что указывает на их роль в патогенезе различных клинических вариантов ФД. Однако важно отметить, что проведенное исследование имело ряд ограничений. Дизайн кросс-секционного (одномоментного) исследования не позволяет проследить ход изменений секреции ГПП-1 и грелина у больных с ФД под воздействием терапии. Определение плазменной концентрации изучаемых гормонов в качестве потенциальных биомаркеров риска развития ФД возможно, но изучаемая выборка больных (n=70) не является достаточно репрезентативной для оценки точности результатов грелина и ГПП-1 в качестве диагностического критерия ФД. Следует учесть, что и полученные показатели уровней гастроинтестинальных гормонов в группе здоровых добровольцев могут быть приняты только за относительную норму, так небольшой размер выборки (n=20) не позволяет утверждать, что они являются средне популяционными параметрами.
Результаты исследования определили потенциальные конечные точки для будущих клинических испытаний. В дальнейшем необходимо нейрофизиологическое изучение взаимного влияния грелина и ГПП-1, так как, не смотря на разнонаправленное действие двух ключевых гастроинтестинальных гормонов, между ними выявлена положительная корреляционная связь. Повышение ГПП-1 в ответ на повышение грелина и наоборот может означать выполнение ими контррегуляторной работы в поддержании равновесного состояния ЖКТ.
СПИСОК ЛИТЕРАТУРЫ
- Drossman D., Hasler W.L. Rome IV—Functional GI Disorders: Disorders of Gut-Brain Interaction // Gastroenterology. – 2016. - №150 (6). – Р. 1257-1261.
- Tack J. Functional dyspepsia—symptoms, definitions and validity of the Rome III criteria. Nat. Rev // Gastroenterol. Hepatol. – 2013. - №10. – Р.134–141.
- Ивашкин В.Т., Шептулин А.А., Трухманов А.С. и соавт. Клинические рекомендации по диагностике и лечению функциональной диспепсии. - М.: 2016. – 43 с.
- Korbonits M. Ghrelin – a gormone with multiple functions // Front Neuroendocrinol. – 2004. - №25. – Р. 27-68.
- Steinert Robert E. The role of the stomach in the control of appetite and the secretion of satiation peptides // American Journal of Physiology - Endocrinology and Metabolism. – 2012. - №302(6). – Р. 666-673.
- Date Y. Ghrelin, a novel growth hormone-releasing acylated peptide, is synthesized in a distinct endocrine cell type in the gastrrointestinal tracts of rats and humans // Endocrinology. – 2000. - №141. – Р: 4255-4261.
- Takakazu Y. The role of ghrelin in patients with functional dyspepsia and its potential clinical relevance (Review) // International journal of molecular medicine. – 2013. - №32. – Р. 523-531.
- Akamizu T. Repeated administration of ghrelin to patients with functionaldyspepsia: its effects on food intakeand appetite // Eur J Endocrinol. – 2008. - №158. – Р. 491–498.
- Horvath T.L. Minireview: Ghrelin and the regulation of energy balance – a hypothalamic perspective // Endocrinology. – 2001. - №142. – Р. 4163-4169.
- Schwartz M.W. Central nervous system control of food intake // Nature. – 2000. - №404. – Р. 661-671.