Иммуноглобулины для внутривенного введения (ВВИГ) занимают заметное место в комплексной терапии инфекционно-воспалительных осложнений. Изучена клиническая эффективность ВВИГ у 67 детей, больных онкогематологической патологией. Отмечено в 92,3% случаев улучшение состояния онкогематологических больных в периоде агранулоцитоза, снижение частоты и тяжести инфекционных осложнений, быстрая нормализация показателей крови.
В настоящее время иммуноглобулины для внутривенного применения (ВВИГ) используются для лечения инфекционно-воспалительных осложнений, которые возникают на фоне вторичного иммунодефицита у больных с острой и хронической лейкемией [1,2]. Наличие инфекционных осложнений у онкогематологических больных в значительной степени усложняет лечение и ухудшает прогноз основного заболевания. Это связано, прежде всего, с подавлением как специфического, так и неспецифического механизма резистентности организма больного к опухолевому заболеванию, а также химиотерапией, которая используется при лечении данного контингента пациентов и еще больше подавляет иммунные реакции организма [3,4].
В периоде миелотоксического агранулоцитоза часто у больных с онкогематологической патологией отмечается развитие септического состояния [1,4,5]. При развитии инфекционных и деструктивных осложнений возникает необходимость прерывания специфического лечения острого лейкоза, не соблюдаются сроки проведения этапов программной полихимиотерапии (ПХТ), что приводит к снижению ее эффективности. В таких ситуациях в качестве сопроводительной терапии, наряду с использованием комплекса антибактериальных, антимикотических и противовирусных препаратов системного и локального действия, стимуляции гранулоцитарного колониестимулирующиего фактора (G-CSF), для профилактики и лечения инфекционных осложнений при эпизодах фебрильной нейтропении применяют ВВИГ [2,5,7]. Таким образом, применение препаратов ВВИГ показано в особо тяжелых случаях инфекций у пациентов с нейтропениями различного генеза (период миелотоксического агранулоцитоза после программной химиотерапии) для быстрой инактивации и удаления инфекционно-токсических факторов [3,8].
Целью нашего исследования явилось изучение эффективности применения ВВИГ у онкогематологических больных.
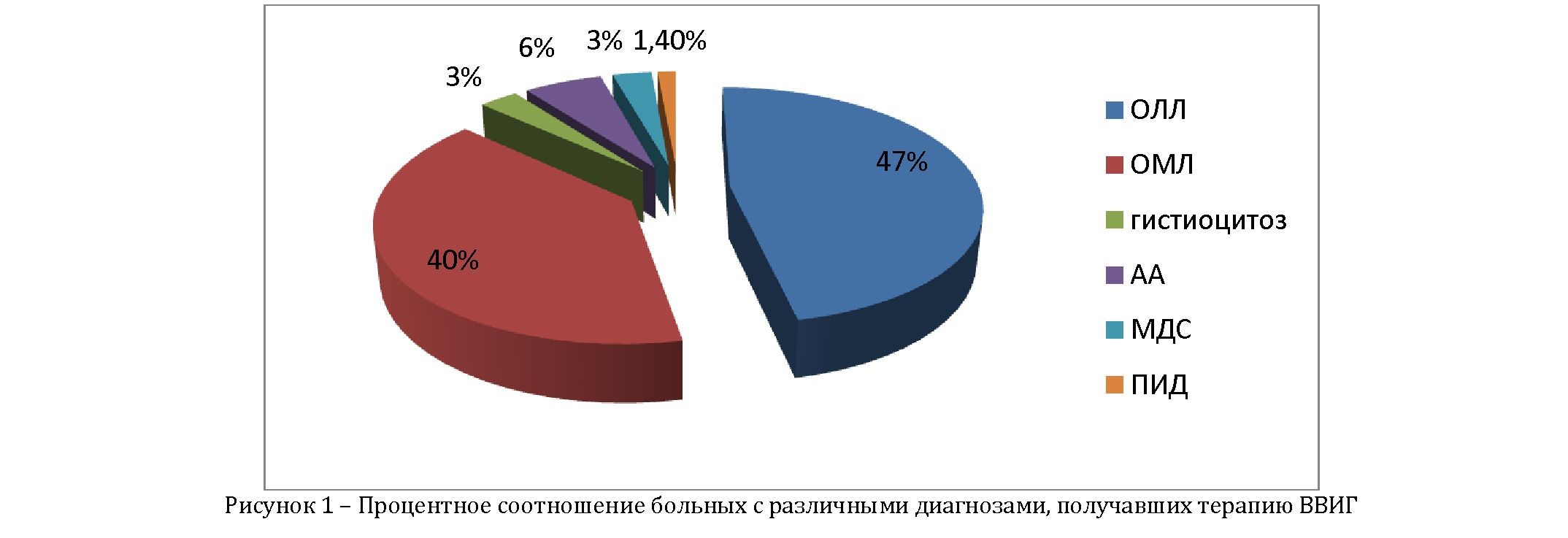
Материал и методы исследования. Изучены 67 историй стационарных больных с различной онкогематологической патологией, находившихся на лечении в Научном центре педиатрии и детской хирургии (НЦПиДХ). ВВИГ, как препарат, обладающий широким спектром опсонизирующих и нейтрализующих антител, в практике НЦПиДХ применялся в следующих ситуациях: для лечения гнойносептических осложнений (при нейтропении) у больных с острым лимфобластныстным лейкозом (ОЛЛ) – 47% (32), острым миелобластным лейкозом (ОМЛ) – 40% (26), гистиоциотозом – 3% (2) на различных этапах терапии, у больных с апластической анемией (АА) – 6% (4), миелодиспластическим синдромом (МДС) – 3% (2) и первичным иммунодефицитом (ПИД) – 1 (1,4%) (рисунок 1).
Больным, получавшим внутривенный иммуноглобулин по поводу инфекционных осложнений, назначалась разовая доза 0,2 г/кг/сутки. ВВИГ вводили ежедневно 1 раз в день, продолжительность курса составляла от 1 до 7 дней.
Эффективность препарата у больных с онкогематологической патологией и инфекционными осложнениями оценивалась по нормализации температуры тела. Состояние пациентов оценивали по результатам общего анализа периферической крови с определением абсолютного содержания гранулоцитов, общего анализа мочи, трехкратного бактериологического посева крови и мочи с постановкой реакции чувствительности к антибиотикам.
Побочные эффекты препарата контролировались как по клиническим проявлениям (головная боль, тошнота, боли в животе, озноб, одышка), так и по лабораторным показателям. В сыворотке крови определяли уровень аланинаминотрансфераз (АЛТ) и аспартатаминотрансферазы (АСТ) мочевину, билирубин.
Результаты и обсуждение. Пациенты, получавшие ВВИГ в связи с наличием инфекционных осложнений, были на различных этапах терапии. Больные с острым
лимфобластным лейкозом получали терапию по программе ALL-BFM-2002, c миелобластным лейкозом – AML-BFM-2004, с гистиоцитозом LCH-III, с апластической анемией – иммуносупрессивную терапию.
Из 32 пациентов с ОЛЛ – 65,6% (21) были на I-протоколе, 4 больных (12%) получали рецидивные блоки, 18,7% (6) были на II-протоколе и один пациент был на поддерживающей терапии. Из 26 больных с ОМЛ – 46% (12) были на этапе индукции, 6 (23%) больных получали противорецидивную терапию, 30,7% (8) были на протоколе – AML-BFM-2004.
На сегодняшний день основным средством профилактики и лечения инфекционных осложнений является антибактериальная терапия, однако в ряде случаев она не позволяет достичь желаемого результата [2,11]. У больных острым лейкозом в периоде агранулоцитоза отмечается развитие септического состояния без локализованных очагов инфекции. От сепсиса погибает 10-20% пациентов [3,7,9,11].
Инфекционные осложнения у исследуемых пациентов включали сепсис, протекавший в виде сепсиса без локализованных очагов инфекции -15,3%, септицемии – 2,6%, сепсис с септикопиемией – 10,2%, фебрильной нейтропении – 78,6%. Локализация пиемических очагов включала в себя бактериальный кардит – 2,8%, язвеннонекротический колит – 8,5%, пневмонию – 10,8%, язвеннонекротический стоматит – 20,8%.
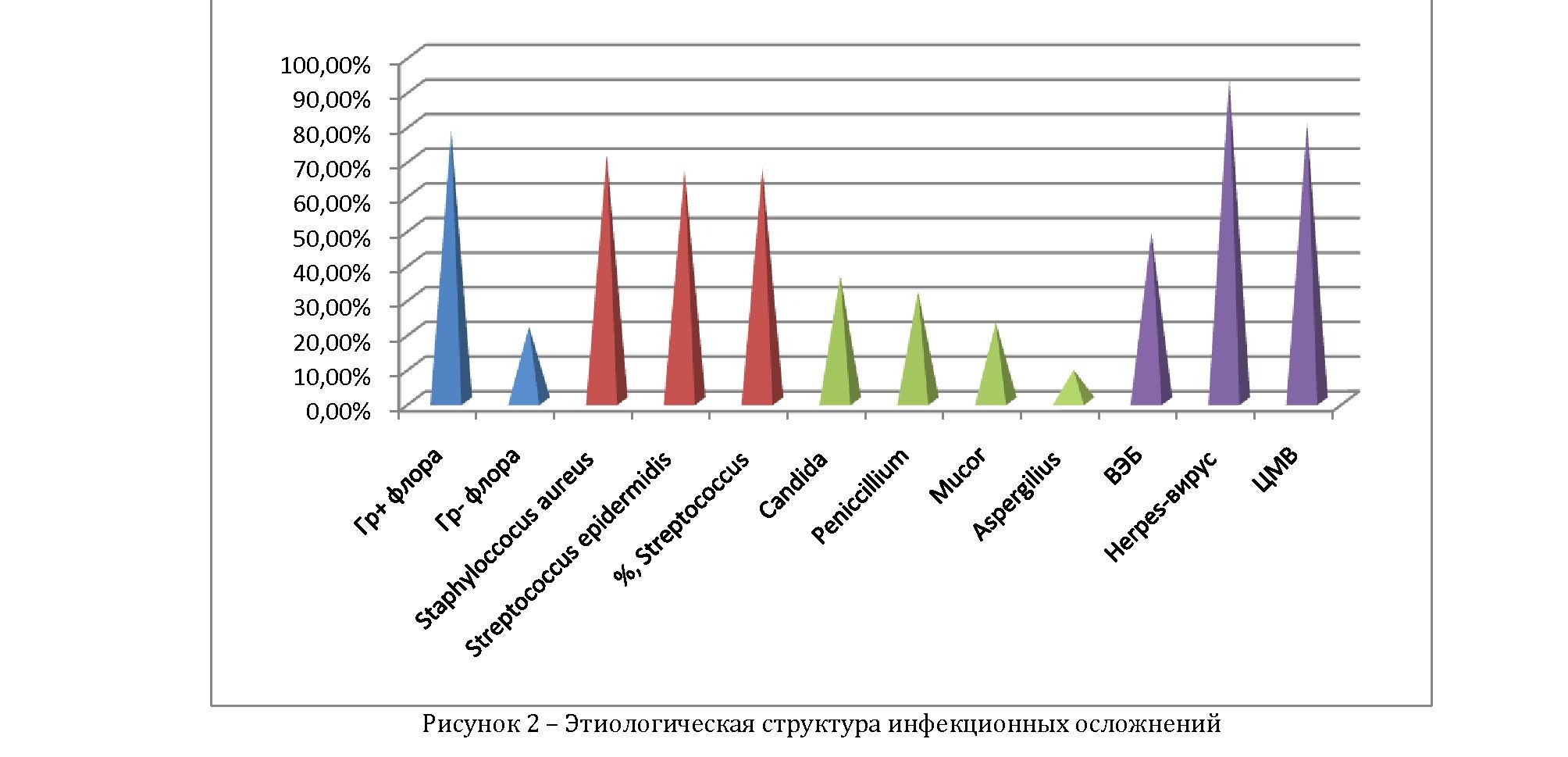
Присоединение инфекции протекало на фоне глубокой цитопении–нейтропении (лейкоциты менее 1х109/л, гранулоциты менее 0,5х109/л). Микробный пейзаж больных был представлен в 78,4% случаях грамположительными микроорганизмами, в 21,6% – грамотрицательными микроорганизмами. Из крови больных высевалась грамположительные патогенны – 55%. Среди них наиболее часто Staphyloccocus aureus – 71,2%, Streptococcus epidermidis – 66,7%, Streptococcus – 67,5% (рис 2).
В структуре грибковой инфекции высевались Candida (36,4%), Peniccillium (31,8%), Mucor (22,7%), Aspergilius (9,1%). Грибы чаще, чем из других источников инфекции, высевались из крови (72,6%).
Маркеры к вирусу Эпштейн-Барра (ВЭБ) были серопозитивны у 48,9% детей, к Herpes-вирусу у 93,3% детей, к цитомегаловирусу (ЦМВ) у 80,2%. Из них уровень IgМ был повышен к ВЭБ в 7,8% и к Herpes-вирусу в 5,5% случаев.
Таким образом, использование ВВИГ в терапии тяжелой бактериальной, грибковой и вирусно-бактериальной инфекции у детей имело убедительное патогенетическое обоснование. Известно, что при тяжелой, особенно генерализованной, инфекции в организме больного образуется избыток продуктов нормального или нарушенного обмена веществ, продуктов клеточного реагирования [6,10]. Эти вещества, накапливаясь, становятся для организма эндогенными токсическими субстанциями, вызывающими интоксикацию. Наличие одновременно бактериальной антигенемии и токсемии у больного усугубляет интоксикацию и приводит к нарушению нормальных межклеточных взаимодействий в иммунном ответе. Эта ситуация усиливается при развитии полиорганной недостаточности, сопровождающей тяжелую инфекцию и сепсис [8,11].
Лечение иммуноглобулином начиналось после назначения антибиотиков широкого спектра (цефалоспорины II, III, IV поколения) и отсутствия от них эффекта в течение суток или одновременно с антибиотиками при наличии признаков бактериального шока и прекращалось после нормализации температуры. Продолжительность лечения препаратом составила от 1 до 7 дней. Всего зарегистрировано 162 эпизода применения ВВИГ. 7 дней получали два пациента (4%), по одному дню получали 27 больных (40%), остальные 56% по 2-3дня введения ВВИГ.
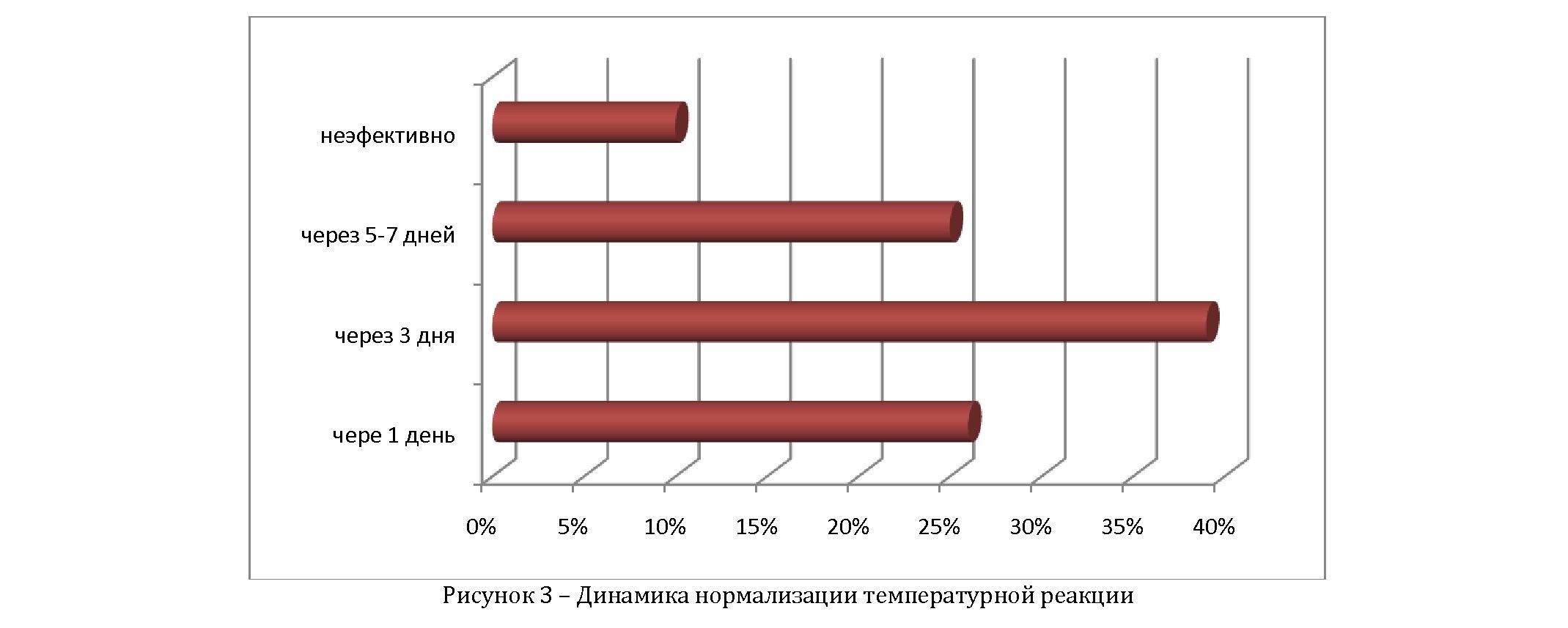
Динамика температурной реакции была следующей: исходная температура – 38,4±0,36°С; через 1 день от начала введения нормализовалась у 18 больных (26%), через 3 дня от начала введения ВВИГ у 25 больных (39%), через 5-7 дней у 17 больных (25%) (рис.3). Положительное действие препарата проявлялось в стабилизации и улучшении общего состояния ребенка. Наряду с нормализацией температуры отмечено, снижение явлений интоксикации, восстановление гранулоцитов.
Из пациентов, у которых ВВИГ был неэффективен в 10% (7) случаях, в основном были больные с прогрессированием основного заболевания, рецидивами ОЛЛ (1) и ОМЛ (2), один пациент с МДС – резистентный к терапии, с проявления грибкового сепсиса (1) и не достигшие ремиссии (1). У больных с апластической анемией и у пациентов с МДС, клинически наблюдались нормализация температуры тела и полное рассасывание пневмонических очагов, но не получено эффекта в плане значимого прироста тромбоцитов, а также сохранялась гранулоцитопения.
Побочные реакции при применении ВВИГ проявлялись в виде возникновения субфебрильной температуры (3,2%), головной боли (1,8%), гиперемии кожи (2,7%), которые легко купировались уменьшением скорости инфузии или назначением антигистаминных средств. Ни у одного из пациентов не отмечалось угрожающих жизни состояний. И ни в одном случае лечение не было прекращено.
В некоторых случаях у больных с острыми лейкозами лечение иммуноглобулином начиналось при незначительно повышенном уровне билирубина, АЛТ, АСТ и мочевины, после лечения ВВИГ он снижался или оставался прежним, но не было, ни одного случая повышения исходных показателей. Исследование уровня иммуноглобулинов сыворотки крови проводилось не всем пациентам, но тем пациентам (4,2%), которым проводилось, в ходе терапии ВВИГ не выявило каких-либо значимых изменений количеств IgA и IgM. У больных, получавших ВВИГ свыше 3 дней, имело место повышение уровня IgG по сравнению с исходным уровнем.
Выводы. Применение иммуноглобулина в комплексной терапии онкогематологических больных в периоде миелотоксического агранулоцитоза позволило добиться улучшения состояния в 92,3% случаев.
Снизились частота и тяжесть инфекционных осложнений, происходило более быстрое восстановление гемопоэза, ускорялась нормализация анализов крови, что позволило уменьшить перерывы в проведении химиотерапии.
Высокая частота инфекций, увеличивающих перерывы в приеме цитостатиков, побуждает к профилактическому введению иммуноглобулинов на фоне проведения стандартной антибиотикотерапии для снижения частоты инфекций у пациентов групп риска.
СПИСОК ЛИТЕРАТУРЫ
- Аверченков В.М., Палагин И.С. Внутривенный иммуноглобулин: механизм действия и возможности клинического применения // Проблемы терапии. – 2004. - №3. - С. 273-281.
- Румянцев А.Г.Основные свойства внутривенного иммуноглобулина и показания к их применению // Вопросы гематологии/онкологии и иммунопатологии в педиатрии. – 2011. - №2. - С. 39-43.
- Шарыгин С.Л., Целоусова О.М., Лазыкина А.В. и др. Клиническая эффективность иммуноглобулина для внутривенного введения в комплексной терапии острого лейкоза у детей // Сборник научных статей. – 2008. – Вып.2. – С. 16-24.
- Blanchette v.S., Kirby М.А., Turner С. Role of intravenous Immunoglobulin G in Autoimmune Hematologic Disorders // Sem. In Hem. – 1992. - Vol.29., №3. - Р.72-82.
- George J.N., Woolf S.H., Raskob G.E. et al. Idiopathic Trombocytopenic Purpura // A Practice Guideline Developed by Explicate Methods for American Society of Hematology. – 1996. - Vol.88., №1. - Р.33-40.
- Nydegger U.E. Intravenous Immunoglobulin in combination with other prophylactic and therapeutic measures // Transfusion. – 1992.- Vol.32., №1. - Р.72-81.
- Pajkrt D., Van Deventer S.J.H. Immunomodulation of Septic Shock // Antiinf. Drugs and Chemotherapy. – 1995. - Р.125-128.
- Sacher R.А., Intravenous Gammaglobulin Therapy: Current Role in Bone Marrow Transplant, Malignancy, and Immune Hematologic Disorders // Sem. In Hem. - 1992. - Vol.29., №3. - Р.1–5.
- Бебеппсо В.Т., Бруслова К.М., Чумак А.А. и др. Застосування імуноглобуліну для внутрішньовенного введения у дітей із гострими лейкеміями // Украинский журнал гематологии и трасфузиологии. – 2005. - №2. - С.16–20.
- Боровикова Н.В., Гришин А.В., Благовестов Д.А. и др. Профилактический эффект введения внутривенного иммуноглобулина у больных с тяжелым острым панкреатитом // Проблемы гематологии и переливания крови. – 2006. - №1. - С.12-19.
- Искакова А.С. Патогенетические особенности инфекционных осложнений и их лечение у детей с острым лейкозом на программной терапии: Автореф. Дисс. ... д-р.мед.наук – Алматы, 2007. – 32 с.