В данной статье описывается подбор оптимального твердого носителя для иммобилизации хемолито- трофных бактерий для разработки проточного биореактора. В результате иммобилизации бактериальных клеток время окисления свежей питательной среды было сокращено с 6 до 4 суток при использовании шлака, до 3 суток — керамзита и до 2 суток — пенополиуретана. Изучена эффективность окисления двухвалентного железа в проточном биореакторе иммобилизованными бактериями при различных концентрациях серной кислоты. Во всех биореакторах при коэффициенте разбавления в диапазоне от 0,051 до 0,14 ч–1 производительность трехвалентного железа и степень окисления двухвалентного железа были сравнительно высокими. Наибольшая производительность трехвалентного железа была достигнута при рН 1,6, которая составила 1,16 г·л–1·ч–1, что в 23,2 раза выше, чем в суспензионной культуре. Также проведены модельные испытания в перколяционных колоннах для сравнения динамики извлечения меди при традиционной сернокислотной технологии и бактериальной технологии. Испытания по выщелачиванию меди были проведены в колоннах высотой 2 м и диаметром 0,2 м на руде с крупностью 10 мм. В результате проведения модельных испытаний в течение 155 суток выход меди при бактериальном выщелачивании оказался на 34,8 % больше, чем при сернокислотном выщелачивании.
Введение
Постоянно истощающиеся запасы рентабельных месторождений вызывают необходимость разработки новых высокоэффективных и экономически привлекательных методов извлечения металлов из бедных месторождений [1].
В последнее время для руд с низким содержанием ценного металла активно развивается метод подземного выщелачивания меди. Тем не менее, в связи с сокращением запасов окисленных медных руд, возникает необходимость в переработке упорных руд. Однако такие руды общепринятыми методами плохо поддаются выщелачиванию. В этом аспекте большую помощь оказывает биогеотехнология, которая основана на природной способности хемолитотрофных бактерий (Acidithiobacillus ferrivorans, Acidithiobacillus ferrooxidans, Acidithiobacillus thiooxidans и др.) разрушать упорные сульфидные минералы и высвобождать ценные металлы [2, 3].
В настоящее время промышленное применение хемолитотрофных бактерий, с целью извлечения ценных компонентов из руд, достигло широких масштабов во многих странах [3, 4].
Материалы и методы исследований
Объектом исследования являются процессы выщелачивания сульфидных руд и хемолито- трофные бактерии, окисляющие соединения серы и железа: Acidithiobacillus ferrivorans, Acidithiobacillus ferrooxidans, Acidithiobacillus thiooxidans.
В работе были использованы следующие питательные среды:
Среда Ваксмана, г/л: сера (серный цвет) — 10,0; (NH4)2SO4 — 0,3; KH2PO4 — 3,0; CaCl2∙6H2O — 0,25; MgSO4∙7H2O — 0,5; FeSO4∙7H2O — 0,01; вода дистиллированная — 1000 мл.
Среда Сильвермана и Люндгрена 9К [5]: 1-й раствор: в 700 мл дистиллированной воды растворяют (г): (NH4)2SO4 — 3,0; K2HPO4 — 0,5; KCl — 0,1; MgSO4∙7H2O — 0,5; Ca(NO3)2∙4H2O — 0,01.
2-й раствор: в 300 мл дистиллированной воды добавляют 1 мл 10 н. серной кислоты и растворяют 44,2 г FeSO4∙7H2O (рН ≈ 1,5–2,5).
Величину рН и окислительно-восстановительный потенциал (Eh) исследуемых растворов определяли с помощью профессионального многоканального рН-метра Mettler Toledo SevenMulti.
Концентрацию серной кислоты в растворах определяли титрованием 10 мл образца 0,05 н. раствором NaOH, в качестве индикатора использовали фенолфталеин [6].
Концентрацию ионов Fe3+ и Fe2+ в жидкой фазе определяли спектрофотометрическим методом на колориметре фотоэлектрическом концентрационном КФК-2 [7].
Содержание металлов в растворах и твердых образцах определяли методом атомной абсорбции на спектрометре «Квант-2АТ» и атомно-эмиссионной спектрометрии — на спектрометре iCAP 7200 ICP-OES Analyzer, Thermo Scientific [7].
Результаты исследований
Для большей части Казахстана характерны резко континентальные климатические условия, низкие температуры. В связи с этим для разработки технологии биовыщелачивания меди являются актуальными выделение и применение хемолитотрофных психротолерантных и мезофильных бактерий, которые приспособлены к низким температурным условиям. По этой причине мы сосредоточили свое внимание на выделении аборигенных психротолерантных и мезофильных бактерий. Для этого из руд Северо-Казахстанской области нами были выделены бактерии с серо- и железоокисляющей активностью. По культурально-морфологическим и физиологическим свойствам выделенные моноизоляты были идентифицированы как Acidithiobacillus ferrivorans Кок и Acidithiobacillus ferrivorans KP, Acidithiobacillus ferrooxidans КокМ, Acidithiobacillus thiooxidans KS и Acidithiobacillus thiooxidans BS2 [8].
Оптимизированы условия культивирования выделенных серо- и железоокисляющих штаммов. Проведена направленная селекция штаммов на предмет устойчивости к повышенному содержанию серной кислоты. В результате устойчивость штаммов At. ferrivorans KP и At. ferrivorans Kok была увеличена с 2 г/л до 10 г/л, At. ferrooxidans KokM — до 12 г/л. Данные концентрации серной кислоты соответствуют технологическим требованиям подземного выщелачивания.
На основе штаммов Acidithiobacillus ferrivorans Кок и Acidithiobacillus ferrivorans KP, Acidithiobacillus ferrooxidans КокМ, Acidithiobacillus thiooxidans KS и Acidithiobacillus thiooxidans BS2 был составлен консорциум для извлечения меди. Данный консорциум депонирован в Депозитарии ТОО «Казахский научно-исследовательский институт перерабатывающей и пищевой промышленности» под номером B-758.
При подземном выщелачивании продуктивные растворы многократно рециркулируют с целью достижения оптимальной концентрации меди для последующего электролиза. Химический анализ продуктивных растворов при бактериальном выщелачивании показал наличие ионов железа преимущественно в двухвалентной форме. Данный факт доказывает косвенный механизм окисления сульфидных руд. Косвенное выщелачивание происходит за счет окисления сульфида ионами Fe3+, образовавшимися при бактериальном окислении ионов Fe2+. Следовательно, сульфид меди окисляется ионами Fe3+ [9]:
CuS + 2Fe3+ → Cu2+ + S + 2Fe2+
В связи с этим для оптимизации технологического процесса необходима разработка регенерирующего реактора, который будет обеспечивать окисление двухвалентного железа в трехвалентную форму. Использование материалов с высокой удельной поверхностью позволяет существенно увеличить количество биомассы в реакторе за счет прикрепления микроорганизмов к поверхности носителя. Таким образом, окислительная активность проточного биореактора увеличивается за счёт снижения вымывания микроорганизмов.
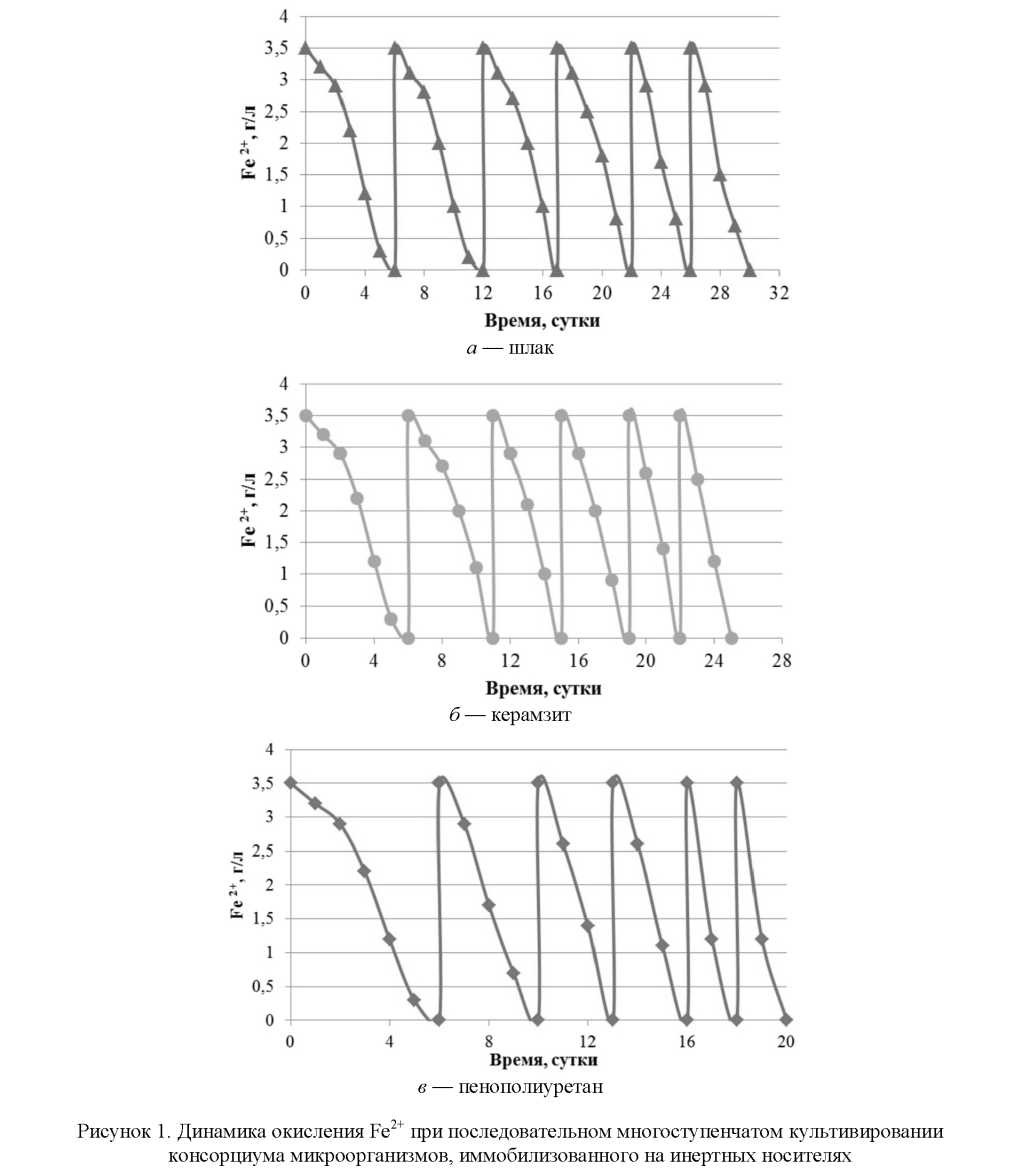
С целью повышения активности бактериального консорциума регенерирующего железа проводились эксперименты по подбору твёрдого носителя. В качестве материалов исследовали шлак, керамзит и пенополиуретан. Для проведения ступенчатой иммобилизации клеток на твердом носителе консорциум штаммов культивировали в периодическом режиме на среде 9К с содержанием железа 3,5 г/л, рН 1,9–2,0. При переходе двухвалентного железа в окисленное состояние на 95 % осуществляли смену культуральной жидкости и вносили в биореактор новую среду. Процедуру повторяли несколько раз. Результаты экспериментов представлены на рисунке 1.
На рисунке 1 отчётливо видно сокращение времени окисления Fe2+ при каждой последующей смене среды. В результате иммобилизации бактериальных клеток время окисления свежей питательной среды было сокращено при использовании: шлака — с 6 до 4 суток, керамзита — до 3 суток и пенополиуретана — до 2 суток. Наиболее эффективным носителем является полиуретановая пена, время окисления Fe2+ сократилось в 3 раза (рис. 1в). Таким образом, применение пенополиуретана существенно повысило удельную окислительную активность биореактора и открывает большие возможности для применения хемолитотрофных микроорганизмов в технологии подземного извлечения меди.
Следующим этапом важно было оценить степень регенерации трехвалентного железа при различных концентрациях серной кислоты, так как с увеличением концентрации кислоты происходит
ингибирование жизнедеятельности бактерии. После ступенчатой иммобилизации консорциума микроорганизмов на полиуретановой пене биореактор запустили в непрерывный проточный режим с коэффициентом разбавления 0,051 ч–1. Эксперимент проводили при температуре 12 ºС, концентрации железа 4,2 г/л и при различных рН среды: 1,4; 1,5 и 1,6. Каждые сутки измеряли соотношение форм железа в культуральной жидкости биореактора. При постоянном окислении двухвалентного железа в протоке увеличивали коэффициент разбавления на 0,017 ч–1. На рисунке 2 представлена производительность трехвалентного железа и степень окисления двухвалентного железа в иммобилизованных биореакторах при различных рН среды.
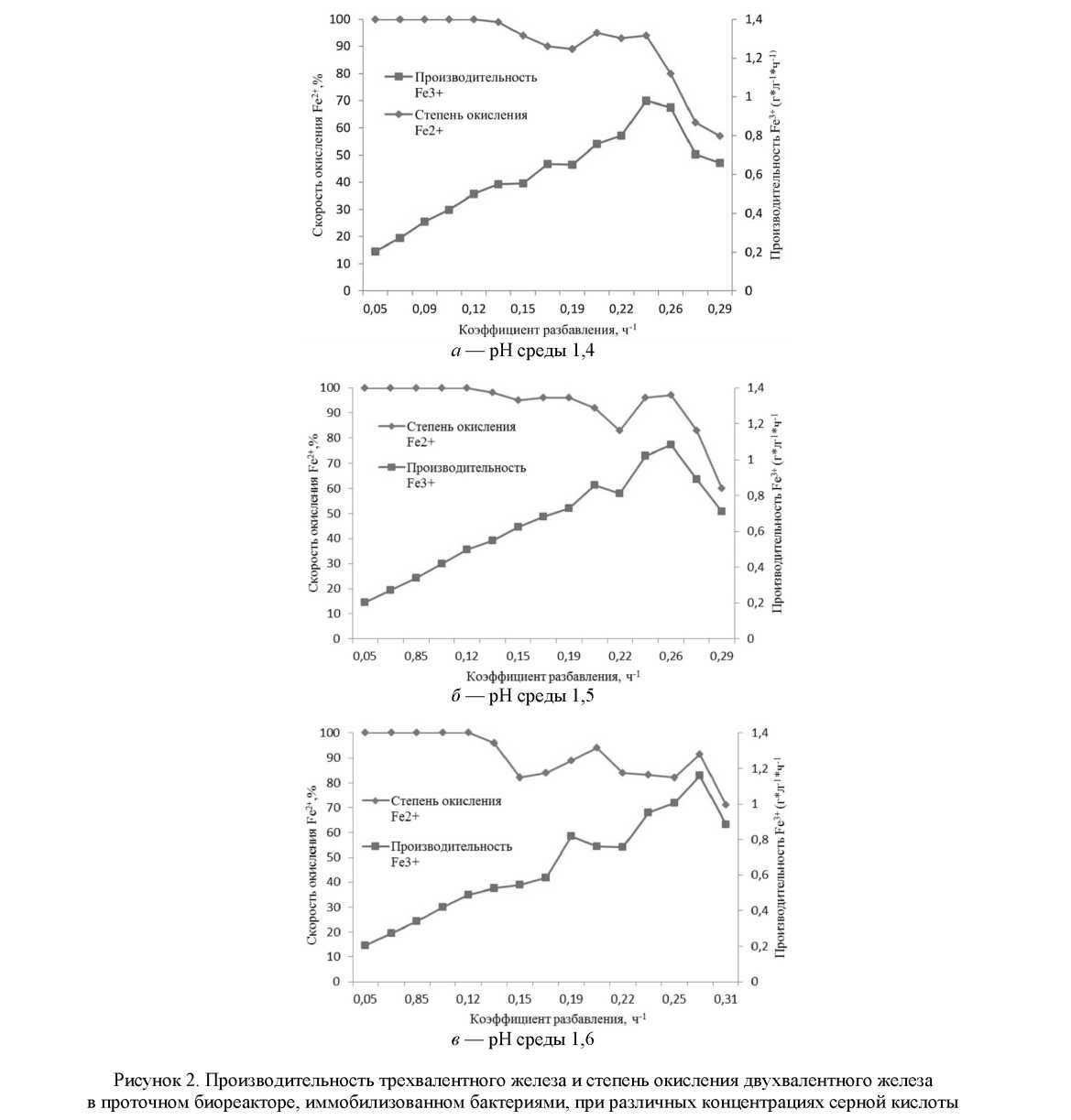
Во всех биореакторах при коэффициенте разбавления в диапазоне от 0,051 до 0,14 ч-1 производительность трехвалентного железа и степень окисления двухвалентного железа являются сравнительно высокими. При коэффициенте разбавления 0,25 ч-1 в биореакторе с рН 1,4 степень окисления двухвалентного железа составила 94 %, а производительность Fe3+ показала максимальное значение 0,98 г·л-1·ч-1, что в 20 раз выше, чем в суспензионной культуре. При дальнейшем увеличении коэффициента разбавления степень окисления Fe2+ и производительность Fe3+ уменьшались. При коэффициенте разбавления 0,26 ч-1 и 0,28 ч-1 в биореакторе с рН 1,5 и 1,6 степень окисления двухвалентного железа составила соответственно 97 % и 91,5 %, а производительность Fe3+ показала максимальное значение — 1,08 г·л-1·ч-1 и 1,16 г·л-1·ч-1 соответственно.
Таким образом, наибольшая производительность трехвалентного железа была достигнута при рН 1,6, которая составила 1,16 г·л-1·ч-1, что в 23,2 раза выше, чем в суспензионной культуре. Также при данном рН коэффициент разбавления является максимальным — 0,28 ч-1.
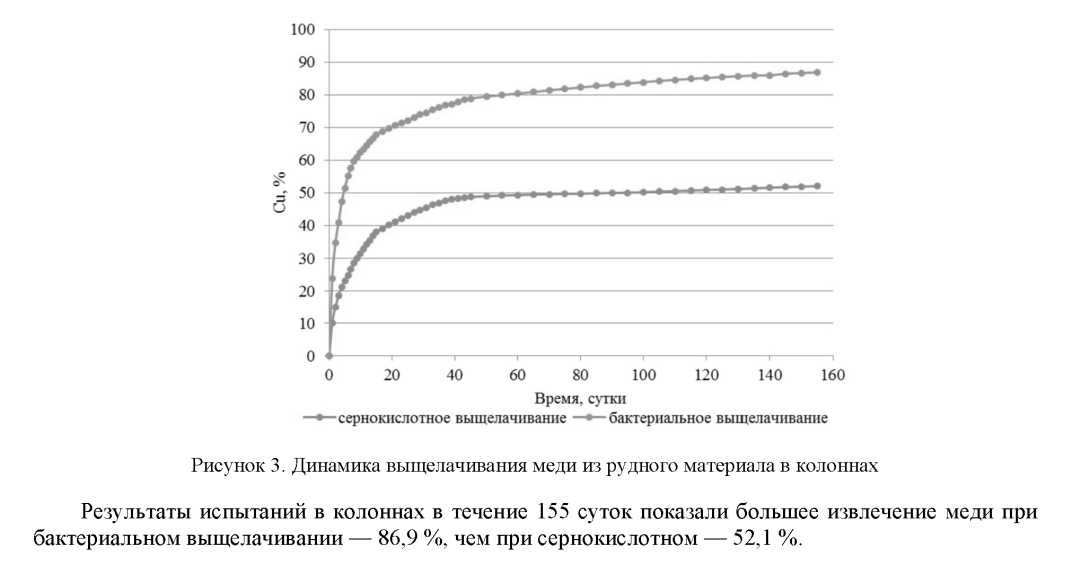
После были проведены модельные испытания для сравнения динамики извлечения меди при традиционной сернокислотной технологии и бактериальной технологии. Испытания по выщелачиванию меди проводили в колоннах высотой 2 м и диаметром 0,2 м на руде с крупностью 10 мм. На колонну, орошаемую по традиционной сернокислотной технологии, подавали раствор серной кислоты с рН 1,6. Колонну бактериального выщелачивания орошали из биореактора бактериальным раствором, содержащим консорциум микроорганизмов, рН среды 1,6 и Eh >550 мВ. Результаты экспериментов представлены на рисунке 3.
Список литературы
- Johnson D.B. Biomining — biotechnologies for extracting and recovering metals from ores and waste materials / D.B. Johnson // Curr. Opin. Biotechnol. — 2014. — Vol. 30. — P. 24-31.
- Jerez C.A. Bioleaching and biomining for the industrial recovery of metals / C.A. Jerez // Comprehensive Biotechnology. — 2011. — Vol. 3. — P. 717-729.
- Watling H.R. The bioleaching of sulphide minerals with emphasis on copper sulphides — A review / H.R. Watling // Hydrometallurgy. — 2006. — Vol. 84. — P. 81-108.
- Watling H.R. Bioleaching of a low-grade copper ore, linking leach chemistry and microbiology / H.R. Watling, D.M. Collinson, J. Li, L.A. Mutch, F.A. Perrot, S.M. Rea, F. Reith, E.L.J. Watkin // Miner. Eng. — 2014. — Vol. 56. — P. 35-44.
- Silverman M.P. Studies on the chemoautotrophic iron bacterium Ferrobacillus ferrooxidans. I. An improved medium and a harvesting procedure for securing high cell yields / M.P. Silverman, D.G. Lundgren // J. Bacteriol. — 1959. — Vol. 77. — P. 642647.
- Золотов Ю.А. Основы аналитической химии / Ю.А. Золотов. — М .: Высш. шк., 2004. — 503 с.
- Mendham J. Vogel's Textbook of Quantitative Chemical Analysis / J. Mendham, R.C. Denney, J.D. Barnes, M.J. Thomas. — K. Prentice Hall, 2000. — 836 p.
- Жаппар Н.К. Выделение железо- и сероокисляющих бактерий, перспективных при подземном выщелачивании меди / Н.К. Жаппар, В.М. Шайхутдинов, Е.Ж. Жакупов, О.А. Тен, Д.С. Балпанов // Наука и инновации — 2015: материалы XI Ме- ждунар. науч.-практ. конф. — Пшемысль, Польша, 7–15 окт. 2015. — С. 47–55.
- Cvetkovski V. Mesophilic leaching of copper sulphide sludge / V. Cvetkovski, V. Conic, M. Vukovic, M. Cvetkovska // J. Serbian Chem. Soc. — 2009. — Vol. 74. — P. 213–221.