АННОТАЦИЯ
Представлены материалы по использованию плазмафереза в терапевтических целях. Раскрыт механизм действия лечебного плазмафереза на организм. Рассмотрены лечебные эффекты эксфузионнотрансфузионных методов очищения крови и показания к их применению. Статья рассчитана на врачейтрансфузиологов, хирургов и врачей терапевтического профиля.
Плазмаферез относится к экстракорпоральным эфферентным методам трансфузионной гемокоррекции. Основной принцип в процедуре плазмафереза это отделение клеточного состава консервированной крови от ее жидкой составляющей плазмы. Методы разделения крови на компоненты, в том числе и плазму, основаны на использовании центробежных сил. При центрифугировании крови происходит разделение ее на составные части с последующим селективным удалением определенных компонентов. В настоящее время способы выполнения процедуры плазмафереза разделяются на аппаратный и неаппаратный (центрифужный), а в зависимости от способа отделения плазмы на гравитационный и фильтрационный. Аппаратный плазмаферез подразделяется на дискретный (прерывистый) и непрерывистый [1].
В процессе центрифугирования под воздействием центробежных сил форменные элементы располагаются вокруг оси вращения делительной камеры слоями. Эритроциты, имеющие наибольшую плотность, остаются на периферии. Ближе к центру располагаются лейкоцитарный и тромбоцитарный слой, а плазма концентрируется в центре делительной камеры (табл. 1).
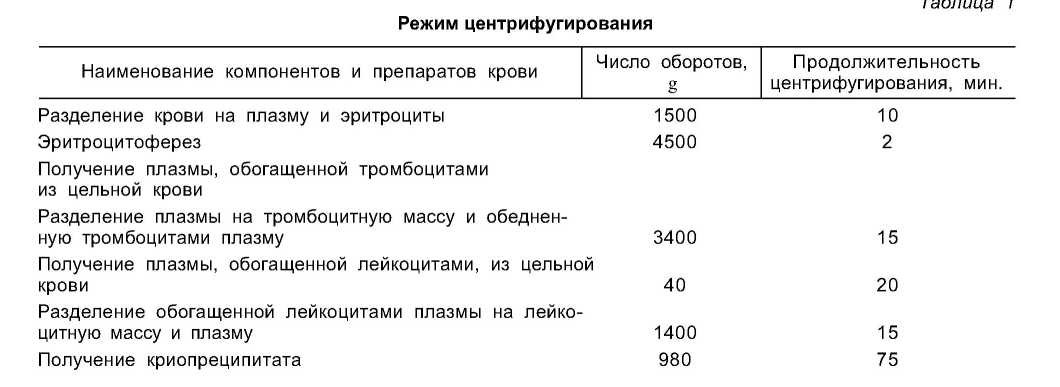
По окончании центрифугирования компоненты крови располагаются послойно: снизу как наиболее тяжелые эритроциты, далее лейкотромбоцитарный слой и сверху плазма [4].
В медицине (и при заготовке донорской крови, и в клинической практике) используется как центрифужный, так и аппаратный метод плазмафереза. Неаппаратный метод проведения процедуры доступен и прост.
В технике проведения процедуры плазмафереза выделяют (П. А. Воробьев) следующие этапы:
- взятие крови в контейнер с консервантом;
- центрифугирование (выполняется на центрифуге с рефрижераторным или воздушным охлаждением);
- удаление плазмы из контейнера;
- возврат эритроцитов.
В последние годы большой объем процедур плазмафереза выполняется аппаратным способом, осуществляемым на сепараторах непрерывного или дискретного типа. В клинической практике аппаратный плазмаферез более производителен при проведении высокообъемного плазмафереза, особенно в экстренной ситуации. Наиболее продуктивен непрерывистый аппаратный плазмаферез, позволяющий удалять требуемое количество плазмы за короткий промежуток времени. Однако сепараторы такого типа требуют двух венозных доступов, что на практике не всегда возможно.
Дискретный аппаратный плазмаферез представляет собой промежуточный вариант между центрифужным и непрерывным аппаратным способом выполнения процедуры.
В отделении трансфузиологии РНЦХ им. Б. В. Петровского РАМН выполнено более 1000 процедур лечебного плазмафереза с использованием приборов фирмы «Haemonetics», тип доступа одноигольный. Сепараторы оснащены замкнутыми одноразовыми магистралями со встроенным колоколом-ротором. Это позволяет проводить процедуру плазмафереза в различных условиях: не только в операционной или отделении интенсивной терапии, но и в палате.
Аппаратный плазмаферез наиболее комфортен для пациента и имеет свои преимущества [3]:
- небольшой объем заполнения системы для крови;
- непрерывный цикл взятия, разделения крови и возвращения клеток;
- удобство в эксплуатации, значительная быстрота;
- длительность сеанса 60-90 мин, объем удаляемой плазмы 600-1000 мл.
В основе действия этих аппаратов лежит прерывисто-поточная методика. Разделение крови на эритроцитную массу и плазму производится в разделительном колоколе (объем заполнения 225 мл), помещенном в центрифугу аппарата. Кровь у пациента берется До заполнения ротора центрифуги. После завершения цикла отделения плазмы аппарат автоматически переключается в режим возврата клеточной массы с гематокритом 65 %, которая реинфузируется в ту же вену, т.е. процедура выполняется в прерывистом режиме. Максимальный объем крови, требующийся для заполнения магистралей и колокола, с учетом удаленной за цикл плазмы, не более 400 мл. Скорость эксфузии и возврата крови можно изменять в пределах 20-70 мл/мин.
В качестве стабилизатора крови используется 4 %-ный цитрат натрия в соотношении 1:16 или 1:12. Цитрат натрия позволяет избежать дополнительной гепаринизации больного, снижая риск возникновения или усугубления нарушений в свертывающей системе крови. Цитрат натрия полный антикоагулянт, блокирующий все фазы коагуляции крови. Основное его действие практически мгновенная инактивация в организме, так как цитрат натрия является естественным метаболитом цикла Кребса. Передозировка наблюдается крайне редко и обусловлена снижением уровня ионизированного кальция в плазме пациента. Это состояние кратковременно, что связано с быстрой мобилизацией кальция из эндогенных депо и метаболизмом цитрата в печени.
Учитывая большую роль паренхиматозных органов в утилизации цитрата, особенного внимания требуют больные с патологией печени, почек, панкреатитом, шоком различного генеза, после длительной терапии кортикостероидами и цитостатиками. У пациента отделения интенсивной терапии цитратная интоксикация может быть спровоцирована не только снижением уровня кальция, но и снижением pH и повышением концентрации калия.
Цитратную интоксикацию довольно легко предупредить или же значительно ослабить ее проявление внутривенным введением 10 мл 10 %-ного раствора хлорида или глюканата кальция. Во время плазмафереза около 70 % консерванта удаляется вместе с плазмой, поэтому если для замещения не используется свежезамороженная плазма, то избыточное количество цитрата в организме не накапливается.
Вышеперечисленные способы отделения плазмы осуществляются под воздействием сил гравитации. Фильтрационный метод основан на фильтрации крови в специальных плазмафильтрах. Эту методику выполнения плазмафереза следует признать не только более физиологичной, но и более доступной в практике многих лечебных учреждений. Тем не менее мембранный плазмаферез оказался до определенного времени недостаточно освещенным в отечественной медицинской литературе. Это могло быть обусловлено множеством причин. Вопервых, многочисленные зарубежные фирмы создавали плазмофильтры на основе пористых полых волокон. Это довольно сложная технология, обеспечивающая создание высокофункциональных, но дорогостоящих мембранных фильтров. Наладка производства такого типа фильтрующих устройств не увенчалась успехом из-за отсутствия технологии и материалов.
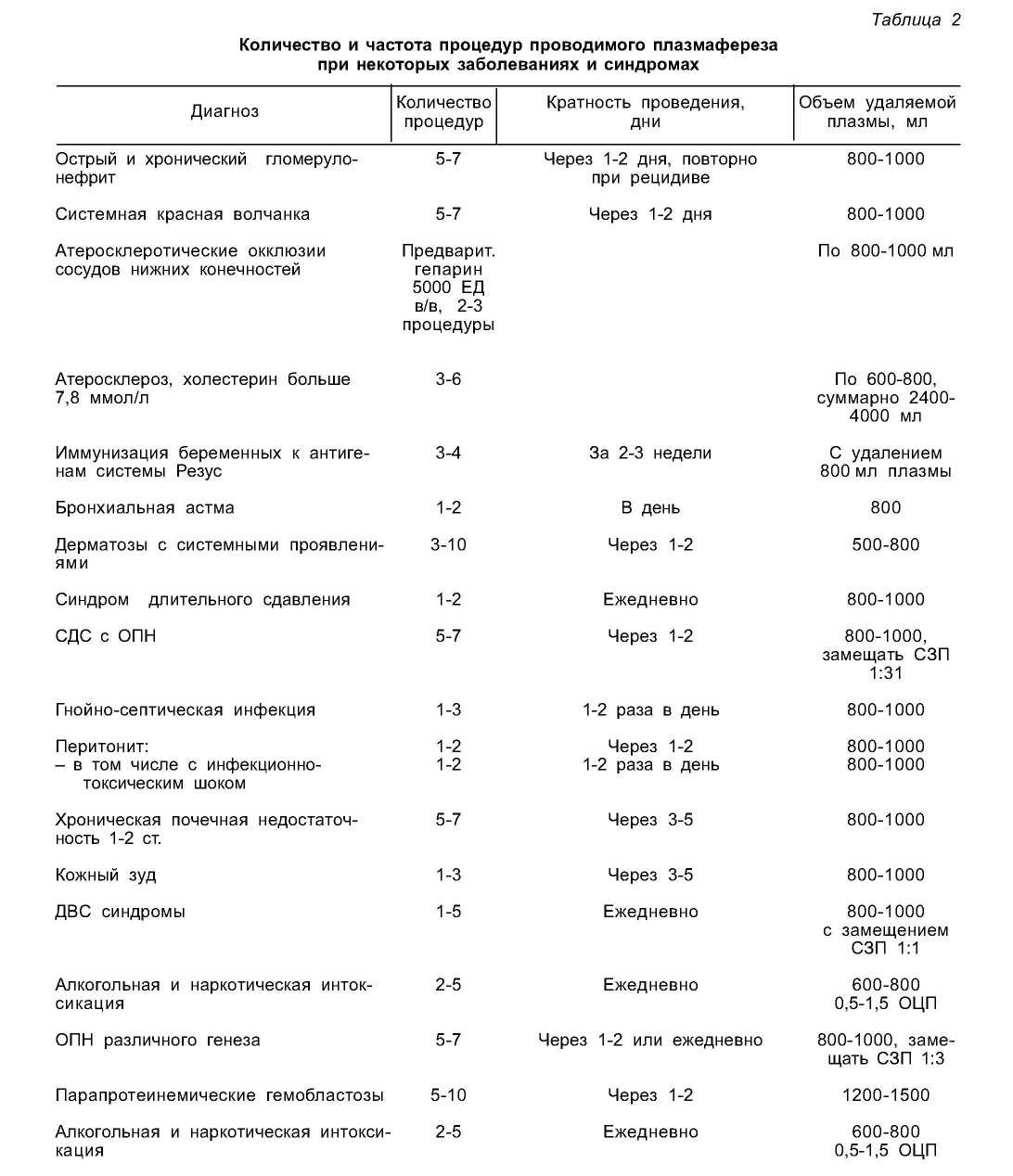
Объемы удаления циркулирующей плазмы (ОЦП) следующие: в основном за сеанс удаляют 1-2 л плазмы. Общий объем за курс 5 л в течение 710 дней. Удаление за одну процедуру до 800 мл плазмы позволяет снизить концентрацию исходных веществ до 50-70 %, ОЦП до 37 % за счет разбавления крови растворами и выхода плазмы из тканевого депо [4,5].
Используя эти формулы, можно рассчитать объем удаления плазмы (ОУП) в процентах


За 1 сеанс от ОЦП выводится 63,2 %; за 2 сеанса ОЦП 86,5 %; за 3 сеанса ОЦП 95 % патологических субстанций. Замещение удаленной плазмы производится в соотношении 1 ∶ 1 раствором хлорида натрия или переливанием альбумина или донорской плазмы.
Аппаратный плазмацитоферез проводится в соответствии инструкцией и протоколами, регламентируемыми заводом-изготовителем и стандартными операционным процедурами (СОП), которые утверждаются первым руководителем организации службы крови и проводятся врачом-трансфузиологом и эксфузионистом.
Клинические эффекты плазмафереза проявляются уже после первого сеанса. Значительно снижается концентрация патологических продуктов. Однако уже через несколько часов содержание их в крови приближается к исходному уровню. Это говорит о том, что в сосудистое русло поступили вещества, находившиеся до того во внеклеточном межтканевом пространстве, или в клетках. Последующие сеансы плазмафереза способствуют удалению и этих веществ, что приводит к более полноценной санации всей внутренней среды, учитывая, что основная часть вредных продуктов находится во внесосудистых пространствах. Для стойкого положительного эффекта необходимо 3-6 сеансов, с удалением в общей сложности 1-1,5 объемов циркулирующей плазмы. Удаляемая плазма достаточно эффективно возмещается солевыми растворами. Таким образом, включение плазмафереза в комплекс лечебных мероприятий способствует более благоприятному течению заболеваний, особенно трудно поддающихся медикаментозной терапии, добиться значительного улучшения состояния пациентов и уменьшить им лекарственную нагрузку [5].
Ведущую роль здесь играет плазмаферез, позволяющий помимо выведения эндотоксинов, удалить и все некомпетентные компоненты гуморального иммунитета. Замещение удаляемого объёма донорской плазмой способствует более эффективному восстановлению системы защиты и более быстрому и полному выздоровлению. В целом значительно сокращаются период нахождения пациентов в отделениях интенсивной терапии, общая продолжительность лечения, снижается летальность.
Однако и при самых разных хронических болезнях человека нарушения состава его внутренней среды, расстройства биохимического и иммунного состояния определяют тяжесть их течения и саму причину хронизации патологии. При этом только с помощью плазмафереза возможно удаление аллергенов, аутоантител и иммунных комплексов при аллергиях и аутоиммунных заболеваниях. Введение плазмафереза в схему комплексной терапии аутоиммунных диссеминированных болезней лёгких способствует более стойкой ремиссии при сокращении объёма гормональной терапии на 40 % и почти полном отказе от цитостатиков, практически вдвое увеличить продолжительность жизни этой категории больных.
Выведение продуктов нарушенного липидного обмена позволяет контролировать течение атеросклероза и его осложнений. Плазмаферез в состоянии ликвидировать тяжёлые последствия лучевой и химиотерапии в онкологии. Показана его высокая эффективность при хрониоинтоксикациях, в том числе наркомании и алкоголизме, что имеет не только медицинскую, но и высокую социальную значимость.
Широкие перспективы открываются в лечении токсикозов беременных, резус-конфликтов, "скрытых" урогенитальных инфекций, антифосфолипидного синдрома, что может надёжно предупреждать нарушения внутриутробного развития плода и снизить уровень перинатальной смертности, восстановить демографический баланс.
После перенесённого вирусного гепатита, особенно В и С, неизбежно формируется аутоиммунный хронический гепатит с последующим переходом в необратимый цирроз печени и даже первичный рак печени. C помощью плазмафереза можно удалить аутоантитела и патологические метаболиты, что способно приостановить прогрессирование поражений печени. Учитывая огромное количество людей, инфицированных этими вирусами гепатита, эта проблема также имеет большое социальное значение.
На первый взгляд сахарный диабет не представляет серьёзной угрозы, поскольку с помощью инсулина или таблеток удаётся поддерживать уровень сахара на приемлемом уровне. Однако и при таком лечении не предотвращаются вторичные обменные нарушения, неминуемо ведущие к сосудистым расстройствам, вызывающим необратимую потерю зрения, нарушения проходимости сосудов нижних конечностей, сердца и головного мозга, что значительно сокращает общую продолжительность жизни. C помощью плазмафереза можно заметно снизить потенциальный риск этих вторичных осложнений диабета.
Показания и противопоказания к проведению плазмафереза
Осложнения при его проведении:
- Аллергические и аутоиммунные заболевания: бронхиальная астма, ревматоидный артрит, системная красная волчанка, склеродермия, дерматомиозит, аутоиммунный тириоидит (зоб Хашимото), отек Квинке, гломерулонефрит и другие.
- Болезни кожи: экзема, псориаз, нейродермит, атопический дерматит, фурункулез, угревая болезнь.
- Неврологические заболевания: миастения, боковой амиотрофический склероз, синдром Гийена-Барре.
- Сердечно-сосудистые заболевания: атеросклероз сосудов нижних конечностей, повышенный уровень холестерина, синдром повышенной вязкости крови, болезни сосудов (облитерирующий эндартериит, тромбоангиит, узелковый артериит, геморрагический васкулит).
- Заболевания печени: токсический гепатит, гепатоз, цирроз печени, неинфекционные желтухи, болезнь Жильбера.
- Болезни обмена веществ: сахарный диабет, подагра, болезнь Вильсона, гемохроматоз.
- Акушерско-гинекологические заболевания: токсикозы (гестозы) беременных, наследственная тромбофилия, АФС-синдром, аутосенсибилизация к ХГЧ, профилактика резус-конфликтной беременности.
- Урологические заболевания: хронический простатит, хронический пиелонефрит, хроническая почечная недостаточность.
- Болезни крови: тромбоцитопеническая пурпура, криоглобулинемия, миеломная болезнь, макроглобулинемия Вальденстрема, аутоиммунная гемолитическая анемия.
- Токсикологические состояния: снятие токсических проявлений при различных отравлениях, в том числе наркотической и алкогольной интоксикации.
Противопоказания к проведению плазмафереза:
- Кровотечения (язвы, эрозии, опухоли желудочно-кишечного тракта, легких, мочеполовой системы и Т.Д.).
- Острая стадия инфекционных и гнойновоспалительных процессов (абсцессы, флебиты, пневмонии и др.).
- Гипертермия, миопия высокой степени более 6 диоптрий, период менструации у женщин.
- Артериальная гипотония, шок АД<90 мм рı.с г.
- Истощение, общий белок крови <55 г/л.
Осложнения при проведении плазмафереза:
- Общие: сердечно-сосудистые, волемические, нарушение сердечного ритма, цитратная интоксикация.
- Связанные с замещением: анафилактические, пирогенные реакции, развитие периферических отеков, отек легких, сенсибилизация, заражение инфекционными и вирусными заболеваниями.
- Связанные с использованием антикоагулянтов: кровотечения, тромбозы, аллергические.
- Технического характера: обтурация,перекрут и изгиб трубок, пережатие систем, т.е. нарушение кровотока. Гемолиз эритроцитов.
- Иммунные осложнения чаще у больных с поражениями легких, почек, аллергическими дерматозами, рассеянным склерозом, гематологической патологией после удаления 1 л и более плазмы.
Внутривенное введение свежезамороженной плазмы является единственным способом профилактики неспецифических инфекционных осложнений.
ЛИТЕРАТУРА
- Рагимов А. А., Порешина С. А., Салимов Э. Л. Плазмаферез при системном воспалительном ответе // Практическая медицина. M., 2008. С. 56.
- Сагатбаева H. А., Жаримбетов A. A., Сейдинов Ш. М. Аутотрансфузионные приемы хирургии крови в малых хирургических стационарах. M., 2004. 56 с.
- Козинец Г. И., Рагимов А. А., Постников А. А. Практическая трансфузиология // Практическая медицина. M., 2005. С. 281-350.
- Токарев Ю. Н. Техническое руководство американской ассоциации банков крови ⁄ пер. с англ.: 12-е изд. Милан, 1996. 996 с.
- Румянцев А. Г., Аграненко В. А. Клиническая трансфузиология. M., 1997. 361 с.