Исследования последних лет указывают на возрастающую частоту возникновения острого почечного повреждения (ОПП) у детей [3], достигающую 8-15 случаев на 1 млн. детского населения [5, 11]. Дети с ОПП составляют примерно 10% от общего числа пациентов, госпитализируемых в педиатрические отделения интенсивной терапии и реанимации [10]. Летальность у них широко варьирует в зависимости от природы основного заболевания, достигая наиболее высокого уровня при развитии полиорганной недостаточности [7, 8, 9].
В настоящее время все лечебные тактики при ОПП направлены на оптимизацию почечного перфузионного давленияиликвидациютканевойгипоксиипутемкомбиниро- ванного применения инфузионной нагрузки, инотропной и нутритивной поддержки, почечной заместительной терапии с минимализацией нефротоксичных эффектов от используемых лекарственных средств. В то же время лишь немногие из предлагаемых методов лечения имеют убедительные доказательства эффективности [4]. Кроме того, негативное влияние на течение и исход ОПП могут оказывать высокая степень инвазивности применяемых методик мониторинга и лечения [1] и неблагоприятные побочные эффекты отдельных компонентов комплексной интенсивной терапии [6, 12]. В связи с этим актуальным становится поиск оптимальных сочетаний методов консервативной и почечной заместительной терапии детей с ОПП, повышающих безопасность и эффективность проводимого лечения.
цель работы. Обобщить опыт лечения и обосновать принципы интенсивной терапии детей с ОПП.
материал и методы. В основу исследования положен опыт интенсивной терапии 272 детей с ОПП различной этиологии, находившихся на лечении в городской клинической больнице скорой медицинской помощи г. Минска. Средний возраст детей составил 35,31±2,58 месяца (от 4 месяцев до 14 лет). Мальчиков было 155 (56.99%), девочек – 117 (43,01%). Основными причинами ОПП были гемолитико-уремический синдром – 73,16% детей, острый гломерулонефрит – 6,25% и острый интерстициальный нефрит – 5,51% детей.
С целью оценки тяжести состояния и эффективности проводимой терапии осуществлялся мониторинг параметров гомеостаза, функций важнейших органов и систем пациентов с использованием лабораторных, электрофизических, рентгенологических и ультразвуковых методов исследования. Полученные результаты сравнивались с нормативными показателями соответствующих возрастных групп, а также сопоставлялись в динамике между умершими и выжившими детьми.
Статистическая обработка данных осуществлялась с помощью пакета статистического анализа “STATISTICA 6.0” (StatSoft). Различия считались достоверными при P<0,05.
Результаты и обсуждение. Независимо от варианта развития и причины ОПП основная роль в ее патогенезе принадлежит ишемии, бактериальному эндотоксину, цитокинам, оксидантному повреждению. Исходя из этого, главными целями патогенетической терапии ОПП являются:
- Нормализация микроциркуляции и устранение ишемии почечной ткани
- Стимуляция процессов естественной детоксикации организма
- Ограничение продукции уремических токсинов и цитокинов и предупреждение их повреждающего действия на органы и ткани
- Искусственная детоксикация организма
Нормализация микроциркуляции и устранение ишемии почечной ткани осуществлялась путем проведения инфузионно-трансфузионной терапии (ИТТ), нормализующей коллоидно-осмотическое давление плазмы (КОД), тканевую перфузию и водно-электролитный гомеостаз.
Если в начальном периоде ОПП инфузионная терапия носила характер интенсивной волемической коррекции, то в периоде развернутых клинических проявлений, при отсутствии или резком снижении диуреза и ликвидации явлений гиповолемии, она являлась «терапией поддержания», направленной на восполнение суточной потребности в жидкости и компенсацию физиологических и патологических потерь. Данный видтерапии существенноразличается в разные периоды ОПП. Это касается не только ограничений в объемах вводимых растворов, но и качественного состава инфузионных сред. Изменение реологических свойств крови и КОД плазмы опасно для ребенка в той же степени, что и перегрузка объемом либо гиповолемия.
Одной из основных причин, вызывающих негативное отношение многих врачей к ИТТ при ОПП, является угроза перегрузки объемом. Однако главные причины осложнений ИТТ у детей с данной патологией – это несоблюдение скоростей инфузии и нарушение баланса между коллоидами и кристаллоидами, приводящее к резкому снижению КОД плазмы и развитию выраженных органных отеков.
С целью повышения безопасности ИТТ необходимо обязательное выполнение следующих условий:
- Поддержание нулевого водного баланса в периоде олигоанурии;
- Соблюдение оптимальных соотношений объемов кристаллоидов и коллоидов.
В периоде олигоанурии 60-80% расчетного объема вводились внутривенно, в периоде полиурии основным путем возмещения потерь жидкости (до 60% объема) был пероральный прием.
На фоне гиперкатаболизма, гипопротеинемии и снижения КОД инфузии кристаллоидов приводили к увеличению содержания воды в легочной ткани и возрастанию нагрузки на дыхательную систему, что сопровождалось рентгенологическими признаками застоя в легких (тесная положительная корреляционная связь, r=0,90). Изменения функции внешнего дыхания в периоде олигоанурии были менее выраженными у выживших детей, поскольку у них программа инфузионной терапии строилась более рационально в плане соотношения кристаллоидов и коллоидов, т.е. кристаллоидные растворы в общем объеме инфузионно-трансфузионной терапии у выживших детей составляли примерно 30%, тогда как у умерших их доля равнялась 75%.
Программа ИТТ в периоде полиурии была направлена в первую очередь на компенсацию потерь воды и электролитов, поддержание нормального ОЦК, улучшение органной и тканевой перфузии, реологических свойств крови.
Важнейшимусловием ИТТ является поддержание необходимого соотношения кристаллоидов и коллоидов с учетом периода ОПП: в периоде олигоанурии это соотношение должно быть примерно 0,3:1, в периоде восстановления диуреза объем коллоидных растворов и препаратов крови должен быть не менее 1:1. В периоде полиурии основой ИТТ являются кристаллоидные растворы. По мере увеличения диуреза и улучшения функции ЖКТ главным путем восстановления водного баланса становится пероральный прием жидкости.
Антиагреганты и препараты сосудистого действия. Постишемическое реноваскулярное повреждение повышает выработку оксидантов, цитокинов и протеиназ, повышающих чувствительность к вазоконстрикторным стимулам, что приводит к повреждению механизмов ауторегуляции и повышает уязвимость почек к повторным ишемическим воздействиям. Вследствие этого наряду с нормализацией внутрисосудистого объема применялись вазоактивные препараты разнонаправленного действия,
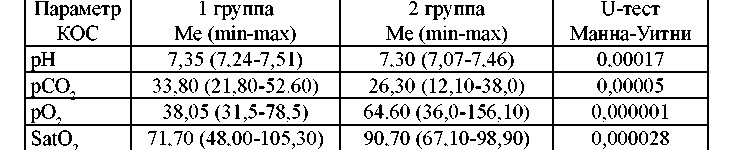
Приведенные данные показывают, что у детей с неблагоприятным исходом ОПП отмечается достоверно более высокое парциальное напряжение кислорода и сатурация венозной крови, свидетельствующие о нарушении доставки кислорода к тканям по причине наличия блока на уровне обменного звена сосудистого русла.
ограничение продукции и повреждающего действия уремических токсинов, цитокинов, медиаторов воспаления. опп является состоянием, сопровождающимся преобладанием катаболических процессов, что приводит к избыточному образованию в плазме больного продуктов белкового обмена (мочевина, креатинин). циркуляторные нарушения в органах и тканях, ограничение поступления питательных веществ и энергии при возросшей потребности в них указывают на необходимость восполнения повышающие клубочковый фильтрационный градиент, в первую очередь блокаторы кальциевых каналов: изоптин, нифедипин и др. в возрастных дозах.
С целью улучшения микроциркуляции назначали антиагреганты: пентоксифиллин, дипиридамол. Лечение пентоксифиллиномначинали с нагрузочной дозы (3-4 мг/ кг) с последующей внутривенной инфузией (1,2 мкг/кг/час) в течение 5 дней. Необходимо помнить о риске применения пентоксифиллинапри выраженной тромбоцитопении! Дипиридамол назначали по 1,5-5,0 мг/кг в сутки в течение 7-10 дней. Для улучшения реологических свойств крови, устранения гиперкоагуляционного синдрома, блокады микроциркуляторного русла и нарушения проницаемости гломерулярного фильтра использовали антикоагулянты (гепарин, фраксипарин, фрагмин). Доза гепарина – 150-200 ЕД/кг в сутки, низкомолекулярных гепаринов – 100-150 МЕ/кг в сутки. Лечение проводилось под контролем АЧТВ, которое не должно превышать нормальные значения более чем на 40-50%.
Несмотря на попытки устранения микроциркуляторного блока, который является основой развития полиорганной дисфункции при ОПП и причиной неблагоприятных исходов заболевания, в тяжелых случаях не удавалось ликвидировать микроциркуляторные нарушения и восстановить перфузию периферических тканей, что подтверждается результатами патоморфологического исследования умерших детей.
В течение всего периода заболевания во внутренних органах детей с нарушением выделительной функции почек превалируют морфологические маркеры ДВС-синдрома, сопровождающиеся блокадой микроциркуляторного русла, дистрофически-некротическими изменениями ишемического генеза и кровоизлияниями, обусловленными гипокоагуляцией [2]. Сохранение или усиление указанных нарушений на фоне присоединения инфекционных осложнений, в первую очередь со стороны органов дыхания, является ведущей причиной прогрессирования полиорганной дисфункции и неблагоприятного исхода ОПП в детском возрасте.
Косвенным подтверждением выраженных нарушений перфузии периферических тканей при неблагоприятном исход ОПП являются сравнительные данные параметров КОС венозной крови (таблица 1).
Таблица 1. Сравнительная характеристика параметров КОС венозной крови в зависимости от исхода ОПП энергодефицита и снижения гиперкатаболизма, стимуляции синтеза белков и нуклеиновых кислот.
При расчете необходимой нутритивной поддержки следуетучитывать скорость утилизации глюкозы, которая должна составлять не менее 0,16 - 0,25 г/кг/час, посколькупри более низкой скорости утилизации глюкозы введение других нутриентов нецелесообразно. Через 3-6 часов удержания нормогликемии (на фоне оптимизированных газообмена, гемодинамики, перфузии, транскапиллярного обмена) присоединяли аминокислотные смеси в дозе 0,15-0,25 г/кг/сут., жировые эмульсии в дозе 1,5-2 г/кг/сут. присоединялись при сохранении нормогликемии в течение 9-12 часов. Продолжали увеличивать подачу глюкозы и липидов каждые 6-12 часов до уровня 60-90% калорической потребности основного обмена. Обязательным компонентом терапии являлись контроль и коррекция электролитов(К, Na, Ca, Mg), введение витаминов и микроэлементов, контроль азотного баланса и коррекция дозы аминокислот и липидов.
Ингибиция синтеза цитокинов осуществлялась путем подавления продукции белков транскрипции и трансляции (пентоксифиллин, кортикостероиды в терапевтических дозах). Кортикостероиды назначались при наличии иммунного процесса короткими курсами, с учетом имеющихся противопоказаний для их применения.
Снижение уровня антиоксидантной защиты и высокая активность свободно-радикального окисления у больных с ОПП корригировалась применением антиоксидантов:
- ɑ-токоферол. Назначался в дозе до 1000 мг/м2 площади поверхности тела в день;
- аскорбиновая кислота. Назначалась в высоких дозах (до 20 мг/кг в сутки). Обязательно сочеталась с токоферолом, поскольку при его дефиците она способна усиливать пероксидацию свободных жирных кислот в присутствии ионов железа и меди. Необходимо помнить о том, что метаболитом аскорбиновой кислоты является оксалат кальция, который при избыточном образовании способен привести к блоку канальцев вследствие образования кристаллов в их просвете. Наиболее целесообразным является применение аскорбиновой кислоты при явлениях метаболического алкалоза.
стимуляция процессов естественной детоксикации организма:
Стимуляция мочеотделения. С первого дня пребывания в стационаре, независимо от объема диуреза, назначался фуросемид внутривенно по 4-5 мг/кг/сут. Его применение, даже при отсутствии мочи, способствует улучшению почечной гемодинамики, ускоряет вымывание клеточного детрита из просвета канальцев, повышает выживаемость канальцевого эпителия в условиях имеющейся ишемии и тканевой гипоксии. Отменяли фуросемид только после развития стойкой полиурии (диурез на протяжении 2-3 суток – не менее 5 мл/кг/час), постепенно уменьшая его суточную дозу во избежание синдрома отмены.
Стимуляция выделительной функции кишечника. У детей с ОПП частым проявлением нарушения выделительной функции кишечника являются стойкие запоры, особенно упорные при ограниченном поступлении жидкости через рот. Для устранения этого источника интоксикации и фактора риска эрозивно-язвенного поражения слизистой кишечника необходима стимуляция функции кишечника (слабительные – растительные, солевые, масляные, очистительные клизмы). Использование этого метода должно сопровождаться тщательным мониторингом водно-электролитного обмена во избежание тяжелой дегидратации и электролитных расстройств.
Улучшение печеночной функции с целью усиления образования малотоксичного метаболита (мочевина) из более токсичного аммиака осуществлялось терапией, направленной на коррекцию нарушений водно-электролитного обмена, субстратно-энергетической поддержкой (глюкоза), деконтаминацию кишечника, назначением препаратов, улучшающих функцию гепатоцитов (эссенциале).
Селективная деконтаминация кишечника (профилактика дизбактериоза, транслокации кишечной микрофлоры и инфекционных осложнений). При развернутой клинической картине кишечного дисбактериоза основной задачей являлось подавление патогенной и восстановление нормальной кишечной микрофлоры. С этой целью применяли монокомпонентные (бифидумбактерин, лактобактерин, бактисубтил, бификол и др.) и комбинированные (линекс) пробиотики. В случае упорной диареи с лабораторным подтверждением наличия в содержимом толстой кишки патогенной микрофлоры дополнительно назначали антибиотики широкого спектра действия (цефалоспорины II-III поколения, фторхинолоны). Прием антибиотиков и пробиотиков был раздельным, с интервалом между их приемом не менее 2 часов.При дисбактериозе назначали энтеросорбенты (активированный уголь, белосорб, полифепан).
В связи с недостаточностью секреторной функции желудка и поджелудочной железы, нарушением процессов кишечного пищеварения, наблюдаемых у детей с ОПП и усиливающихся при дисбактериозе, в схему лечения включали ферментативные препараты (фестал, панзинорм и др.).
Профилактика и лечение стресс-повреждений желудочно-кишечного тракта. Желудочно-кишечный тракт (ЖКТ), является одним из органов-мишеней, подверженных воздействию повреждающих факторов при ОПП. Для профилактики и лечения стресс- повреждений ЖКТ использовались гастропротекторы (смекта, облепиховое масло), антагонисты Н2-гистамино- вых рецепторов (ранитидин по 2-4 мг/кг 2-3 раза в сутки) и ингибиторы протонной помпы.
При желудочно-кишечном кровотечении продолжали применение антагонистов H2-гистаминовых рецепторов и проводили гемостатическую терапию по общепринятым схемам. Для устранения острой постгеморрагической анемии переливали свежую взвесь отмытых эритроцитов, не обладающих недостатками длительно хранящейся эритроцитарной массы.
Респираторная поддержка у детей с ОПП. Острая дыхательная недостаточность является частым и опасным осложнением у детей с ОПП, требующим длительной респираторной поддержки (необходимость проведения ИВЛ составляла от 42 до 67%). Присоединение дыхательной недостаточности значительно удлиняло сроки лечения и ухудшало прогноз заболевания.
Основным режимом вентиляции являлась управляемая вентиляция с контролем по давлению (IPPV). Поскольку в большинстве случаев респираторная поддержка начиналась на фоне признаков отека головного мозга, ИВЛ начинали в режиме умеренной гипервентиляции с минутным объемом дыхания, превышающим возрастную норму на 15-20%. Средний дыхательный объем не превышал 10-12 мл/кг, а при выраженном снижении легочного комплайнса проводилась вентиляция с дыхательным объемом 6-8 мл/кг.
При остром респираторном дистресс-синдроме осуществлялась вентиляция с положительным давлением к концу вдоха (PEEP – 3-5 мбар и более) и увеличением времени вдоха (оптимальное соотношение вдоха к выдоху – 1:1). Одним из параметров, который при ИВЛ увеличивался в последнюю очередь, являлосьҒіО2. Его поддерживали на уровне 35-50% во избежание дополнительного повреждения легких, и только при отсутствии эффекта от подбора режимов и параметров ИВЛ концентрация кислорода во вдыхаемой смеси увеличивалась выше указанных значений.
Острая дыхательная недостаточность у детей имела разные причины в зависимости от сроков течения ОПП: в 1-2 сутки главными показаниями для перевода детей на ИВЛ являлись терминальные нарушения деятельности сердечнососудистой системы, отек легких, головного мозга, судорожный синдром.
Летальность при раннем развитии дыхательной недостаточности составляла почти 100%. В последующем ведущими причинами ОДН становились синдром острого легочного повреждения и пневмонии, повышающие общую летальность среди детей с ОПП до 66,7%.
Коррекция нарушений иммунитета. Выявленные у детей с ОПП расстройства иммунитета затрагивают как клеточное, так и гуморальное его звенья, при этом у детей с неблагоприятным исходом ОПП они более значительны (таблица 2), что доказывает необходимость активной коррекции выявленных нарушений.
Примечание: * - достоверное различие с показателями доноров; # - достоверное различие с показателями 1-й группы.
С заместительной целью применяли «иммуноглобулин человека нормальный» в дозе 3 мг/кг в сутки в виде внутривенных вливаний с интервалом в 24 часа. Курс лечения – 3-4 инфузии. При тяжелом состоянии ребенка доза могла быть увеличена до 5 мг/кг в сутки. При необходимости проводился повторный курс через 7 дней.
Профилактика нозокомиальных инфекций у детей с ОПП. Согласно литературным данным и нашему опыту, мероприятия по предупреждению нозокомиальных инфекционных осложнений должны воздействовать на все пути передачи возбудителей госпитальной инфекции и основные патогенетические механизмы их возникновения. К таким мероприятиям относятся:
- снижение степени инвазивности лечебных мероприятий;
- селективная деконтаминация желудочно-кишечного тракта;
- иммунопрофилактика;
- ранняя идентификация возбудителя инфекционного процесса, послужившего причиной ОПП (острые кишечные инфекции, инфекции респираторного тракта, хирургические инфекции и др.) и проведение целенаправленной антибактериальной терапии;
- соблюдение санитарно-противоэпидемического режима медицинским персоналом.
Отказ от постоянной катетеризации мочевого пузыря на период олигоанурии и замена их памперсами – один из способов снизить степень инвазивности медицинских манипуляций. Для учета объема диуреза взвешивали памперсы. Применение такого подхода в последние годы сократило число случаев инфекции мочевых путей в среднем на 18-20%.
При необходимости зондового кормления ребенка стремились к максимальному сокращению сроков интубации желудка. При переводе ребенка на ИВЛ избегали назначения антацидных препаратов. Обязательным условием являлось положение ребенка в постели с приподнятым головным концом, частые повороты на бок, на живот, постоянная санация полости ротоглотки и трахеи. Для уменьшения риска экзогенного инфицирования дыхательных путей при проведении ИВЛ в последние годы применяются воздушные бактериальные фильтры. Согласно нашим исследованиям использование таких фильтров, особеннов сочетании с деконтаминацией полости рта и ЖКТ, значительно отодвигает сроки возникновения вентилятор-ассо- циированных пневмоний.
Селективная деконтаминация ЖКТ проводилась по следующей схеме: нистатин по 250 000-500 000 ЕД внутрь 4 раза в сутки + эубиотик внутрь до 20 доз в сутки + энтеросорбент по 0,5-1,0 г/кг в сутки. Дополнительно парентерально назначали антибиотик из группы цефалоспоринов II-III поколения в возрастной дозировке, обычно в сочета-
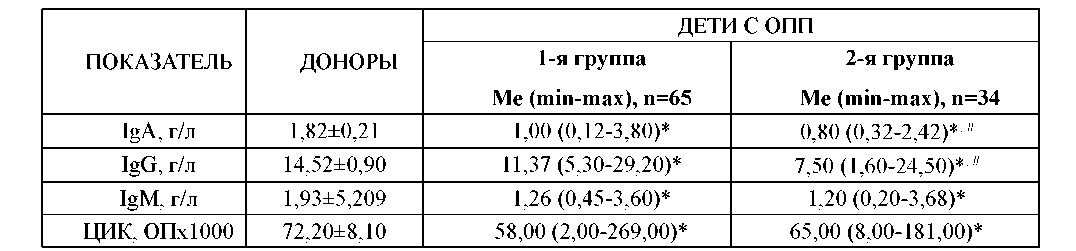
Таблица 2. Уровень иммуноглобулинов в сыворотке крови у детей с ОПП в зависимости от ее исхода нии с метронидазолом. Обеспечивали также условия для поддержания регулярного стула.
Лечение нозокомиальных инфекционных осложнений.При появлении признаков инфекционного процесса безотлагательно начиналась эмпирическая антибактериальная терапия. В качестве препаратов выбора использовались цефалоспорины III поколения (цефтриаксон, цефотаксим) в максимально допустимых до- зах,авкачествеальтернативныхпрепаратов–фторхинолоны (ципрофлоксацин, офлоксацин) и карбапенемы (имипенем, меронем). Биосреды ребенка (кровь, мокрота, моча и др.) направлялись на бактериологическое исследование. После идентификации возбудителя и определения его чувствительности к антибиотикам переходили к целенаправленной антибактериальной терапии.
Заключение. Интенсивная терапия детей с ОПП, с нашей точки зрения, предполагает осторожное (с максимально низкой степенью агрессии) использование лечебных методик, не допускающих значительных колебаний гомеостатических констант больного ребенка. Адекватная инфузионная терапия, нормализующая волемический статус и гемореологические характеристики пациента, в сочетании с применением сосудорегулирующих средств, антиагрегантов и антикоагулянтов обеспечивает эффективное восстановление почечной перфузии, ликвидацию тканевой гипоксии/ишемии с минимализацией риска возникновения полиорганной дисфункции и улучшение результатов лечения детей с данной патологией. Используемые нами на протяжении последних десяти лет представленные подходы к интенсивной терапии ОПП привели к значительному снижению общей летальности в детском возрасте: с 47,94 до 29,65%.
списоК литератУры
- Миронов Л.Л. Причины неблагоприятных исходов острой почечной недостаточности у детей // AR- SMedica. – 2009. – № 7. – С.108-114.
- Миронов Л.Л., Сукало А.В., Летковская Т.А. Патоморфологические аспекты течения острой почечной недостаточности у детей // Медицина. – 2007. – № 1 (56). – С. 32-37.
- Andreoli S.P. Acute kidney injury in children // Pedi- atr. Nephrol. – 2009. – Vol. 24. – P. 253-263.
- Basu R.K., Wheeler D. Approaches to the management of Acute Kidney Injury in Children // Recent Pat. Biomarkers. – 2011. – Vol. 1. – P. 49-59.
- Bunchman T.E., McBryde K.D., Mottes T.E. et al. Pediatric acute renal failure: Outcome by modality and disease // Pediatr. Nephrol. – 2001. – Vol. 16. – P. 1067-1071.
- Gallego N., Perez-Caballero C., Gallego A. et al. Prognosis of patients with acute renal failure without cardiopathy /N. Gallego [et al.] // Arch. Dis. Child. – 2001. – Vol. 84. – P. 258-260.
- Leblanc M., Tapolyai M., Paganini E. P. What dialysis dose should be provided in acute renal failure? A review // Adv. Ren. Replace Ther. – 1995. – Vol. 2. – P. 255-264.
- Marik P.E.,Mohedin M. The contrasting effects of dopamine and norepinephrine on systemic and splanchnic oxygen utilization in hyperdynamic sepsis // JAMA. – 1994. – Vol. 272. – P. 1354-1357.
- Milliner D.S. Pediatric Renal-Replacement Therapy – Coming of Age // N. Engl. J. Med. – 2004. – Vol. 350, № 26. – P. 2637-2639.
- Schneider J., Khemani R., Grushkin C. et al. Serum creatinine as stratified in the RIFLE score for acute kidney injury is associated with mortality and length of stay for children in the pediatric intensive care unit // Crit. Care Med. – 2010. – Vol. 38. – P. 933-939.
- Shanoy M., Plant N. Management of acute renal failure in children // Pediatr. Child Health. – 2008. – Vol. 18. – P. 375-380.
- Shulman G., Hakim R. Hemodialysis membrane biocompatibility in acute renal failure // Adv. Ren. Replace Ther. – 1994. – Vol. 1. – P. 75-82.