Казахстан считается страной, благополучной по катаральной лихорадке овец (КЛО). В то же время мокрецы рода Culicoides, являющиеся основными переносчиками вируса, вызывающего КЛО, распространены в стране практически повсеместно. На юге Казахстана сложились идеальные условия для распространения КЛО в случае заноса вируса из других стран, включающие оптимальный для размножения мокрецов климат, высокую плотность восприимчивого к вирусу скота и постоянный приток импортируемого племенного скота из районов, где инфекция является эндемичной. Неконтролируемое распространение КЛО на территории Казахстана может быть сопряжено с колоссальными экономическими потерями в силу того, что овцеводство имеет чрезвычайно важное значение для отечественного животноводства. Экономические затраты в этом случае не будут ограничиваться лишь падежом животных: существенный ущерб может быть нанесен имиджу нашей страны как экспортёру баранины. В настоящем обзоре приведены сведения, подчеркивающие значимость программ по контролю КЛО в Казахстане и эпидемиологический анализ рисков распространения данной инфекции в стране.
Введение
Катаральная лихорадка овец (КЛО, блютанг, синий язык, болезнь Морро) — инфекционное трансмиссивное вирусное заболевание, поражающее домашних и диких жвачных животных (в основном овец, коз, крупный рогатый скот, буйволов, оленей и верблюдов), вызывая геморрагические и язвенные поражения слизистой оболочки ротовой полости и желудочно-кишечного тракта, воспаление кожи и эпителия венчика копыт, дегенеративные изменениями скелетной мускулатуры, некроз скелетной и сердечной мышцы, перикардиальные, плевральные и брюшные выпоты, отек легких, а также аборты или рождение ослабленного потомства. Тяжесть заболевания варьирует у разных видов, при этом тяжелое течение наблюдается, в основном, у овец, что приводит к гибели, потере веса и нарушению роста шерсти [1, 2]. В первичных эпизоотических очагах летальность в случае овец может достигать 90 %, при этом в стационарных она обычно не превышает 30 %. Всемирная организация по охране здоровья животных (ранее Международное эпизоотическое бюро — МЭБ) относило КЛО к категории А наиболее опасных болезней животных. Диагноз ставят по эпизоотологическим, клиническим, патологоанатомическим и лабораторным данным. Клиническая картина: кровоизлияния и язвы в полости рта и верхних отделах желудочно-кишечного тракта; коронит; субинтимальное кровоизлияние в легочную артерию; отек легких, вентральной подкожной клетчатки и фасций мышц шеи и брюшной стенки.
К вирусу блютанга (BTV) наиболее восприимчивы овцы. Коровы, буйволы, козы и дикие жвачные длительное время могут быть вирусоносителями, не проявляя клинических признаков болезни [2]. Последнее обстоятельство, а также наличие мезогенных штаммов, которые и у овец могут не вызывать видимых симптомов, осложняет оценку риска возникновения эпизоотий, связанных с этой инфекцией. Кроме этого, трансмиссивный характер инфекции существенно осложняет контролирующие мероприятия по сдерживанию и искоренению инфекции на заданной территории.
Хотя нет официальных данных о случаях блютанга в нашей стране, в литературе имеются свидетельства, указывающие на присутствие серопозитивных животных на территории Южного Казахстана [3]. Отсутствие клинических проявлений у инфицированных животных позволяет предположить,
что циркулирующие по территории РК штаммы BTV являются мезогенными, линии которых используются для создания аттенуированных и инактивированных вакцин. Циркуляция по территории страны лишь вакциноподобных генотипов BTV не является причиной лишения ее статуса «благополучной по инфекции» и не требует введения ограничительных зон и карантинных мероприятий [4]. Подобные случаи были зарегистрированы в 2009 г. в Германии и Нидерландах (BTV-6); в 2009 г. в Бельгии (BTV-11); в 2012 г. в Литве, Латвии, Эстонии, Польше и в западных областях России (BTV- 14) [5]. Однако существует опасность заноса патогенных штаммов BTV на территорию Казахстана с завозом скота из других стран.
Несмотря на то, что в Казахстане на постоянной основе проводится тестирование чувствительных к КЛО животных серологическими методами, данные исследования ограничены, в основном, импортируемым скотом. Кроме этого, государственные программы по контролю КЛО в Казахстане не предусматривают тестирование основных переносчиков инфекции, Culicoides sp. Также они не затрагивают диких жвачных животных. При этом дикие животные могут стать резервуаром инфекции, повышая риски быстрого распространения вируса.
В настоящем обзоре приведены сведения об эпизоотологической ситуации в Казахстане по катаральной лихорадке овец в Казахстане, результаты эпидемиологической оценки рисков распространения инфекции на территории страны, а также оценка размеры выборки образцов от крупного и малого рогатого скота для проведения мониторинговой программы изучения циркуляции данной инфекции в стране.
Материалы и методы
Эпидемиологические методы. Все расчеты эпидемиологических параметров проводились в программе EpiInfo v. 7.2.2.2 (CDC).
Общий размер выборки для проведения мониторингового исследования в отношении катаральной лихорадке овец был определен по формуле:
Результаты и обсуждение
Описание вируса, способы его передачи и распространения. РНК-содержащий вирус блютанга (BTV) относится к семейству Reoviridae, роду Orbivirus. Вирион лишён липидной оболочки. Вирус достаточно устойчив во внешней среде, а в сгустках крови он может сохранять жизнеспособность в течение нескольких лет.
Геном BTV представлен десятью линейными двухцепочными сегментами РНК. Вирусный геном кодирует пять неструктурных (NS1, NS2, NS3, NS3A, NS4) и семь структурных (VP1-VP7) белков [6].
Сегменты вирусного генома значительно отличаются по степени консервативности. Второй сегмент, кодирующий основной поверхностный вирусный белок VP2, является наиболее вариабельным. VP2 является основной мишенью для нейтрализующих антител, и именно он, в основном, определяет серотип вируса. В формировании серотипа также принимает участие второй поверхностный белок вируса VP5, хотя и в значительно меньшей степени [1].
В настоящее время выделяют 29 типичных серотипов BTV, в рамках которых могут выделяться отдельные топотипы [7], а также известно несколько претендентов на новые серотипы, вплоть до BTV-36, которые называют атипичными серотипами [8, 9].
Структурные белки, формирующие частицы BTV (VP1, VP3, VP4, VP6 и VP7), а также неструктурные белки (NS1, NS2, NS3, NS4 и NS5) являются значительно более консервативными в сравнении с поверхностными белками VP2 и VP5.
Компетентными переносчиками вируса являются кровососущие мокрецы рода Culicoides. Из более чем 1400 видов мокрецов этого рода, только для нескольких десятков видов доказана способность

к амплификации и переносу BTV [10]. Вирус также может передаваться механическими переносчиками, в которых он не амплифицируется, такими как мухи-кровососки [11], мухи-жигалки [12] и некоторые виды клещей [2, 13]. Помимо трансмиссивного пути переноса вируса, описаны случаи вертикальной передачи BTV от матери плоду, а также с аттенуированной вакциной против BTV [14]. Один из серотипов вируса (BTV-26) может передаваться в популяциях коз без векторов.
Способности вируса вызывать персистирующую инфекцию у некоторых особей или видов копытных животных и длительному сохранению в векторах делает болезнь трудно искоренимой [15].
Методы диагностики блютанга
В наибольшей концентрации вирус обнаруживается между пятым и одиннадцатым днями после инфицирования в селезенке и лимфатических узлах, затем в крови животных. Вирус довольно долго может циркулировать в инфицированном организме и может продолжать детектироваться в крови даже по достижении высокого титра нейтрализующих антител.
Для диагностических целей применяются различные серологические методы: реакция иммунодиффузии в агаровом геле, иммуноферментный анализ (ИФА), метод флуоресцентных антител, реакция связывания комплемента, реакция нейтрализации, реакция непрямой гемагглютинации [1]. Но в настоящее время ИФА практически полностью вытеснил другие серологические методы, хотя реакция нейтрализации продолжает оставаться «золотым стандартом» при определении серотипа вируса. ИФА позволяет прослеживать динамику развития иммунитета и отличается быстротой и удобством в работе. Главным недостатком этого метода является то, что он позволяет детектировать антитела на возбудителя, но не сам возбудитель. Наборы, в основе которых лежит конкурентный ИФА, более чувствительны и могут быть использованы для тестирования различных видов животных, включая диких жвачных. Наборы, основанные на методе непрямого ИФА, обычно применяются для выявления антител в молоке.
Из серологических методов лишь реакция нейтрализации вируса может быть успешно использована для дифференциации серотипов BTV. Однако этот метод имеет свои ограничения: его затруднительно использовать при смешанных инфекциях и в случае выявления новых серотипов вируса, он является чрезвычайно затратным, трудоемким и сложным для реализации.
Методы на основе гибридизации нуклеиновых кислот позволяют дифференцировать серотипы и топотипы BTV. В то же время все они являются достаточно сложными в исполнении, требуют наличия специального оборудования и проведения оптимизации условий тестирования, что существенно ограничивает их применение на практике для рутинной диагностики блютанга [16].
Методы на основе ПЦР хорошо зарекомендовали себя и при детекции вируса в мониторинговых исследованиях, и в подтверждающей лабораторной диагностике, и в определении серотипа вируса, и для генетической характеризации BTV. Они позволяют выявлять вирус на самых ранних стадиях болезни у павших животных, при персистенции вируса в организме особей со слабым иммунитетом, в латентной стадии болезни, а также в организмах векторов BTV. Важно, что методы на основе ПЦР позволяют достоверно различать вакцинные и невакцинные штаммы вируса [1].
Анализ рисков распространения катаральной лихорадки овец в Республике Казахстан
Несмотря на то, что территория Республики Казахстан является благополучной по КЛО, существует риск заноса возбудителя из других стран, в первую очередь, связанный с завозом скота из стран, где циркулирует вирус BTV, или с территории сопредельных государств. В случае заноса инфекции извне, риск распространения КЛО на территории страны зависит от нескольких параметров: климатических характеристик, распространенности потенциальных и компетентных переносчиков инфекционного агента и плотности восприимчивых к вирусу животных.
Анализ климатических параметров и распространенности переносчиков
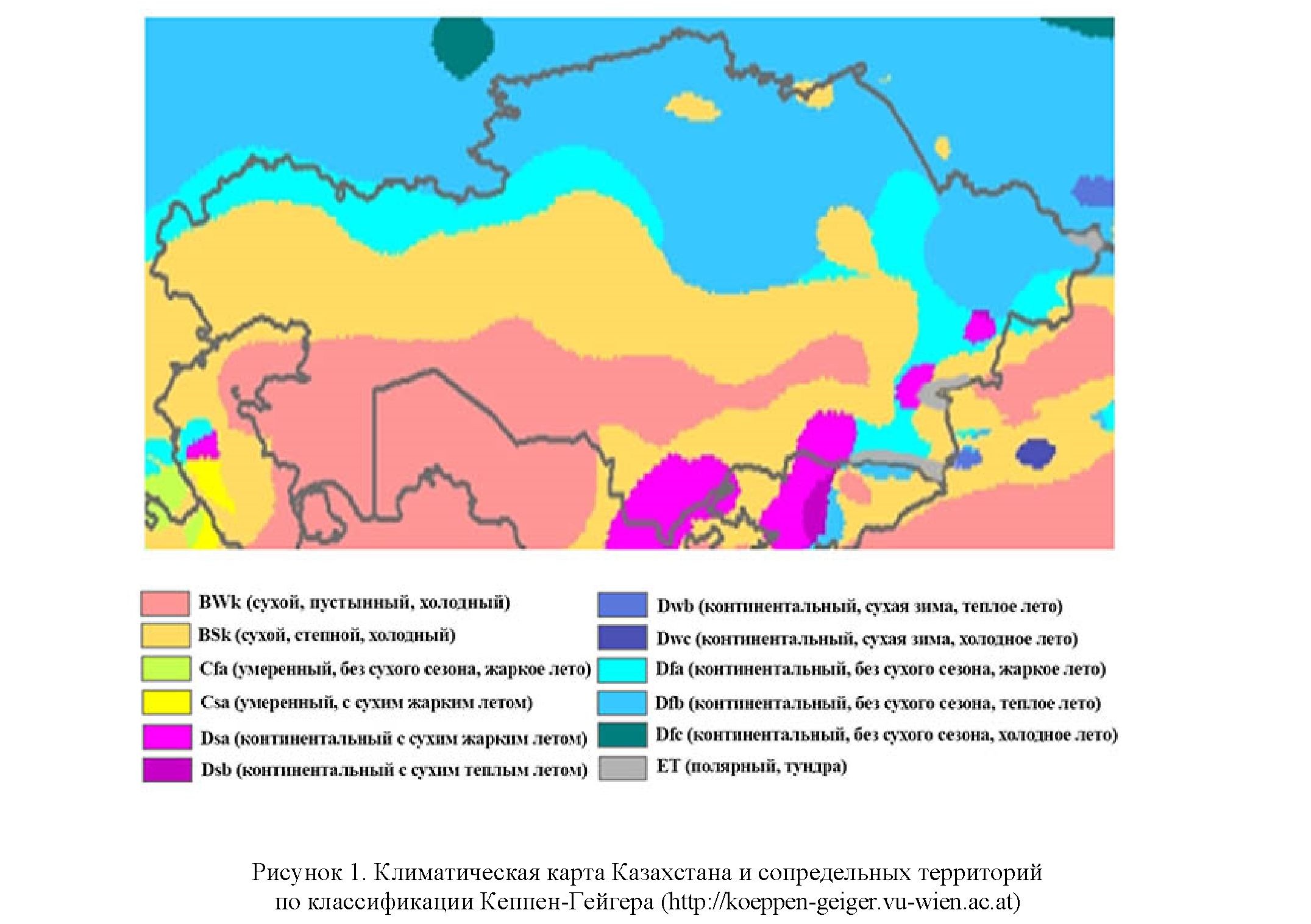
Представители компетентных переносчиков блютанга, Culicoides spp., распространены почти по всей территории Казахстана, но максимальная их численность наблюдается в районах, где лето не очень сухое, а зима теплая. На рисунке 1 представлена климатическая карта Республики Казахстан и сопредельных регионов по Кеппен-Гейгеру. Наиболее оптимальные зоны для размножения и развития Culicoides sp. из тех, что присутствуют в Казахстане — Dsa и Dsb. Эти зоны занимают достаточно значительные территории Туркестанской, Жамбылской и Алматинской областей (рис. 1).
В Казахстане распространены представители следующих подродов мокрецов: Culicoides: Avaritia (C. obsoletus, C. dewulfi, C. chiopterus, C. scoticus, C. glushchenkovae, C. fulvus, C. dewulfi), Cu- licoides (C. punctatus, C. Newsteadi, C. pulicaris, C. grisescens), Hofmania, Monoculicoides (C. riethi, C. puncticollis, C. helveticus, C. nubeculosus), Remmia (C. oxystoma), Oaecata (C. heliophilus, C. longipennis, C. mongolensis, C. kurensis, C. pictipennis, C. shaklawensis, C. cubitalis (kibunensis)), Wirthomyia (C. minutissimus, C. reconditus), Silvaticulicoides (C. fastivipennis, C. subfascipensnis, C. pallidicornis), Beltranmyia (C. desertorum, C. sphagnumensis, C. circumscriptus) [17].
Согласно литературным данным, в Южном Казахстане наиболее многочисленны C. punctatus, C. newsteadi и C. obsoletus [18]; в Центральном Казахстане — C. obsoletus, C. dewulfi и C. montanus [18]; в Северном Казахстане — C. obsoletus, C. punctatus и C. chiopterus [19]; в Восточном Казахстане — C. grisescens и C. obsoletus [19].
Помимо компетентных переносчиков, вирус блютанга может переноситься механически различными кровососущими двукрылыми: мокрецами подрода Lasiohelea рода Forcipomyia, мухами- кровососками, слепнями, мухами-жигалками. Все эти кровососущие двукрылые насекомые широко распространены на территории Казахстана в различных климатических зонах. Поэтому потенциальный ареал распространения BTV может быть шире, чем мокрецов рода Culicoides. Важно, что слепни способны подниматься на достаточно большие высоты, куда другие кровососущие двукрылые никогда не поднимаются. Видимо, именно эти кровососущие мухи переносят вирус блютанга в популяциях высокогорных яков.
Риски в связи с численностью поголовья восприимчивых к КЛО животных
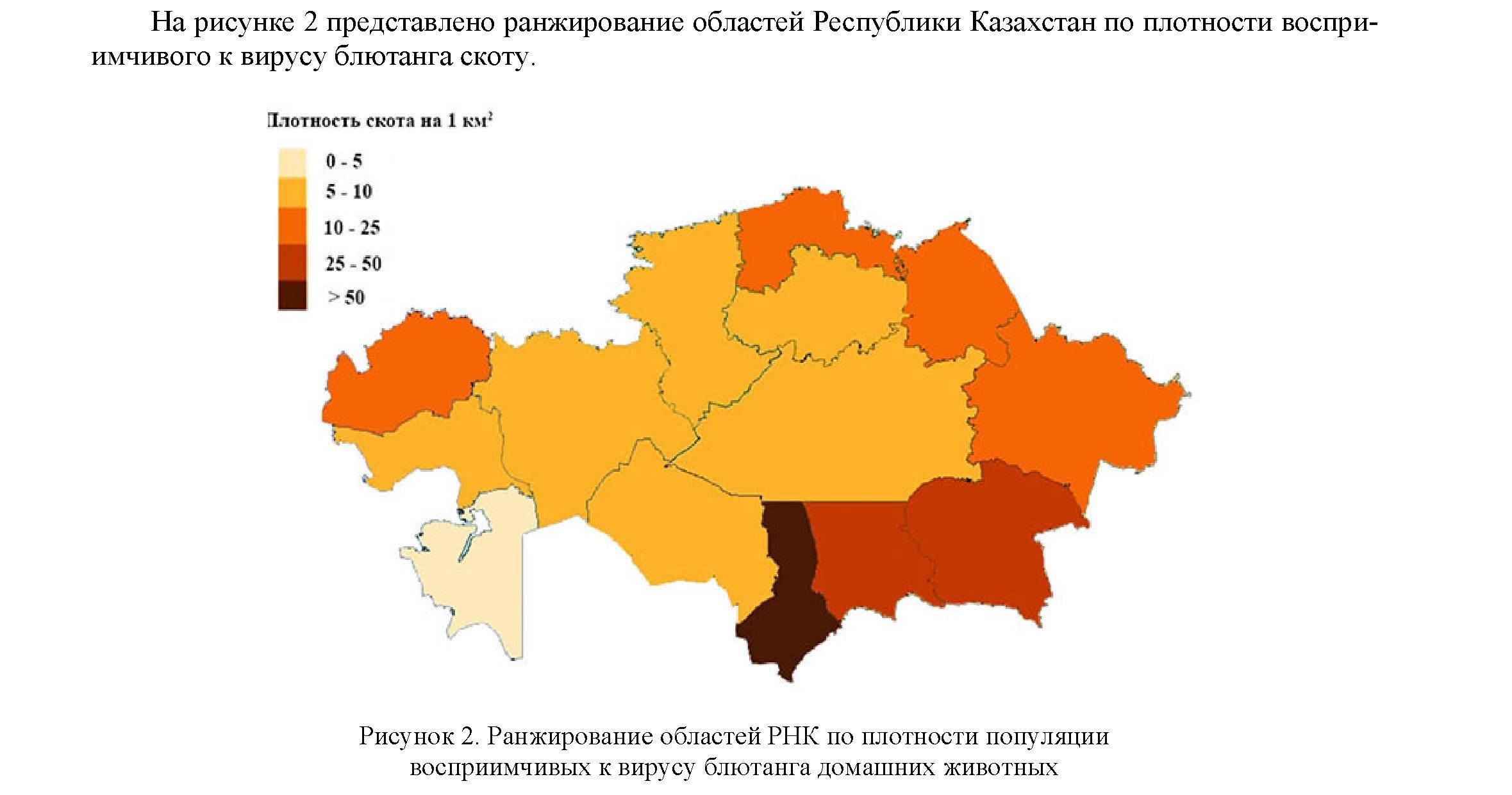
Известно, что чем выше плотность восприимчивых к вирусу животных, тем выше риск потенциального возникновения и распространения инфекции. Хотя основными хозяевами для вируса блю- танга являются овцы, плотность представителей других парнокопытных, а также мозоленогих, которые могут быть носителями вируса блютанга и не проявлять при этом видимых клинических проявлений, также должна учитываться при оценке риска распространения КЛО. Важную роль в распро-
странении блютанга могут играть дикие животные, но достоверная информация об их поголовье часто отсутствует в открытых источниках информации.
В таблице 1 представлена информация по численности восприимчивого к вирусу блютанга домашнего скота по областям страны.
Поголовье восприимчивого к BTV скота по областям
|
Область |
Поголовье МРС, тыс. голов |
Поголовье КРС, тыс. голов |
Поголовье верблюдов, тыс. голов |
Общее поголовье восприимчивых к BTV животных, тыс. голов |
|
Акмолинская, включая г. Нур-Султан |
727,113 |
538,9 |
0,1 |
1266,056 |
|
Актюбинская |
1464,524 |
632,5 |
19,2 |
2116,196 |
|
Алматинская, включая г. Алматы |
4809,915 |
1315,1 |
8,9 |
6133,885 |
|
Атырауская |
714,361 |
209,3 |
36,0 |
959,655 |
|
Восточно-Казахстанская |
2210,174 |
1323,4 |
0,6 |
3534,198 |
|
Жамбылская |
3702,388 |
533,7 |
8,5 |
4244,651 |
|
Западно-Казахстанская |
1466,599 |
753,9 |
2,5 |
2222,921 |
|
Карагандинская |
1382,277 |
808,7 |
1,8 |
2192,786 |
|
Костанайская |
551,109 |
532,5 |
0,3 |
1083,869 |
|
Кызылординская |
847,370 |
387,1 |
57,5 |
1291,977 |
|
Мангыстауская |
603,099 |
28,7 |
84,8 |
716,558 |
|
Павлодарская |
740,717 |
568,1 |
0,1 |
1308,866 |
|
Северо-Казахстанская |
623,083 |
495,2 |
0,0 |
1118,331 |
|
Туркестанская, включая г. Шымкент |
5944,736 |
1407,8 |
39,8 |
7392,398 |
|
Республика Казахстан |
25787,47 |
9534,88 |
260,00 |
35582,35 |
Таблица 1
Анализ рисков заноса блютанга на территорию страны из сопредельных государств. Хотя общее поголовье диких полорогих и мозоленогих в нашей стране не сопоставимо с общим поголовьем домашнего скота, восприимчивого к BTV, эти животные, тем не менее, могут играть важную роль в заносе инфекции с территории регионов сопредельных государств, в которых КЛО распространена. Дикие яки, горные козлы и бараны способны легко преодолевать горные хребты, являющиеся естественной преградой для домашних животных. С этими животными инфекция вполне может перейти с
территории Китая, где циркулируют более десятка серотипов BTV (BTV-1, -2, -3, -4, -5, -7, -9, -12, -15, -16, -25, -27) [20, 21]. Так, было показано, что серопревалентность к BTV среди яков в Синьцзян- Уйгурском автономном районе Китая составляет от 2 до 5 % [22], что указывает на циркуляцию вируса в этих популяциях животных. В 2014 г. появились данные о циркуляции BTV в популяциях яков в Киргизии [23]. Узбекистан не предоставляет открытой информации относительно циркуляции на его территории BTV, но необходимо признать, что особенности климата этой страны оптимальны для размножения компетентных переносчиков вируса блютанга и распространения КЛО.
Наибольший же риск в отношении заноса инфекции на территорию нашей страны представляет импортируемый из Европы племенной скот (большей частью КРС). Именно в ЕС блютанг распространен очень широко, там ежегодно фиксируются вспышки этой инфекции, причём выявляются самые различные серотипы BTV. Благодаря Государственной программе по развитию отечественного сельского хозяйства для местных фермеров создаются благоприятные условия для завоза скота из-за рубежа (благодаря субсидиям на приобретение скота и проведение тестирования завозимого скота).
Больше всего племенного скота импортируется в нашу страну из России, но следующими после России крупными импортерами скота в РК являются Германия и Австрия, где болезнь является эндемичной. Важно, что коровы переносят инфекцию обычно бессимптомно, и при этом во многих европейских странах от блютанга прививается не только МРС, но и КРС (особенно от девятого серотипа, способного и у коров вызывать выраженные клинические проявления), поэтому серологическими методами невозможно идентифицировать инфицированных BTV животных (вакцинация штаммом одного серотипа BTV обычно не дает никакой кросс-реактивной защиты от других серотипов вируса).
В ряде стран ЕС применяются аттенуированные вакцины против BTV, что создает угрозу проникновения на территорию РК хотя бы мезогенных штаммов вируса. Распространение таких штаммов на территории страны если не приведет к серьёзным экономическим потерям, то создаст немалые сложности при мониторинговых исследованиях, поскольку серологическими методами невозможно дифференцировать вакцинные мезогенные штаммы вируса от немезогенных полевых штаммов.
Больше всего племенного скота в течение последних трёх лет импортируется в Алматинскую область. Достаточно много скота также импортируется в Северо-Казахстанскую, Акмолинскую, Актюбинскую и Восточно-Казахстанскую области.
Зонирование территории РК по уровню риска распространения блютанга
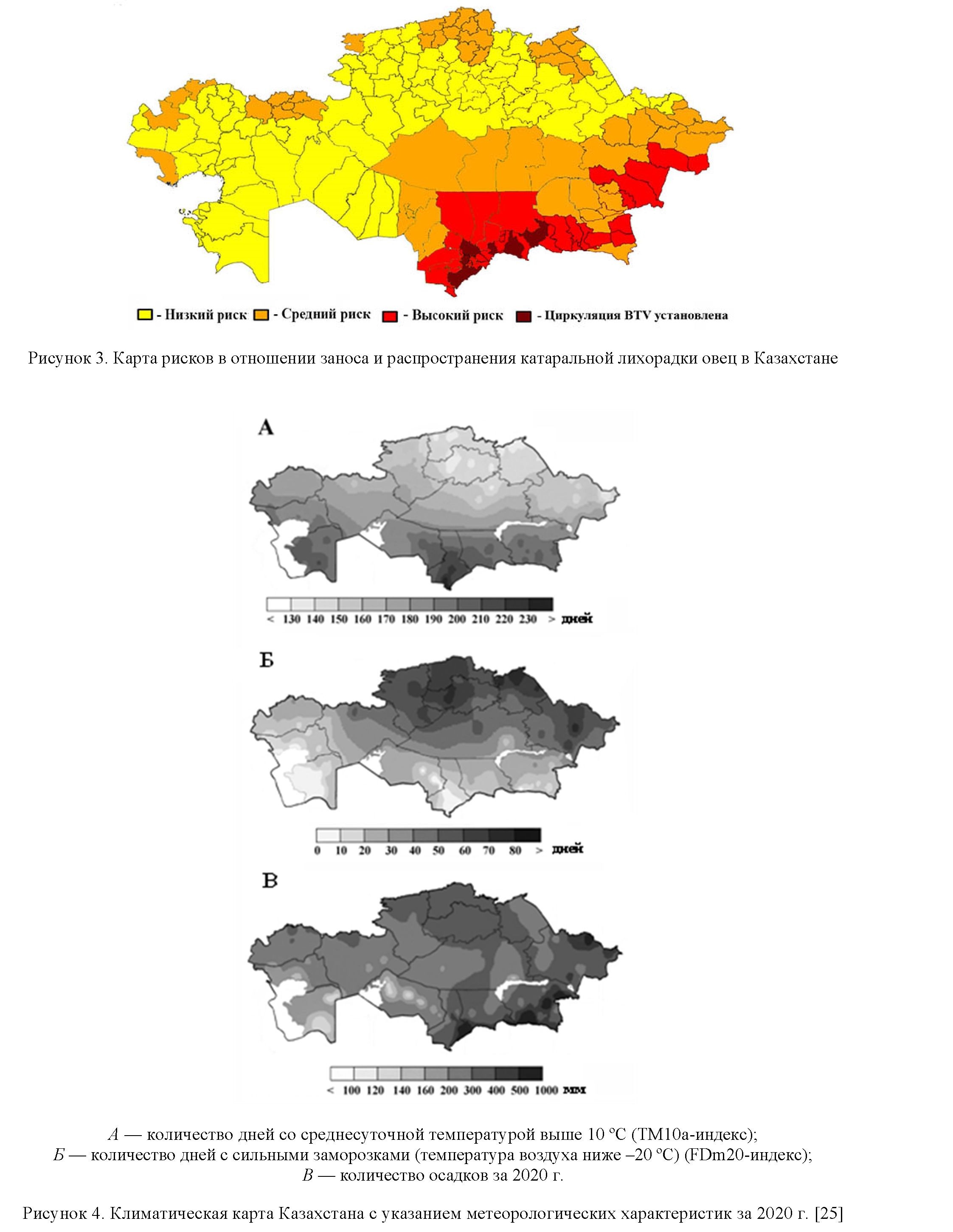
Основываясь на данных о плотности поголовья восприимчивого к BTV скота, климатических параметрах, ареалах распространения компетентных и механических переносчиков вируса, количестве голов импортируемого ежегодно скота и результатах анализа риска заноса инфекции из приграничных регионов, литературных данных о выявлении серопозитивных животных, а также на данных лабораторных исследований мониторингового исследования КЛО на территории РК, проводимого в 2018–2020 гг. Министерством сельского хозяйства РК, в которое наша исследовательская группа была вовлечена, мы построили карту рисков распространения КЛО в Казахстане (рис. 3).
Следует отметить, что в последние годы в Казахстане наблюдается значительное повышение температуры воздуха (в среднем на 0,31 ºС каждые 10 лет) [24]. Метеорологи заметили тенденцию изменения климата за период 1976–2021 гг. в юго-восточном Казахстане, включая: 1) тенденцию к уменьшению повторяемости морозных дней (когда суточная минимальная температура опускается ниже нуля) и дней с сильными заморозками (температура воздуха ниже –20 ºС) (тенденция характерна для всей территории страны); 2) зимой, весной и летом наблюдается тенденция к увеличению количества осадков на 1,3–3,8 мм/10 лет (на остальной территории страны ситуация обратная); 3) снижается частота случаев ночных и дневных заморозков (тенденция характерна для всей территории страны); 4) увеличивается продолжительность вегетационного периода (при температуре выше 10 ºС) (тенденция характерна для всей территории страны); 5) наблюдается отрицательный тренд суточной амплитуды температуры (на западе страны ситуация обратная, на остальной территории без заметных изменений) (рис. 4) [24].
Повышение температуры, смягчение климата и увеличение количества осадков в юго-восточном регионе Казахстана способствуют повышению темпов размножения, активности и выживаемости мошек Culicoides, скорости репликации вируса и могут усилить векторную способность мокрецов. Таким образом, инфекция может проникнуть в новые районы к северу от казахстанско-узбекской границы.
Определение размера выборки и сбор полевых образцов
для мониторинга катаральной лихорадки овец
Как видно из данных, представленных на рисунке 3, наиболее рисковыми по инфекции оказались Туркестанская, Жамбылская и Алматинская области. Именно в этих областях было решено провести сбор образцов для мониторинга распространения BTV в рамках выполнения проекта AP09259102.
Для определения общего размера выборки для проведения широкомасштабного мониторинга по КЛО в Казахстане общее поголовье крупного и малого рогатого скота было принято равным 33972,6 тысяч голов (на 1 января 2022 г.) [26]. Для эпидемиологических исследований доверительный интервал в подавляющем большинстве случаев принимается равным 95 %, поэтому при расчетах использовали это значение. Величину допустимой погрешности приняли равной 5 %. При расчетах полагали, что ожидаемая превалентность в популяции крупного и мелкого рогатого скота на территории Казахстана составляет 50 % (согласно рекомендациям МЭБ). Общий размер выборки составил 400 животных (в том случае, если в одной точке сбора отбирать по двадцать образцов). Исходя из результатов анализа рисков, было решено провести сбор образцов по областям, как указано в таблице 2.
Таблица 2
План по сбору образцов от крупного и мелкого рогатого скота для целей мониторинга
|
Область |
Поголовье на 01.01.2022 г., тыс. голов |
Размер выборки, голов |
|
Туркестанская |
6980,5 |
180 |
|
Жамбылская |
4201,5 |
180 |
|
Алматинская |
5947,3 |
140 |
|
Итого |
500 |
|
Общее число задействованных в исследовании животных было решено увеличить до 500, чтобы обеспечить возможность отбраковки образцов (например, гемолизированных сывороток).
Заключение
В обзоре представлены результаты проведенного анализа эпизоотологической ситуации по КЛО на территории Казахстана, проведена эпидемиологическая оценка рисков в отношении заноса и распространения инфекции в стране, определен размер выборки для проведения мониторинга по КЛО и проведен сбор биологического материала от животных для целей мониторинга.
Работа выполнена в рамках гранта КН МОН РК AP09259102 «Генетическая характеризация изолятов вируса блютанга, выявляемых в Казахстане, и разработка отечественной тест-системы для их дифференциальной детекции».
Список литературы
- Mertens P.P.C. Bluetongue virus diagnosis. Bluetongue. 1st ed. / P.P.C. Mertens, S. Maan, C.A. Batten, K.E. Darpel, A.R. Shaw, N.S. Maan. — London: Elsevier, Academic Press, 2009. — P. 101–125.
- Sperlova A. Bluetongue: a review / A. Sperlova, D. Zendulkova // Veterinarni Medicina. — 2011. — Vol. 56, No. 9. — P. 430–452.
- Lundervold M. First evidence if bluetongue virus in Kazakhstan / M. Lundervold, E.J. Milner-Gulland, C.J. O’Callaghan, C. Hamblin // Veterinary Microbiology. — 2003. — Vol. 92. — P. 281–287.
- OIE — Terrestrial Animal Health Code. Infection with Bluetongue Virus / World Organisation for Animal Health. — Paris, 2019. — Vol. 2, Ch. 8.3. — Р. 75017.
- Koltsov A. Identification and Characterization of Bluetongue Virus Serotype 14 in Russia / A. Koltsov, S. Tsybanov, A. Gogin, D. Kolbasov, G. Koltsova // Frontiers in Veterinary. — 2020. — Vol. 7. — P. 26.
- Zaher K.S. Molecular characterization of bluetongue disease / K.S. Zaher // Middle East Journal of Scientific Research. — 2015. — Vol. 23, No. 11. — P. 2689–2694.
- Maan S. Development and evaluation of Real Time RT-PCR assays for detection and typing of bluetongue virus / S. Maan, N.S. Maan, M.N. Belaganahalli, A.C. Potgieter, V. Kumar, K. Batra, I.M. Wright, P.D. Kirkland, P.P.C. Mertens // PLoS ONE. — 2016. — Vol. 11, No. 9. — e0163014.
- Ries C. Putative novel serotypes '33' and '35' in clinically healthy small ruminants in mongolia expand the group of atypical BTV / C. Ries, T. Sharav, E.O. Tseren-Ochir, M. Beer, B. Hoffmann // Viruses. — 2020. — Vol. 13, No. 1. — P. 42.
- Ries C. Putative Novel Atypical BTV Serotype '36' Identified in Small Ruminants in Switzerland / C. Ries, A. Vögtlin, D. Hüssy, T. Jandt, H. Gobet, M. Hilbe, C. Burgener, L. Schweizer, S. Häfliger-Speiser, M. Beer, B. Hoffmann // Viruses. — 2021. — Vol. 13, No. 5. — P. 721.
- Meiswinkel R. The taxonomy of Culicoides vector complexes — unfinished business / R. Meiswinkel, L.M. Gomulski, J.-C. Delecolle, M. Goffredo, G. Gasperi // Vet. Italiana. — 2004. — Vol. 40. — P. 151–159.
- Luedke A.J. Preliminary bluetongue Transmission with the sheep ked Melophagus ovinus (L.) / A.J. Luedke, M.M. Jochim, J.G. Bowne // Canadian Journal of Comparative Medicine and Veterinary Sciences. — 1965. — Vol. 29, No. 9. — P. 229–231.
- Baldacchino F. Transmission of pathogens by Stomoxys flies (Diptera, Muscidae): a review / F. Baldacchino, V. Muenworn, M. Desquesnes, F. Desoli, T. Charoenviriyaphap, G. Duvallet // Parasite. — 2013. — Vol. 20, No. 26. — P. 2013026.
- Hoffmann B. Monitoring of putative vectors of bluetongue virus serotype 8, Germany / B. Hoffmann, B. Bauer, Ch. Bauer, H. -J. Bätza, M. Beer, P.-H. Clausen, M. Geier, J.M. Gethmann, E. Kiel, G. Liebisch, A. Liebisch, H. Mehlhorn, G.A. Schaub, D. Werner, F.J. Conraths // Emerging Infectious Diseases. — 2009. — Vol. 15, No. 9. — P. 1481–1484.
- Evermann J.F. Accidental introduction of viruses into companion animals by commercial vaccines / J.F. Evermann // Veterinary Clinics of North America. — 2008. — Vol. 38. — P. 919–929.
- Miranda M.A. Bluetongue: control, surveillance and safe movement of animals / M.A. Miranda, J.A. Stegeman, D. Bicout, A. Botner, A. Butterworth, P. Calistri, K. Depner, S. Edwards, B. Garin-Bastuji, M. Good, C.G. Schmidt, et al. // EFSA Journal. — 2017. — e04698.
- Rojas J.M. Diagnosing bluetongue virus in domestic ruminants: current perspectives / J.M. Rojas, D. Rodríguez-Martín, V. Martín, N. Sevilla // Veterinary medicine. — 2019. — Vol. 10. — P. 17–27.
- Глухова В.М. Кровососущие мокрецы родов Culicoides и Forcipomyia (Ceratopogonidae) / В.М. Глухова // Фауна СССР. Насекомые двукрылые. — Т. 3, Вып. 5а. — Л.: Наука, 1989. — 408 с.
- Bulatov Ye. Prevalence of Bluetongue Virus among goats, sheep, and cattle in the southern regions of Kazakhstan / Ye. Bulatov, K. Zhugunissov, D. Taranov, Zh. Amanova, Zh. Koshemetov, G. Nakhanova, G.R. Risatti, N. Sandybayev // 99th Conference of Research Workers in Animal Diseases At: Chicago Marriott, Downtown Magnificent Mile Chicago, Illinois. — 2018.
- Аубакирова А.М. Фауна и экология мокрецов высокогорных пастбищ Юго-Западного Алтая / А.М. Аубакирова // Вестн. Алтай. гос. ун-та. — 2017. — Т. 10, № 154. — С. 92–95.
- Yang H. Phylogenetic Characterization Genome Segment 2 of Bluetongue Virus Strains Belonging to Serotypes 5, 7 and 24 Isolated for the First Time in China during 2012 to 2014 / H. Yang, L. Xiao, J. Wang, J. Meng, M. Lv, D. Liao, J. Song, L. Gao, H. Xiong, Y. He, et al. // Transboundary Emerging Diseases. — 2016. — Vol. 64. — P. 1317–1321.
- Ma J. Spatial Patterns and Risk Factors of Bluetongue Virus Infection in Inner Mongolia, China / J. Ma, X. Gao, B. Liu, J. Xiao, H. Chen, H. Wang // Vector Borne Zoonotic Diseases. — 2019. — Vol. 19. — P. 525–532.
- Li J. Seroprevalence of Bluetongue virus in domestic yaks (Bos grunniens) in Tibetan regions of China based on circulating antibodies / J. Li, K. Li, M. Shahzad, Z. Han, F. Nabi, J. Gao, J. Han // Tropical animal health and production. — 2015. — Vol. 47, No. 6. — P. 1221–1223.
- Avci O. Detection of antibodies against Blue tongue virus in yaks (Bos grunniens) in Issyk kul, first report / O. Avci, Y. Orhan, B. Oya, K. Mehmet, Y. Sibel, S. Atilla // J. Anim. Plant. Sci. — 2014. — Vol. 24, No. 4. — P. 1220–1223.
- Жакатаева Б.Т. Тенденции изменения среднегодовой температуры воздуха на территории Казахстана / Б.Т. Жакатае- ва // Вопросы географии Казахстана: Тр. Каз. геогр. общ-ва. — Т. 2. — Караганда: Изд-во КарГУ, 2010. — С. 21–27.
- Ежегодный бюллетень мониторинга состояния и изменения климата Казахстана: 2021. Министерство экологии, геологии и природный ресурсов Республики Казахстан. — 2021. — 54 с. Электронный ресурс. Режим доступа: https://www.kazhydromet.kz/en/klimat/ezhegodnyy-byulleten-monitoringa-sostoyaniya-i-izmeneniya-klimata-kazahstana
- Казстат. Динамика основных социально-экономических показателей в регионах Казахстана. — 2022. Бюро национальной статистики Агентства по стратегическому планированию и реформам Республики Казахстан. [Электронный ресурс]. — Режим доступа: http://www.stat.gov.kz/region