Резюме
К природным соединениям, представляющим большую ценность для медицины в качестве основы для получения новых высокоэффективных лекарственных средств для лечения и профилактики вирусных инфекций и иммунодефицитов различной этиологии относится тритерпеноид экстракта корня солодки - глицирризиновая кислота (ГК). В связи с этим актуальны исследования по стандартизации комбинированных лекарственных препаратов, содержащих компоненты корня солодки. Данный литературный обзор посвящен исследованию стандартизации комбинированных лекарственных препаратов корня солодки.
Ключевые слова: глицирризиновая кислота, корни солодки, стандартизация, глицирретовая кислота, аскорбиновая кислота
Современная терапия вирусных заболеваний сопровождается трудностями, связанными с общей токсичностью и гепатотоксичностью, формируемой вирусной инфекцией и лекарственными средствами, обладающими побочными реакциями, понижением иммунного статуса организма человека, мутацией вирусов по отношению к синтетическим противовирусным препаратам. Поэтому в последнее время наблюдается тенденция к сочетанному применению противовирусных и иммунотропных средств, позволяющих уменьшить дозировки используемых препаратов, а, следовательно, уменьшить их побочные реакции.
Особенно перспективным представляется применение препаратов, имеющих широкий спектр действия и сочетание фитопрепаратов с лекарственными средствами синтетического происхождения, в большинстве случаев обладающих нежелательными побочными реакциями.
К таким природным соединениям, представляющим большую ценность для медицины в качестве основы для получения новых высокоэффективных лекарственных средств для лечения и профилактики вирусных инфекций и иммунодефицитов различной этиологии относится тритерпеноид экстракта корня солодки - глицирризиновая кислота (ГК) [1].
В связи с этим актуальны исследования по контролю качества и стандартизации лекарственных препаратов, содержащих компоненты корня солодки. Весьма актуальным является унификация методов контроля качества сырья солодки, субстанций и препаратов из них по содержанию глицирризиновой кислоты.
Солодка содержит целый ряд комплексов биологически активных веществ (БАВ), а также сотни индивидуальных природных соединений, отнесенных к различным химическим классам веществ с разнообразными фармакотерапевтическими свойствами. В корнях и корневищах солодки содержатся такие группы биологически активных веществ, как сапонины (глицирризин в виде калиевых и кальциевых солей глицирризиновой кислоты), флавоноиды, халконы (изоликвиритигенин, изоликвиритин, ликуразид и др.) [14,7]. Особую ценность среди компонентов солодки представляют глицирризиновая кислота (ГК) и ее производные, которые обладают широким спектром действия: противовоспалительным, иммуномодулирующим, гепатопротекторным, антиоксидантным, антитоксическим и др. [1,5-7]. Поэтому методики контроля качества основаны на анализе ГК в составе препаратов солодки.
Глицирризиновая кислота ГК (20β-карбокси-11-oксo-30-нoрoлеан-12-ен-3β-ил-2-О-β-D-глюкопирануронозил-α-D-глюкопиранозидуроновaя кислота) – основной фармакологически активный компонент корня солодки, содержание которого может достигать 25% от массы сухого материала. Общее содержание экстрактивных веществ может достигать 40% [5]. Температура плавления (Т пл.) – ГК (220°C). УФ-спектр глицирризиновой кислоты показывает, что максимальный пик ее поглощения находиться в области 254 нм [9-12]. Агликоном ГК является одноосновная β – глицирретиновая (глицирретовая) кислота с характерной для нее кетогруппой, которая находится в 11 положении. Ее сахаристая часть представляет собой 2 молекулы глюкуроновой кислоты. Кроме β-формы в корнях солодки голой присутствуют следы α- формы глицирретиновой кислоты, однако она не обладает фармакологической активностью [18].
В корнях солодки ГК находится в виде смешанных калиево-кальциево- магниевых солей ГК, а также образует органические соли с металлами и аммонием. Самая распространенная ее соль: глицирризат аммония – глицирам [2]. Соли щелочных металлов растворимы в воде, а соли тяжелых металлов нерастворимы и легко разлагаются сероводородом с образованием свободной глицирризиновой кислоты и это свойство используется часто при очистке ГК [19].
Сравнительный анализ фармакопейных методов стандартизации лекарственного сырья
солодки.
Качество корня солодки регламентируется ведущими фармакопеями мира, которые включают в себя солодку обыкновенную (G. glabrа) и солодку уральскую G. urаlensis [9-16]. Ссылки идут беспорядочно
Для оценки соответствия действующей нормативной документации на корни солодки современным требованиям мы сравнили отечественную монографию «Солодки корни» и доступную зарубежную нормативную документацию, регламентирующую качество корней солодки. Были проанализированы фармакопейные статьи на корни солодки, входящие в Европейскую Фармакопею 7.0 и 8.0, Государственную Фармакопею Республики Беларусь 1 и 2 издания [16], Британскую фармакопею [17], Государственную Фармакопею Японии XVII [13], Китайскую Государственную Фармакопею 2005 и 2010 [11], Американскую Фармакопею [12], Государственную Фармакопею Российской Федерации ГФ РФ ХIV (Россия) 2018 г [15]. Кроме корней солодки голой и солодки уральской, в ряде стран допускается также заготовка корней солодки вздутой (Glycyrrhiza inflata Bat.).
Как указано в таблице 1, процентное содержание ГК в корне солодке варьируется от 2,0% (Фармакопея Китай) до 6,0% (ГФ СССР Х, ныне ГФ РФ ХIV). Такое низкое содержание в фармакопее КНР можно пояснить наличием солодки вздутой, а также тем, что китайские виды G. uralensis и G. glabra содержат ГК 2,1-6,1% [11]. Фармакопеи USP (США) [12] и Японии [13] разрешают, также как ГФ РФ - только солодку голую и солодку уральскую, при этом в ГФ РФ нормируемое содержание ГК 6% (СФ в УФ- области) на аналогичные виды солодки, что на 40% выше, чем в других странах. Фармакопеи Республик Казахстан и Беларусь [16] гармонизированы с Европейской Фармакопеей и предел содержания ГК установлен на уровне 4%. (ВЭЖХ).
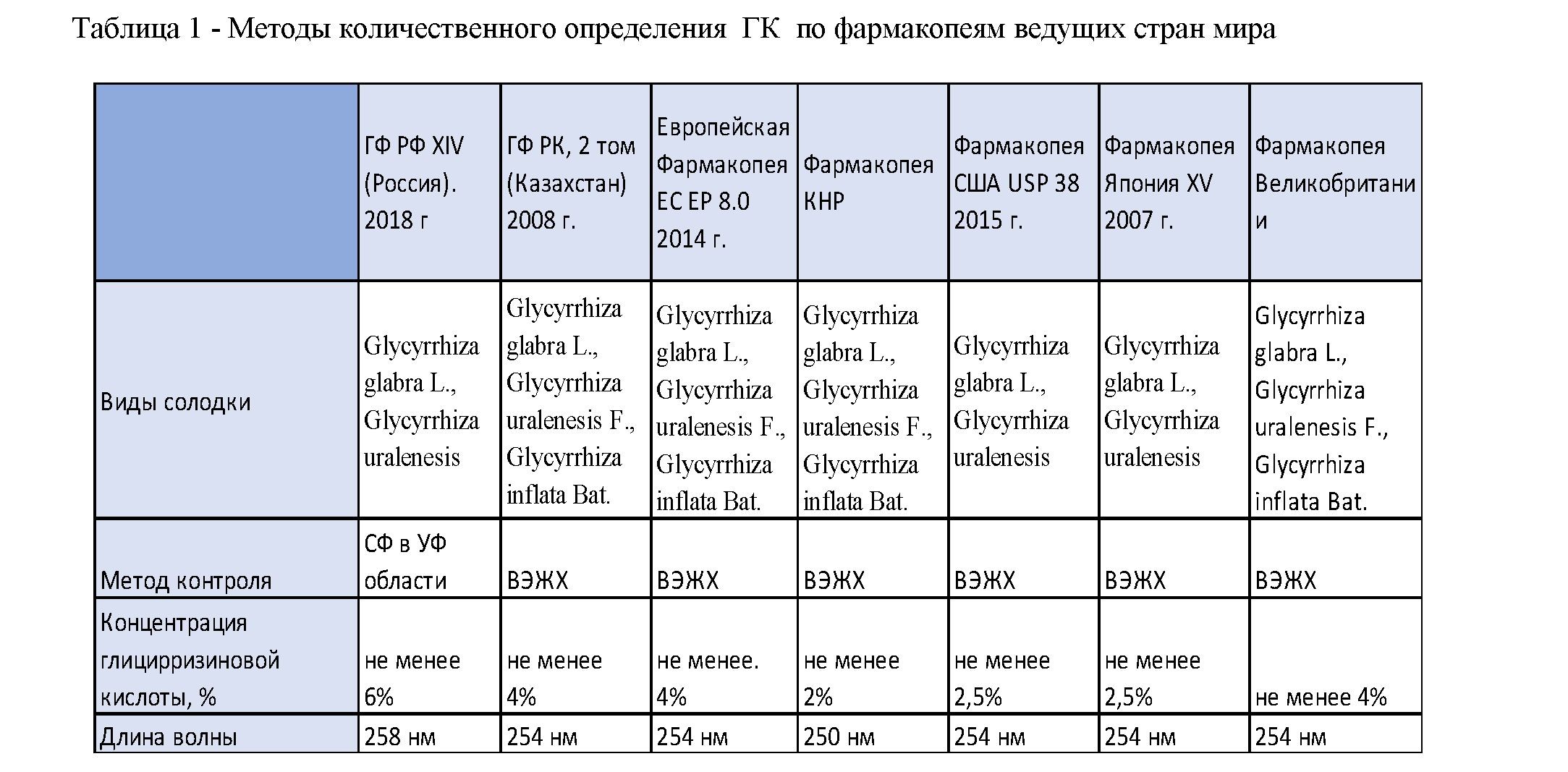
Помимо солодки голой (G. glabra) и солодки уральской (G. urаlensis), государственные фармакопеи ЕС [10], Казахстана [9], Китая [11] и Великобритании [17] включают в себя солодку вздутую (Glycyrrhiza inflata Bat.)
Фармакопея Великобритании, кроме указанных в таблице 1 видов солодки, также содержит отдельные монографии на аммониевую соль глицирризиновой кислоты (Ammonium Glycyrrhizinate), сухой экстракт солодки с содеранием ГК от 5% до 7% (Liquorice Dry Extract for Flavouring Purposes), жидкий экстракт солодки (Liquorice Liquid Extract), корень используемый в традиционной китайской медицине (ТКМ) (Liquorice Root for use in THM), обработанный корень солодки для использования в ТКМ 2% и стандартизированный жидкий спиртовый эсктракт 3-5% (Standardised Liquorice Ethanolic Liquid Extract)
Все перечисленные фармакопеи при определении количественного содержания ГК используют метод высокоэффективной жидкостной хроматографии (ВЭЖХ); только ГФ РФ ХIV [15], рекомендует использовать метод спектрофотометрии в УФ области.
Основные условия методов хроматографирования, указанные в фармакопеях Европейского Союза, США, Китая и Японии свидетельствуют, что длина волны, при которой определяется ГК составляет 254 нм – ЕС, США, Япония; 250 нм – Китай; 258нм – РФ методом СФМ
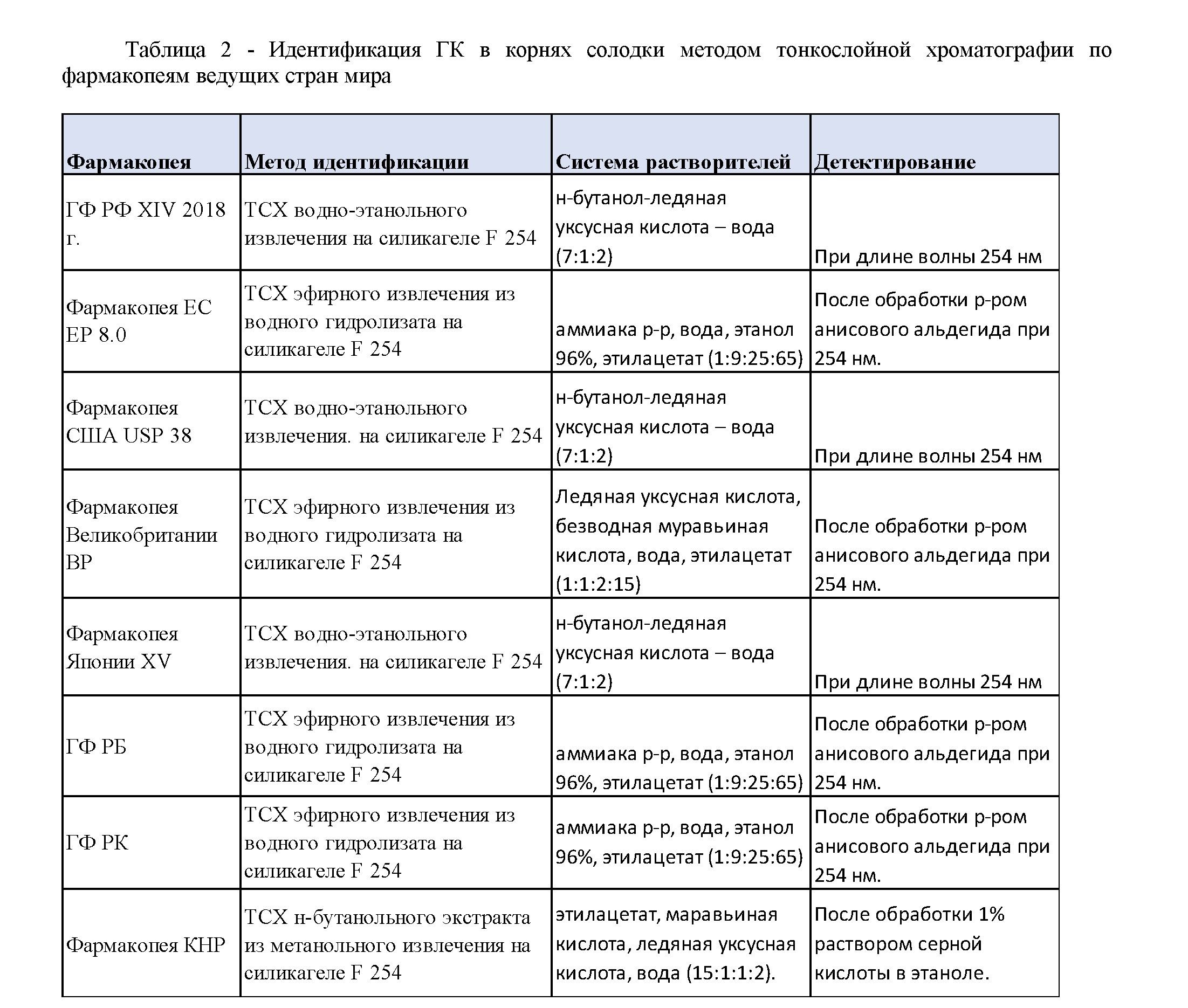
Для определения подлинности ГК в образцах солодки обыкновенной (G. glabrа) и солодки уральской G. urаlensis согласно приведенным в таблице 2 фармакопейным методикам используют метод тонкослойной хроматографии (ТСХ).
Как показал сравнительный анализ фармакопейных методик идентификации ГК и определения посторонних примесей методом ТСХ, хроматографирование проводится в системах полярных растворителей нейтрального и основного характера [9-16]. В качестве детектирующего устройства используют УФ-спектр, позволяющий идентифицировать с высокой чувствительностью как активные компоненты, так и их примеси. В качестве раствора сравнения используют кислоту глицирретиновую и тимол [9]. Зоны проявляются в УФ-свете в виде соответствующих фиолетовых пятен кислоты глицирретовой, красных пятен тимола и желтых пятен примеси изоликвиридигенина. Допускается при этом присутствие других зон [9-17]. Значение Rf для ГК в пределах 0,3 ± 0,02 [9].
26
Номенклатура показателей качества на примеси идентичны во всех фармакопеях (влажность, зола общая и зола нерастворимая в хлористоводородной кислоте). Однако раздел «Посторонние примеси» приведен не во всех статьях, а только в ГФ РБ и ГФ РФ, подробно описан в ГФ XIV. Следует отметить, что только в European Pharmacopoeia 7.0 [10] (и гармонизированной с ней ГФ РБ) нормируется содержание охратоксина (не более 20 мкг/кг). Статьи Ф ЕС, ГФ РБ и ГФ РК гармонизированы. Практически идентичны фармакопейные статьи на корни солодки Ф Японии [13] и Ф США [12].
Для оценки соответствия действующей нормативной документации на корни солодки современным требованиям было проведено сравнение отечественной монографии на «Солодки корни» с доступной зарубежной нормативной документацией, регламентирующую качество корней солодки. Сравнительный анализ показал, корни солодки входят практически во все ведущие мировые фармакопеи. Фармакопейные методики стандартизации сырья корней солодки в некоторых странах отличаются и отсутствует нормативная документация на отдельные препараты
 27
27
солодки. Монография ГФ РК на «Солодки корни» отвечает современным требованиям по полноте и качеству испытаний.
Стандартизации лекарственных препаратов солодки
Растительные материалы, используемые в биологически активных добавках, обычно идентифицируются с помощью макроскопических и микроскопических исследований, выполняемых на сырье, с последующим применением химических методов идентификации, обычно выполняемых на сырых экстрактах. Такие химические методы включают тонкослойную хроматографию (ТСХ) или высокоэффективную жидкостную хроматографию (ВЭЖХ) в сочетании с УФ- или масс-спектрометрическим детектированием. Эти методы идентификации могут быть дополнены методами штрих-кодирования ДНК, которые предпочтительно выполняются на растительном сырье, поскольку экстракты и высоко обработанные растительные материалы обычно имеют низкое качество ДНК, непригодное для точной идентификации ДНК [20,21]. Контроль качества пищевых добавок также требует количественного измерения химических компонентов в исходном материале и в готовом продукте.
В случае солодки для измерения химических компонентов в сырых экстрактах, но редко в сложных растительных пищевых добавок, использовались различные аналитические методы, такие как электрофорез в капиллярной зоне [22], ВЭЖХ-УФ 18-22, ядерный магнитный резонанс (ЯМР) [23], ВЭЖХ-масс-спектрометрия (МС) [24], и ВЭЖХ-тандемная масс-спектрометрия (МС/МС) [25,26]. В случае солодки для измерения химических компонентов в сырых экстрактах использовались различные аналитические методы, такие как ВЭЖХ-УФ, [27-31] ядерный магнитный резонанс (ЯМР) [23], ВЭЖХ-масс-спектрометрия (МС/МС). Метод ВЭЖХ-МС/МС более оказался более специфичен, чувствителен и позволяет проводить более быстрое разделение ГК, чем методы ВЭЖХ-УФ в растительных пищевых добавках [32].
Гель для местного применения с алоэ вера и экстрактом солодки используют в качестве ранозаживляющего, антибактериального и противовоспалительное средство. Физико-химические методы стандартизации позволяют анализировать каждый компонент при совместном присутствии при низких концентрациях [33]. Уровень поглощения определенного количества порошка экстракта солодки после процесса соединения измеряли с помощью спектрофотометра при 640 нм [33]. Результаты показали 7,36±0,1% ГК на каждый грамм порошка экстракта солодки [33].
В работе Егорова М. В. [34] для количественного содержания ГК был исследован ряд различных лекарственных препаратов солодки голой (сухой, густой экстракт) методом спектрофотометрии. Оптическую плотность определяли при длине волны 258 нм в кювете с толщиной слоя 10 мм в качестве раствора сравнения использовали стандартный образец (СО) глицирама [34]. Содержание ГК в сырье было определено в пределах 10,51% до 15,24 в сухом экстракте от 18,35% до 21,80%, в густом экстракте 7,08% до 13.92% и 0,25% до 0,73% в сиропе.
В работе Ш. М. Халед [35] подобраны оптимальные условия экстракции шрота корня солодки этанолом, позволяющие дополнительно получить 4,66% флавоноидов и 0,88% глицирризиновой кислоты и определен качественный состав веществ, извлекаемых из шрота этанолом.
Для одновременного определения глицирризиновой кислоты и глицирретиновой кислоты из экстракта корня Glycyrrhiza glabra используется метод разделения ВЭЖХ с обращенной фазой на фотодиоидном матричном детекторе (RPLC-PDA) [36]. Разработанный метод был апробирован в соответствии с Международной конференцией по гармонизации. Метод продемонстрировал хорошую линейность (r2 >0,9989) с высокой точностью и достиг хорошей точности от 97,5 до 101,3 % количественных результатов. Метод является более чувствительным и быстрым (решается в течение десяти минут), чем ранее разработанные методы с использованием обычных ЖК- колонок [36].
В работе [37] теоретически и экспериментально подтверждены технология и стандартизация дермальной мази, состоящей из густого экстракта корня солодки и эфирных масел ромашки и чайного дерева, предназначенных для лечения атопического дерматита. Количественное определение ГК в мази заключалось в экстрактивном выделении GA из препарата, получении его аммонийной соли и измерении оптической плотности этого раствора при 258 ± 2 нм. Содержание ГК в грамме мази рассчитывали с использованием стандартного образца глицирама в шести параллельных определениях. Содержание GA на грамм мази должно составлять 0,0028 г в пересчете на глицирам. ГК в мази идентифицировали параллельно с ее спектрофотометрическим определением с использованием ТСХ и ультрафиолетового света с длиной волны 254 нм (желтое пятно с Rf ~0,3 на уровне стандарта глицирама). [37]
Для доказательства подлинности экстракта корня солодки в суппозиториях оптимальным решением является система хлороформ-метанол-вода (26:14:3). Установлено, что основные активные соединения экстракта корня солодки имели значения Rf для глицирризиновой кислоты около 0,3; для ликуразида – около 0,5. Проведенные исследования количественного определения глицирризиновой кислоты показали, что ее содержание в одном суппозитории составляет не менее 0,035 г в пересчете на глицирам [38].
Анализ Аювердческих препаратов [39] на основе компонентов солодки проводили с использованием высокоэффективной жидкостной хроматографии с обратной фазой оптимизирован для одновременного выделения глицирризина, глабридина и 18β-глицирретиновой кислоты при времени удерживания 6,6, 8,1 и 10,2 мин соответственно. Сырье, его отвар и остатки, образовавшиеся на стадиях приготовления, экстрагировали в метаноле, в то время как липидные композиции экстрагировали с использованием бинарной системы растворителей метанола и н- гексана. Разделение проводили на колонке Hypersil gold при температуре 40 °C, с использованием 0,2% ортофосфорной кислоты с рН 3,5 в воде и ацетонитрила в качестве подвижной фазы. Соединения были обнаружены при длинах волн 230 (глабридин) и 254 (глицирризин и 18β- глицирретиновая кислота) нм. Метод позволил разделить деглицированные готовые продукты, содержащие глабридин и 18β-глицирретиновую кислоту, обладающие лекарственной ценностью [39].
Таким образом, проведение информационно-аналитического исследования методов анализа по фармакопеям ведущих стран мира и других литературных источников показал, что для идентификации и количественного определения биологически активных веществ корня солодки используются современные инструментальные методы как ВЭЖХ, СФ в УФ и ИК- областях и ТСХ.
Списсок литературы
- Baltina LA. (2003) Chemical modification of glycyrrhizic acid as a route to new bioactive compounds for medicine // Current Medicinal Chemistry, 10, –P. 155-177.
- Толстиков Г.А., Шульц Э.Э., Балтина Л.А., Толстикова Т.Г. Солодка. Неиспользуемые возможности здравоохранения России. // Химия в интересах устойчивого развития.- 1997.- No 5.- с.57-73.
- Glycyrrhiza glabra Linn. collected locally. Ind. J. Chem., 19, 128. Esaki, S., Konishi, F. & Kamiya, S. (1978). Synthesis and taste of some glycosides of glycyrrhetic acid. Agric. Biol. Chem., 42, 1599-600.
- Jatav VS., Singh SK., Sharma AK. Recent Pharmacological trends in Glycyrrhiza glabra. International Journal of Pharmaceutical Frontier Research 2011. –№1– P. 170-85.
- Lakshmi T., Geetha RV. Glycyrrhiza glabra commonly known as licorice- a therapeutic review // International Journal of Pharmaceutics & Pharmaceutical Sciences 2011; 3: 20-25.
- Монография ВОЗ о лекарственных растениях, широко используемых в новых независимых государствах (ННГ) [Электронный ресурс]. – ВОЗ, 2010. – 464 с.
- Ковалев В. Н. Практикум по фармакогнозии: учеб. Пособие для ВУЗов/ В., Н.В. Попова, В.С. Кисличенко. – Харьков: Золотые страницы: 2003. – 512 с.
- А.С. Рыбальченко. Исследование экстракции солодкового корня /А.С. Рыбальченко, В.П. Голицын, Л.Ф. Комарова // Химия растительного сырья. 2002. – No4. – С. 55–59
- Государственная Фармакопея Республики Казахстан, том II. – 2008. – 653 c.
- European Pharmacopoeia 7th edition: Liquorice root - Liquiritiae radix 01/2010: 0277 (under minor revision).
- Pharmacopoeia of the people’s republic of China. Vol.1, 2005. P.207-2009.
- Pharmacopoeia – National Form USP 29-NF. Р.2263-4.
- The Japanese Pharmacopoeia, 14th edition. Ministry of Health, Labour and Welfare, Tokyo, Japan Part 2, 2002. P.932-933.
- Государственная Фармакопея РФ ХIII изд. Москва, 2016.
- Государственная Фармакопея РФ ХIV изд. Москва, 2018.
- ГосударственнаяФармакопеяРеспубликиБеларусь2016г.Т.2
- British Pharmacopoeia, Volume I, II, London 2009. \
- Claude B, Morin P, Lafosse M, Belmont AS, Haupt K. Selective solid-phase extraction of a triterpene acid from a plant extract by molecularly imprinted polymer. Talanta 2008, Vol.75. P.344–350.
- Бровченко Б.В. Совершенствование методов контроля качества измельченного сырья и препаратов солодки: дис. на соиск. канд. фарм. наук. Моск. гос. мед. университет им. Сеченова, Москва, 2020.
- Techen N. et al. DNA barcoding of medicinal plant material for identification //Current opinion in Biotechnology. – 2014. – Т. 25. – С. 103-110.
- De Boer, H. J.; Ichim, M. C.; Newmaster, S. G. DNA barcoding and pharmacovigilance of herbal medicines. Drug Saf. 2015, 38, 611- 620.
- Rauchensteiner, F.; Matsumura, Y.; Yamamoto, Y.; Yamaji, S.; Tani, T. Analysis and comparison of Radix Glycyrrhizae (licorice) from Europe and China by capillary-zone electrophoresis (CZE). J. Pharm. Biomed. Anal. 2005, 38, 594-600.
- Simmler, C.; Anderson, J. R.; Gauthier, L.; Lankin, D. C.; McAlpine, J. B.; Chen, S.-N.; Pauli, G. F. Metabolite profiling and classification of DNA-authenticated licorice botanicals. J. Nat. Prod.2015, 78, 2007-2022.
- Farag, M. A.; Porzel, A.; Wessjohann, L. A. Comparative metabolite profiling and fingerprinting of medicinal licorice roots using a multiplex approach of GC-MS, LC-MS and 1D NMR techniques. Phytochemistry 2012, 76, 60-72.
- Tao, W.; Duan, J.; Zhao, R.; Li, X.; Yan, H.; Li, J.; Guo, S.; Yang, N.; Tang, Y. Comparison of three officinal Chinese pharmacopoeia species of Glycyrrhiza based on separation and quantification of triterpene saponins and chemometrics analysis. Food Chem. 2013, 141,
1681-1689.
- Xie J. et al. Identification and simultaneous determination of glycyrrhizin, formononetin, glycyrrhetinic acid, liquiritin, isoliquiritigenin, and licochalcone A in licorice by LC-MS/MS //Acta Chromatographica. – 2014. – Т. 26. – №. 3. – С. 507-516.
- Kondo K. et al. Constituent properties of licorices derived from Glycyrrhiza uralensis, G. glabra, or G. inflata identified by genetic information //Biological and Pharmaceutical Bulletin. – 2007. – Т. 30. – №. 7. – С. 1271-1277.
- Liao W. C. et al. Identification of two licorice species, Glycyrrhiza uralensis and Glycyrrhiza glabra, based on separation and identification of their bioactive components //Food chemistry. – 2012. – Т. 132. – №. 4. – С. 2188-2193.
- Simmler C. et al. Species‐specific standardisation of licorice by metabolomic profiling of flavanones and chalcones //Phytochemical Analysis. – 2014. – Т. 25. – №. 4. – С. 378-388.
- Zhou S. et al. Simultaneous Determination of Five Bioactive Components in Radix Glycyrrhizae by Pressurised Liquid Extraction Combined with UPLC–PDA and UPLC/ESI–QTOF–MS Confirmation //Phytochemical Analysis. – 2013. – Т. 24. – №. 6. – С. 527-533.
- Wei S. S. et al. Simultaneous determination and assignment of 13 major flavonoids and glycyrrhizic acid in licorices by HPLC-DAD and Orbirap mass spectrometry analyses //Chin. J. Nat. Med. – 2015. – Т. 13. – С. 232-240.
- Habib A. A. M., El-Sebakhy N. A., Kadry H. A. New and simple methylene blue colorimetric assay for glycyrrhizin in pharmaceuticals //Journal of pharmaceutical sciences. – 1979. – Т. 68. – №. 10. – С. 1221-1223.
- Ahmadi F., Rezaee S., Alipour S. Formulation and evaluation of an Aloe vera-Licorice combination topical gel: a potential choice for wound healing //Trends in Pharmaceutical Sciences. – 2017. – Т. 3. – №. 2. – С. 105-112.
- Егоров М.В. Стандартизация сырья и препаратов солодки: дис…. канд. фарм. наук:15.00.02 / Егоров Максим Валерьевич. – Пермь, 2005. – 145 с.
- Халед Ш. М. Состав и свойства биологически активных веществ шрота Glycyrrhizae radices : дис. – Халед Шади Мунир.–Казань, 2017.–150 с.: ил, 2017.
- Gupta S. et al. Chromolithic method development, validation and system suitability analysis of ultra-sound assisted extraction of glycyrrhizic acid and glycyrrhetinic acid from Glycyrrhiza glabra //Natural product communications. – 2012. – Т. 7. – №. 8. – С. 1934578X1200700808.
- Yarnykh T. G., Garkavtseva O. A., Chushenko V. N. Development and standardization of dermalic ointment //Pharmaceutical Chemistry Journal. – 2012. – Т. 45. – №. 12. – С. 750-753
- Yarnykh T., Rukhmakova O. THE ASPECTS OF DEVELOPMENT AND STANDARDIZATION OF CHILDREN’S SUPPOSITORIES WITH EXTRACT OF LICORICE ROOT //Technology transfer: innovative solutions in medicine. – 2018. – С. 49-51.
- Kumbhalkar B. et al. Simultaneous identification and estimation of glycyrrhizin, glabridin, and 18β‐glycyrrhetinic acid in de‐glycyrrhized Ayurvedic lipid‐based formulation of Glycyrrhiza glabra using dual wavelength reverse phase‐high‐performance liquid chromatography
//Separation Science Plus. – 2020. – Т. 3. – №. 10. – С. 460-471.