РЕЗЮМЕ
Предложена тактика оперативных вмешательств правосторонней гемигепатэктомии при обширных резекциях печени. Выполнение которых возможно только в специализированных центрах хирургии печени, располагающих необходимым диагностическим и специальным операционным оборудованием, а также квалифицированным персоналом с опытом работы при операциях на печени. Для успешного выполнения правосторонней гемигепатэктомии предпочтительно использовать анатомический метод резекций, который предполагает предварительную перевязку глиссоновых элементов в портальных воротах.
Ключевые слова: очаговое поражение печени, обширная резекция печени, правосторонняя гемигепатэктомия, оперативное вмешательство, правая доля печени.
Актуальность
На сегодняшний день опыт и результаты ведущих хирургов-гепатологов стран СНГ и зарубежья показывают, что успешное хирургическое лечение больных с различными очаговыми заболеваниями зависит от многих факторов и условий: размеров очагового заболевания и объема резекции, локализации опухоли, характера очага, степени вовлечения в процесс нижней полой вены, печеночных вен или элементов сосудисто-секреторной ножки в портальных воротах печени, от исполнения резекционной техники оператора и технического оснащения операционной [1,2,3,4]. Техника выполнения операции в определенной степени играет свою роль при вовлечении в опухолевый или паразитарный процесс нижней полой или воротной вен, их притоков и ветвей, которые при современном уровне развития технологии могут быть удалены вместе с участком пораженного сосуда на более или менее значительном ее протяжении [5, 6,7].
Материалы и методы
Работа основана на анализе результатов исследований и хирургического лечения (резекция печени) 193 пациентов, оказанного больным с различными очаговыми заболеваниями печени в возрасте от 2 до 73 лет за период с 1990 по 2017гг. в отделе хирургии печени ННЦХ им. А.Н.Сызганова и №7 городской клинической больницы г. Алматы.
В основную (I) группу был включен 81 пациент с очаговыми заболеваниями печени, опери-рованные с 2004 по 2017гг. У больных в процессе диссекции паренхимы печени применяли ультразвуковой гармонический скальпель, при обработке сосудисто-секреторных элементов по линии рассечения паренхимы выполняли наложение танталовых клипс. Гемостаз резецированной поверхности достигали аргоновой коагуляцией и адгезией пластин ТахоКомба (фирмы «Nycomed», Австрия). С целью профилактики и восполнения больших кровопотерь операции сопровождались сосудистой изоляцией в виде приема Прингла. Реинфузия крови при массивных кровопотерях производилась с применением кровосберегающего оборудования «Секвестр -1000».
Группу клинического сравнения (контрольная, II-группа) составили 112 пациентов, которым выполнены различного объема резекции печени в НЦХ им. А.Н.Сызганова с 1990 по 2003гг. Операции больным производились по общепринятой ранее технике оперативных вмешательств на печени с помощью диатермокоагуляции, прошивания паренхимы печени П51
образными швами Кузнецова-Пенского и его модификациями (частью с оментогепатопексией), без приема Прингла, наложения ТахоКомба и использования аппаратов кровосбережения.
В последние годы наряду с улучшением диагностики и техники выполнения операций с использованием кровосберегающих технологий возросло как общее количество резекций, так и число обширных резекций печени. Так, общее количество обширных резекций было выполнено у 133 пациентов: 62 (46,6%) больных в основной и 71 (53,4%) в контрольной группах.
Большинство больных (около 30%) было оперировано по поводу гемангиомы печени. За последний 5-летний период значительно увеличилось количество оперированных больных по поводу альвеолярного эхинококкоза (19,7%), первичного рака печени (18,5%), в то время как отсутствовали оперированные в объеме обширной резекции печени по поводу одиночных непаразитарных кист печени. Это связано с тем, что тактика хирургического лечения в нашей клинике в случаях непарази-тарного кистозного поражения печени выбрана в пользу фенестраций кист. Единичные наблюдения резекции печени у больных контрольной группы объясняются их выполнением на начальных этапах становления гепатохирургии в нашем центре.
В обеих исследуемых группах одинаково часто в процентном выражении определялось очаговые поражения печени небольших размеров: от 4 см до 10 см – около 28%, размеры которой составляли в среднем 7,2±2,6 см. Немногим более в основной группе выявлены опухоли больших и гигантских размеров (18,2±3,1см) – 44,4%, тогда как в контрольной группе частота выявления этой категории образований составила 32,1% (16,6±2,4см). Количество больных со средними размерами очаговых поражений превалировало в контрольной группе и составило соответственно 39,3% и 28,4%. У 139 (72%) больных размеры очаговых заболеваний превышали 10 см в диаметре, что является свидетельством позднего поступления больных в хирургический специализированный стационар.
Цель
Цель работы заключалась в разработке тактики выполнения оперативных вмешательств при обширных резекциях печени: правосторонней гемигепатэктомии.
Результаты исследования
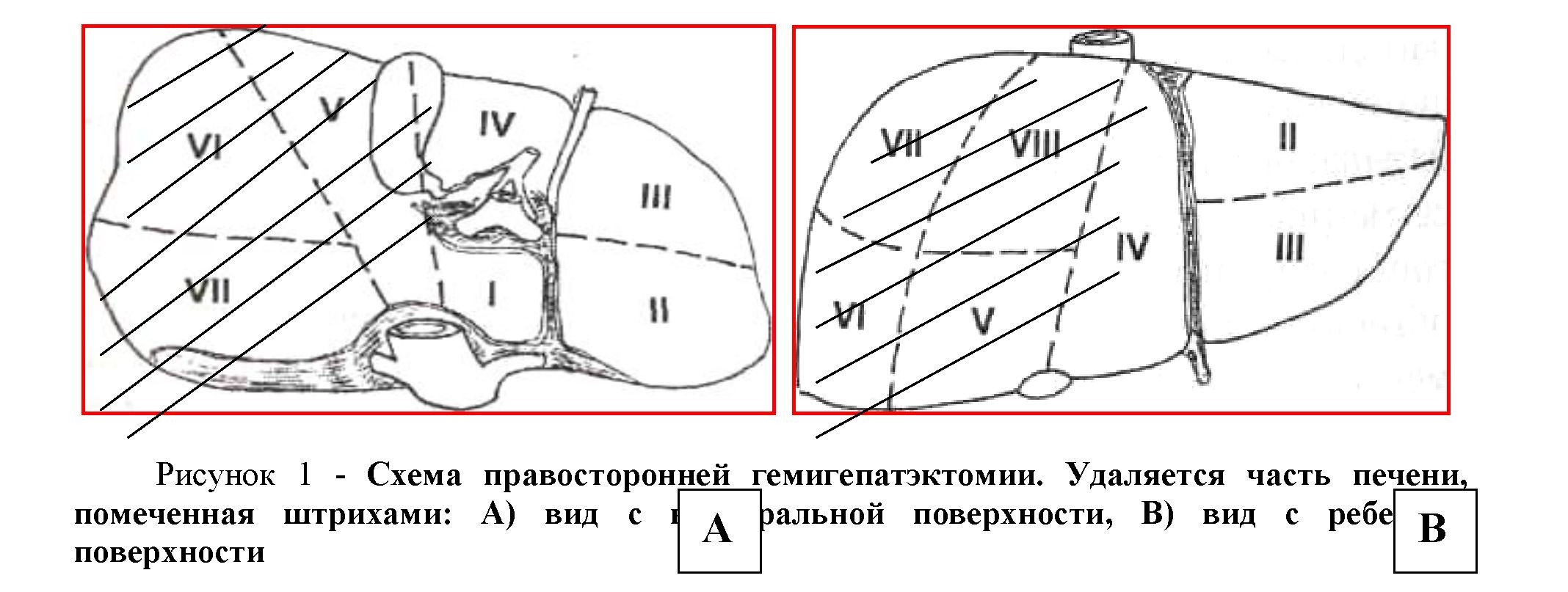
При выполнении стандартной правосторонней гемигепатэктомии удаляется вся правая доля печени, состоящая из V,VI, VII, VIII сегментов печени (рисунок 1).
Техника выполнения нами правосторонней гемигепатэктомии воротным способом состояла из 5 этапов:
- ревизия и мобилизация печени;
- выделение методом препаровки области бифуркации и правых элементов глиссоновой триады портальных ворот;
- выделение элементов кавальных ворот и дополнительных печеночных вен правой половины органа;
- диссекция паренхимы печени по плоскости резекции;
- достижение окончательного гемо-, холестаза резекционной поверхности культи печени и дренирование брюшной полости.
Ревизию печени осуществляли из верхне-срединного лапаротомного доступа. Визуально оценивали возможность выделения и лигирования правой ветви сосудисто-секреторной ножки ворот печени и объем непораженной доли печени. При отсутствии канцероматоза или объема поражения менее 70%-75% паренхимы выполняли расширение доступа по Черни. Проводили мобилизацию правой доли печени путем пересечения круглой и треугольной связок, рассечения серповидной и коронарной связок, разъединения париетальной брюшины от нижней поверхности печени. Бимануально с висцеральной и диафрагмальной поверхностей печени пальпировали элементы кавальных ворот и нижней полой вены, определяли степень вовлечения в процесс этих образований. Мобилизацию правой доли производили до нижней полой вены.
Печеночный отдел нижней полой вены обнажали путем рассечения париетальной брюшины снизу-вверх и осторожной препаровкой слабо выраженной клетчатки между задней поверхностью печени и диафрагмой. В процессе приближения к нижней полой вены с задней стороны производили мобилизацию печени от правого надпочечника, который в пяти случаях оказывался интимно вовлеченным в опухолевый процесс. Собственные надпочечниковые сосуды при этом удавалось сохранить. Окончательно визуально и бимануально оценивали возможность выполнения радикальной резекции печени и принимали решение о резектабельности патологического очага в печени и выборе оперативного объема в пользу правосторонняя гемигепатэктомия.
Выделяли гепатодуоденальную связку и её элементы в толще друг от друга и от окружающих тканей. На резиновый турникет превентивно брали печеночно-двенадцатиперстную связку. Путем раздельной перевязки пузырной артерии и протока выполнялась стандартная холецистэктомия «от шейки». Выделялись сосудисто-секреторные элементы правой печеночной ножки. Препаровкой выделяли правую печеночную артерию. Её обнаружение по пульсации обычно не представляло особых трудностей. В подавляющем большинстве случаев выделить короткую правую ветвь воротной вены не представлялось возможным без предварительного выделения и перевязки печеночной артерии.
После разведения концов пересеченной правой ветви печеночной артерии, диссектором выделяли из рыхлой клетчатки правую ветвь воротной вены, максимально используя при этом дистальную культю артерии для препаровки. Сосудистым пинцетом натягивая и перемещая культю вверх, влево и вправо, предельно осторожно разделяли клетчатку позади и латеральнее артерии, выделяли вначале переднюю, а затем и боковые стенки правой ветви воротной вены. Осторожно сомкнутым диссектором стремились обойти правую воротную вену. Предельная осторожность возникала при прохождении за заднюю стенку вены. В этих случаях манипулировали инструментом так, чтобы всегда видеть кончик диссектора.
53
При низкой топографии очагового поражения в воротах, прорастании паразитарного узла или опухолевой ткани в правую ветвь воротной вены, печеночную артерию или желчный проток прецизионно производили фенестрацию печеночной или патологической ткани с целью изолированного выделения сосудов. Далее окончательно выделяли правую печеночную ножку, раздельно проводили пробное пережатие правой ветви воротной вены и печеночной артерии сосудистым зажимом или чаще всего зажимом Блэлока до вычерчивания на поверхности печени линии аноксемии.
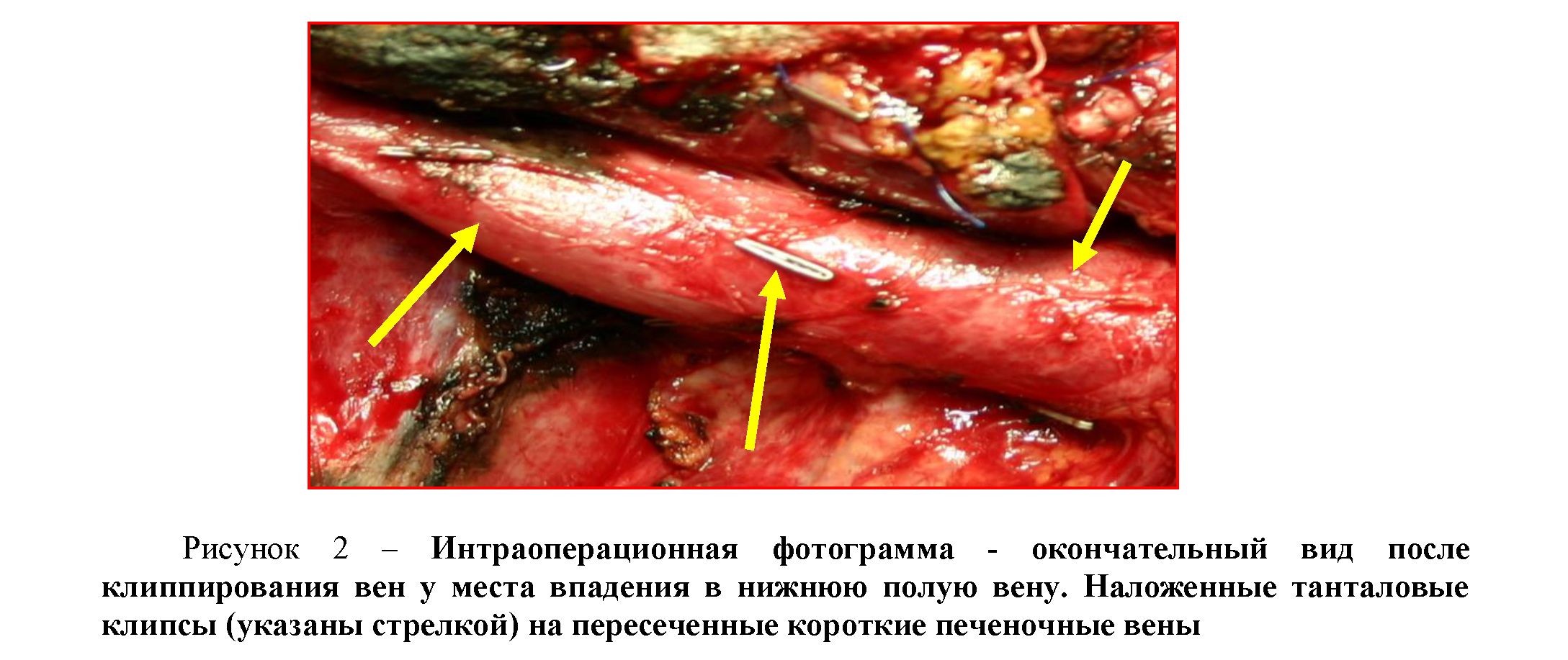
Вновь возвращались к ретропеченочной части. Благодаря вышеописанной мобилизации правой доли при осторожной и правильной тракции правой доли книзу и медиально перед нами, как правило, выслеживались короткие печеночные вены, которые встречались у больных в количестве до 12, а в среднем 5-6 вен. С применением сосудистых ножниц и диссектора выполняли со всех сторон выделение, пересечение и перевязку или клиппирование (рисунок 2) коротких печеночной вены. В единичных случаях соскальзывания клипс или лигатур гемостаз с культи коротких печеночных вен достигали прошиванием монофиламентной нитью пролена № 4/0 или № 5/0.
Правая печеночная вена впадает в нижнюю полую вену под очень острым углом. Поэтому, одним из главных условий при её мобилизации являлось сохранение стенки нижней полой вены. Печеночная вена выделялась у ретропеченочного отдела нижней полой вены осторожными движениями диссектора, при необходимости – в сочетании с ножницами, со стороны полой вены вверх для того, чтобы случайно кончиками диссектра не перфорировать стенку нижней полой вены. После обхода со всех сторон правой печеночной вены сосуд брали на резиновый турникет. При дальнейшей ревизии у значительного числа больных встречались добавочные средняя и нижняя правая печеночная вена, взятие которых на турникеты производилось по той же технологии, что и с правой веной. Печеночные вены последовательно, начиная с добавочных (при их наличии), пережимались сосудистыми зажимами Сатинского, пересекались и прошивались обвивными проленовыми (№4/0) швами дважды в направлении «туда-обратно». Культя печночной вены на удаляемой части печени прошивалась в одном направлении. Таким образом достигалась полная эфферентная изоляция удаляемой части печени.
Следующим этапом приступали к диссекции паренхимы печени. Он далеко небезопасный в отношении травмирования с последующим профузным кровотечением из нижней полой вены, левой воротной и срединной вены. Выполнение данного, не менее важного по своей значимости
 54
54
этапа, проводили двумя способами: «воротным» и «фиссуральным». После описанного выше выделения элементов глиссоновых ворот приступали к «воротному» способу рассечения паренхимы. Применяли рассечение паренхимы печени «воротным» способом как с пережатием, так и без наложения турникета на гепатодуоденальную связку. Кровопотеря во время разделения паренхимы, по данным многих хирургов составляет от 1 до 3 литров, а по некоторым источникам – до 4-6 литров крови [60, с. 42]. Однако, в последние годы благодаря наличию технического оснащения операционной и развитию резекционной технологии, интраоперационную кровопотерю удалось значительно снизить в среднем до 1000 мл и менее.
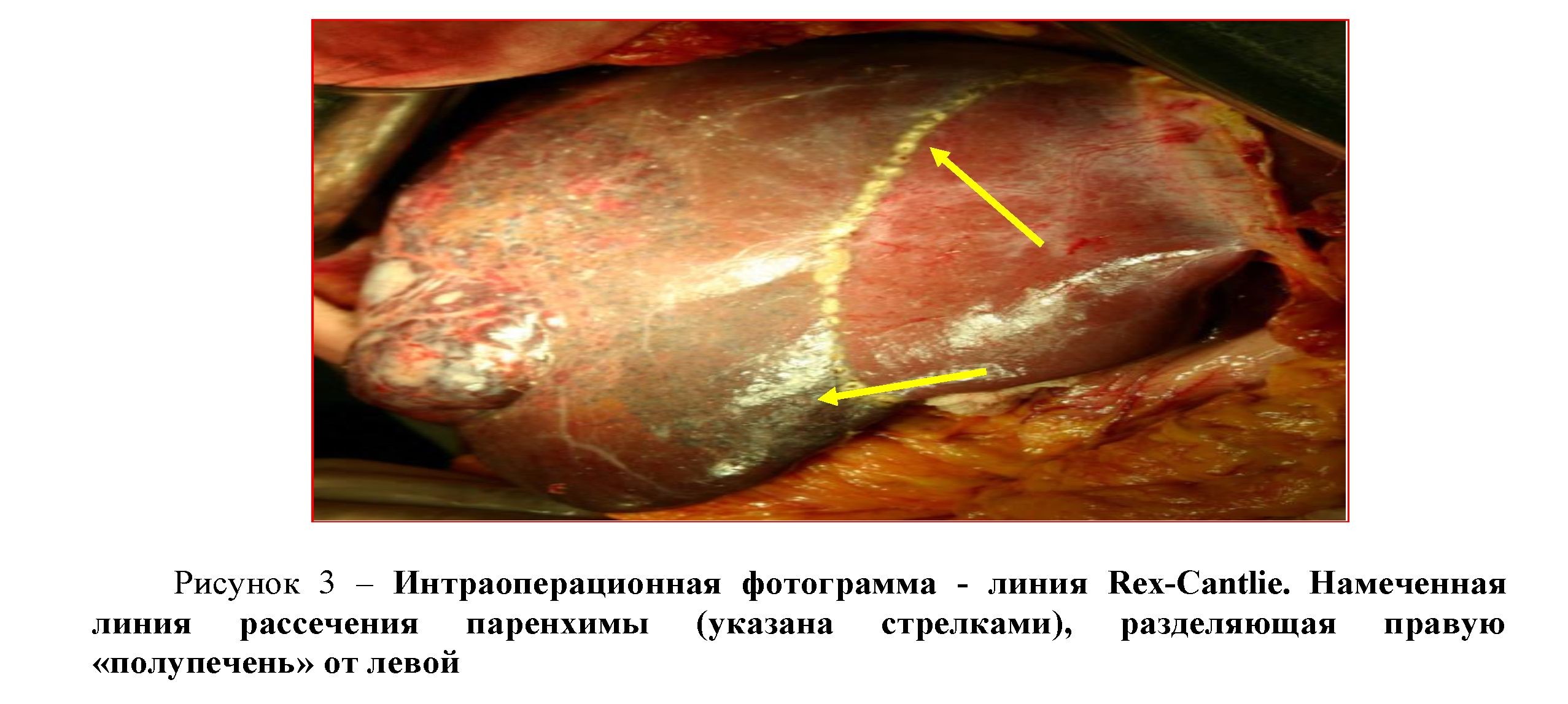
После пробного пережатия правой ветви воротной вены и печеночной артерии вычерчивалась электрокоагулятором латеральнее на 4-5 мм от линии Rex-Cantlie траектория разделения паренхимы на две доли (рисунок 3).
Выполняли между зажимами пересечение и перевязку печеночной артерии и желчного протока нитью «фторэкс» № 4/0 или № 5/0. Портальную правую вену пересекали с
образованием между ними «мостика» для того, чтобы лигатура на дистальной культе не соскользнула или не прорезалась. Ушивание проксимальной культи проводилось обвивными швами нитью «пролен» №3/0 или №4/0.
Правый желчный проток мы не стремились выделить отдельно и перевязать, так как его лигирование с прошиванием выполняли на этапе разделения паренхимы.
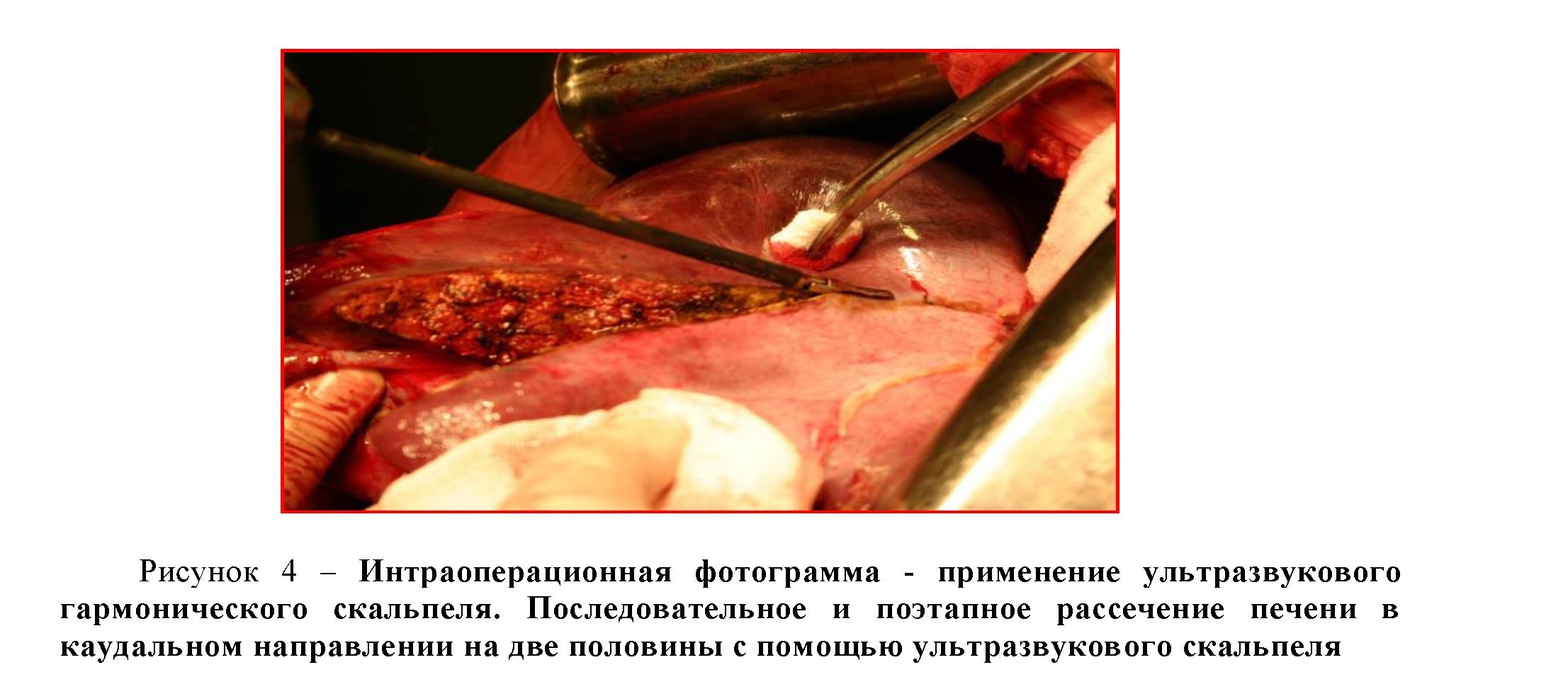
По намеченной линии рассекали последовательно и поэтапно капсулу Глиссона ультразвуковым скальпелем, начиная от переднего края печени (рисунок 4).
 55
55
До появления в нашей клинике современного оборудования диссекцию осуществляли тупым разделением паренхимы способом дигитоклазии указательным и большим пальцами, сомкнутыми сосудистыми ножницами или диссектором. Трубчатые структуры в плоскости резекции коагулировали, прошивали или лигировали. При этом пересекались и перевязывались поперечная ветвь средней печеночной вены от Sg V, VI и веточка от Sg VIII печени.
Для предотвращения кровотечения из остающейся доли печени на период разделения паренхимы применяли пережатие гепатодуоденальной связки при помощи предварительно наложенного турникета. Этот прием был обязателен при «фиссуральном» способе разделения паренхимы и выделения правой печеночной ножки.
На последнем этапе выполнения правосторонней гемигепатэктомии наружное дренирование общего желчного протока и пробу с метиленовой синькой не проводили. Перед завершением операции на поверхность остающейся части печени накладывали фибринколлагеновую субстанцию «Тахокомб» с целью достижения окончательного гемостаза. Пластины «Тахокомба» использовали у больных основной группы, однако не у всех пациентов. Из числа 62 обширной резекции печени фибрин-коллагеновую субстанцию применили у 42 (67,7%) больных. Среди 27 пациентов, перенесших правостороннюю гемигепатэктомию, указанную субстанцию прикладывали на резецированную поверхность культи печени у 16 (59,2%) больных.
Полость в правом поддиафрагмальном пространстве после удаления правой доли дренировали двумя широкопросветными (диаметром около 2 см) силиконовыми трубками. Гепатизацию в последние годы не выполняли, чтобы не деформировать и не лишать кровоснабжения оставшуюся левую долю печени. По цвету оставшейся левой доли убеждались в сохраненном ее кровоснабжении.
Затем следовала окончательная проверка на гемостаз, восстановление связочного аппарата оставшейся левой доли в последующем с послойным ушиванием раны.
Клиническое наблюдение.
Пациентка Нурлыбекова Л, 38 лет, история болезни №2136 поступила 08.11.2014 в №7 городскую клиническую больницу г. Алматы в плановом порядке с жалобами на общую слабость, тошноту, головокружение, ощущение тяжести и умеренные боли в правом подреберье.
 56
56
Из анамнеза: считает себя больной в течение 5 лет, когда стали впервые беспокоить вышеперечисленные жалобы, которые в динамике интенсифицировались и приняли частый характер.
В 2000 г. произведено УЗИ: тканевое образование правой доли печени. Консультирована хирургом, от предложенной операции отказалась. По мере нарастания и интенсификации вышеперечисленных жалоб обратилась вновь в ННЦХ и госпитализирована.
Анамнез жизни, эпидемиологический анамнез без особенностей.
Объективно при поступлении: общее состояние средней тяжести, самочувствие удовлетворительное. Пульс – 80 ударов в минуту. АД-100/70 мм.рт.ст. Дыхание в легких везикулярное, ЧДД – 20 в минуту. ЭКГ – вертикальное положение электрической оси сердца, ритм синусовый. Живот симметричный, не вздут, участвует в акте дыхания, мягкий и умеренно болезненный в правом подреберье, где определяется увеличенная на 3-4 см правая доля печени, селезёнка не пальпируется.
ОАК: эритроциты - 3,55х1012/л, гемоглобин – 103 г/л, лейкоциты - 4,5х109/л, эозинофилы - 7, палочкоядерные-5, сегментоядерные-36, лимфоциты-46, моноциты-11, СОЭ-28 мм/ч. ОАМ - без особенностей.
БАК: сахар - 5,4 ммоль/л, общий билирубин – 14,8 мкмоль/л, общий белок – 72 г/л, креатинин - 0,06 ммоль/л, АСТ - 0,14 ммоль/л, АЛТ - 0,29 ммоль/л, диастаза - 10,9 ммоль/л.
При поступлении проведено УЗИ: печень увеличена, выступает на 3,0 см ниже реберной дуги; правая доля - 10,1 см, левая – 7,4 см, ткань неоднородная. В проекции Sg VII-VIII определяется изоэхогенное образование округлой формы 10,5х10х7,6 см с четкими контурами, эхогенность по периферии повышена, в центре - снижена, образование аваскулярное, протоки печени не расширены. Заключение: УЗ-картина более характерна для альвеококкоза правой доли печени.
На серии КТ сканов органов брюшной полости в правой доле печени отмечается наличие округлого гиподенсивного образования с нечёткими контурами, размерами 10,4х10,4х9,5 см, плотность 45-46 Ед. Хаунсфильда, при внутривенном введении 20 мл омнипака накопление вещества на первой минуте и с отсрочкой нет. Левая доля печени увеличена.
Клинический диагноз: Альвеококкоз правой доли (Sg VI-VII-VIII) печени. Хронический гепатит, панкреатит.
После обследования 23.11.04 произведена лапаротомия по Черни. При ревизии печень увеличена в проекции Sg VI-VIII. На висцеральной поверхности сегментов определяется опухолевидное образование 10х12х10 см плотной консистенции с бугристой поверхностью, белесоватого цвета. При определении границ очаговое поражение прорастает Sg V на небольшом участке интимно связано с НПВ, мышечно-апоневротической частью диафрагмы, оттесняет правую почку вниз (рисунок 39).
Пересечены круглая, серповидная треугольная и коронарная связки. Выделена ГДС и взята на турникет, произведена мобилизация правой половины печени с отделением альвеококкового узла от диафрагмы и сосудисто-секреторной ножки правой почки, с которой был рыхло сращён на незначительном протяжении.
Образование острым и тупым путем выделено, выполнена холецистэктомия. Скрупулезной препаровкой выделены ворота печени, обнажена сосудисто-секреторная ножка правой доли печени. После контрольной пробы с пережатием и намеченной линией резекции правой доли печени правые желчный проток, артерия и портальная вена перевязаны и прошиты.
Правая доля печени мобилизована путем острого и тупого разъединения паразитарной ткани от париетальной брюшины, диафрагмы, паранефральной клетчатки. Выделены и лигированы пять дополнительных печеночных вен. При мобилизации и в процессе доступа к правой печеночной вене выявлено, что участок паразитарной ткани печени на протяжении 4-5 см интимно спаян с НПВ. Решено выполнить радикальную операцию без оставления
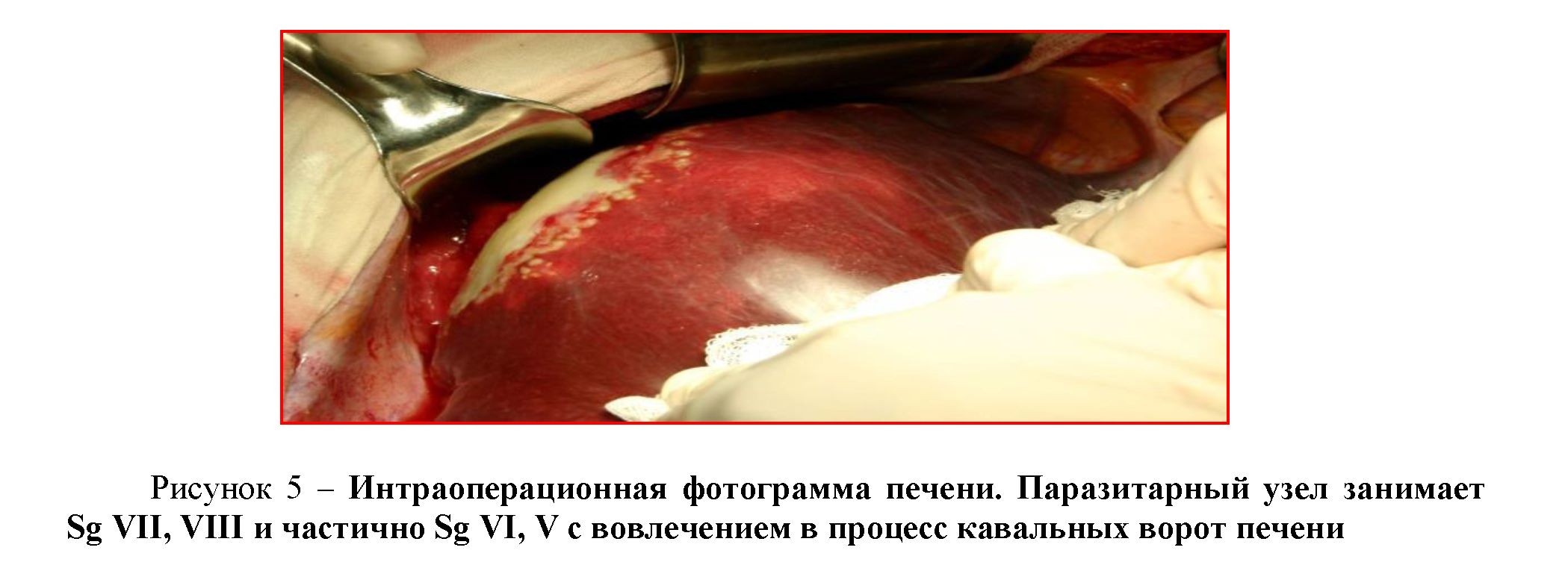
паразитарной ткани на стенке нижней полой вены, с краевой резекцией ее стенки. После пристеночного наложения зажимов Сатинского произведена резекция участка стенки НПВ вместе с паразитарной тканью правой доли печени. НПВ прошита на зажимах обвивными проленовыми швами двухрядно. Правая печеночная вена выделена диссектором, взята на сосудистые зажимы, пересечена и прошита в два ряда проленом №4/0.
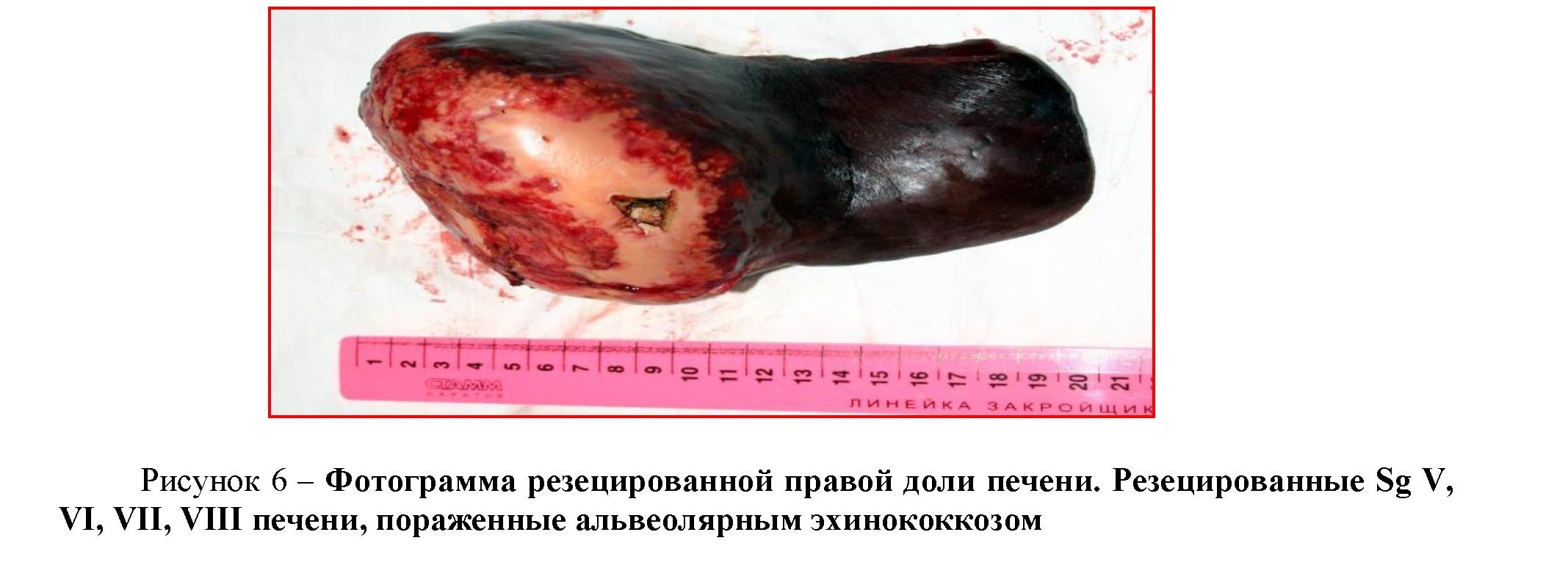
После определения границ резекции печени по линии аноксемии рассечена глиссонова капсула. Поэтапно путем дигитоклазии рассечена паренхима печени с клиппированием и перевязкой внутрипечёночных протоков и сосудов. Выполнена стандартная ПГГЭ (рисунок 6). Выполнен окончательный гемо-, холестаз культи печени. На резецированную поверхность печени наложены пластины ТахоКомба. Дефект диафрагмы 10,0х6,0 см ушит узловыми капроновыми швами. Дренирование ложа правой доли печени, правой плевральной полости по Бюлау, послойное ушивание раны.
Время пережатия ГДС составило 21 минуту. Общая интраоперационная кровопотеря – 520 мл. Длительность операции 190 минут.
Морфологическое заключение: альвеококкоз печени.
В послеоперационном периоде больная получала медикаментозную терапию: перелито 6 доз (1360 мл) свежезамороженной плазмы под контролем показателей свертываемости, альбумина 10%-200 мл под контролем показателей общего белка с альбуминовой фракцией.
58
Дважды проводилась пункция плевральной полости справа с аспирацией по 650 и 300 мл серозной жидкости.
Выписана через 26 дней, из них - после операции 18койко-дней.
Правосторонней гемигепатэктомии была выполнена у 27 первой и 30 больных второй групп. Летальность при выполнении этой категории операций составили: один больной в основной и двое больных в контрольной группах.
Выводы
Таким образом, выполнение обширных резекций печени по поводу различных очаговых заболевании печени возможно только в специализированных центрах хирургии печени, располагающих необходимым диагностическим и специальным операционным оборудованием, а также квалифицированным персоналом с опытом работы при операциях на печени. Для успешного выполнения гемигепатэктомий и расширенных гемигепатэктомий у пациентов с различными очаговыми заболеваниями печени необходимо использовать анатомический метод резекций и, в частности, «воротный» способ его исполнения, который предполагает предварительную перевязку глиссоновых элементов в портальных воротах.
Литература
- Рудаков В.А. Очаговые поражения печени. Диагностика и лечение: дисс. докт. мед. наук. – Омск, 1995. – 366 с.
- Jaeck D. et al. Surgical resection of HCC. Post-operative outcome and long-term results in Europe: an overview // Liver Trans. - 2004. – Vol. 10.2.supl.1. – Р. 58-63.
- Rudiger HA, Kang KJ, Sindram D, Riehle HM, Clavien PA. Comparison of ischemic preconditioning and intermittent and continuous inflow occlusion in the murine liver//Ann. Surg. 2002.– 235.– Р.400–407.
- Вишневский В.А., Кубышкин В.А., Чжао А.В., Икрамов Р.З. Операции на печени (руководство для хирургов). – М., 2003. – 162 с.
- Патютко Ю.И. Хирургическое лечение злокачественных опухолей печени. - М.: Практическая медицина, 2005. – 312 с.
- Альперович Б.И. (ред.) Хирургия печени и желчных путей. – Томск. 1997. – 607 с.
- Вишневский В.А. и др. Пути улучшения результатов обширных резекций печени // Анн. хир. геп. – 2005. - Т.10, №1. – С. 12-17.