Резюме
У 65% больных ишемической болезнью сердца (ИБС) симптомы индуцированных нестероидными противовоспалительными средствами (НПВС) гастропатий не соответствуют эндоскопическим изменениям. Выявлена высокая степень корреляции (R2=0.95) между частотой НПВП-гастропатий и длительностью применения препаратов. В патогенетических механизмах повреждения слизистой оболочки желудка у больных ИБС является H.pylori. Наиболее безопасным и высокочувствительным и высокоспецифичым методом диагностики инфекции у данной категории больных является 14С уреазный дыхательный тест. Алгоритм лечебно-профилактических мероприятий НПВС-гастропатий у больных ИБС предусматривает применение ингибиторов протонной помпы и невсасывающихся антацидов. При выявлении инфекции H.pylori необходимо проведение 10-дневой базисной эрадикационной терапии.
Ключевые слова: НПВС-гастропатии, диагностика, лечение.
Ишемическая болезнь сердца (ИБС) характеризуется развивающимися и прогрессирующими нарушениями системы гемостаза, что диктует необходимость использования постоянной антиагрегантной терапии (ААТ). «Золотым» стандартом для этой цели являются препараты, созданные на основе ацетилсалициловой кислоты (АСК) [1]. Репрезентативными исследованиями установлено, что применение АСК и нестероидных противовоспалительных средств (НПВС) у 1/3 пациентов с высоким риском окклюзии коронарных артерий вызывает статистически значимое уменьшение риска развития инфаркта миокарда и инсульта, а также летальных исходов [2]. Однако, несмотря на высокую эффективность, применение АСК в 25% случаев сопровождается развитием побочных эффектов. Самыми значимыми из них является НПВС–гастропатии. Потенциально развитие гастропатии угрожает любому пациенту длительное время принимающему АСК [3,4].
НПВС-гастропатия – собирательное понятие, включающее язвы и эрозии слизистой оболочки гастродуоденальной зоны (СО ГДЗ) и особую форму гастрита – «химический», в соответствии с Сиднейской классификацией [5,6].
НПВС способны в кислой желудочной среде непосредственно проникать в клетки СО. Измене-ние слизисто-бикарбонатного барьера и обратная диффузия ионов водорода приводят к “контактно-му” повреждению покровного эпителия и появлению эрозивно-язвенных процессов, нарушению про-цессов регенерации СО [7].
Факторами риска НПВС-гастропатии являются гастродуоденальная язва в анамнезе; высокие дозы НПВС; их комбинированный прием с АСК, антиагрегантами, стероидами, антикоагулянтами; возраст >65 лет; курение; наличие хеликобактерной инфекции; активность хронического гастрита в антральном отделе по данным морфологического исследования. Инфекция H.pylori ассоциирована с повышением риска возникновения неосложненных и осложненных гастродуоденальных язв у пациентов, принимающих НПВП и низкие дозы АСК (НДА) [8].
Согласно рекомендациям последнего согласительного совещания Европейской рабочей группы «Маастрихт-5» (2015) инфекция H.pylori рассматривается как независимый фактор риска развития гастродуоденальных язв и их осложнений при приеме НДАСК. Эрадикация инфекции снижает риск возникновения неосложненных и осложненных гастродуоденальных язв, ассоциированных с приемом препаратов аспирина. Эрадикация Helicobacter pylori у пациентов, длительно принимающих НДАСК, предотвращает развитие ЭЯП ГДЗ, ЖКК и рецидивов патологии ГДЗ. [9].
В этой связи, ранняя диагностика инфекции H.pylori у больных ИБС с эрозиями и язвами СО ГДЗ является важным аспектом при менеджменте пациентов с кардиоваскулярной патологией для проведения адекватной эрадикационной терапии и профилактики ЖКК. В настоящее время сущест-вует множество тестов для диагностики инфекции H.pylori. Инвазив-ные тесты (гистологический, быстрый уреазный, бактериологический) - проводятся с применение гатсробиоптатов, взятыми при эндоскопическом исследовании СОЖ больного. Однако, учитывая наличие коагулопатии, у больных ОИМ принимающих двойную антиагрегантную терапи. (НДАСК+клопидогрель, тикагрелор) при взятии биоптатов может возникнуть высокий риск ЖКК [10,11]. Поэтому, применение неинвазивных тестов у данной категории больных является предпочтительным. В частности, с помощью 14С уреазного дыхательного теста. Проведение исследования совершенно безвредно для самочувствия и здоровьяиспытуемого, является высочувствительным (95%) и высокоспецифичным (95%) методом определения уреазной активности инфекции H.pylori в выдыхаемом воздухе больного человека.
НПВС-гастропатии приблизительно у 50% больных протекают клинически латентно. Зачастую, только кровотечения могут быть единственным признаком эрозивнно-язвенных поражений СО ГДЗ. Лишь у части больных наблюдается диспепсия, боль и дискомфорт в эпигастральной области. Как правило, гастродуоденальные осложнения при приеме НПВС манифестируют без предшествующей диспепсии.Критерии диагностики НПВС-гастропатии [12]: появление на фоне применения НПВС острых, обычно множественных гастродуоденальных эрозий и/или язв с преимущественной локализацией в антральном отделе желудка; отсутствие локального воспаления и гистологических признаков гастрита; малосимптомное или асимптомное течение; частая манифестация осложнением; склонность язв к заживлению при отмене НПВС.
Большинство пациентов с факторами желудочно-кишечного риска, кратковременно или длительно принимающие НПВС или АСК, в течение всего времени лечения должны профилактически ежедневно принимать антисекреторные препараты из группы ингибиторов протонной помпы (ИПП), что уменьшает диспепсию и улучшает качество жизни больных [13]. Длительно протекающая бес-симптомная НПВС-гастропатия нередко осложняется гастродуоденальным кровотечением или перфорацией язвы, что является причиной летального исхода. В этой связи вопросы ранней диагностики и адекватной терапии НПВС-гастропатии у больных ИБС представляется весьма актуальной. Проблема имеет особую значимость, как для кардиологов, так и для гастроэнтерологов.
Цель исследования – изучение клинических и эндоскопических проявлений гастропатий, индуцированных приемом нестероидных противовоспалительных средств у больных ишемической болезнью сердца.
Материал и методы. Нами обследовано 65 больных с различными формами ИБС, находившихся на стационарном лечении в 1 городском кардиологическом центре г.Алматы. Гастродуоденальная патология (ГДП), обусловленная приемом препаратов АСК (кардиомагнил, тромбоас, аспирин-кардио), имела в 34,9% случаев от общего числа наблюдений. Средний возраст больных составил 68,9±6,5 лет. Мужчины составили 75,5%, женщины – 24,5%.
Нами был проведен анализ данных истории болезней пациентов, включающие: оценку основного заболевания, структуры гастропатий и ее осложнений, клинических (диспепсический и болевой) и объективных (локализация и выраженность болевого абдоминального) гастроэнтерологических симптомов, детализацию анамнеза (длительность приема НПВС, возраст, пол, “язвенный анамнез”). Проанализированы заключения эзофагогстродуоденоскопии (ЭГДС): характер, выраженность, локализация воспалительных и эрозивно-язвенных изменений СО ГДЗ. Эндоскопические исследования проводились больным ИБС по показаниям: с имеющимися гастроэнтерологическими симптомами; перед проведением коронарографии, операции аорто-коронарного шунтирования, стентирования коронарных артерий.
В нашей работе у больных ИБС с патологией ГДЗ проводили диагностику инфекции H.Pylori c помощью неинвазивного 14С дыхательного уреазного теста с применением устройства HUBT 20P (Производитель: Shenzhen Zhonghe Headway Bio-Sci & Tech Co., Ltd) в Республике Казахстан проводится впервые.
 Результаты исследования и их обсуждение. Из общего количества обследованных у 34,9% больных была выявлена патология ГДЗ, обусловленная приемом НПВС - кардиомагнил, тромбоас, аспирин-кардио (рис.1).
Результаты исследования и их обсуждение. Из общего количества обследованных у 34,9% больных была выявлена патология ГДЗ, обусловленная приемом НПВС - кардиомагнил, тромбоас, аспирин-кардио (рис.1).
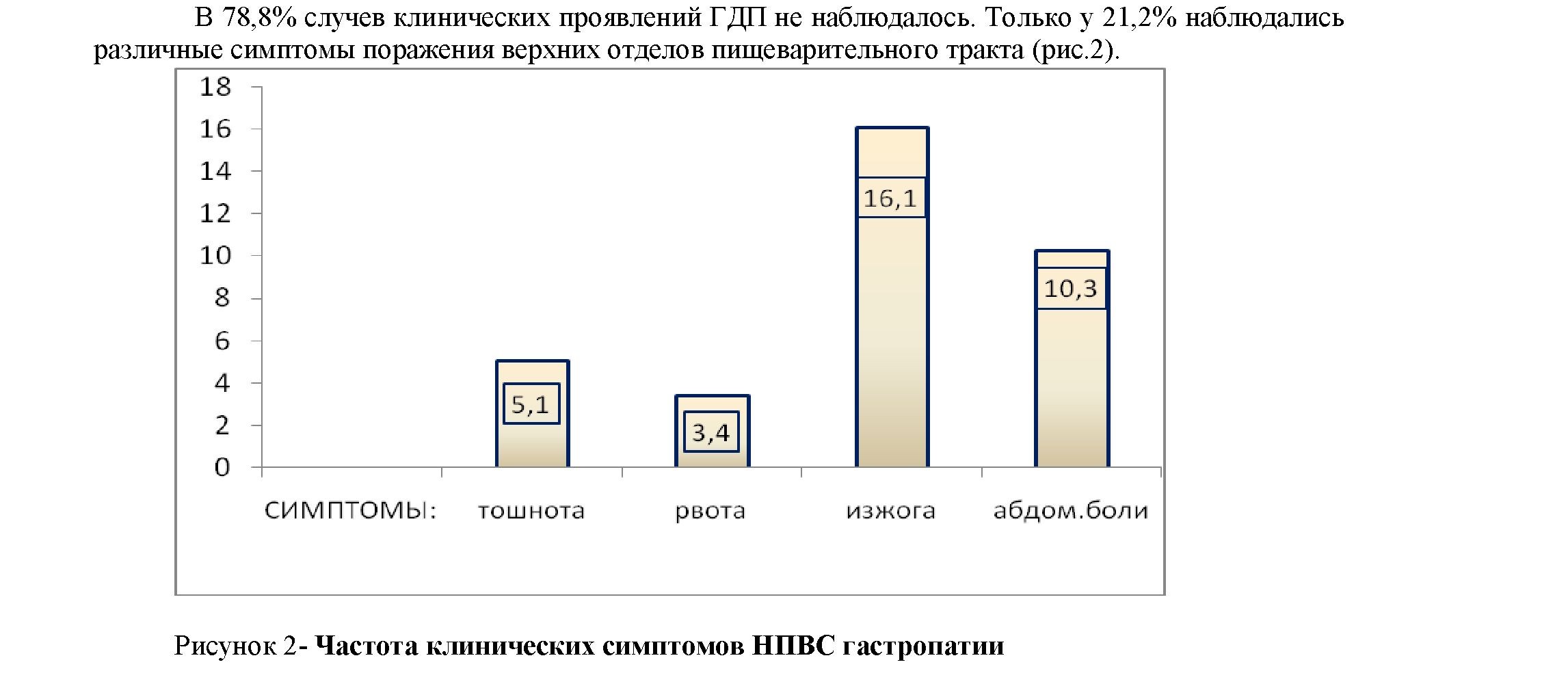
При анализе жалоб оказалось, что наиболее частыми симптомами у больных были изжога (16,1%) и непостоянные слабо выраженные абдоминальные боли (14,3%). Диспепсические симптомы тошнота и рвота отмечались лишь в 5,1% и 3,4% случаев соответственно. У большинства пациентов (68,5%) с эрозивно-язвенными поражениями СО ГДЗ отсутствовали клинические симптомы диспепсии и абдоминальных болей. Признаки гастродуоденального кровотечения - рвота «кофейной гущей» и черный цвет стула (мелена) наблюдались у 14 (из 261) больных, что составило 5,4%. Это преимущественно были пациенты с синдромом Мэлори Вейса (4 случая) и эрозиями (2 случая) и язвами (8 случаев) СО ГДЗ.
Кровотечения при эрозивно-язвенных поражениях СО ГДЗ наблюдались преимущественно у пациентов с острым или повторным инфарктом миокарда. Во всех случаях проведенная консервативная гемостатическая терапия (квамател 40 мг в 200 мл изотонического раствора NaCl внутривенно капельно в системе, этамзилат 40 мг внутривенно), позволяла остановить кровотечение. Летального исхода, обусловленного тяжелой кровопотерей не наблюдалось. Анализ факторов риска показал, что у пациентов ИБС с НПВС-гастропатией превалируют в основном два фактора риска: возраст старше 65 лет (82,5%) и длительный прием препаратов АСК или НПВС (79,6%). «Язвенный» анамнез был выявлен лишь в 7,7% случаев.
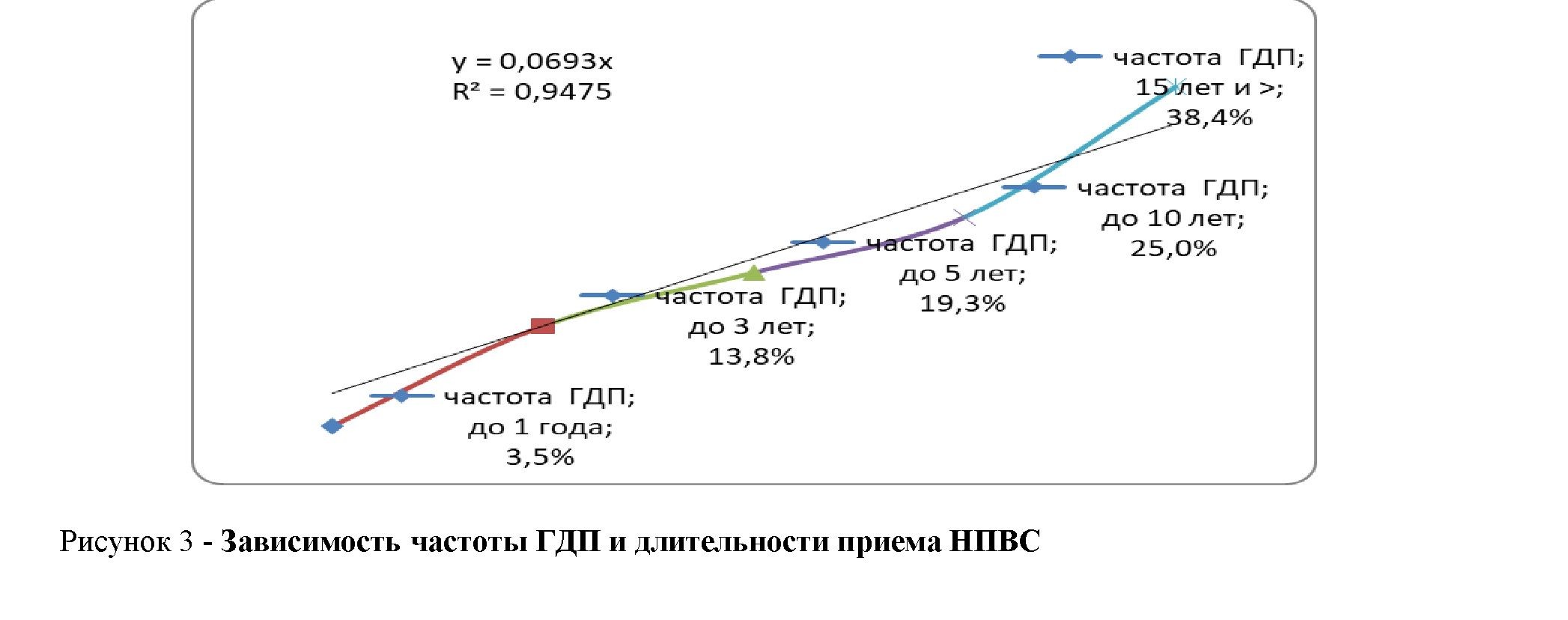
Детализация данных анамнеза позволила установить, что по мере возрастания длительности течения заболевания и, соответственно, длительности применения НПВС в качестве профилактической антиагрегантной терапии, отмечается прямо-пропорциональная зависимость повышения частоты гастропатии (рис.3).
Линия тренда на графике показывает высокую степень корреляционной зависимости (R2=0.95) частоты ГДП от длительности применения препаратов из группы НПВС или АСК. Основную массу составляли пациенты, принимающие НПВС и препараты АСК от 10 до 15 лет (25,0%) и более 15 лет (38,4%). Меньше всего было пациентов принимающих эти лекарственные препараты до 1 года (3,5%).
Анализ нозологических форм ИБС показал, что наибольший удельный вес составили пациенты с прогрессирующей стенокардией (49,5 %) и острым инфарктом миокарда (26,1%). Пациентов с повторным инфарктом миокарда оказалось 17,6%, с впервые возникшей стенокардией – 6,5%. Детализация данных анамнеза позволила установить, что и пациентам с впервые возникшей стенокардией назначались препараты АСК в связи с имеющейся в течение ряда лет артериальной гипертензией различной степени.
Клиническая картина при НПВС индуцированных гастропатиях характеризовалась дисбалансом между симптоматикой и эндоскопическими изменениями. Так, у ряда пациентов, отмечающих боли или другие диспепсические расстройства, при ФЭГДС выявлялись минимальные изменения СО ГДЗ. Напротив, при наличии множественных эрозий и язв НПВС-гастропатии часто протекали бессимптомно. При ФЭГДС у больных ИБС выявлялись различные изменения СО ГДЗ (табл.1).
Таблица 1 - Эндоскопические признаки НПВС- гастропатии
|
№ |
Эндоскопические изменения |
абс |
% |
|
Хронический поверхностный гастрит |
93 |
35,6 |
|
|
Дуоденогастральный рефлюкс |
38 |
14,6 |
|
|
Острые эрозии желудка |
34 |
13,0 |
|
|
Острые язвы желудка |
22 |
8,4 |
|
|
Острые эрозии двенадцатиперстной кишки |
29 |
11,1 |
|
|
Острые язвы двенадцатиперстной кишки |
10 |
3,8 |
|
|
Хронические эрозии желудка |
11 |
4,2 |
|
|
Хроническая язва желудка |
14 |
5,4 |
|
|
Хроническая язва ДПК |
6 |
2,3 |
|
|
Синдром Мэллори Вейса |
4 |
1,5 |
|
|
ИТОГО |
261 |
100,0 |
Анализ результатов эндоскопических исследований позволил констатировать, что у пациентов, длительное время принимающих препараты АСК или НПВС, преимущественно наблюдались изменения по типу хронического гастрита (35,6%). На втором месте по частоте наблюдался дуодено- гастральный рефлюкс (14,6%). Острые эрозии и язвы локализовались преимущественно в желудке, составив 13,0% и 8,4%, в двенадцатиперстной кишке они составили 11,1% и 3,8% соответственно.
В клинической практике трудно провести четкую грань между НПВС-гастропатиями и т.н. «стрессовыми» эрозиями и язвами, возникающими у пациентов с острым инфарктом миокарда и другой тяжелой патологией или оперативными вмешательствами. Только тщательно детализированный анамнез, указывающий на длительность приема препаратов АСК и НПВС позволяет идентифицировать эти повреждения верхних отделов пищеварительного тракта.
Нами было установлено, что все пациенты длительное время принимали различные препараты АСК или НПВС. Поэтому, все представленные случаи ГДП у больных ИБС, выявленные при проведении ретроспективного анализа истории болезней, позволяют нам полагать наличие у них НПВС- гастропатии. У 65% больных нами вывялено наличие инфекции H.pylori с помощью 14С дыхательного уреазного теста на устройстве HUBT 20P (HEADWAY, China)
По результатам проведенного анализа истории болезней алгоритм лечения НПВС-гастропатия включал следующие положения: назначение лечебной диеты (Стол 1); у всех больных с эрозивноязвенными поражениями СО ГДЗ решался вопрос о возможности отмены или снижении дозы НПВС и антиагрегантов; ИПП назначались в стандартных дозах и режимах.
Пациентам с язвенным анамнезом, а также при обнаружении инфекции Helicobacter pylori (H.pylori) с помощью иммуноферментного анализа (ИФА) или 14С уреазного дыхательного теста, назначалась эрадикационная 14-дневная терапия, которая включала: омепрозол 20 мг по 1таб 2 раза в день+ амоксициллин 1000 мг по 2 таб 2 раза в день+кларитромицин 500 мг по 2 таб 2 раза в день.
При обнаружении H.pylori эрадикацию необходимо провести до применения НПВС или АСК. Эрадикация имеющейся инфекции целесообразна и в случае предполагаемого длительного профилактического применения ИПП. При отсутствии язвенного анамнеза и в условиях уже продолжающейся терапии НПВС или АСК также следует проводить эрадикационную терапию. Следует учитывать, что во всех ситуациях успешная эрадикация инфекции H.pylori не исключает необходимости последующего профилактического применения ИПП [12].
Проведенный нами анализ истории болезней позволил выявить, что больным ИБС проводилось адекватное лечение и профилактика НПВС-гастропатии и их осложнений.
Эрозивные изменения СО ГДЗ, при отсутствии признаков кровотечения, не требовали отмены НПВС или АСК. В случае выявления язвенных поражений на любом этапе НПВС-терапии наиболее рациональной тактикой была их отмена и назначение ИПП. Эти же средства применялись в случаях, когда прекратить прием НПВС был невозможен из-за высокого риска тромбоэмболических осложнений ИБС. Больным рекомендовалось продолжение лечения ИПП от 4 до 8 недель с последующим эндоскопическим контролем.
Выводы:
- Клинические проявления НПВС-гастропатии и выявляемые при эндоскопическом исследова-нии изменения в СО ГДЗ больных ИБС в большинстве случаев не соответствуют, поэтому эндоскопичес-кий контроль, особенно в ранние сроки лечения (первые 1–2 месяца), является обязательным и адекватным методом профилактики тяжелых осложнений.
- У больных ИБС при наличии язв и эрозии СО ГДЗ с кровотечением или его угрозой рекомендуется отменить НПВС, если это невозможно, то дозу препаратов АСК необходимо снизить и назначить ИПП+антациды.
- Cтратегия лечения и профилактики НПВС-гастропатий должна заключатся на назначении гастропротекторов при наличии факторов риска и симптомов диспепсии.
- В 65% случаев у больных ИБС имеет место вывеление инфекции H.pylori, что указывает на синергитическое влияние 2-х патогенетических факторов в развитии НПВП-индуцированной гастропатии у больных ИБС. Поэтому, в соответствии с рекомендациями консенсуса Маастрихт IV (2011 г) необходимо проведение 10- или 14-дневой базисной эрадикационной терапии.
Литература
- Вёрткин А.Л., Аристархова О.Ю., Адонина Е.В. и др. Безопасность и фармакоэкономическая эффективность применения различных препаратов ацетилсалициловой кислоты у пациентов с ИБС //Русс.мед.журн. - 2009. - №8. - С.15-19
- Терещенко С.Н., Джаиани Н.А. Антитромботическая терапия как основа профилактики сердечнососудистых осложнений. Фокус на ацетилсалициловую кислоту //Трудный пациент. – 2008. - №11. – С.34-37.
- Fletcher E.H., Johnston D.E., Fisher C.R., et al. Systematic review: Helicobacter pylori and the risk of upper gastrointestinal bleeding risk in patients taking aspirin. Aliment Pharmacol. Ther. 2010;32:831–39.
- Пахомова И.Г. НПВП-индуцированные поражения желудочно-кишечного тракта: проблемы, особенности и пути решения . Consilium Medicum. Гастроэнтерология. (Прил.) 2009; 02: 71-76
- Fletcher E.H., Johnston D.E., Fisher C.R., et al. Systematic review: Helicobacter pylori and the risk of upper gastrointestinal bleeding risk in patients taking aspirin. Aliment Pharmacol. Ther. 2010;32:831–39.
- Ивашкин В.Т., Шептулин А.А., Маев И.В. и др. «Клинические рекомендации Российской гастроэнте-рологической ассоциации по диагностике и лечению эрозивно-язвенных поражений желудка и двенадцатиперстной кишки, вызванных нестероидными противовоспалительными препаратами». //Росс.ж.гастроэнтерол., гепатол., колопроктол. 2014;19(6): 89-94.
- Дроздов В.Н. Гастропатии, вызванные нестероидными противовоспалительными препаратами: патогенез, профилактика и лечение //Гастроэнтерология. Приложение к журналу “Consilium medicum” – 2005/ - Том 07. - №1. – C.29-33.
- Fletcher E.H., Johnston D.E., Fisher C.R., et al. Systematic review: Helicobacter pylori and the risk of upper gastrointestinal bleeding risk in patients taking aspirin. Aliment Pharmacol. Ther. 2010;32:831–39
- Malfertheiner P., Megraud F., O'Morain C.A. European Helicobacter and Microbiota Study Group and Consensus panel. Management of Helicobacter pylori infection-the Maastricht V/Florence Consensus Report. Gut. 2017 Jan;66(1):6-30.
- Chan F.K.L., Ching J.Y..L, Suen B.Y., et al. Effects of Helicobacter pylori infection on long-term risk of peptic ulcer bleeding in low-dose aspirin users. Gastroenterology. 2013;144:528–35.,
- Lanas Á., Carrera-Lasfuentes P., Arguedas Y., et al. Risk of upper and lower gastrointestinal bleeding in patients taking nonsteroidal anti- inflammatory drugs, antiplatelet agents, or anticoagulants. Clin. Gastroenterol. Hepatol. 2015;13:906–12.e2
- Iwamoto J., Saito Y., Honda A., Matsuzaki Y. Clinical features of gastroduodenal injury associated with long-term low-dose aspirin therapy //World J Gastroenterol. 2013; 19(11): 1673–1682.
- Uemura N, Sugano K, Hiraishi H, Shimada K, Goto S, Uchiyama S, et al. Risk factor profiles, drug usage, and prevalence of aspirin-associated gastroduodenal injuries among high-risk cardiovascular Japanese patients: The results from the MAGIC study. J Gastroenterol.2014;49:814–24.