В продолжение химических исследований тритерпеновых соединений растений рода астрагал (Бобовые) [1-3], нами выделено из надземной части растения Astragalus lehmannianus Bunge новый тритерпеновый гликозид, названный нами циклолехманозид А (1).
Выделение циклоартановых гликозидов. Воздушно-сухую надземную часть растения (1.2 кг), заготовленную в мае 2007 года Республики Каракалпакстана (низкогорья Султануздаг), исчерпывающе экстрагировали метанолом (8л × 5). Метанольные экстракты упарили до сиропообразного состояния, а к оставшейся после отгонки растворителя массе добавляли двойной объём воды, водный раствор экстрагировали сначала хлороформом, затем н-бутиловым спиртом. Бутанольное извлечение упаривали досуха, сухой остаток хроматографировали на колонке с силикагелем. После упаривания растворителей в вакууме получили 68 г бутанольного извлечения. Дальнейшее разделение веществ на индивидуальные соединения проводился методом колоночной хроматографии на силикагеле элюированием системами 4 и 5. При этом из бутанольной фракции выделены 75 мг (0.0063 % здесь и далее выход дан в пересчёте на воздушно-сухое сырьё) соединения 1, названное нами циклолехманозидом А (1), C47H80O19, т.пл. 196-198 ºС (из метанола).
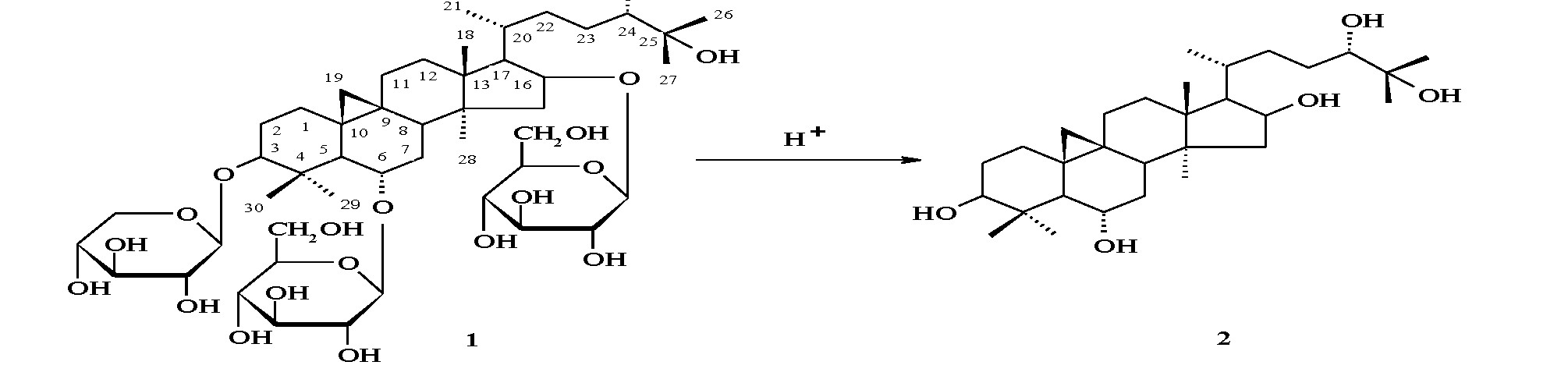
Кислотный гидролиз соединения 1. Циклолехманозид А (35 мг) растворяли в 10 мл метанола, содержащего 0.5% серной кислоты, и кипятили на водяной бане в течение 1 ч, затем реакционную смесь разбавили 20 мл воды и упарили метанол. Выпавший осадок отфильтровали, промывали водой и сушили. Фильтрат нейтрализовали карбонатом бария. После нейтрализации в фильтрате методом БХ в сравнении с заведомыми образцами обнаружили D-ксилозу и D-глюкозу.
Остаток хроматографировали на колонке, элюируя системой 1. Выделили 8 мг генина 2, идентифицированного с циклокантогенином сравнением с заведомым образцом на ТСХ и по данным спектра 1Н ЯМР.
Спектр 1Н ЯМР циклокантогенина (400 МГц, C5D5N, δ, м.д., J/Гц, 0-ТМС): 0.34 и 0.62 (2Н-19, д, 2J=4.0 Гц), 1.05, 1.38, 1.44, 1.49, 1.90, 1.90 (6xCH3, с), 1.11 (CH3-21, д, J=6.5 Гц), 3.67 (H-3, дд, J=11.4 Гц), 3.94 (H-24, дд, J=10.2 Гц), 4.74 (H-6, тд, J=6.3 Гц), 4.76 (H-16, тд, J=6.3 Гц) [4].
Установление химического строения соединения 1. В спектре 1Н ЯМР нового гликозида 1 в сильном поле при δ 0.35 и 0.58 м.д. прослеживаются два однопротонных дублета с характерной геминальной константой спин-спинового взаимодействия (КССВ) 2J=4 Гц и сигналы семи метильных групп в пределах δ 0.99-1.29 м.д. Эти данные свидетельствуют о принадлежности рассматриваемого гликозида к тритерпеноидам циклоартанового ряда [5-7].
Как уже было сказано выше, кислотный гидролиз соединения 1 приводит к получению циклокантогенина (2), D-ксилозы и D-глюкозы.
Аномерные протоны моносахаридных остатков резонируют в спектре 1Н ЯМР гликозида 1 при δ 4.42 м.д. (H-1 остатка β-D-ксилопиранозы), δ 4.48 м.д. и δ 4.65 м.д. (H-1 остатка β-D-глюкопиранозы) в виде дублетов с КССВ 3J=7.4, 3J=7.8 и 3J=7.9 Гц соответственно. Значит, моносахаридные остатки в составе изучаемого гликозида имеют пиранозную форму, 4С1-конформацию и β-конфигурацию. Об этом же свидетельствуют величины химических сдвигов углеродных атомов моносахаридных остатков в спектре 13С ЯМР соединения 1. Упомянутые показатели спектра ЯМР 13С указывают также на терминальный характер обоих моносахаридных остатков. Следовательно, соединение 1 представляет собой тридесмозидный гликозид.
Действительно, сравнительный анализ спектров 13С ЯМР соединения 1 и циклокантогенина показывает, что атомы С-3, С-6 и С-16 испытывают эффект гликозилирования и резонируют при 90.22, 78.21 и 82.23 м.д. соответственно.
В спектре 13С ЯМР соединения 1 аномерные углеродные атомы моносахаридных остатков прослеживаются при δ 106.51 м.д. (С-1 остатка β-D-ксилопиранозы), δ 104.78 м.д. и δ 105.05 м.д. (С-1 двух остатков β-D-глюкопиранозы). Величины химических сдвигов аномерных углеродных атомов свидетельствуют о том, что остаток D-ксилозы расположен при С-3, а остаток D-глюкозы – при С-6 и С-16.
Наличие в спектрах ЯМР 1Н и 13С сигналов трёх аномерных протонов при 4.42, 4.48 и 4.65 м.д., а также трёх аномерных углеродных атомов при 104.78, 105.05 и 106.51 м.д., свидетельствует о том, что соединение 1 является триозидом [8,9].
Таким образом, результаты проведённых химических и спектральных исследований позволяют нам заключить, что новый тритерпеновый гликозид циклоартанового ряда циклолехманозид А имеет структуру 3-О-β-D-ксилопиранозид, 6, 16-ди-О-β-D-глюкопиранозид-24S-циклоартан-3β,6α,16β,24,25-пентаола.
Список литературы
- Т.Х. Наубеев, А.А. Жанибеков, М.И. Исаев, Химия природ. соедин., 724 (2012)
- А.А. Жанибеков, Т.Х. Наубеев, К.К. Утениязов, Х.М. Бобакулов, Н.Д. Абдуллаев, Химия природ. соедин., 405 (2013)
- T.X. Naubeev, А.А. Janibekov, К.Dzh. Kucherbayev., Uzbek Biological Journal, 35 (2017)
- E. Bedir, I. Calis, R. Aquino, S. Piacente, C. Pizza, J. Nat. Prod., 61, 1469 (1998)
- E. Bedir, I. Calis, R. Aquino, S. Piacente, C. Pizza, J. Nat. Prod., 62, 563 (1999)
- Т.Х.Наубеев, К.К.Утениязов, М.И.Исаев, Химия природ. соедин., 229 (2011)
- М.И.Исаев, Б.А.Имомназаров, Ю.М.Фадеев, П.К.Кинтя, Химия природ. соедин., 360 (1992)
- Наубеев Т.Х., Утениязов К.К. Химия природ. соедин., 460 (2007)
- Кучербаев К.Дж., Утениязов К.К., Качала В.В., Саатов З., Шашков А.С., Химия природ. соедин., 364 (2002)