Резюме
Изучен аминокислотный и полисахаридный состав листьев и цветоложаCуnarascolymusL выращиваемого в Узбекистане. Установлено, что в белках из листьев преобладают свободные аминокислоты, в белках цветоложе – связанные. Выделены водорастворимые полисахариды, пектиновые вещества и гемицеллюлозы, получен их сравнительный моносахаридный состав. Содержание белка в листьях - 8,64%, а в цветоложе – 8,4%. В белках из листьев и цветоложа артишока содержится весь набор незаменимых аминокислот. По сумме аминокислот в листьях артишока преобладают свободные аминокислоты, в то время как в цветоложе – связанные. Молекулярная масса гетерогенных белковых компонентов от 55,6 кДа до 7,7 кДа с единственным пептидом с молекулярной массой 4,0 кДа. По данным масс-спектрального анализа цветоложа обнаружены следующие компоненты: бензиловый спирт, азулен и его производные, производные индена, сиреневый альдегид и производные пирогаллола; тритерпеновый спирт – фитол, пальмитиновая кислота и высшие углеводороды и их производные.
Ключевые слова:CуnarascolymusL., цветоложе, листья, свободные и связанные аминокислоты, полисахариды, ИК-спектроскопия.
Артишок колючий (CуnarascolymusL.) относительно новое растения для Узбекистана. В составе данного растения содержатся ряд биологически активных веществ определяющих его лечебные свойства. Лекарственные препараты на основе артишока колючего проявляют широкий спектр фармакологического действия, как гепатопротекторное, желчегонное, гипохолестеринемическое, противоатерослеротическое и др. [2,4]. Спектр такой биологической активности служит причиной пристального изучения вышеуказанного растения.
Целью данного исследования является сравнительное изучение аминокислотного и полисахаридного состава листьев и цветоложа артишока колючего выращиваемого в Узбекистане.
Материалы и методы. Выделение белка из объектов проводили экстракцией 0,2 Н гидроокисью натрия мелкоизмельченного сырья на магнитной мешалке при 500 об/мин при соотношении 1:10 в течение 1 часа. Полученный экстракт центрифугировали на рефрижераторной центрифуге при 6000 об/мин в течение 30 мин. В полученном супернатанте проводили осаждение сухим 60% сульфатом аммония (100 мл 36,88 г (NH)4SO4) и оставляли на 16 часов в холодильнике для формирования белка. Затем экстракт центрифугировали при 6000 об/мин в течение 30 мин. Полученный осадок растворяли в 0,2 Н гидроокиси натрия и определяли в растворе количественное содержание белка спектрофотометрическим методом Каркалья [2].
Определение аминокислотного состава проводили следующим образом: точную навеску протеина (50 мг) гидролизовали 5,7 Н серной кислотой при 110°С в течение 24 ч в вакуумных условиях. Гидролизаты упаривали и передавали на аминокислотный анализатор марки Т-339 (Microtechna- Prague) с программным управлением.
Определение молекулярной массы белковых фракций проводили методом ВЭЖХ на приборе AgilentTechnologies 1100 серии с использованием дегазатора G1322A, насоса для подачи растворителей 1311А, автосамплера G1313A, термостата колонки G1316A и диодноматричного детектора DADG 1315B. Колонка ZorbaxGF-250; 4,6x250 мм, 4 μm с использованием предколонки Zorbaxdiol; 4,6х12,5 мм 5 μm. Подвижная фаза: 0,1 М раствора натрий фосфатного буфера (pH=7), содержащий 0,1% SDS, скорость потока - 0,25 мл/мин, термостатирование колонки при температуре 50ºС, концентрация белков в растворе - 5 мг/мл, детектирование пиков при длине волны 210 нм. Для определения молекулярной массы белков колонка предварительно была откалибрована при помощи стандартных растворов белков с известной молекулярной массой: иммуноглобулина (160 кДа), обычного сывороточного альбумина (67 кДа), овальбумин (45 кДа), ингибитора трипсина (20 кДа). Молекулярную массу определяли путем построения калибровочного графика, используя в качестве параметров зависимость логарифма молекулярной массы белков от их объема удерживания.
Масс-спектральный анализ цветоложа проводился на хромато-масс-спектрометре «AgilentTechnology» GС/МS АТ 5973N, с применением капиллярной колонки размером 30м×0,25 мм с 5% фенилметилсилоксана при температуре инжектора 2800С, при программировании температуры термостата колонки от 80 до 2800С, величина пробы 1 мкл. Цветоложа измельчали,заливали 15 мл толуола и оставляли на 12 часов, толуол сливали и концентрировали до 1 мл.
Нисходящую бумажную хроматографию выделенных фракций полисахаридов проводили, применяя хроматографическую бумагу Filtrak-FN 18 в системе растворителей бутанол-1-пиридин-вода (6:4:3), для идентификации пятен использовали кислый фталат анилина (гексозы и пентозы) и 5% -ный раствор мочевины (кетосахара).
ВРПС гидролизовали 1Н H2SO4 в течение 8 ч при 100°С, ПВ и ГМЦ -2Н H2SO4 в течение 20 ч при 100°С), нейтрализовали карбонатом бария, деминерализовали с помощью катионита КУ-2 в Н+- форме. Далее проводили идентификацию моносахаридов БХ методом, сопоставляя со стандартными образцами. Соотношение моносахаридов анализировали методом ГЖХ в виде ацетатов альдонитрилов. Хроматограмму регистрировали на хроматографе Chrom-5 с пламенно-ионизационным детектором, колонка из нержавеющей стали (200 х 0,3 см), 5 % Silicone ХЕ - 60 на хроматоне NAW - 0,200 - 0,250 меш., температура термостата - 210ºС, температура детектора - 280ºС, газ-носитель - азот, скорость газа - 60 мл/мин.
Количество галактуронового ангидрида определяли фотоэлектроколо-риметрическим методом на основе цветной реакции с карбазолом [ 1,3].
Количественные характеристики ПВ установили титриметрическим методом [1,3]. Вязкость растворов полисахаридов измеряли в вискозиметре Оствальда с диаметром капилляра 0,73 мм.
ИК-спектры образцов снимали на ИК-спектрометре фирмы Perkin-Elmer, модель 2000, в таблетках прессованных с KBr. Инактивацию сырья проводили следующим образом: 100г измельченного сырья (листья, цветоложа по отдельности) обрабатывали кипящим хлороформом (1:5) в течение 1 ч дважды. Сырье отделяли и высушивали.
Выделение спирторастворимых сахаридов (СРС). Остаток сырья экстрагировали кипящим 82° спиртом дважды по 1 ч. Экстракты отделяли, упаривали и хроматографировали.
Экстракция ВРПС. Остаток сырья экстрагировали водой комнатной температуры в течение 1 ч, дважды при гидромодуле 1:4, 1:2. Экстракты объединяли, упаривали и осаждали спиртом 1:4. осадок ВРПС-Х отделяли центрифугированием, промывали и высушивали спиртом. ВРПС-Г выделяли аналогично при 75-80°. Выход и моносахаридный состав представлены в табл.1.
Выделение ПВ. Остаток сырья обрабатывали смесью 0,5-ных растворов щавелевой кислоты и оксалата аммония (1:1) при 80-85° в течение 2 ч при гидромодуле 1:8. Экстракты отделяли фильтрованием, диализовали против проточной воды, осаждали спиртом 1:4. Выпавший осадок ГВ отделяли, высушивали спиртом.
Экстракция ГМЦ. После извлечения ПВ сырье экстрагировали дважды 5%-ным раствором КОН (1:3, 1:2) при комнатной температуре в течение 2 ч. Экстракты отделяли, нейтрализовали СН3СООН, диализовали, упаривали и осаждали спиртом (1:3), осадок отделяли, высушивали спиртом.
Таблица 1-Состав и содержание свободных и связанных аминокислот листьев и цветоложа CуnaraScolymusL. (%)
|
Название аминокислот |
Листья артишока |
Цветоложе артишока |
|||
|
свободные |
связанные |
свободные |
связанные |
||
|
Аспарагин |
Asp |
0,72 |
0,17 |
0,51 |
0,55 |
|
Треонин* |
Thr |
0,28 |
0,10 |
0,33 |
0,24 |
|
Серин |
Ser |
0,29 |
0,15 |
0,33 |
0,33 |
|
Глутамин |
Glu |
1,19 |
0,52 |
1,08 |
1,07 |
|
Пролин |
Pro |
0,20 |
0,27 |
0,5 |
0,58 |
|
Глицин |
Gly |
0,26 |
0,17 |
0,31 |
0,31 |
|
Аланин |
Ala |
0,28 |
0,20 |
0,32 |
0,38 |
|
Цистеин |
Cys |
- |
- |
- |
следы |
|
Валин* |
Val |
0,27 |
0,16 |
0,18 |
0,34 |
|
Метионин* |
Met |
0,08 |
0,07 |
0,06 |
0,07 |
|
Изолейцин* |
Ile |
0,22 |
0,10 |
0,17 |
0,21 |
|
Лейцин* |
Leu |
0,28 |
0,28 |
0,38 |
0,54 |
|
Тирозин |
Tyr |
0,14 |
0,09 |
0,16 |
0,15 |
|
Фенилаланин* |
Phe |
0,23 |
0,12 |
0,17 |
0,25 |
|
Гистидин* |
His |
0,23 |
0,10 |
0,18 |
0,17 |
|
Лизин* |
Lys |
0,09 |
0,16 |
0,20 |
0,30 |
|
Аргинин |
Arg |
0,23 |
0,25 |
0,36 |
0,57 |
|
Сумма аминокислот |
∑ 4,99 |
∑ 2,91 |
∑ 5,24 |
∑ 6,06 |
|
* - незаменимые аминокислоты
Результаты и их обсуждения. Содержание белка в листьях составило - 8,64%, а в цветоложе –
8,4%. Полученные белковые растворы диализовали в проточной воде в течение 24 часов. Обессоленные растворы лиофильно сушили. Брали точную навеску (50 мг) белковых образцов из листьев и цветоложа, проводили количественное определение содержания свободных и связанных аминокислот. Сравнительный анализ состава и содержания аминокислот в белках приводится ниже в таблице 1.
Исходя из данных таблицы 1, в белках из листьев и цветоложа артишока содержится весь набор таких незаменимых аминокислот, как валин, треонин, метионин, изолейцин, лейцин, лизин, фенилаланин, гистидин, аргинин. По сумме аминокислот в листьях артишока преобладают свободные аминокислоты, в то время как в цветоложе – связанные.
Определена молекулярная масса белковых фракций выделенных из листьев артишока методом ВЭЖХ. Молекулярная масса белковых компонентов негомогенная, а представляет собой гетерогенный белок, состоящий из белковых компонентов с молекулярной массой от 55,6 кДа до 7,7 кДа с единственным пептидом с молекулярной массой 4,0 кДа, как это видно на рис. 1.
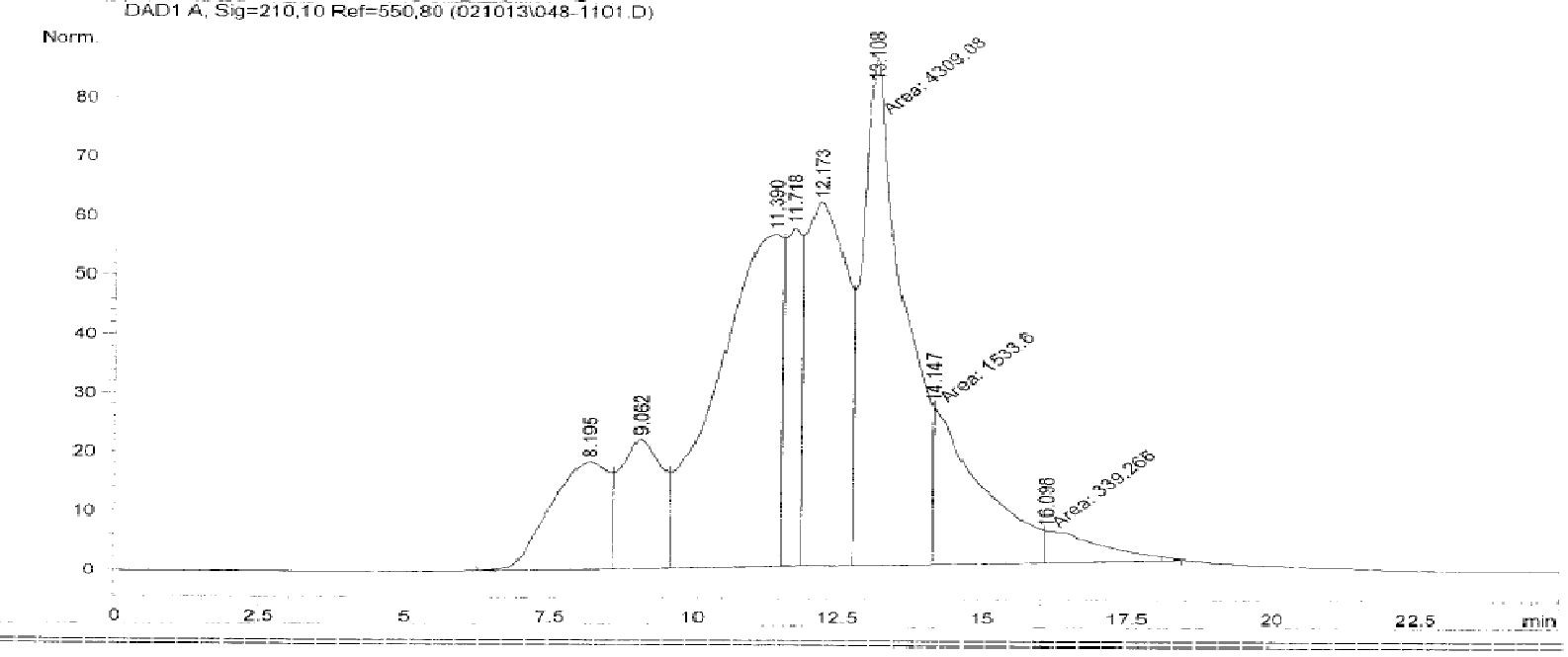
Рисунок 1 - Хроматограмма молекулярной массы выделенного белка из листьев артишока колючего
Также нами проведен масс-спектральный анализ цветоложа артишока колючего. В результате анализа в бензиновом экстракте цветоложе артишока были обнаружены следующие компоненты: бензиловый спирт, азулен и его производные, производные индена (тетрагидроциклопентадиен, 2- метилиндиен), сиреневый альдегид и производные пирогаллола; тритерпеновый спирт – фитол, насыщенная жирноя кислота (пальмитиновая кислота) и высшие углеводороды (трикозан, эйкозан, пентокозан) и их производные.
Далее проводили выделение углеводного комплекса по известной методике [1]. Воздушно-сухое сырье (по отдельности листья и цветоложа) инактивировали кипящим хлороформом для удаления красящих и низкомолекулярных соединений. Экстрагируя остаток сырья последовательно 82° спиртом, водой, смесью 0,57-ных растворов щавелевой кислоты и оксалата аммония и 5% раствором КОН, получили спирторастворимые сахара (СРС), водорастворимые полисахариды (ВРПС), пектиновые вещества (ПВ) и гемицеллюлозу (ГМЦ) соответственно. Водорастворимые полисахариды получали экстракцией холодной и горячей водой и получили ВРПС-Х, ВРПС-Г. Выделенные полисахариды в листьях и цветоложе (или цветах) артишока колючего находятся в различных количествах. Результаты исследования приведены в таблице 2.
Таблица 2-Содержание и моносахаридный состав углеводов листьев и цветоложа CуnarascolymusL.
|
Фракции полисахаридов |
Выход (%) |
Соотношение моносахаридных остатков в листьях, ГЖХ |
|||||
|
галак-тоза |
глюкоза |
арабиноза |
ксилоза |
рамноза |
уроновые кислоты, % |
||
|
ВРПС-Х |
9,75 |
10,0 |
сл. |
1,0 |
1,0 |
- |
8 |
|
ВРПС-Г |
2,25 |
1,5 |
1,0 |
1,0 |
1,0 |
сл. |
25,4 |
|
ПВ |
8,47 |
2,33 |
сл. |
1,0 |
сл. |
3,08 |
73,7 |
|
ГМЦ |
6,67 |
3,33 |
сл. |
1,0 |
0,18 |
сл. |
15,8 |
|
Соотношение моносахаридных остатков в цветоложе, ГЖХ |
|||||||
|
ВРПС-Х |
1,3 |
4,2 |
2,5 |
4,8 |
1 |
сл. |
28,2 |
|
ВРПС-Г |
2,3 |
3,0 |
1,8 |
4,5 |
1 |
сл. |
31,5 |
|
ПВ |
2,6 |
4,8 |
1 |
3,5 |
1 |
1,5 |
75,3 |
|
ГМЦ |
10 |
3,2 |
1 |
1 |
12 |
1,4 |
32,5 |
Данные таблицы 2 показывают, что в листьях содержание ВРПС-Х, ПВ и ГМЦ достаточно высокое, ВРПС-Г содержатся меньше. В гидролизатах выделенных полисахаридов обнаружили кислые и нейтральные полисахариды. Для ПВ характерно преобладание уроновых кислот – 73,5%, остальные полисахариды также содержат в своем составе уроновые кислоты, но в меньших количествах. Нейтральные моносахариды находятся в различных соотношениях.
Все выделенные полисахариды представляют собой аморфные порошки, хорошо растворимые в воде, гемицеллюлозе, в разбавленных щелочах. Водорастворимые образуют вязкие растворы с относительной вязкостью 1% раствора 3,5-4,6. Пектиновые вещества, растворяясь в воде, образуют более вязкие растворы. Наличие метоксильных групп в ПВ является важным показателем, который позволяется отнести изучаемый ПВ к группе высоко- или низкоэтерифицированных.
Для ПВ листьев и цветоложа установили количественные характеристики. Полученные результаты приведены в таблице 3.
Таблица 3 - Количественные характеристики пектиновых веществ листьев и цветоложа CуnarascolymusL.
|
Орган растения |
Кс, % |
Кэ, % |
λ, % |
|
листья |
5,2 |
7,8 |
60,0 |
|
цветоложа |
4,5 |
7,2 |
61,53 |
Полученные данные свидетельствуют о высокой степени этерификации изучаемых пектиновых веществ.
Основными по содержанию полисахаридов в цветках являются гемицеллюлозы, их количество достигает 10%.
Все выделенные полисахариды в своем составе содержат как кислые, так и нейтральные моносахариды. По моносахаридному составу ВРПС являются арабиногалактанами, причем кислыми. Пектиновые вещества также содержат, в основном, нейтральные моносахариды: галактозу и арабинозу, кислые – уроновые кислоты. Гемицеллюлозы отличаются высоким содержанием уроновых кислот, ксилозы и галактозы, т.е. основу ГМЦ составляют кислые ксилоны. Таким образом, из цветков и листьев артишока колючего выделен углеводный комплекс. Показано наличие СРС, ВРПС, ПВ и РМЦ (полностью). Дана их качественная и количественная характеристика.
Установлено, что пектиновые вещества являются высокоэтерифицированными.
Выделенные полисахариды в составе имеют остатки уроновых кислот. При этом часть карбоксильных групп метилирована, часть гидроксильных групп может быть ацетилирована. Благодаря такому разнообразию группировать ИК-спектры полисахаридов достаточно сложно.
В ИК-спектрах полисахаридов были обнаружены характерные полосы поглощения.
Цветоложе
ВРПС-Х – 3435, 2879, 1753, 1640, 1622, 1423, 1387, 1267, 1239, 1110, 1012, 890, 815, 690, 618, 532 см-1; ВРПС-Г – 3432, 2923, 1748, 1643, 1622, 1530, 1362, 1241, 1150, 1060, 1029, 934, 890, 815, 716, 532 см-1;
ПВ – 3422, 2935, 1744, 1618, 1424, 1370, 1328, 1240, 1148, 1102, 1015, 1046, 954, 889, 832, 759, 635, 533 см-1;
ГМЦ – 3435, 2924, 1632, 1417, 1314, 1244, 1163, 1093, 1041, 979, 897, 777, 599, 533 см-1.
Листья
ВРПС-Х –3200-3600, 2941, 1616, 1093-1500, 841 и 875 см-1.
ВРПС-Г –3364, 2946, 1599, 1413, 1728, 1255, 1096, 1026 см-1.
ПВ –3482-2918, 1745 и 1645, 1424, 1328-1258, 1149, 1370, 1099 – 1015, 951, 830 см-1.
ГМЦ –3284-2908, 1671, 1592-1552, 1406, 1315, 1247, 1145-1015, 950, 892, 775см-1
Сопоставление ИК-спектров полисахаридов листьев и цветоложа показывает, что они во многом совпадают, т.е. имеют одинаковые полосы поглощения, которые различаются интенсивностью и сдвигом в низко- или высокочастотные области. Совпадение основных полос поглощения связано также и с наличием остатков уроновых кислот в изучаемых полисахаридах.
В ИК-спектрах присутствуют полосы поглощения гидроксильных групп 3435-3422 см-1. Валентные колебания ионизированных групп С=О, связанных с металлами, проявляются в области 1745- 1413 см-1. Наличие последней, достаточно интенсивной полосы поглощения в ИК-спектре, является характерным для карбоксиполисахаридов, т.е. ПВ это связано также с тем, что основную цепь ПВ составляют остатки галактуроновой кислоты, а боковые ответвления представлены нейтральными сахарами. Благодаря такому разнообразию ИК-спектры ПВ представляют собой сложную картину. Полосы поглощения в области 13281258 см-1 вызваны колебаниями эфирных и гидроксильных групп. Полоса поглощения 1149 см-1 показывает наличие этерифицированных групп, а полоса поглощения 1370 см-1 конкретно указывает, что этерифицированные группы представлены метильной группой. Колебания пиранозных колец отражаются широким диапазоном 1200-1000 см-1. Деформационные колебания метильных и метиленовых групп проявляются в области 970-951 см-1. Эта полоса поглощения характерна для ПВ и кислых полисахаридов. Кроме того, эти полисахариды дают в ИК-спектрах такие полосы поглощения 890 см-1 и 830 см-1, характеризующие α-1→4гликозидную связь между остатками уроновых кислот, а боковые цепи присоединяются к основной цепи α-гликозидной связью, что соответствует полосе поглощения 777-775 см-1.
Таким образом, анализ полисахаридов методом ИК-спектроскопии дает информацию о наличии этерифицированных, свободных карбоксильных групп, а также о типе гликозидной связи между моносахаридными остатками.
Выводы. Таким образом, содержание белка в листьях - 8,64%, а в цветоложе – 8,4%.В белках из листьев и цветоложа артишока содержится весь набор незаменимых аминокислот. По сумме аминокислот в листьях артишока преобладают свободные аминокислоты, в то время как в цветоложе – связанные. Молекулярная масса гетерогенных белковых компонентов от 55,6 кДа до 7,7 кДа с единственным пептидом с молекулярной массой 4,0 кДа. По данным масс-спектрального анализа цветоложа обнаружены следующие компоненты: бензиловый спирт, азулен и его производные, производные индена, сиреневый альдегид и производные пирогаллола; тритерпеновый спирт – фитол, пальмитиновая кислота и высшие углеводороды и их производные. В листьях содержание ВРПС-Х, ПВ и ГМЦ достаточно высокое, ВРПС-Г содержатся меньше. В гидролизатах выделенных полисахаридов обнаружены кислые и нейтральные полисахариды. Для ПВ характерно преобладание уроновых кислот – 73,5%. Анализ полисахаридов методом ИК-спектро- скопии дает информацию о наличии этерифицированных, свободных карбоксильных групп, а также о типе гликозидной связи между моносахаридными остатками.
Список литературы
- Миррахимова Т.А. ИК-спектроскопическое исследование полисахаридного состава листьев Сynarasco-lymusL. /Т.А.Миррахимова, А.Н.Юнусходжаев // Фармацевтический журнал.- Ташкент,2013.- №1.-С.18-22.
- Миррахимова Т.А., Юнусходжаев А.Н. Изучение липидного и аминокислотного состава листьев артишока колючего // Фармацевтический журнал. -Ташкент, 2013.- №3.- С.23-27.
- Орловская Т.В. Изучение углеводов Cynara scolymus /Т.В. Орловская, И.Л. Лунева, В.А. Челомбитько //Химия природ. соединений. –Ташкент, 2007. - №1. — С. 89-90.
- Орловская Т.В. Химический состав листьев Cynara scolymus /Т.В. Орловская, И.Л. Лунева, В.А. Челомбитько //Химия природ. соединений. – Ташкент, 2007. - №2. - С. 197-198.